La diabetes tipo 1 (DT1) y la enfermedad celíaca (EC) son 2 enfermedades autoinmunes frecuentes en la infancia y comparten su predisposición genética (HLA-DQ2 y DQ8). La prevalencia de ambas se ha incrementado en el mundo. En el estado de Sonora (15 habitantes/km2), se desconoce información sobre su riesgo genético o la distribución de los alelos asociados en la población general.
ObjetivoComparar la frecuencia alélica HLA-DQ de una muestra representativa de recién nacidos sonorenses con la de pacientes DT1 y EC para determinar el gradiente de riesgo e identificar la presencia de autoinmunidad celíaca en el grupo de DT1.
MétodosSe incluyeron 397 recién nacidos sonorenses, 44 casos DT1 y 25 EC, diagnosticados clínicamente y con autoanticuerpos por ELISA. Se colectó una muestra de sangre, se extrajo ADNg y tipificaron HLA-DQ2 y DQ8 por PCR. El gradiente de riesgo se calculó comparando las frecuencias alélicas de los casos con respecto a los recién nacidos.
ResultadosLa proporción de heterodímeros de riesgo en sonorenses fue de 16.1% para HLA-DQ2 y de 13.6% para HLA-DQ8 con una proporción HLA-DQ2:DQ8 de 1.2:1. El genotipo DQ8/DQ2 representó un riesgo de 1:14 para DT1, mientras que para EC el DQ8/DQB1*0201 generó un riesgo de 1:6. La prevalencia de autoinmunidad asociada a EC fue del 7% en los niños DT1.
ConclusiónLos sonorenses tienen una distribución de alelos HLA-DQ distintiva debido a su ascendencia. Las combinaciones del HLA-DQ8 con DQ2 o uno de sus alelos confirieron el máximo riesgo para ambas enfermedades. La DT1 y EC frecuentemente se presentan juntas.
Type 1 diabetes (T1D) and celiac disease (CD) are the 2 most common autoimmune childhood diseases that share their HLA-DQ2 and DQ8 genetic origin. There has currently been an increase in both diseases worldwide. In children from the low-population State of Sonora (15 inhabitants/km2) in north-western Mexico, there is no information on their genetic risk or the distribution of the related alleles in the general population.
AimsTo compare the HLA-DQ allele frequency in a representative sample of newborns from Sonora with that of T1D and CD patients to determine the risk gradient, and to identify the presence of celiac autoimmunity in the T1D group.
MethodsThe study included 397 Sonoran newborns, with 44 cases of T1D, and 25 CD cases. The CD and T1D cases were clinically diagnosed by specialists at the Hospital Infantil del Estado de Sonora, and the autoantibodies were determined by ELISA. Whole blood was collected, gDNA was extracted, and HLA-DQ2 and DQ8 were typed by PCR-SSP. The risk gradient was calculated by comparing the allele frequencies of the cases with those of the newborns.
ResultsThe Sonoran HLA-DQ risk heterodimer proportion was 16.1% for HLA-DQ2 and 13.6% for HLA-DQ8, with an HLA-DQ2:HLA-DQ8 ratio of 1.2:1. The DQ8/DQ2 genotype represented a 1:14 risk for T1D, whereas the DQ8/DQB1*0201 combination showed a 1:6 risk for CD. The prevalence of CD autoimmunity in T1D children was 7%.
ConclusionThe Sonoran population has a distinctive HLA-DQ allele distribution due to its ancestry. The HLA-DQ8 combinations with DQ2 or one of its alleles conferred the highest risk for both diseases, and T1D and CD frequently appear together.
La diabetes tipo 1 (DMT1) es una enfermedad crónica causada por la destrucción de las células beta del páncreas, mediada por el sistema autoinmune, que usualmente llevan a una deficiencia absoluta de insulina1. La enfermedad celíaca (EC) es otro trastorno sistémico inflamatorio, que afecta primariamente al intestino delgado, causado por una reacción inmune al gluten en la dieta (proteína de almacenamiento del trigo, cebada y centeno) en individuos con una predisposición genética resuelta al excluir el gluten de la dieta2.
La DMT1 y la EC son 2 de las enfermedades autoinmunes más comunes de la niñez, con una prevalencia de 1:100 a 1:200 para la EC3 y de 1:300 para la DMT14. Adicionalmente, la prevalencia de EC en pacientes con DMT1 parece ser 20 veces mayor5, siendo frecuentemente subdiagnosticada ya que el apego a los lineamientos diagnósticos en la práctica actual varía ampliamente6. Estas enfermedades mediadas por el sistema inmune comparten algunas características ambientales y genéticas7.
El sistema del antígeno de leucocitos humanos clase ii (HLA) es el factor genético más importante para las enfermedades autoinmunes como la DMT1 y la EC, principalmente los isotipos DQ y DR8. Por lo tanto, los haplotipos HLA-DQ2 y DQ8 contribuyen en más del 50% de la carga genética para ambas enfermedades9,10. Las moléculas HLA-DQ expresadas son heterodímeros de las cadenas polimórficas α y β que pueden ser codificadas en cis o trans11. En las células presentadoras de antígenos del sistema inmune, estas moléculas específicamente fijan los péptidos, como aquellos que son derivados del gluten que inducen la EC, así como los péptidos de los autoantígenos de los islotes, incluyendo la insulina, que se degenera en la DMT112.
En Europa, alrededor del 90-95% de los pacientes celíacos tienen el haplotipo HLA-DQ2, compuesto por los alelos DQ1*0501/DQB1*0201, mientras que el otro 5-10% tiene el haplotipo HLA-DQ8 con DQA1*0301/DQB1*030213. Estos mismos haplotipos están presentes en un 90% de los pacientes con DMT114. Sin embargo, se ha asociado un riesgo más alto con el HLA-DQ8, en contraste con la EC, en la cual HLA-DQ2 produce el mayor riesgo15. Aunque se han estudiado otros factores para estas enfermedades, tales como la presencia de parientes afectados, patrón de alimentación e infecciones intestinales tempranas, el genotipo HLA es el único factor de riesgo conocido que se asocia significativamente con el desarrollo de autoinmunidad a la EC16. Por lo tanto, la posibilidad de estratificar a los individuos basados en su estatus de HLA-DQ es necesaria en la implementación de intervenciones dirigidas a la prevención y tratamiento de estas enfermedades17,18. Este enfoque favorecería el desarrollo de un cuidado de la salud personalizada, adaptado a las características locales de cada población.
En el noroeste de México, el estado de Sonora presenta características únicas con respecto a los habitantes de su territorio. Sonora es el segundo estado más grande en México, con un área de 179,516km2 y una población de 2,662,480 personas19 que corresponde a una densidad de población menor de 15 habitantes/km2. Además, debido a que la mayoría del territorio de Sonora es desértico, sus habitantes se han mantenido relativamente aislados del resto del país. Por lo tanto, la población de Sonora que se ha mezclado tiene el más alto linaje europeo y el más bajo componente amerindio en comparación con otras poblaciones mexicanas20. Sin embargo, hasta la fecha no existen datos en cuanto a la frecuencia de alelos HLA-DQ2 y DQ8 en la población en general.
En la actualidad hay un aumento en los casos de DMT1 y EC en niños de Sonora cuya población pertenece a un grupo de mestizaje especial. Por lo tanto, el objetivo de este estudio fue comparar la frecuencia del alelo HLA-DQ en recién nacidos de Sonora con pacientes que padecen de DMT1 y EC para determinar su gradiente de riesgo e identificar la presencia de autoinmunidad celíaca en el grupo de DMT1.
MétodosSujetosEstudio analítico transversal que se llevó a cabo en Sonora, México, con niños que acudieron al Hospital Infantil del estado de Sonora. Este es el hospital regional infantil más grande y por lo menos el 90% de los padres y abuelos de los pacientes nacieron en el noroeste de Mexico21.
El tamaño de muestra apropiado para el grupo de referencia fue determinado por la fórmula de proporciones, n=(Z2αpq)/d2, tomando en consideración el total de la población sonorense (2,662,384 personas), una prevalencia estimada del 30% de haplotipos HLA-DQ2 y DQ8 en otras poblaciones, y un intervalo de confianza del 95% con un margen de error del 5%. De igual forma, para los grupos con DMT1 y EC, se consideró una prevalencia esperada de 1:300 y 1:200, así como el hecho de que más del 90% de estos pacientes con estas enfermedades tienen haplotipos DQ. De acuerdo con este enfoque, se requerían 323 controles, 16 casos de EC y 8 casos de DMT1.
Con base en lo anterior, la muestra control consistió en 397 infantes, nacidos entre finales del 2010 y comienzos del 2011 y que representaban el 14.5% de los recién nacidos en el Hospital Infantil del Estado de Sonora durante el periodo de recolección de la muestra. Para los grupos de casos, un total de 44 niños y adolescentes con DMT1 y 25 con EC, con un rango de edad de 2 a 18 años, fueron reclutados durante los años 2012-2014. La muestra de pacientes representa el total de casos de DMT1 y EC detectados en el hospital durante el periodo de muestreo. El diagnóstico de EC fue confirmado mediante la clasificación de Marsh determinada por biopsias del intestino delgado y anticuerpos séricos antitransglutaminasa tisular (tTG)/antigliadina. De la misma forma, los diagnósticos de DMT1 se establecieron de acuerdo con los criterios de la Asociación Americana de Diabetes1, incluyendo anti-GAD y/o anticuerpos anti-IA2.
Aprobación éticaTodos los procedimientos fueron aprobados por el comité de ética del Centro de Investigación en Alimentación y Desarrollo (CIAD) y por el Comité de Enseñanza e Investigación del Hospital Infantil del Estado de Sonora, de acuerdo con los estándares de la declaración de Helsinki de 1964 y sus lineamientos de Buenas Prácticas Clínicas. Se obtuvo consentimiento informado de los guardianes legales de los participantes de este estudio.
Recolección de las muestrasLa sangre del cordón umbilical fue colectada al momento del nacimiento en todos los controles y almacenada a 4°C para la tipificación de HLA. Además, se colectaron 5mL de sangre periférica de todos los niños con casos de DMT1 y EC, de la cual 2mL fueron utilizados para la extracción de ADN. El suero de la muestra restante se separó y reservó para su revisión serológica.
Extracción de ADN y tipificación del HLASe extrajo el ADN genómico de las muestras de sangre completas utilizando el QIAamp DNA Mini Kit (Qiagen®, Hilden, Alemania), de acuerdo con las instrucciones del fabricante. La tipificación de HLA-DQ2 y DQ8 fue llevada a cabo utilizando la reacción de polimerasa en cadena con los cebadores de secuenciación específicos (PCR-SSP) para los alelos DQA1*0501, DQA1*0301, DQB1*0201, y DQB1*0302 (IDT-Integrated DNA Technologies, Tucson, AZ, EE. UU.), como fue reportado por Olerup et al.22. Los productos amplificados por PCR que se obtuvieron fueron analizados con gel agarosa del 1.8% teñido con GelRed™ (Biotium Inc., Hayward, CA, EE. UU.), y visualizados bajo luz ultravioleta (Molecular Imager®Bio-Rad, Hercules, CA, EE. UU.). Los haplotipos HLA-DQ2 y DQ8 fueron confirmados evaluando los alelos DRB1*03 y DRB1*04 asociados de la fracción HLA-DR, a través de PCR-SSP.
La frecuencia de los alelos HLA en nuestra muestra fue calculada utilizando el método de conteo directo y comparado a través de la prueba de Chi-cuadrada utilizando el programa de análisis NCSS versión 2007. Un valor de p<0.05 fue considerado estadísticamente significativo.
Gradiente de riesgoDespués de la evaluación de los 4 alelos de riesgo del HLA-DQ, se esperaban 16 patrones positivos posibles, obteniendo así las combinaciones distintas en loa cuales los alelos de riesgo del HLA-DQ se presentaban tanto en los casos de DMT1 como en EC. Estas combinaciones fueron utilizadas para el análisis. A propósito de la nomenclatura, el término DQ2 se utilizó únicamente cuando el paciente tenía el alelo de DQA1*0501 y el alelo DQB1*0201. Asimismo, el DQ8 se refería únicamente a los pacientes con ambos alelos, DQA1*0301 y DQB1*0302. Los fenotipos codificados con solo uno de estos alelos, formando dímeros con una cadena distinta, fueron etiquetados como A1*0501, B1*0201, A1*0301, o B1*0302, respectivamente.
El riesgo para DMT1 y EC fue expresado como 1:N, donde N es el número de individuos entre los cuales un solo paciente se encuentra presente, como lo describieron previamente Megiorni et al.23. Por lo tanto, N se calculó como el porcentaje de controles (recién nacidos sonorenses de la población en general) con ese estatus particular de HLA-DQ multiplicado por 100 y dividido por el porcentaje de pacientes con la misma tipificación de DQ. Para este análisis, consideramos la prevalencia reportada de 1:300 para DMT1 y de 1:100 a 1:200 para EC, para poner los resultados en perspectiva. Para confirmar el poder del gradiente estimado, se calculó la razón de momios (RM) para cada combinación de alelos.
Tamizaje serológicoLos diagnósticos de DMT1 se complementaron por la cuantificación de anti-GAD y anticuerpo anti-IA2 con un kit de ELISA de acuerdo con las instrucciones del fabricante. (Kronus®, EE. UU.). La antitransglutaminasa IgA y antigliadina IgG y los títulos de IgA del suero también se midieron por ELISA, utilizando gliadinas enzimáticamente digeridas extraídas de nuestro laboratorio. Se usó ELISA como se realiza en nuestro laboratorio24, incluyendo la definición de los valores de corte.
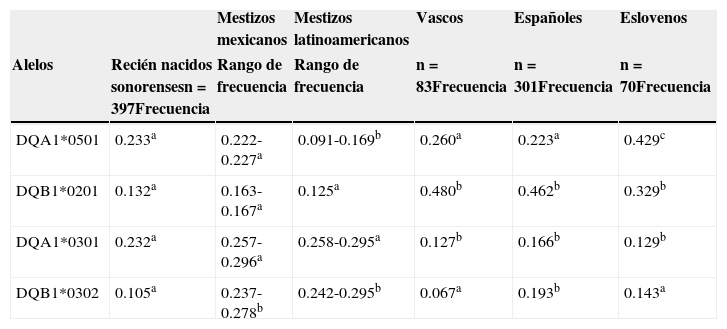
ResultadosLa frecuencia de proporción de heterodímero de riesgo para los recién nacidos de Sonora en el noroeste de México fue del 16.1% para el HLA-DQ2 y del 13.6% para el HLA-DQ8, con una proporción HLA-DQ2: HLA-DQ8 de 1.2:1. La frecuencia de alelos HLA-DQ2.5 y HLA-DQ8 en recién nacidos se presenta en la tabla 1. La tercera y cuarta columnas muestran el rango de frecuencias de alelos de otras poblaciones, tales como las de mestizos mexicanos25–27 y mestizos latinoamericanos28,29. Como era de esperar, los alelos de los niños sonorenses eran más parecidos a los de los mestizos mexicanos que a los de otros mestizos latinoamericanos. Únicamente uno de los 4 alelos que fueron comparados (DQB1*0302) tuvo una frecuencia más baja en los niños sonorenses que en los mestizos mexicanos. Además, hubo una mayor frecuencia del DQA1*0501 (p<0.05) en los niños sonorenses que en mestizos latinoamericanos. Las más altas frecuencias de alelos en recién nacidos de Sonora fueron las de DQA1*0501 (0.233) y DQA1*0301 (0.232).
Frecuencia de alelos de los haplotipos HLA-DQ2 y HLA-DQ8 en recién nacidos sonorenses en comparación con diferentes grupos étnicos de mestizos y europeos
| Mestizos mexicanos | Mestizos latinoamericanos | Vascos | Españoles | Eslovenos | ||
|---|---|---|---|---|---|---|
| Alelos | Recién nacidos sonorensesn=397Frecuencia | Rango de frecuencia | Rango de frecuencia | n=83Frecuencia | n=301Frecuencia | n=70Frecuencia |
| DQA1*0501 | 0.233a | 0.222-0.227a | 0.091-0.169b | 0.260a | 0.223a | 0.429c |
| DQB1*0201 | 0.132a | 0.163-0.167a | 0.125a | 0.480b | 0.462b | 0.329b |
| DQA1*0301 | 0.232a | 0.257-0.296a | 0.258-0.295a | 0.127b | 0.166b | 0.129b |
| DQB1*0302 | 0.105a | 0.237-0.278b | 0.242-0.295b | 0.067a | 0.193b | 0.143a |
En las últimas columnas, la tabla 1 muestra la comparación de recién nacidos sonorenses con poblaciones españolas y vascas en general; se utilizó una población eslovena como referencia caucásica. No se encontraron diferencias significativas (p>0.05) entre los recién nacidos sonorenses y los vascos o españoles para la frecuencia del alelo DQA1*0501, como fue reportado por Sánchez-Velasco et al.30 y Planelles et al.31 La baja frecuencia del alelo DQB1*0302 para los recién nacidos sonorenses en este estudio solo era comparable (p>0.05) con la frecuencia del alelo de los vascos30 y los eslovenos. No se encontró ninguna otra similitud entre los niños sonorenses y los eslovenos15 con relación a cualquiera de los 3 alelos analizados restantes.
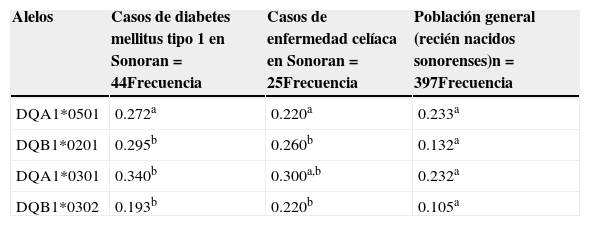
En relación con los casos sonorenses de DMT1 y EC, encontramos una frecuencia similar en los alelos estudiados cuando comparamos los 2 grupos (p>0.05). Sin embargo, la comparación entre estos 2 grupos con la información de los recién nacidos sonorenses muestra que los pacientes con DMT1 y EC tenían una frecuencia de los alelos DQB1*0201 y DQB1*0302 que era significativamente mayor (p<0.05) que en la población en general, como se muestra en la tabla 2. De igual forma, el DQA1*0301 fue el alelo de riesgo más prevalente en pacientes con DMT1 y EC. Sin embrago, la alta frecuencia solo era significativa (p<0.05) cuando el grupo de DMT1 se comparó con los recién nacidos de la población en general, pero no para el grupo de EC.
Frecuencia de alelos de los haplotipos HLA-DQ2 y HLA-DQ8 en casos de DMT1 y de EC en Sonora comparados con la población general (recién nacidos sonorenses)
| Alelos | Casos de diabetes mellitus tipo 1 en Sonoran=44Frecuencia | Casos de enfermedad celíaca en Sonoran=25Frecuencia | Población general (recién nacidos sonorenses)n=397Frecuencia |
|---|---|---|---|
| DQA1*0501 | 0.272a | 0.220a | 0.233a |
| DQB1*0201 | 0.295b | 0.260b | 0.132a |
| DQA1*0301 | 0.340b | 0.300a,b | 0.232a |
| DQB1*0302 | 0.193b | 0.220b | 0.105a |
n: tamaño de la muestra.
Los distintos superíndices indican diferencias significativas (p<0.05) entre la población general, casos de DMT1 y casos de EC.
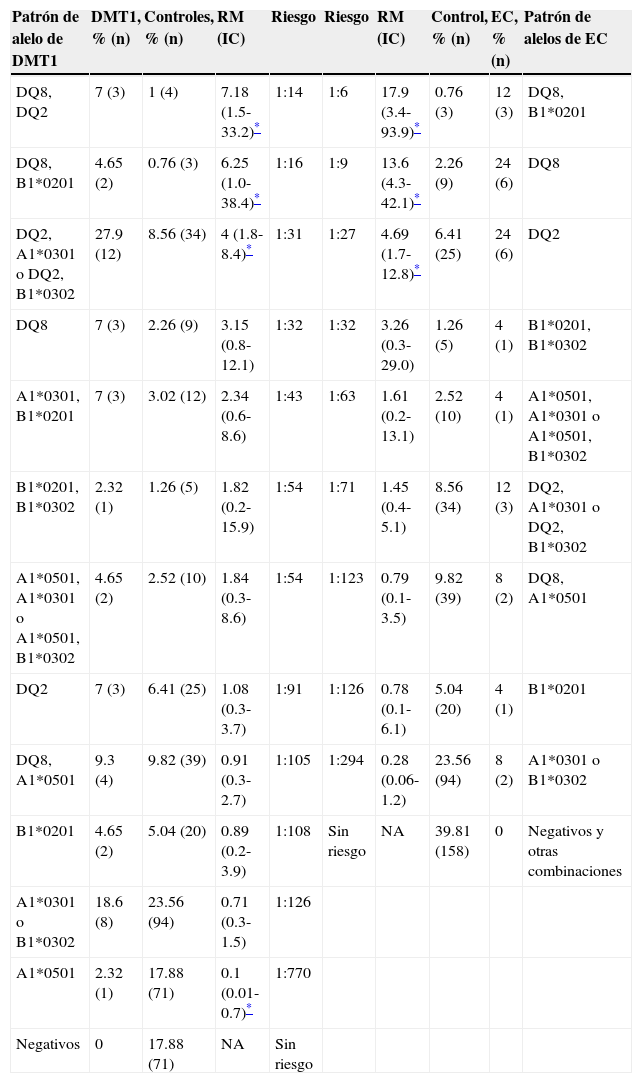
Basado en las frecuencias, se desarrolló un gradiente de riesgo para DMT1 y EC en la población sonorense, de acuerdo con las diferentes combinaciones de los 4 alelos del HLA-DQ2 y DQ8 que se estudiaron (tabla 3). Nuestros hallazgos muestran que el grupo de EC era más homogéneo, resultando en menos combinaciones de alelos de riesgo positivos que aquellos que se encontraban en el grupo de DMT1. Por lo tanto, los pacientes con DMT1 presentaron 16 combinaciones de alelos posibles, mientras que solo encontramos 13 en el grupo de EC. Las 3 combinaciones restantes fueron agrupadas como «otras» para el análisis de EC, para completar el 100% del grupo de control.
Gradiente de riesgo para la enfermedad. Los riesgos para DMT1 y EC se evaluaron a partir de la frecuencia de alelos de HLA-DQ, considerando una prevalencia de la enfermedad de 1:300 para DMT1 y de 1:100 a 1:200 para EC, resaltado en la tabla
| Patrón de alelo de DMT1 | DMT1, % (n) | Controles, % (n) | RM (IC) | Riesgo | Riesgo | RM (IC) | Control, % (n) | EC, % (n) | Patrón de alelos de EC |
|---|---|---|---|---|---|---|---|---|---|
| DQ8, DQ2 | 7 (3) | 1 (4) | 7.18 (1.5-33.2)* | 1:14 | 1:6 | 17.9 (3.4-93.9)* | 0.76 (3) | 12 (3) | DQ8, B1*0201 |
| DQ8, B1*0201 | 4.65 (2) | 0.76 (3) | 6.25 (1.0-38.4)* | 1:16 | 1:9 | 13.6 (4.3-42.1)* | 2.26 (9) | 24 (6) | DQ8 |
| DQ2, A1*0301 o DQ2, B1*0302 | 27.9 (12) | 8.56 (34) | 4 (1.8-8.4)* | 1:31 | 1:27 | 4.69 (1.7-12.8)* | 6.41 (25) | 24 (6) | DQ2 |
| DQ8 | 7 (3) | 2.26 (9) | 3.15 (0.8-12.1) | 1:32 | 1:32 | 3.26 (0.3-29.0) | 1.26 (5) | 4 (1) | B1*0201, B1*0302 |
| A1*0301, B1*0201 | 7 (3) | 3.02 (12) | 2.34 (0.6-8.6) | 1:43 | 1:63 | 1.61 (0.2-13.1) | 2.52 (10) | 4 (1) | A1*0501, A1*0301 o A1*0501, B1*0302 |
| B1*0201, B1*0302 | 2.32 (1) | 1.26 (5) | 1.82 (0.2-15.9) | 1:54 | 1:71 | 1.45 (0.4-5.1) | 8.56 (34) | 12 (3) | DQ2, A1*0301 o DQ2, B1*0302 |
| A1*0501, A1*0301 o A1*0501, B1*0302 | 4.65 (2) | 2.52 (10) | 1.84 (0.3-8.6) | 1:54 | 1:123 | 0.79 (0.1-3.5) | 9.82 (39) | 8 (2) | DQ8, A1*0501 |
| DQ2 | 7 (3) | 6.41 (25) | 1.08 (0.3-3.7) | 1:91 | 1:126 | 0.78 (0.1-6.1) | 5.04 (20) | 4 (1) | B1*0201 |
| DQ8, A1*0501 | 9.3 (4) | 9.82 (39) | 0.91 (0.3-2.7) | 1:105 | 1:294 | 0.28 (0.06-1.2) | 23.56 (94) | 8 (2) | A1*0301 o B1*0302 |
| B1*0201 | 4.65 (2) | 5.04 (20) | 0.89 (0.2-3.9) | 1:108 | Sin riesgo | NA | 39.81 (158) | 0 | Negativos y otras combinaciones |
| A1*0301 o B1*0302 | 18.6 (8) | 23.56 (94) | 0.71 (0.3-1.5) | 1:126 | |||||
| A1*0501 | 2.32 (1) | 17.88 (71) | 0.1 (0.01-0.7)* | 1:770 | |||||
| Negativos | 0 | 17.88 (71) | NA | Sin riesgo |
IC: intervalo de confianza; NA: no disponible; RM: razón de momios.
Para la DMT1 obtuvimos un gradiente de riesgo de 1:14-1:126. De igual forma, para la EC, el gradiente calculado tenía un rango de 1:6-1:126. Los 3 riesgos más altos para la DMT1 eran codificados por el HLA-DQ8 en combinación con DQ2 o uno de sus alelos, o DQ8 por sí solo. Los 2 riesgos más altos para la EC se relacionaban con HLA-DQ8, como HLA-DQ8/DQB1*0201 o DQ8 por sí solo, mientras que el tercero era HLA-DQ2. La RM e intervalos de confianza para estas combinaciones de alelos se muestran en la tabla 3.
De acuerdo con la información obtenida, el alelo con menor riesgo para esta población fue el DQA1*0501 (RM 0.1, p=0.02).
Con respecto al tamizaje serológico, 42/44 pacientes en el panel de casos de diabetes presentaron anticuerpos antigliadinas IgG positivos, y de estos, 8 resultaron positivos para antigliadina IgA y 3 con anticuerpos anti-tTG IgA, también. En el grupo de EC, 16/25 casos resultaron positivos para la antigliadina IgA y 15 tenían anti-tTG IgA en el momento del análisis, indicando una EC activa.
DiscusiónLa frecuencia de alelos distintivos de Sonora se debe seguramente a la mezcla de los grupos de población indígena que se mantuvieron aislados de Mesoamérica y a los primeros europeos que llegaron a la región del noroeste de México. Los primeros inmigrantes probablemente fueron personas que trabajaron en las minas de las montañas al este de lo que hoy en día es el estado de Sonora hace más de 300 años. Los migrantes eran principalmente españoles de Andalucía, Extremadura y de las regiones vascas32, y se mezclaron con los grupos indígenas locales como los Mayos, Yaquis, Seris, Pimas y la nación de Tohono O’odham33. Más aún, es probable que una mezcla adicional ocurriera durante la inmigración reciente de las personas del centro y sur de México, debido al desarrollo agrícola e industrial de la región. Así, el estado de Sonora ha generado una nueva población con una estructura genética compleja que tiene más ancestros europeos y menos amerindios en comparación con los demás mestizos mexicanos20.
El complejo mayor de histocompatibilidad, o HLA en los humanos, es una de las mayores regiones polimórficas del genoma humano34. Por lo tanto, la frecuencia de haplotipos representa una amplia variación en las distintas poblaciones del mundo. La frecuencia de DQ2 en las poblaciones caucásicas de Europa occidental se ha estimado en un 20-30%, mientras que la frecuencia de HLA-DQ8 es común en Sur- y Centroamérica; aproximadamente el 20% de los amerindios presentan el DQ835.
Sin embargo, hay una similitud mundial en la frecuencia de estos alelos en pacientes con DMT1 y EC. Por ejemplo, los resultados presentados para DMT1 son similares a aquellos en pacientes suecos con DMT1 (n=430)36, su frecuencia para los alelos DQA1*0501 (0.272) y DQB1*0201 (0.281) son estadísticamente iguales a aquellos de los mexicanos en este estudio. En cuanto a los alelos asociados a DQ8, los pacientes escandinavos con DMT136 presentan frecuencias significativamente más altas para los alelos DQA1*0301 (0.403) y DQB1*0302 (0.364) que los niños sonorenses con DMT1. Sin embargo, el DQA1*0301 fue el alelo más prevalente en nuestra muestra de DMT1 (0.340).
La distribución de alelos relacionados con los haplotipos HLA-DQ2 y DQ8 tiene relevancia clínica. Los 2 alelos DQB1*0201 y *0302 presentaron la mayor prevalencia en nuestra muestra de DMT1 y de EC, doblando la frecuencia de aquella en los recién nacidos sonorenses. Este hallazgo se correlaciona con el gradiente de riesgo para ambas enfermedades, en el cual las combinaciones de mayor riesgo incluyen las fracciones de DQB1, como ha sido previamente descrito para estas enfermedades en otras poblaciones37.
Por ejemplo, las personas de origen iraní tienen el genotipo DQB1*0201/x o DQB1*0302/x en el 98% de los casos de EC confirmados. Además, en estos casos de iranís, el alelo DQB1*0201 era más prevalente en pacientes con atrofia severa y daño de la mucosa intestinal, evaluadas por biopsias, equivalentes a un iiia-c en la clasificación de Marsh38. En el presente estudio, 4 de los casos de EC presentaron Marsh III en las biopsias de intestino39, y 3 de ellos resultaron positivos para el alelo de riesgo DQB1*0201.
Mientras tanto, en DMT1, la presencia de los alelos DQB1 se ha asociado con una edad más temprana en el diagnóstico en una población europea40 y la presencia de múltiples autoanticuerpos en hispanos de EE. UU.41. En nuestra muestra sonorense, la presencia de ambos alelos se asociada con el desarrollo de DMT1 antes de los 15 años de edad (p<0.05).
Aunque no hubo diferencias entre los grupos de DMT1 y EC en el análisis de frecuencia de los alelos, surgieron algunos cuando evaluamos el gradiente de riesgo. Esto se debe a que, aunque la proporción fue similar, la forma en que estos alelos se distribuyeron y combinaron variaba de una enfermedad a otra. Así, en esta población, la presencia del haplotipo DQ2 por sí solo representaba un riesgo moderado para la DMT1 (1:91), mientras que representaba un alto riesgo para EC (1:27).
Sin embargo, y contrario a lo que se esperaba, el HLA-DQ8 fue más prevalente que el DQ2 en los casos sonorenses de EC. Esto puede atribuirse a la distribución especial de los alelos de riesgo en la población de Sonora, en la cual el DQ8 tenía una prevalencia similar a la del DQ2. Como resultado, el DQ8 es más frecuente en Sonora que en las poblaciones europeas, y así la posibilidad de desarrollar la enfermedad aumenta, a pesar del hecho de que fisiológicamente el DQ8 tiene una afinidad más baja que el DQ2 para fijar los péptidos de gluten inmunogénicos12.
La combinación con más riesgo para la DMT1 fue de HLA-DQ2/DQ8, mientras que no pudimos establecer esta asociación para el grupo de EC, probablemente debido al tamaño de la muestra. Sin embargo, esta combinación también conlleva un muy alto riesgo para desarrollar EC42. Un hallazgo sorprendente fue que la presencia de esta rara combinación de haplotipos en la población general de Sonora aumentó la posibilidad de desarrollar DMT1 al 10%, sin importar los otros factores de riesgo. Además, de acuerdo con nuestros resultados, esa situación en especial fue más común en casos de DMT1 que en los de EC.
Con respecto a los pacientes con DMT1, la RM del genotipo DQ2/DQ8 (7.18) fue mayor que la suma de la RM de los haplotipos DQ2 y DQ8 (4.23). Esto apoya los efectos sinérgicos reportados entre estos haplotipos36.
Sin embargo, para tener una mejor estimación el riego real, sería necesario considerar las situaciones en las que la persona es heterocigota u homocigota por un haplotipo específico, así como para los alelos HLA-DQ2.2 que no fueron analizados. Las células presentadoras de antígenos de individuos que son homocigotos para los alelos de susceptibilidad del HLA presentan péptidos derivados de gliadina más eficientes que los heterocigotos, correlacionando con el riesgo para la enfermedad12. En niños del estudio The Environmental Determinants of Diabetes in the Young (TEDDY), un riesgo acumulativo para EC del 11% fue encontrado entre los niños homocigotos para el haplotipo DR3-DQ2. Esto representa un mayor riesgo que el riesgo estimado del 3% entre aquellos con el haplotipo DR3-DQ2/DR4-DQ843.
Nuestros resultados podrían tener aplicaciones interesantes para identificar y estimar el riesgo para estas enfermedades en grupos especiales de Sonora, tales como familiares de los pacientes, o en aquellos con enfermedades autoinmunes o asociados a factores de riesgo ambientales. En años recientes, el grupo de trabajo de la Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátrica (ESPGHAN por sus siglas en Inglés) ha recomendado realizar una tipificación de haplotipos de HLA para dar poder al diagnóstico de EC en niños sintomáticos. Se aconseja este enfoque por su alto valor predictivo negativo44 cuando las biopsias de intestino delgado no se pueden llevar a cabo, y los títulos de anticuerpos específicos son altos.
Mientras que en más del 90% de los casos el desarrollo de EC requiere de los haplotipos HLA-DQ2 o DQ8, algunos casos de DMT1 también presentaron otras variantes genéticas35. Por lo tanto, siguiendo las recomendaciones de la Asociación Americana de Diabetes, junto con la evaluación de los autoanticuerpos asociados con la EC, el análisis del haplotipos resultara útil como herramienta de evaluación en pacientes con DMT1, aun ante la ausencia de signos y síntomas tipicos1.
En este estudio evaluamos la detección de anticuerpos anti-tTG y antigliadinas en niños con diabetes, identificando así 3 posibles casos de EC en nuestro grupo de DMT1, representando el 7% de nuestra muestra de diabéticos. Estos resultados están por debajo del 10.7% reportado previamente en mestizos mexicanos con DMT145, quizás porque los pacientes con DMT1 que fueron evaluados fueron casos incidentales, y el riesgo de desarrollar EC continúa siendo alto a lo largo de la vida de los pacientes. Con el enfoque actual, encontramos que algunos de los casos de DMT1 tenían anticuerpos IgA antigliadinas. Esto probablemente se debió al hecho de que los niños pasaron por un proceso agudo en el cual la permeabilidad intestinal estaba comprometida, creando anticuerpos contra las gliadinas, y no necesariamente por EC. Por lo tanto, esta evaluación es una opción mínimamente invasiva, costo-efectiva para monitorizar periódicamente el riesgo de desarrollar EC en los niños con DMT1. Esto podría oportunamente detectar posibles casos de EC, evitando las complicaciones relacionadas con un diagnóstico tardío. En este contexto, y especialmente en pacientes asintomáticos, se recomienda una endoscopia y una biopsia para confirmar el diagnóstico de EC.
En resumen, la DMT1 y la EC son enfermedades que frecuentemente aparecen juntas. Debido a que la población sonorense cuenta con características genéticas especiales a causa de su ascendencia, la distribución de haplotipos en DMT1 y EC fue diferente a la reportada en Europa, con una proporción de 1.2:1 para HLA-DQ2: HLA-DQ8. La combinación de alelos que confiere el mayor riesgo para DMT1 en la población de Sonora fue HLA-DQ8/DQ2, seguida por DQ8 por sí solo o combinado con DQB1*0201, mientras que la combinación DQ8/DQb1*0201 presentó el mayor riesgo para EC.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciamientoSe recibió apoyo económico del Consejo Nacional de Ciencia y Tecnología (CONACYT), beca S0008-2009-01-115212.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.
AgradecimientosLos autores agradecen al Dr. N. Sotelo-Cruz, al Dr. J.B. Elizondo y al Dr. G. García sus diagnósticos y a L. López-Domínguez, S. Aguayo-Patrón y J.R. Valenzuela su asistencia técnica.