Se ha validado el uso de los anticuerpos anti-CdtB/anti-vinculina como biomarcadores para discriminar el SII-D de la EII, más no hay experiencia con ellos en Latinoamérica.
Materiales y métodosSe analizaron pacientes que consultaron a una clínica de TGIF/motilidad en los últimos 7 meses por diarrea con dolor/distensión abdominal, y a quienes se les solicitó estos anticuerpos. Los pacientes fueron diagnosticados mediante los criterios de Roma III o con trastornos orgánicos. Se clasificaron a los pacientes con SII en SII-post infeccioso (PI) o SII-no PI.
ResultadosTreinta pacientes fueron estudiados. Se encontraron biomarcadores positivos en sujetos con SII-D y SII-D con sobreposición (58.8%) y SII-M (33.3%), sin diferencias entre aquellos con SII-PI (71.4%) vs. SII-no PI (41.7%) (p=0.21). No hubo positividad en pacientes con otros TGIF o diarrea orgánica, excepto en uno con sobrecrecimiento bacteriano en el intestino delgado (SBID).
ConclusiónNuestros datos apoyan el uso de esta prueba como una herramienta de diagnóstico de primera línea para confirmar la presencia de SII-D/SII-M según los criterios de Roma III.
Circulating anti-CdtB/anti-vinculin antibodies have been validated as biomarkers to distinguish IBS-D from IBD, but there is no experience with them in Latin America.
Materials and methodsThe analysis was carried out on patients seen at a FGIDs/motility clinic over the last 7 months for diarrhea with abdominal pain and/or bloating who were tested for these antibodies. The patients were diagnosed according to the Rome III criteria or with organic disorders, and those presenting with IBS were further classified as post-infectious (PI) or non-PI-IBS.
ResultsThirty patients were studied. Positive biomarkers were found in IBS-D and IBS-D Overlap (58.8%) and IBS-M (33.3%), with no differences between PI-IBS (71.4%) vs. non-PI-IBS (41.7%) subjects (P=.21). There was no positivity in patients with other FGIDs or organic diarrhea, except for one with small intestinal bacterial overgrowth (SIBO).
ConclusionsOur findings support the use of this test as a first-line diagnostic tool to confirm the presence of IBS-D/IBS-M according to the Rome III criteria.
La Fundación Roma publicó recientemente el perfil clínico multidimensional (PCMD) para capturar la dimensionalidad completa de los pacientes con trastornos gastrointestinales funcionales (TGIF) y planear un tratamiento individualizado1. El PCMD consta de 5 categorías: 1. Diagnóstico categórico (criterios de Roma III); 2. Modificadores clínicos (p. ej., subtipo de hábito intestinal: síndrome del intestino irritable con diarrea [SII-D], con estreñimiento [SII-E], mixto [SII-M], post infeccioso [SII-PI], sensibilidad al gluten); 3. Impacto auto-percibido (es decir, leve, moderado y severo); 4. Influencias psicosociales (p. ej., categorías DSM-5, historial de abuso), y 5. Modificadores fisiológicos y biomarcadores (que podrían aumentar el entendimiento del diagnóstico o tener implicaciones de tratamiento)1.
Los anticuerpos circulantes a la toxina de distensión citoletal B (CdtB, por sus siglas en inglés) y vinculina han sido validados en los Estados Unidos como biomarcadores para discriminar el SII-D de la enfermedad intestinal inflamatoria (EII)2. La CdtB es producida por bacterias que causan gastroenteritis aguda incluyendo especies como Campylobacter, Salmonella typhi, Escherichia coli y Shigella dysenteriae3. Un modelo animal post-C. jejuni demostró que anticuerpos del huésped a la CdtB tienen reacciones cruzadas con la vinculina en el intestino, produciendo un fenotipo parecido al SII-PI4,5. Por lo tanto, se investigaron los anticuerpos anti-CdtB/anti-vinculina en pacientes con SII-D según los criterios de Roma III, y se compararon con pacientes con EII, enfermedad celíaca (EC) y controles saludables. Una densidad óptica (DO) ≥2.80 para el anticuerpo anti-CdtB y ≥1.68 para el anticuerpo anti-vinculina proveyeron una especificidad del 91.6 y 83.8%, respectivamente, para la discriminación del SII-D2. La prueba se consideró positiva si cualquiera de los 2 estuviera presente.
En Latinoamérica, no existe experiencia clínica con estos biomarcadores. Sin embargo, un modelo de minimización de costos mostró que utilizándolos como investigación diagnóstica de primera línea en pacientes con sospecha de SII-D, en México, reduce los costos en un 16.3%, con posibilidad de alcanzar un ahorro del 25%6. Además, el Consenso Mexicano publicado recientemente sobre el SII reconoció que los anticuerpos anti-CdtB/anti-vinculina están bien estudiados y validados, aunque no aportaron recomendaciones en cuanto a sus usos como herramientas de diagnóstico7. Por eso, buscamos describir en este artículo la experiencia clínica en el uso de estos biomarcadores en pacientes atendidos en una clínica de TGIF/motilidad privada en la Ciudad de México.
Materiales y métodosSe revisaron retrospectivamente las historias clínicas de pacientes con diarrea crónica que se sometieron a pruebas para los anticuerpos anti-CdtB/anti-vinculina como parte de su abordaje diagnóstico entre el 1/09/2015 (cuando llegaron a estar disponibles los biomarcadores) y el 31/03/2016. Los pacientes fueron atendidos por un solo gastroenterólogo (MS) y se les diagnosticó SII-D, SII-M, diarrea funcional o trastorno funcional intestinal no especificado (TFI-NE), si cumplían los criterios de Roma III respectivos, y fueron clasificados como SII-PI si contaban con historia previa de gastroenteritis infecciosa como factor desencadenante. Los pacientes que no contaban con ninguno de los trastornos anteriormente mencionados, recibieron diagnósticos orgánicos de acuerdo a su presentación clínica y otras pruebas (p. ej., serología EC, endoscopía alta, colonoscopia, biopsias colónicas y/o duodenales, tránsito del intestino delgado, etc.). Describimos la prevalencia de anticuerpos anti-CdtB/anti-vinculina positivos y valores de DO, de acuerdo a los diagnósticos, especialmente en sujetos con SII, y entre aquellos con SII-PI y SII-no PI. Las variables categóricas se reportaron en porcentajes, y fueron comparadas utilizando la prueba χ2. Las variables continuas se expresaron en mediana y rango, y la media±DE cuando era apropiado y se compararon utilizando la prueba t de Student. Se consideró un valor de p<0.05 estadísticamente significativo.
ResultadosSe estudió a un total de 30 pacientes. La edad promedio era 49.1±17.5 años y el 63.3% eran mujeres. La mayoría de los diagnósticos iniciales fueron SII-D (N.°): 14; diarrea funcional: 5; SII-M: 3; TFI-NE: 2; diarrea crónica no funcional: 2; colitis microscópica (CM): 2; esprue tropical (ET): 1 y EC: 1. Aquellos pacientes con ET, EC y uno con CM, respondieron previamente a los tratamientos específicos para dichas enfermedades y posteriormente desarrollaron diarrea recurrente con dolor/distensión abdominal consistente con SII-D (referido en este artículo como SII-D con sobreposición). En total, 20 de los pacientes fueron diagnosticados con SII (tabla 1).
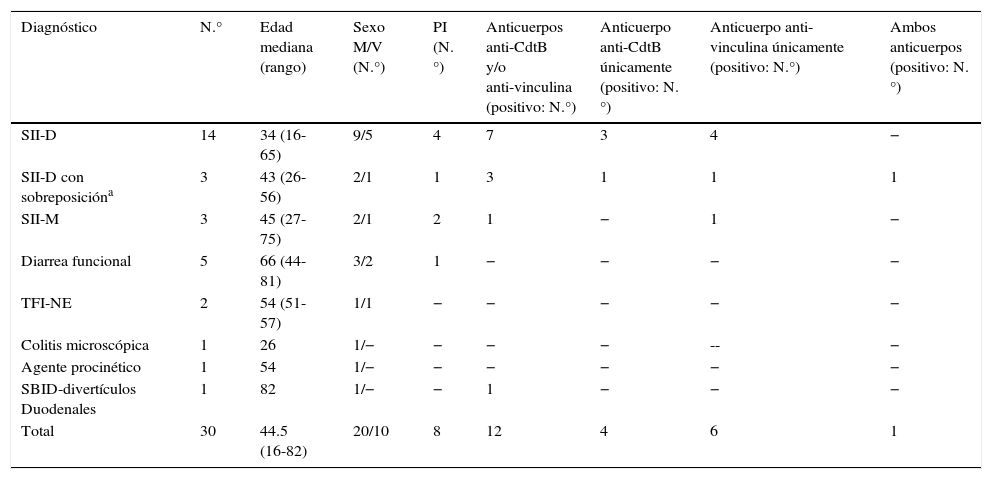
Anticuerpos anti-CdtB y/o anti-vinculina positivos en pacientes con SII relacionado con diarrea y otros
| Diagnóstico | N.° | Edad mediana (rango) | Sexo M/V (N.°) | PI (N.°) | Anticuerpos anti-CdtB y/o anti-vinculina (positivo: N.°) | Anticuerpo anti-CdtB únicamente (positivo: N.°) | Anticuerpo anti-vinculina únicamente (positivo: N.°) | Ambos anticuerpos (positivo: N.°) |
|---|---|---|---|---|---|---|---|---|
| SII-D | 14 | 34 (16-65) | 9/5 | 4 | 7 | 3 | 4 | − |
| SII-D con sobreposicióna | 3 | 43 (26-56) | 2/1 | 1 | 3 | 1 | 1 | 1 |
| SII-M | 3 | 45 (27-75) | 2/1 | 2 | 1 | − | 1 | − |
| Diarrea funcional | 5 | 66 (44-81) | 3/2 | 1 | − | − | − | − |
| TFI-NE | 2 | 54 (51-57) | 1/1 | − | − | − | − | − |
| Colitis microscópica | 1 | 26 | 1/− | − | − | − | -- | − |
| Agente procinético | 1 | 54 | 1/− | − | − | − | − | − |
| SBID-divertículos Duodenales | 1 | 82 | 1/− | − | 1 | − | − | − |
| Total | 30 | 44.5 (16-82) | 20/10 | 8 | 12 | 4 | 6 | 1 |
M: mujeres; PI: postinfeccioso; SBID: sobrecrecimiento bacteriano en el intestino delgado; SII: síndrome del intestino irritable; SII-D: síndrome del intestino irritable con diarrea; SII-M: síndrome del intestino irritable mixto; TFI-NE: trastorno funcional intestinal no especificado; V: varones.
Hubo biomarcadores positivos en el 47.1% de los pacientes con SII-D, en todos los pacientes con SII-D con sobreposición y en el 33.3% de aquellos con SII-M (tabla 1). No hubo resultados positivos en pacientes con diarrea funcional, TFI-NE, CM o en un paciente con diarrea, que más tarde resultó ser un efecto secundario a la prucaloprida. Una excepción fue una mujer de 82 años de edad con divertículos en el segundo y tercer segmento del duodeno, que salió positiva para el anticuerpo anti-CdtB. Se le diagnosticó con sobrecrecimiento bacteriano en el intestino delgado (SBID) secundario.
El 35% de los pacientes con SII presentaban SII-PI. Sin embargo, se encontraron biomarcadores positivos en los sujetos con SII-PI: 5/7 (71.4%), así como en los SII-no PI: 5/12 (41.7%); p=0.21. Además, no hubo diferencias en los valores de DO entre los pacientes con SII-PI, y aquellos con SII-no PI para los anticuerpos anti-CdtB (3.019±0.189 vs. 2.98.6±0.232; p=0.69) y anti-vinculina (2.224±0.616 vs. 2.151±0.503; p=0.14).
ConclusionesEn esta experiencia clínica, en México, con la prueba de anticuerpos anti-CdtB/anti-vinculina realizada en un pequeño número de pacientes, únicamente los sujetos con diagnóstico de SII relacionado con diarrea según los criterios de Roma III tuvieron un resultado positivo. En contraste, ningún paciente con algún otro TGIF relacionado con diarrea o que presentó diarrea orgánica sin SII-D con sobreposición resultó positivo. Ocho pacientes (47.1%) con SII «puro» presentaron anticuerpos anti-CdtB/anti-vinculina. Sin embargo, si añadimos la positividad entre aquellos con SII-D con sobreposición, el 55% de todos los pacientes con un diagnóstico de SII relacionado con diarrea resultaron positivos. Estos resultados son similares al 58.6% encontrado por Pimentel et al. en su estudio de validación2.
Solo hubo un paciente con diarrea orgánica, presuntamente con SBID secundario a divertículos duodenales, que resultó positivo para el anticuerpo anti-CdtB. Esto puede explicarse por el mecanismo patofisiológico hipotético subyacente en la presencia de estos anticuerpos. En un modelo de ratas de SII-PI4, se observó una reducción significativa de las células intersticiales de Cajal (CIC) y se desarrolló SBID8. También hubo una reacción cruzada de anticuerpos anti-CdtB con vinculina5, una proteína citosólica presente en las CIC y en los ganglios mientéricos9. La vinculina también está relacionada con la actina que une las cadherinas, las cuales son necesarias para la contracción de los músculos lisos del intestino9. Es probable que la pérdida de la vinculina, las CIC y los ganglios mientéricos haya disminuido la motilidad del intestino delgado, dando lugar al desarrollo de sobrecrecimiento bacteriano5,8. Esto podría explicar el anticuerpo anti-CdtB positivo en nuestro paciente.
No solo encontramos los anticuerpos positivos para anti-CdtB o anti-vinculina en el subgrupo del SII-PI, sino también en los pacientes con SII-no PI. Esto sugiere la posible relación de otros mecanismos no asociados con una previa infección entérica. Si los anticuerpos anti-CdtB reaccionan en forma cruzada con la vinculina, necesita explicarse la presencia de los anticuerpos de anti-vinculina. Puede especularse que el anticuerpo anti-CdtB altera las propiedades de la vinculina y, por lo tanto, se producen los anticuerpos de anti-vinculina. Si fuese el caso, cada paciente debe de tener ambos anticuerpos, y se presentarían en cada paciente, lo cual no sucedió en el estudio de validación ni en nuestra serie. Así, un mecanismo autoinmune podría explicar la generación de los anticuerpos anti-vinculina. De hecho, un estudio previo encontró que los anticuerpos neuronales anti-entéricos eran más frecuentes en pacientes con SII que en controles, resultando en la propuesta de una neuropatía degenerativa autoinmune10.
Los resultados presentados tienen implicaciones en la práctica clínica. La inclusión de este panel sanguíneo en el proceso de diagnóstico de pacientes con SII, según los criterios de Roma III, tiene el potencial de ahorrar costos en forma significativa, ya que evitaría la realización de pruebas innecesarias para descartar causas orgánicas de diarrea crónica6. Además, un resultado objetivo seguramente sería reconfortante para los pacientes. Sin embargo, nuestro estudio tiene algunas limitaciones. En primer lugar, es una serie retrospectiva pequeña y no todos los pacientes fueron sometidos a las mismas pruebas de diagnóstico y procedimientos para descartar otras posibles comorbilidades. En segundo lugar, solo tuvimos 2 casos de CM, y se desconoce el comportamiento del anticuerpo anti-CdtB/anti-vinculina en una enfermedad que se caracteriza por un tipo de inflamación de bajo grado, que pueda desencadenar autoinmunidad. Sin embargo, nuestro paciente con SII-D sobrepuesto con CM resultó positivo para ambos anticuerpos, mientras que el paciente con CM, únicamente, no presentó los anticuerpos. Tercero, no se estudió a ningún paciente con EII, ya que no es ético realizar esta prueba en pacientes diagnosticados previamente mediante el uso de otros biomarcadores validados, como fue el caso de nuestros pacientes con EII.
En conclusión, más de la mitad de este reducido grupo de pacientes con SII relacionado con diarrea según los criterios de Roma III ofreció resultado positivo para el anticuerpo anti-CdtB y/o anti-vinculina, independientemente del SII-PI. Estos hallazgos apoyan el uso de esta prueba como una herramienta de diagnóstico de primera línea para confirmar el diagnóstico del SII-D/SII-M, según los criterios de Roma III en los pacientes que ofrezcan resultado positivo. Se requiere de estudios futuros para determinar si los niveles de anticuerpos pueden utilizarse para monitorear y predecir la respuesta al tratamiento y/o la recurrencia del SII.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónLos autores declaran que no se recibió patrocinio de ningún tipo para llevar a cabo este estudio.
Conflicto de interesesMax Schmulson ha recibido apoyos de Alfa Wassermann y Nestle Ltd. Ha ejercido en la Junta Consultora de Alfa Wassermann y ha sido consultante para Almirall, Commonwealth Laboratories Inc, Commonwealth Diagnostics International Inc, Janssen, Nestle Ltd, Novartis, Procter and Gamble, Senosiain y Takeda Mexico. También ha sido orador para Alfa Wassermann, Janssen, Mayoli-Spindler, y Takeda Mexico.