La infección por Clostridium difficile (CD) es la causa principal de diarrea en hospitalizados. Los hallazgos clínicos y endoscópicos han sido poco estudiados en nuestro país. El objetivo de este estudio es describir estos hallazgos.
Material y métodosEstudio de cohorte prospectivo, se incluyeron pacientes con diarrea hospitalaria asociada a CD, diagnosticada mediante PCR y determinación de cepa hipervirulenta NAP027. Se analizaron los hallazgos clínicos y endoscópicos, así como las variables asociadas a severidad.
ResultadosDe 127 pacientes con diarrea hospitalaria, se excluyeron 97 por falta de colonoscopia. De los 39 pacientes incluidos, con edad promedio de 48 años, los signos/síntomas más comunes fueron dolor abdominal (49%), moco en heces (41%) y sangre en heces (10%); las alteraciones de laboratorio más comunes fueron leucocitosis en el 49%, leucocitos en heces (61%) e hipoalbuminemia (67%). El factor de riesgo principal fue el uso de antibiótico en un 62%, más comúnmente la ceftriaxona. La cepa hipervirulenta se presentó en el 54%. Se encontraron anormalidades endoscópicas en el 87%, con colitis seudomembranosa en un 38%, presentándose en colon izquierdo (53%) y en derecho (13%). No se encontró asociación entre uso de IBP y diarrea por CD. Se identificó una asociación significativa entre la hipoalbuminemia (<3.3g/dL) y un mayor riesgo de colitis severa, con un RR de 8.2 (p=0.008).
ConclusionesLas lesiones de colitis seudomembranosa asociada a CD de cepa hipervirulenta predominan en colon izquierdo. La hipoalbuminemia es un predictor significativo de severidad.
Clostridium difficile infection is the main cause of hospital-acquired diarrhea, and the clinical and endoscopic findings in those patients have been studied very little in Mexico. The aim of the present study was to describe those findings.
Materials and methodsA prospective cohort study was conducted that included patients with hospital-acquired diarrhea associated with Clostridium difficile diagnosed through polymerase chain reaction. The hypervirulent NAP027 strain was also determined. The clinical and endoscopic findings in the study patients, as well as the variables associated with severity, were analyzed.
ResultsOf the 127 patients with hospital-acquired diarrhea, 97 were excluded from the study due to lack of colonoscopy. The remaining 39 study patients had a mean age of 48 years, and their most common signs/symptoms were abdominal pain (49%), mucus in stools (41%), and blood in stools (10%). The most common alterations in the laboratory results were leukocytosis in 49%, fecal leukocytes (61%), and hypoalbuminemia (67%). The main risk factor was antibiotic use in 62%, and ceftriaxone was the most widely used. The hypervirulent strain was present in 54% of the cases. Endoscopic abnormalities were found in 87% of the patients. Thirty-eight percent presented with pseudomembranous colitis, with lesions in the left colon in 53%, and in the right colon in 13%. No association was found between proton-pump inhibitor use and Clostridium difficile-associated diarrhea. There was a significant association between hypoalbuminemia (< 3.3g/dL) and a greater risk for severe colitis, with a RR of 8.2 (p=0.008).
ConclusionsPseudomembranous colitis lesions associated with the hypervirulent Clostridium difficile strain were predominant in the left colon. Hypoalbuminemia was a significant severity predictor.
La infección por Clostridium difficile (CD) es la principal causa de diarrea en pacientes hospitalizados en el mundo desarrollado y la principal causa de diarrea por uso de antibióticos (10-35% de todos los casos). Durante la última década ha alcanzado niveles de epidemia1,2.
CD es una bacteria grampositiva que crece en condiciones anaerobias estrictas. Las cepas de interés clínico son las productoras de toxina A (TcdA) y toxina B (TcdB); además de estas, algunas cepas producen una toxina binaria3–5.
Desde el 2002 apareció un brote de una cepa hipervirulenta, hiperproductora de toxinas, capaz de producir de 16 a 20 veces más toxinas que el resto de las cepas, así como resistencia a las fluoroquinolonas, la cepa NAP1/BI/027. En el 2008 se reportó una extensión global de esta cepa1,6.
La infección por CD se considera de origen comunitario cuando los síntomas se inician en la comunidad o en las primeras 48h posterior al ingreso hospitalario. El factor de riesgo principal por excelencia para infección por CD es el uso previo de antibióticos; sin embargo, hasta en el 65% de los casos comunitarios no existe ese antecedente7,8.
El diagnóstico de la diarrea por CD se basa en estudio de las heces diarreicas, por detección de sus toxinas A y B mediante inmunoanálisis enzimáticos, con una sensibilidad del 63-94% y una especificidad del 75-100%; o mediante métodos de amplificación de ácidos nucleicos (PCR) con una sensibilidad del 86-93% y una especificidad del 98%. El Colegio Americano de Gastroenterología recomienda esta última como la prueba de diagnóstico estándar1,9,10. No se recomienda realizar endoscopia ante la sospecha de infección, por su baja sensibilidad al inicio de la enfermedad. La lesión característica por infección por CD es la colitis seudomembranosa, presente en el 40-60% de los casos11, sin embargo puede existir infección por CD con aspecto endoscópico normal, o en casos leves, observarse mínimo eritema, edema o erosiones inespecíficas. La presentación de seudomembranas también se ha descrito en infecciones por otras bacterias, virus o incluso amebiasis12–18.
El objetivo de este estudio es describir las características clínicas y endoscópicas de pacientes con diarrea asociada a CD con la cepa hipervirulenta NAP027, así como los factores de riesgo asociados, en un hospital de tercer nivel.
Material y métodosCohorte prospectiva que incluyó a pacientes con diagnóstico de diarrea hospitalaria asociada a infección por CD ingresados al Hospital Civil Fray Antonio Alcalde, de marzo del 2015 a diciembre del 2015.
La división de infecciones nosocomiales, del servicio de Infectología del Hospital Civil Fray Antonio Alcalde, captó a los pacientes con diarrea hospitalaria, se realizó prueba de PCR para CD en heces diarreicas (Bristol 6-7); a aquellos que se reportaron positivos y cumplieron los factores de inclusión se les realizó estudio endoscópico con colonoscopio Olympus Exera 150, todos los procedimientos fueron hechos con sedación intravenosa, administrada por médico anestesiólogo. Los pacientes se prepararon para el estudio con polietilenglicol con electrólitos.
La prueba de PCR que se utilizó fue la prueba «Xpert C. Difficile/Epi», para la detección rápida in vitro de secuencias del gen regulador de la toxina B y la identificación presuntiva de cepa hipervirulenta 027/NAP1/BI, mediante la detección de secuencias del gen regulador de la toxina binaria (CDT) y la eliminación de un solo par de bases en el nucleótido 117 del gen tcd.
Se incluyeron pacientes mayores de 18 años con diagnóstico de diarrea hospitalaria por CD hospitalizados en el Hospital Civil Fray Antonio Alcalde. Se excluyeron: pacientes embarazadas, menores de 18 años de edad, y quienes no aceptaran firmar el consentimiento informado para la realización del estudio endoscópico. Se eliminaron pacientes con megacolon tóxico, íleo prolongado o sospecha de perforación colónica, inestabilidad hemodinámica y/o respiratoria, pacientes que decidieron abandonar el estudio, y los que fueron egresados por el servicio tratante antes de poder realizar la colonoscopia. Las variables a registrar fueron edad, género, antecedente de consumo de inhibidores de bomba de protones (IBP), de cirugía abdominal, comorbilidades como diabetes y enfermedad renal crónica; estancia intrahospitalaria, signos y sintomatología, características de las heces (moco, sangre, etc.), resultados de laboratorio como leucocitosis, leucocitos en heces, identificación de la cepa hipervirulenta NAP027, albúmina sérica, procalcitonina y reactantes de fase aguda.
Análisis estadísticoSe realizó estadística descriptiva de la población estudiada, reportando las variables categóricas como número total y porcentaje y las numéricas como mediana y rango intercuartílico (RIQ), en base a la distribución anormal identificada por la prueba de Shapiro-Wilk. La asociación de variables categóricas se realizó mediante la prueba de X2 de Pearson o exacta de Fisher como correspondiera, reportándose la medida de asociación con riesgo relativo (RR). Para identificar diferencias entre variables continuas distribuidas entre 2 grupos se utilizó la prueba U de Mann-Whitney. Se construyó una curva ROC de los niveles séricos de albúmina para predicción de severidad, determinando la significación de su área bajo la curva, con la prueba de Hanley-McNeil y se calculó el punto de corte óptimo que equilibró la mayor sensibilidad y especificidad, mediante el índice de Youden. Se realizó análisis de regresión lineal con la prueba de correlación de Spearman, para corroborar relación entre las variables continuas. Para todas las pruebas el valor de p calculado fue a 2 colas y se consideró un valor menor a 0.05 como estadísticamente significativo. El análisis estadístico y las gráficas se elaboraron con el paquete estadístico SPSS, versión 20. El comité de ética institucional aprobó el estudio y se obtuvo consentimiento informado para el mismo, acatando los lineamientos de investigación en humanos de la declaración de Helsinki.
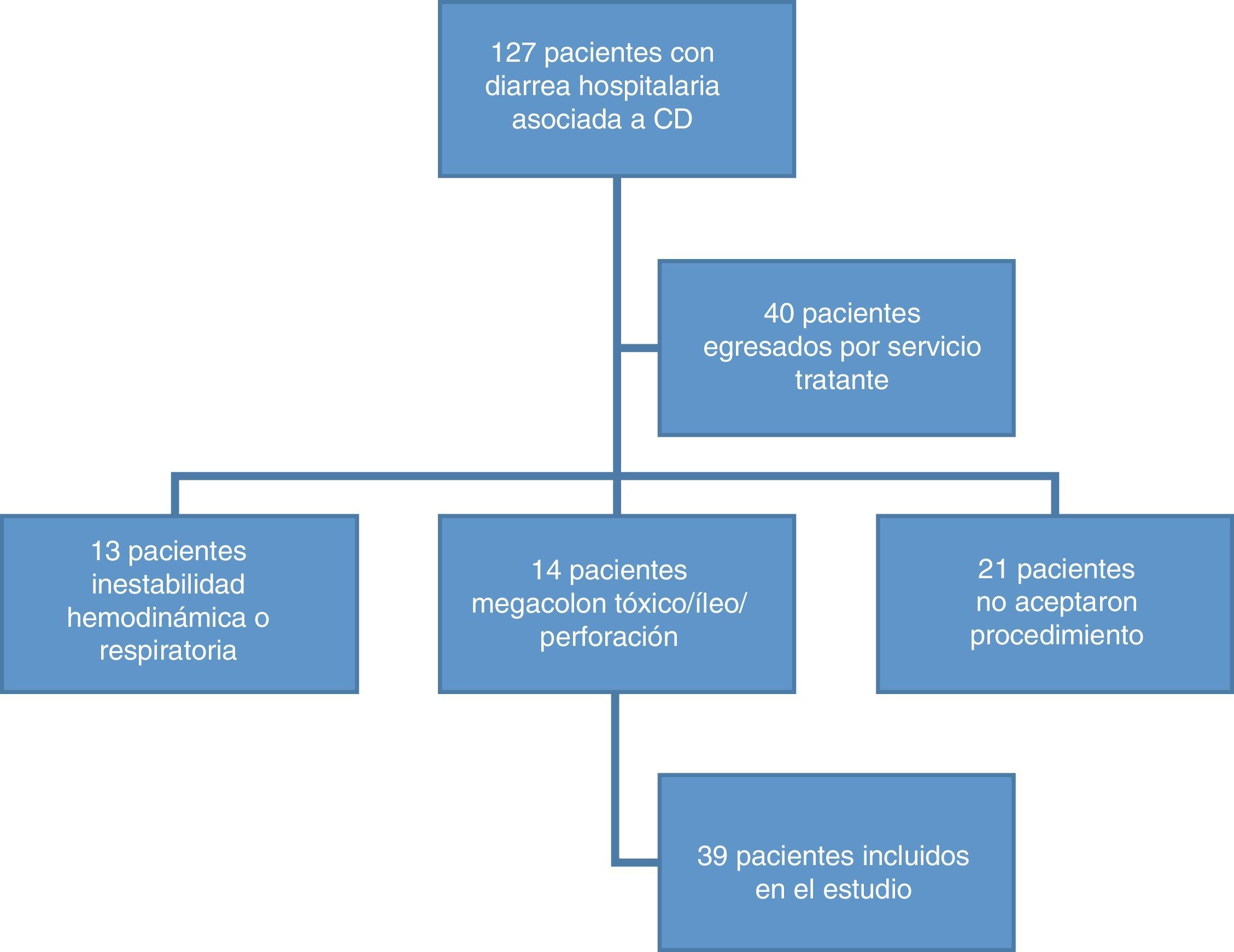
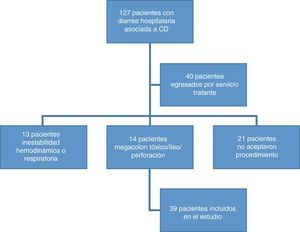
ResultadosHallazgos demográficosSe recolectaron 127 pacientes con diarrea hospitalaria asociada a CD, se excluyeron a 97, ya que el 16% no aceptaron el procedimiento, el 11% presentó megacolon tóxico o íleo metabólico o perforación intestinal, el 10% presentó inestabilidad hemodinámica o respiratoria y el 31% fue egresado por médicos de sus servicios tratantes sin proponerles el estudio endoscópico (fig. 1). Quedaron un total de 39 pacientes que cumplieron nuestros criterios de inclusión. La edad promedio fue de 48.9 años (DE±17), el 67% fueron hombres. El 20.5% eran mayores de 64 años.
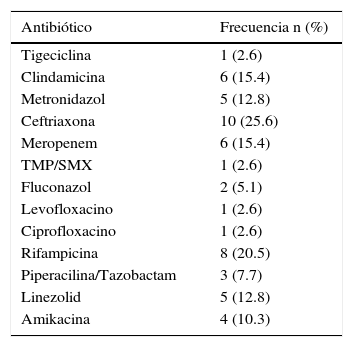
Factores de riesgo y comorbilidadesComo antecedentes de importancia, un 36% tuvieron cirugía previa, cirugía abdominal un 7%, enfermedad renal crónica un 31%, diabetes mellitus un 43%, hipertensión arterial un 33%, neumonía un 5%, pancreatitis un solo paciente, hepatopatía crónica 2 pacientes, 2 pacientes con CUCI, leucemia un paciente, linfoma 2 pacientes y un caso de tumor sólido. Tres pacientes estaban en estado de inmunosupresión, de los cuales 2 estaban recibiendo quimioterapia. La utilización previa de antibiótico se reportó en un 62%, siendo la ceftriaxona el más común con un 26%, seguido por la rifampicina y clindamicina-meropenem (tabla 1). El consumo de IBP fue reportado en el 80% de los pacientes.
Frecuencia de antibióticos utilizados
| Antibiótico | Frecuencia n (%) |
|---|---|
| Tigeciclina | 1 (2.6) |
| Clindamicina | 6 (15.4) |
| Metronidazol | 5 (12.8) |
| Ceftriaxona | 10 (25.6) |
| Meropenem | 6 (15.4) |
| TMP/SMX | 1 (2.6) |
| Fluconazol | 2 (5.1) |
| Levofloxacino | 1 (2.6) |
| Ciprofloxacino | 1 (2.6) |
| Rifampicina | 8 (20.5) |
| Piperacilina/Tazobactam | 3 (7.7) |
| Linezolid | 5 (12.8) |
| Amikacina | 4 (10.3) |
El 49% presentó dolor abdominal, el 41% moco en las heces, el 10% sangre en las heces, la cepa hipervirulenta NAP027 se presentó en el 54%, el 49% tuvo leucocitosis y el 61% leucocitos en heces. El 67% presentó hipoalbuminemia, con una albúmina promedio de 2.3g/dL (DE±0.85). La procalcitonina se reportó con una mediana de 1.2ng/mL (RIQ: 0.47-3), la velocidad de sedimentación globular (VSG) con una media de 52mm/h (DE±45) y proteína C reactiva de 51mg/L (RIQ: 2-9), sin embargo cabe señalar que la VSG y la proteína C reactiva solo se obtuvieron en el 38% de los pacientes.
Se reportó una mediana de estancia intrahospitalaria de 4 días (RIQ: 2-9), con una estancia intrahospitalaria prolongada del 36%. Solo se presentó una muerte de la población estudiada.
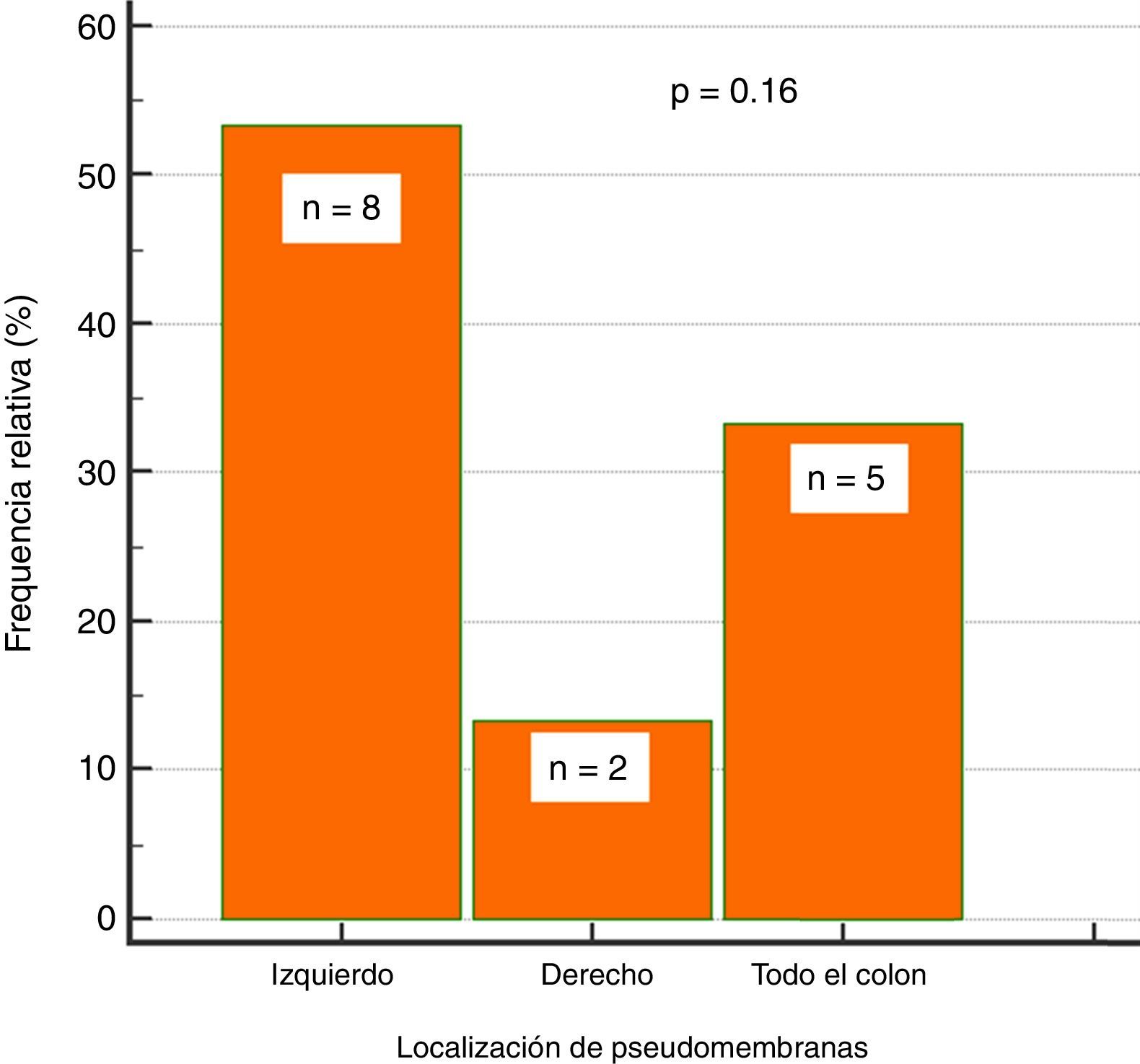
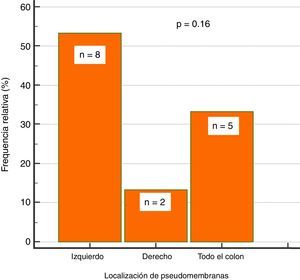
Hallazgos endoscópicosEn cuanto a la colonoscopia, se realizó en tiempo con una mediana de 7 días (RIQ: 5-11.5). Se encontró colonoscopia anormal (colitis) en el 87% de los pacientes, y de estos el 38% presentó colitis seudomembranosa, de los cuales un 53% (n=8) presentó las seudomembranas en el colon izquierdo, el 33% (n=5) afectación de todo el colon y el 13% (n=2) afectación solo en colon derecho, tal tendencia de afectación no alcanzó significación estadística (p=0.16) (fig. 2).
Asimismo, la presencia de seudomembranas no presentó ninguna asociación significativa con la severidad de la enfermedad, y no se encontró ningún otro factor de riesgo independiente para la presencia de estas (tabla 2).
Asociación entre colitis seudomembranosa y factores de riesgo
| Con seudomembranas (n=15) | Sin seudomembranas (n=24) | RR | p | |
|---|---|---|---|---|
| IRC, n (%) | 3 (20) | 9 (37) | 0.74 | 0.21 |
| Leucocitos en heces, n (%) | 9 (60) | 15 (62) | 0.96 | 0.87 |
| Qx previa, n (%) | 7 (47) | 7 (29) | 1.36 | 0.30 |
| Diabetes, n (%) | 6 (40) | 11 (49) | 0.91 | 0.71 |
| Hipertensión, n (%) | 4 (27) | 9 (37) | 0.83 | 0.46 |
| Qx abdominal, n (%) | 2 (13) | 7 (29) | 0.72 | 0.18 |
| Uso de antibióticos, n (%) | 11 (73) | 13 (54) | 1.35 | 0.21 |
| >1 antibiótico, n (%) | 4 (36) | 3 (23) | 1.37 | 0.51 |
| Edad, mediana (RIQ) | 45 (25-56) | 55 (46-61) | — | 0.11 |
| Albúmina, mediana (RIQ) | 2.3 (1.6-2.9) | 2.3 (1.9-2.8) | — | 0.85 |
En esta serie de pacientes no se encontró ninguna asociación significativa entre el uso de IBP y la presencia de diarrea asociada a CD. Tampoco se asoció su uso a la presencia de colitis seudomembranosa en la endoscopia (p=0.94). La única variable significativa encontrada con el uso de estos medicamentos fue el número de evacuaciones por día, siendo de 6/día vs. 4/día en pacientes con y sin uso de IBP respectivamente (p=0.04).
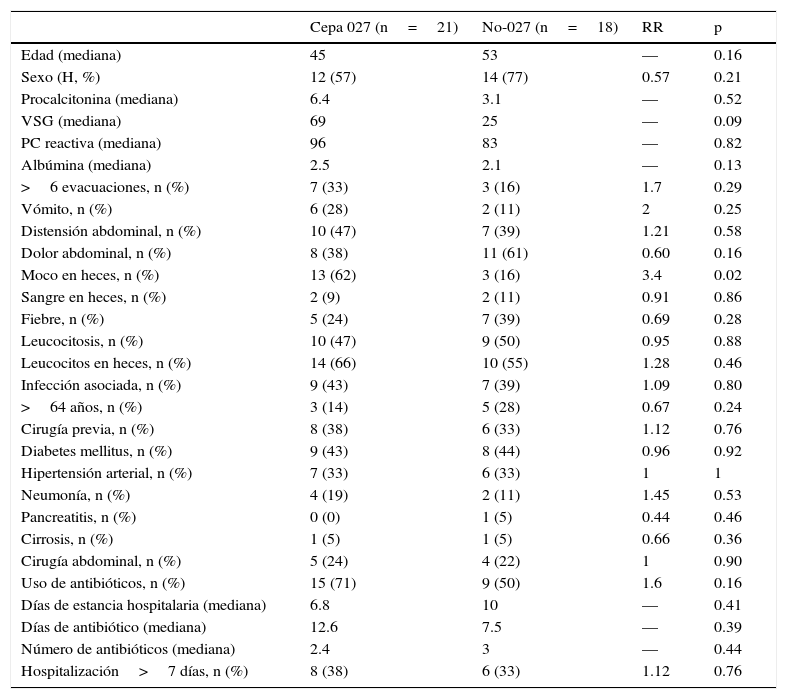
Con relación a la cepa hipervirulenta NAP027 (tabla 3), se demostró que la única variable con asociación significativa con tal cepa fue la presencia de moco, con un RR de 3.4 (62 vs. 16% p=0.02). La presencia de leucocitos en heces mostró una tendencia de aumento a relacionarse con NAP027, aunque no significativa (66 vs. 55%) (RR: 1.28, p=0.46). Aunque la procalcitonina se encontró al doble en los pacientes con la cepa NAP027, se presentó anormal en ambos grupos, y la diferencia no fue significativa (6.4ng/mL vs. 3.1ng/mL, p=0.52). Respecto a los antibióticos, solo se observó cierta tendencia de mayor riesgo con la rifampicina (28 vs. 11%) aunque no significativa (p=0.25). La colonoscopia se reportó anormal en la mayoría de ambos grupos, y la colitis seudomembranosa tuvo cierta tendencia a presentarse más frecuentemente con la cepa hipervirulenta (47 vs. 28%) pero sin significación estadística (RR: 1.62, p=0.23). La severidad fue similar en ambos grupos, así como el tiempo de realización de colonoscopia (mediana de 7 días).
Análisis bivariado entre cepa hipervirulenta NAP027 y cepas no-027
| Cepa 027 (n=21) | No-027 (n=18) | RR | p | |
|---|---|---|---|---|
| Edad (mediana) | 45 | 53 | — | 0.16 |
| Sexo (H, %) | 12 (57) | 14 (77) | 0.57 | 0.21 |
| Procalcitonina (mediana) | 6.4 | 3.1 | — | 0.52 |
| VSG (mediana) | 69 | 25 | — | 0.09 |
| PC reactiva (mediana) | 96 | 83 | — | 0.82 |
| Albúmina (mediana) | 2.5 | 2.1 | — | 0.13 |
| >6 evacuaciones, n (%) | 7 (33) | 3 (16) | 1.7 | 0.29 |
| Vómito, n (%) | 6 (28) | 2 (11) | 2 | 0.25 |
| Distensión abdominal, n (%) | 10 (47) | 7 (39) | 1.21 | 0.58 |
| Dolor abdominal, n (%) | 8 (38) | 11 (61) | 0.60 | 0.16 |
| Moco en heces, n (%) | 13 (62) | 3 (16) | 3.4 | 0.02 |
| Sangre en heces, n (%) | 2 (9) | 2 (11) | 0.91 | 0.86 |
| Fiebre, n (%) | 5 (24) | 7 (39) | 0.69 | 0.28 |
| Leucocitosis, n (%) | 10 (47) | 9 (50) | 0.95 | 0.88 |
| Leucocitos en heces, n (%) | 14 (66) | 10 (55) | 1.28 | 0.46 |
| Infección asociada, n (%) | 9 (43) | 7 (39) | 1.09 | 0.80 |
| >64 años, n (%) | 3 (14) | 5 (28) | 0.67 | 0.24 |
| Cirugía previa, n (%) | 8 (38) | 6 (33) | 1.12 | 0.76 |
| Diabetes mellitus, n (%) | 9 (43) | 8 (44) | 0.96 | 0.92 |
| Hipertensión arterial, n (%) | 7 (33) | 6 (33) | 1 | 1 |
| Neumonía, n (%) | 4 (19) | 2 (11) | 1.45 | 0.53 |
| Pancreatitis, n (%) | 0 (0) | 1 (5) | 0.44 | 0.46 |
| Cirrosis, n (%) | 1 (5) | 1 (5) | 0.66 | 0.36 |
| Cirugía abdominal, n (%) | 5 (24) | 4 (22) | 1 | 0.90 |
| Uso de antibióticos, n (%) | 15 (71) | 9 (50) | 1.6 | 0.16 |
| Días de estancia hospitalaria (mediana) | 6.8 | 10 | — | 0.41 |
| Días de antibiótico (mediana) | 12.6 | 7.5 | — | 0.39 |
| Número de antibióticos (mediana) | 2.4 | 3 | — | 0.44 |
| Hospitalización>7 días, n (%) | 8 (38) | 6 (33) | 1.12 | 0.76 |
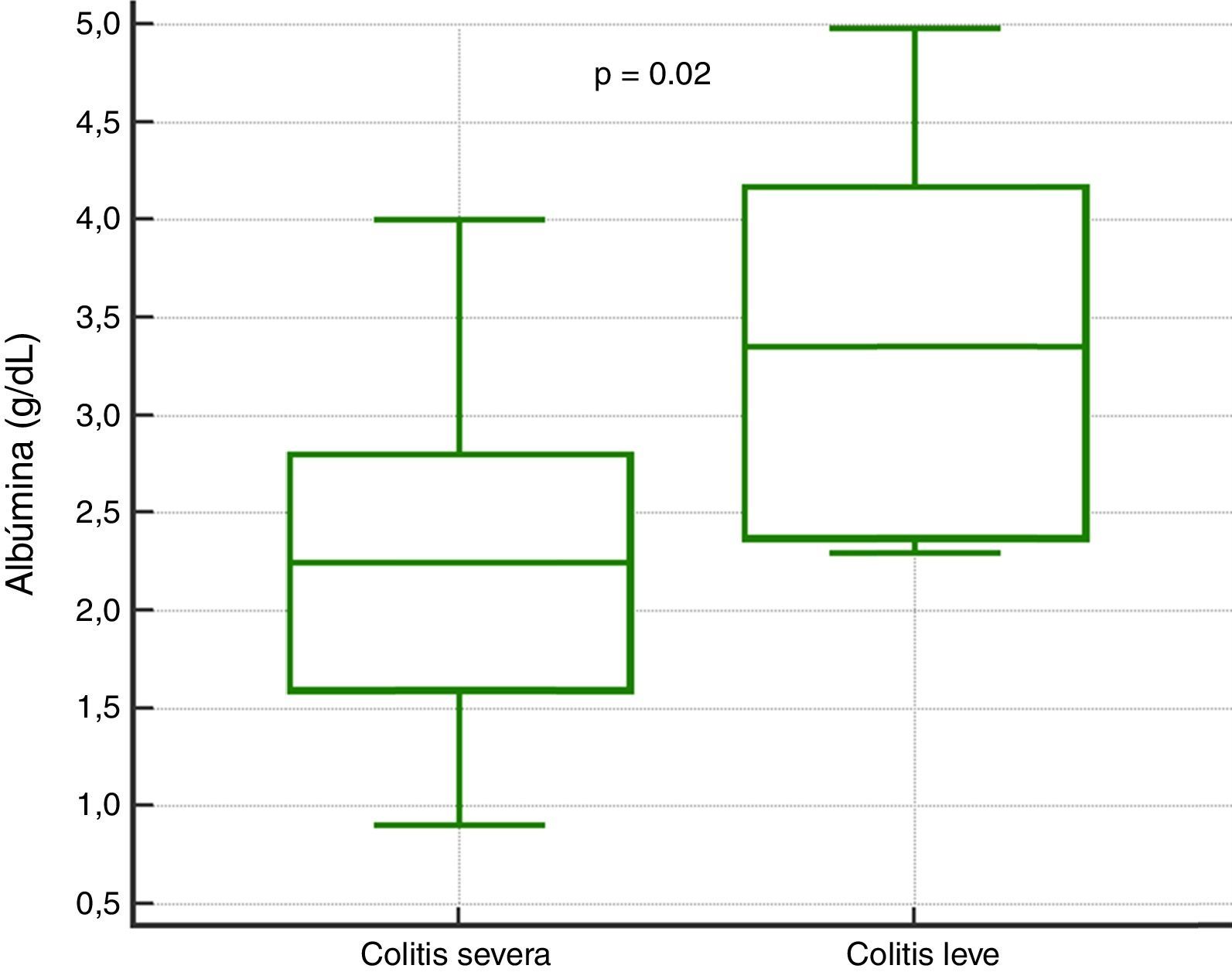
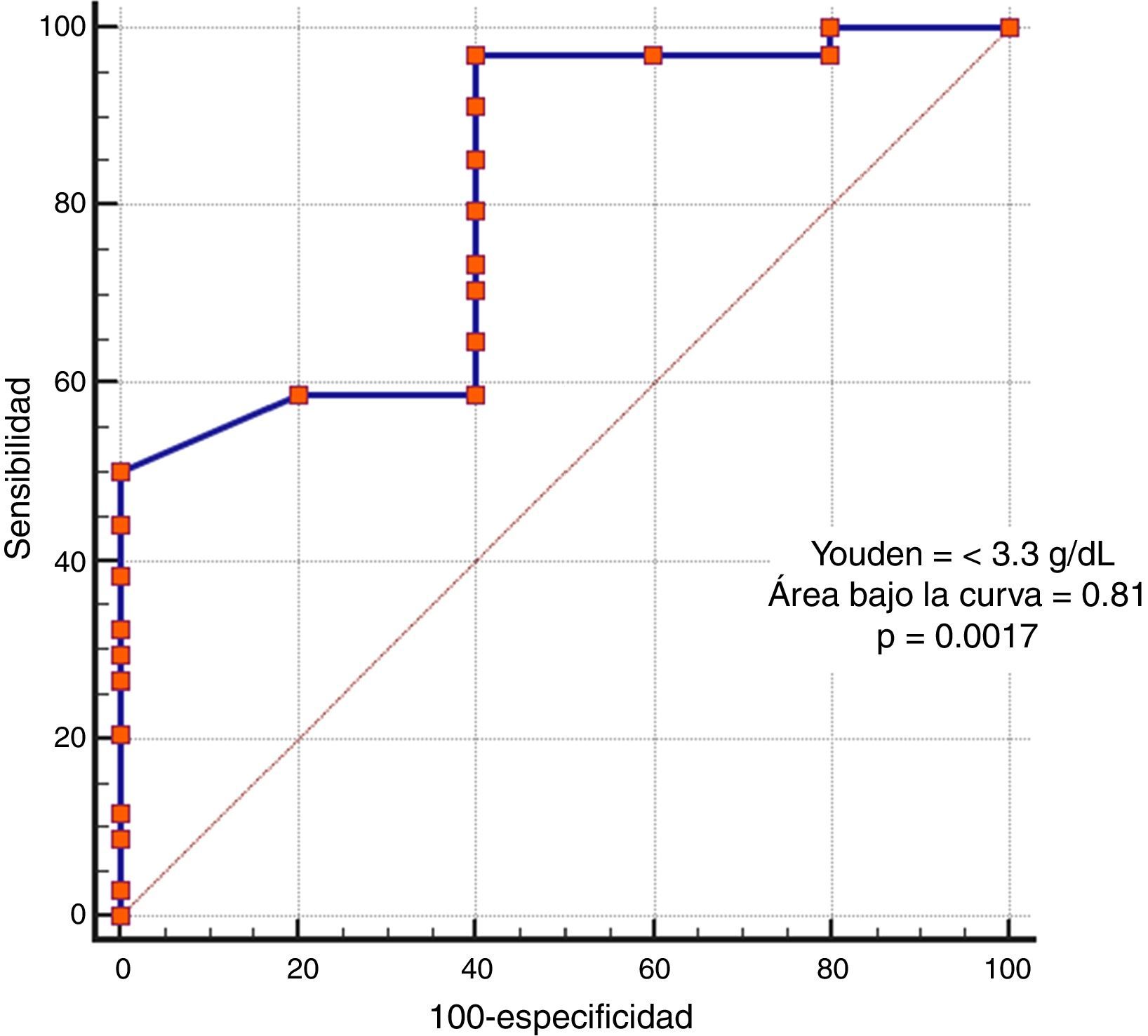
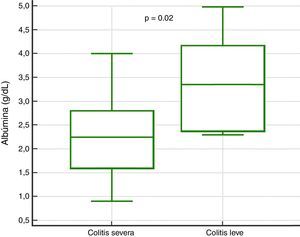
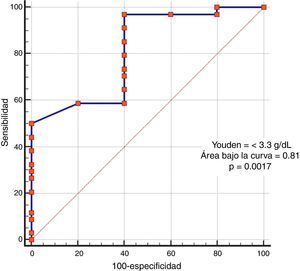
En el análisis de severidad de la presentación clínica, la única variable que presentó significación estadística fue el nivel sérico de albúmina (p=0.02) (tabla 4, fig. 3). A la construcción de la curva ROC y cálculo del índice de Youden, se determinó un área bajo la curva significativa de 0.81 (p=0.0017) y un punto de corte de≤3.3g/dL para predicción de cuadro severo/complicado (fig. 4), calculándose un RR de 8.2 (p=0.008), con sensibilidad del 97% y especificidad del 60%, así como valor predictivo positivo del 52% y valor predictivo negativo del 82%.
Severidad de la diarrea
| Severa/complicada (n=34) | Leve/moderada (n=5) | RR | p | |
|---|---|---|---|---|
| IRC, n (%) | 11 (32) | 1 (20) | 1.7 | 0.58 |
| Leucocitos en heces, n (%) | 21 (62) | 3 (60) | 1 | 0.93 |
| Cirugía previa, n (%) | 11 (32) | 3 (60) | 0.37 | 0.24 |
| Diabetes, n (%) | 13 (38) | 4 (80) | 0.19 | 0.12 |
| Hipertensión, n (%) | 11 (32) | 2 (40) | 0.75 | 0.73 |
| Cirugía abdominal, n (%) | 7 (20) | 2 (40) | 0.45 | 0.33 |
| Uso de antibióticos, n (%) | 21 (62) | 3 (60) | 1 | 0.93 |
| >1 antibiótico, n (%) | 7 (33) | 0 | 3.1 | 0.43 |
| Edad, mediana (IQR) | 48 (33-61) | 57 (45-60) | — | 0.64 |
| Albúmina, mediana (IQR) | 2.2 (1.6-2.8) | 3.3 (2.3-4.1) | — | 0.02 |
Las características clínicas de nuestros pacientes difieren un poco de las reportadas a nivel mundial1,7,9, ya que la edad media de presentación fue de 49 años, a pesar de que quienes presentan mayor riesgo son los mayores de 65 años; en nuestro estudio solo un 20% fue mayor de esa edad. Solo el 36% presentó estancia intrahospitalaria prolongada (mayor de 15 días). El 30-40% de nuestra población presentó antecedentes de enfermedades crónicas (diabetes, hipertensión, enfermedad renal crónica).
La frecuencia de los síntomas, así como la de leucocitosis sistémica (49%) y de leucocitos en heces (61%) coinciden con la literatura mundial2–4. En cuanto a marcadores de inflamación se encontró la procalcitonina elevada en la mayoría de los pacientes (90%) con una mediana de 1.2ng/mL, la VSG con una media de 52mm/h y la proteína C reactiva con una mediana de 51mg/L. Sin embargo, estas últimas se reportaron en un porcentaje bajo de nuestra muestra.
El uso previo de antibióticos se reportó en el 62% de los pacientes, concordante con la literatura actual4,9,10. Una tercera parte de los pacientes no contaron con antecedentes de uso de antibiótico, lo cual se intenta explicar con 2 teorías: la primera, el uso de otros fármacos, como los IBP que aumentan el riesgo de infección por CD; y la segunda, el contacto con algún compañero (paciente) de cuarto o piso que haya recibido antibióticos de amplio espectro19. Cabe señalar que las fluoroquinolonas solo se reportaron en un 6%, esto debido a que nuestro centro es hospital hiperendémico para CD, y una de las medidas del servicio de infecciones nosocomiales fue restringir el uso de fluoroquinolonas desde hace 3 años, en especial por su asociación con la cepa hipervirulenta.
Actualmente existe controversia en cuanto al uso previo de IBP y el riesgo de infección por CD; en nuestro estudio se reporta en aproximadamente un 80% de los pacientes, sin embargo no se demostró riesgo de asociación. La explicación más factible es el tamaño de muestra relativamente pequeño y el criterio de inclusión tan específico que se utilizó para el estudio (PCR positiva). De cualquier forma, la evidencia reciente indica que el continuar con el uso de IBP posterior a un primer cuadro de diarrea por CD aumenta el riesgo de recaída, y se sugiere interrumpir su uso si no existe alguna indicación precisa20–22.
Solo se presentó una muerte en nuestra población estudiada. Este número está claramente sesgado, ya que para nuestro estudio se excluyeron los pacientes en estado de mayor gravedad. Sin embargo, la mortalidad en nuestro hospital por esta entidad, recientemente publicada por el servicio de infecciones nosocomiales, es del 5%23.
En cuanto a los hallazgos endoscópicos, la colonoscopia fue anormal en la gran mayoría de los pacientes, con hallazgos normales solo en el 13%; esto concuerda con algunos estudios en los que se reporta normalidad en el 6-31% de los pacientes11,12.
Entre los pacientes con colitis seudomembranosa predominó la afección en colon izquierdo en más de la mitad, y menos comúnmente aislada a colon derecho. Ya que la diferencia en la frecuencia de localización no fue significativa, nuestro estudio no apoya la idea de realizar solo rectosigmoidoscopia, como se ha hecho en algunos estudios12, pues aunque la frecuencia es baja, se pueden presentar las lesiones solo en el colon derecho, con una incidencia reportada en un16%11,24. Además estudios previos refieren una sensibilidad del 91% con sigmoidoscopia flexible para el diagnóstico de colitis seudomembranosa, y del 100% con colonoscopia25.
La colonoscopia no está exenta de riesgos debido a la posibilidad de una perforación, por lo que se recomienda realizarla con una mínima insuflación de aire y evitando la formación de asas con el endoscopio, y ante la duda de poder producir una complicación, suspender la exploración11,18. Nuestra recomendación es la realización de estudio endoscópico completo, con revisión de colon derecho en la medida de lo posible; sin embargo, de presentar lesiones clásicas (seudomembranas) en colon izquierdo, tomar muestras y dar por terminado el estudio.
Cabe hacer mención que debido al objetivo primario del estudio la colonoscopia se realizó en todos los pacientes incluidos solo con fines de investigación, pues se sabe que ante un resultado de PCR positivo, el procedimiento no es indispensable a menos que no haya respuesta al tratamiento12,18.
En el análisis extendido de riesgo para seudomembranas no se encontró asociación con la severidad, sin embargo, observamos una tendencia no significativa a presentar seudomembranas en aquellos pacientes que utilizaron más de un antibiótico (RR: 1.37, p=0.51) y aquellos con cirugía previa (RR: 1.36 p=0.30).
La única variable que presentó significación estadística para severidad fue un nivel de albúmina sérica≤3.3g/dL, lo que nos permite realizar 2 hipótesis, la primera es que los pacientes con hipoalbuminemia asociada a otros estados patológicos (desnutridos, colitis severa con enteropatía perdedora de proteínas) presentarán cuadros severos de la enfermedad en caso de adquirir esta infección; y la segunda es que la albúmina, al ser un reactante de fase aguda negativo, disminuye sus niveles como respuesta al cuadro inflamatorio. En base a estos resultados, la utilidad de los niveles de albúmina radica en la capacidad de predicción de severidad, aunque se requerirán estudios aleatorizados y con seguimiento de la tendencia de los niveles a lo largo de la enfermedad, para establecer con certeza este dato.
Una de las fortalezas principales del presente estudio es que se analizó una variable no reportada previamente en México, a saber, las características endoscópicas de la afección por CD; además de a que todos los pacientes incluidos se les realizó el diagnóstico por método de PCR e identificación de la cepa hipervirulenta NAP027, lo que agrega confiabilidad a la asociación de dichas lesiones con el patógeno estudiado. Las limitaciones incluyen el tamaño de muestra limitado, lo que impide aceptar conclusiones sólidas respecto a comparaciones entre grupos, sin embargo, la mayoría de los reportes que abordan este tema en específico consisten de número limitado de pacientes incluidos12,25.
ConclusiónLa colonoscopia no está indicada en todos los pacientes con diarrea hospitalaria asociada a infección por CD, sin embargo en los pacientes que lo ameritan, debe preferirse este método en lugar de solo rectosigmoidoscopia. Nuestro estudio muestra que un nivel de albúmina sérica<3.3g/dL es un factor que podría predecir los cuadros de severidad en este grupo específico de pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónLos autores declaran que no se recibió ningún tipo de financiamiento para este estudio.
Conflicto de interesesLos autores declaran que no tiene ningún conflicto de intereses.