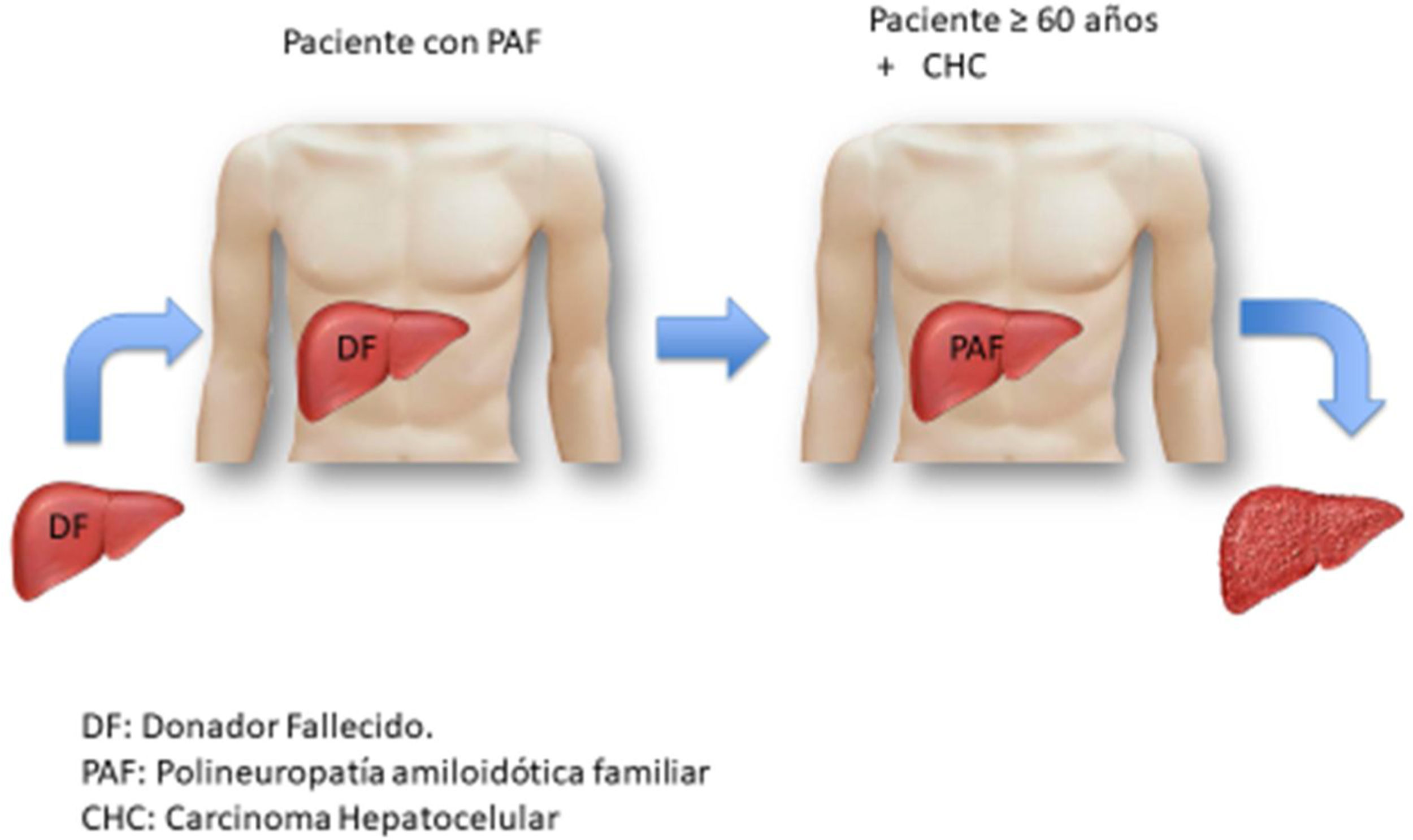
Ante la escasez de órganos a nivel mundial, la comunidad médica ha desarrollado distintas medidas para incrementar el número de donadores1–3, una de las cuales es el trasplante hepático dominó (THD). El primer THD se realizó en 1995 en Portugal por Furtado et al.4 al trasplantar a un paciente con polineuropatía amiloidótica familiar (PAF) con un hígado de donador fallecido y el hígado del paciente con PAF se asignó en otro paciente de 56 años con cirrosis y carcinoma hepatocelular (CHC).
La PAF es una enfermedad hereditaria autosómica dominante ocasionada por la mutación del gen que codifica la transtiretina (TTR), que se localiza en el cromosoma 18q. Se conocen más de 100 mutaciones y cualquiera de estas conlleva a inestabilidad de la proteína correspondiente y al depósito extracelular de amiloide en varios tejidos (nervios autonómicos y periféricos, pared del tracto gastrointestinal, corazón, etc.). Los síntomas ocurren entre los 25 y 35 años y los más comunes son: polineuropatía de los miembros periféricos, diarrea y diversas arritmias5. El amiloide de TTR es predominantemente producido en el hígado y solo el 5% se produce en la retina y los plexos coroides. Por lo tanto, el trasplante hepático (TH) es el tratamiento de elección cuando inician las afecciones sistémicas y antes de que aparezcan síntomas incapacitantes6,7. Salvo la presencia de esta alteración genética, el hígado de un paciente con PAF tiene una morfología y función completamente normales, por lo que se puede utilizar para trasplantar a otro paciente con cirrosis, con o sin CHC y con cierta urgencia de recibir TH (fig. 1). A continuación, presentamos los dos primeros THD realizados en México.
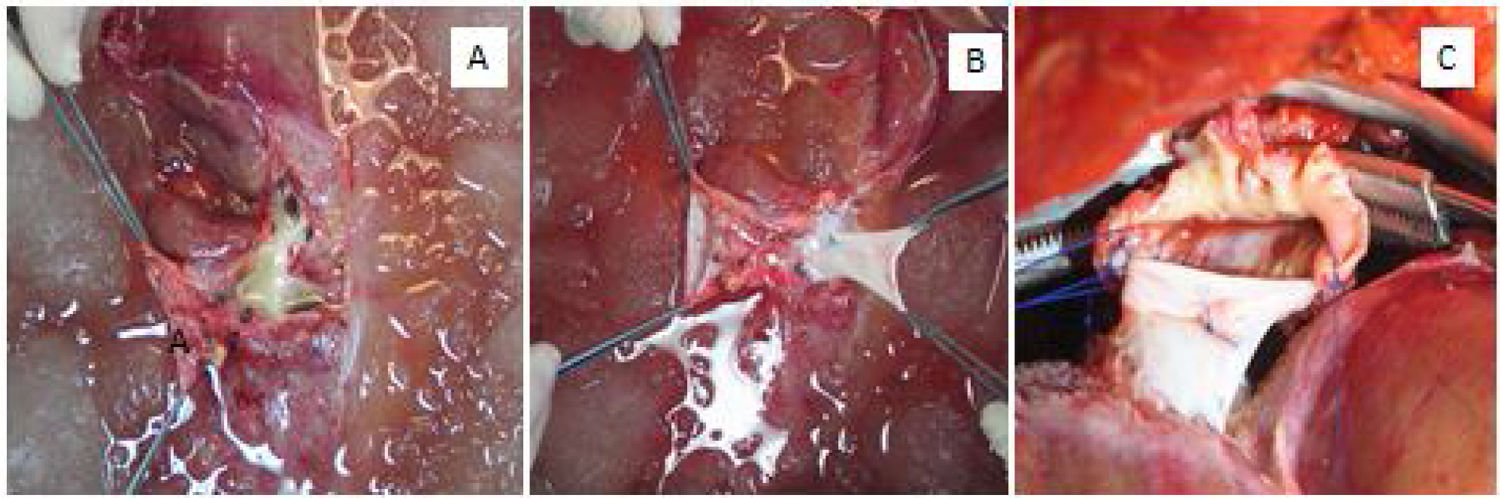
El primer caso se realizó en un paciente masculino de 41 años, con diagnóstico de PAF desde el 2012 por mutación TTR Ser50Arg. Presentaba neuropatía segmentaria en ambos nervios medianos en Estadio 1 de discapacidad por neuropatía (polyneuropathy disability score [PND]), miocardiopatía infiltrativa por amiloide con New York Heart Association (NYHA) Estadio 1, extrasístoles ventriculares y la fracción de eyección ventricular izquierda (FEVI) del 61%. En el 2013, el paciente fue receptor de un hígado de donador fallecido de 20 años. La hepatectomía del paciente con PAF se realizó de manera habitual con exclusión total de la vena cava inferior, salvo las siguientes diferencias: Se dividió la vía biliar, porta y la vena cava suprahepática e infrahepática en un punto equidistante, se dividió la arteria hepática en la bifurcación con la arteria gastroduodenal. El hígado explantado del paciente con PAF fue perfundido con 2 L de Custodiol® (Alemania) por la vena porta y 2 L por la arteria hepática. Para poder utilizar el hígado del paciente con PAF, fue necesario realizar una reconstrucción compleja de las venas suprahepáticas y cava retrohepática con vasos del donador fallecido (fig. 2A, B).
A) Vista posterior del hígado del paciente con PAF después de la perfusión durante la cirugía de banco. Se observa pérdida importante de la vena cava retrohepática y suprahepática y se aprecia la desembocadura de las venas suprahepáticas. B) Reconstrucción de cava retrohepática con cava inferior del donador fallecido. C) Anastomosis de la reparación vascular con la cava suprahepática de la primera receptora.
La receptora para este injerto con PAF fue una paciente de 60 años, con diagnóstico de colangitis biliar primaria (CBP), hipertensión portal hemorrágica severa y colocación de derivación portosistémica intrahepática transyugular (TIPS) por ascitis refractaria, model for end-stage liver disease (MELD) 15. El TH se realizó de manera habitual con técnica clásica de exclusión total.
El segundo caso se realizó en el 2014, en una paciente de 31 años con diagnóstico de PAF con mutación TTR Ser52Pro desde el 2012. La paciente presentaba parestesias en extremidades superiores con estadio PND 1, infiltración leve por resonancia magnética en el ventrículo izquierdo del corazón, así como en grasa perirrectal, confirmado por biopsia. La donadora fue una mujer con muerte cerebral de 41 años. La hepatectomía de la paciente con PAF se realizó de la misma forma que en el primer caso, sin necesidad de reconstrucción vascular y únicamente se perfundió con Custodiol®. Posteriormente se realizó el TH en una paciente de 59 años con cirrosis criptogénica y CHC dentro de criterios de Milán.
La evolución de los cuatro pacientes fue adecuada y se dieron de alta sin complicaciones.
El receptor de un hígado con PAF, debe presentar una edad cercana a los 60 años, ya que normalmente se estima que el tiempo que pasa posterior al TH y que pueda desarrollarse PAF es entre 10 y 15 años8, aunque algunos autores reportan la aparición de síntomas en menos tiempo9. En el caso de nuestros pacientes con PAF, presentan mutaciones no Val30Met, y de estas, existen más de 100 mutaciones, con mayor riesgo de presentar progresión de la enfermedad y con una supervivencia media de 7.1 años después del trasplante. La afección cardiaca en estos casos es mayor y es la principal causa de fallecimiento si no son trasplantados del corazón10.
Nuestros dos pacientes con PAF, con un tiempo de evolución del diagnóstico al trasplante similar y en el mismo estadio de la enfermedad, presentaron diferente evolución. El paciente masculino con la mutación Ser50Arg presentó progresión de la enfermedad cardiaca grave en cinco años y falleció en espera de un trasplante cardiaco. La paciente con mutación Ser52Pro ha permanecido estable de la enfermedad amiloidea en el mismo periodo de tiempo. La primera receptora de un hígado con PAF no ha presentado manifestaciones de la enfermedad. Sin embargo, la segunda receptora ya presenta infiltración cardiaca leve por amiloide.
Consideraciones éticasEn este trabajo de investigación se solicitó a los pacientes el consentimiento informado para revisión de los expedientes. El trabajo cumple con la normativa vigente en investigación bioética y no es necesario que sea sometido al Comité de Ética, ya que solo se trató de revisión de expedientes y en ningún momento se afecta la privacidad de los pacientes. En las imágenes presentadas en esta publicación, no es posible identificar a ninguno de los pacientes.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.