El índice proteína C reactiva/albúmina (IPA) es un marcador inflamatorio que es considerado de valor para el pronóstico en muchas enfermedades. En este estudio, nuestro objetivo fue investigar el desempeño diagnóstico del IPA para determinar la gravedad clínica de la colitis ulcerosa crónica idiopática (CUCI) grave.
Materiales y métodosEstudio retrospectivo de 200 pacientes con CUCI ingresados en la unidad de Gastroenterología de la Universidad de Alejandría durante un período de 8años, desde enero de 2012 hasta enero de 2020. En la evaluación se incluyeron los datos demográficos, los resultados de laboratorio y de las escalas endoscópicas y clínicas de actividad de la enfermedad. Se registraron los niveles de proteína C reactiva (PCR) y albúmina. Se calculó el IPA para determinar la gravedad clínica.
ResultadosDe los 200 pacientes, 135 (67.5%) fueron hombres y 65 (32.5%) fueron mujeres. La edad promedio fue de 43.5±9.8 años. Los pacientes fueron divididos en grupos con enfermedad leve, moderada y severa. Hubo diferencias estadísticamente significativas entre el IPA, la velocidad de sedimentación globular (VSG) y los niveles de albúmina y de PCR (p=0.001; p<0.05). El IPA mostró un mejor desempeño, con un punto de corte de 0.6, para definir pacientes con enfermedad grave, con un área bajo la curva (AUC por sus siglas en inglés) de 0.985, 98% de sensibilidad, 100% de especificidad, valor predictivo positivo (VPP) 100% y valor predictivo negativo (VPN) 97%, p<0.001. Los valores de AUC para el diagnóstico de enfermedad grave fueron 0.985, 0.88, 0.72, y 0.65 para IPA, PCR, albúmina y VSG, respectivamente.
ConclusiónSe encontró una relación estadísticamente significativa entre el IPA y la actividad clínica de la enfermedad en la CUCI. El IPA es una herramienta confiable y práctica para detectar CUCI grave.
The C-reactive protein/albumin ratio (CAR) is an inflammatory marker that is considered to have prognostic value in many diseases. Our aim in the present study was to investigate the diagnostic performance of the CAR in determining the clinical severity of acute severe ulcerative colitis (ASUC).
Materials and methodsA retrospective study on 200 UC patients that were admitted to the Gastroenterology unit of the Alexandria University, over an 8-year period from January 2012 to January 2020, was conducted. Patient demographic data, laboratory values, and clinical and endoscopic disease activity scores were evaluated. C-reactive protein (CRP) and albumin levels were recorded. The CAR was calculated to determine clinical severity.
ResultsOf the 200 patients, 135 (67.5%) were men and 65 (32.5%) were women. Mean age was 43.5±9.8 years. Patients were divided into groups with mild, moderate, or severe disease activity and there were statistically significant differences in the CAR, the erythrocyte sedimentation rate (ESR), CRP levels, and albumin levels (P=.001; P<.05). With a cut-off value of 0.6, the CAR performed best in defining patients with severe disease, with an area under the curve (AUC) of 0.985, 98% sensitivity, 100% specificity, positive predictive value (PPV) of 100%, and negative predictive value (NPV) of 97%, P<0.001. AUC values for the diagnosis of severe disease were 0.985, 0.88, 0.72, and 0.65 for the CAR, CRP, albumin, and the ESR, respectively.
ConclusionThere was a statistically significant association between the CAR and clinical disease activity in patients with UC. The CAR is a reliable and practical tool for detecting ASUC.
La colitis ulcerosa crónica idiopática (CUCI) se caracteriza por una inflamación crónica no controlada de la mucosa intestinal. La CUCI típicamente se caracteriza por una inflamación de mucosa con recaída y remisión, que comienza con un patrón continuo desde el recto y se extiende al colon proximal1,2.
Se prefiere el término «colitis aguda grave» al término «colitis fulminante», debido a que el término «fulminante» carece de una definición clara. Aproximadamente el 20% de los pacientes con brotes iniciales de la enfermedad tienen CUCI grave3.
La CUCI grave es una emergencia médica. De acuerdo con los criterios de Truelove y Witts, esta se caracteriza por la presencia de sangre en heces más de 6 ocasiones por día, en conjunto con cualquiera de los siguientes: taquicardia >90lpm, fiebre >37.8°C, hemoglobina (Hb) >10.5g/dl y/o velocidad de sedimentación globular (VSG) >30mm/h4.
Los niveles elevados de proteína C reactiva (PCR) y los niveles bajos de albúmina son asociados con actividad grave de la enfermedad5-9.
El índice PCR/albúmina (IPA) es un marcador inflamatorio cuyo valor predictivo ha sido utilizado relacionado con varios cánceres, sepsis y pancreatitis aguda10,11. Un nivel elevado de IPA está asociado con una alta carga inflamatoria, mal prognosis y mortalidad12.
Determinar la gravedad de la enfermedad por medio de la utilización de indicadores inflamatorios objetivos, no invasivos y coste-efectivos podría ser un método práctico y sin sesgos. Nuestro objetivo en el presente estudio fue investigar el desempeño diagnóstico del IPA para determinar la gravedad clínica de la enfermedad en pacientes egipcios con CUCI.
Materiales y métodosParticipantesSe recolectaron datos retrospectivos de un periodo de 8años (enero de 2012 a enero de 2020) de una base de datos de pacientes con CUCI activa que fueron admitidos en la unidad de gastroenterología de la Facultad de Medicina de Alejandría. De los 592 pacientes que fueron analizados retrospectivamente, solo 200 sujetos cumplieron con los criterios de inclusión para el presente estudio. Todos los pacientes tuvieron confirmación histológica de CUCI activa. En la evaluación se incluyeron los datos demográficos de los pacientes, los valores de laboratorio, la actividad clínica de la enfermedad, las escalas endoscópicas de actividad y los tratamientos. Se determinaron y registraron los niveles de PCR y de albúmina, y se calculó el IPA.
Criterios de exclusiónMalignidad; intervención quirúrgica reciente del intestino grueso o delgado en los últimos 6meses; diarrea infecciosa, incluida la diarrea bacteriana, viral y por parásitos; uso prolongado de antibióticos o de medicamentos no esteroideos antiinflamatorios; uso de corticoesteroides durante los últimos 3meses; terapia biológica durante los últimos 6meses, otras enfermedades autoinmunes; embarazo; quemadura grave; sepsis; enfermedades crónicas renales, hepáticas o cardíacas; diabetes mellitus; enfermedad celiaca; falta de datos sobre PCR o albúmina al ingreso hospitalario.
El presente estudio fue realizado siguiendo los principios de la Declaración de Helsinki y fue aprobado por el Comité de Ética e Investigación de nuestro hospital.
Gravedad de la enfermedadLa CUCI grave fue definida utilizando los criterios de Truelove y Witts como más de 6 heces con sangre por día, además de una o más de las siguientes: temperatura >37.8°C; pulso >90lpm; Hb<10.5g/dl; VSG>30mm/h, o PCR>30mg/l. La actividad moderada fue definida como 4 o más heces con sangre por día, además de todas las siguientes: temperatura ≤37.8°C; pulso ≤90 lpm; Hb ≥10.5g/dl, y VSG ≤30mm/h. La actividad leve fue definida como menos de 4 heces con sangre por día, además de todas las siguientes: temperatura <37.8°C; pulso <90lpm; Hb>11.5g/dl; VSG <20mm/h9. La remisión fue definida como 3 movimientos intestinales por día, sin sangre en heces y sin dolor abdominal ni urgencia fecal.
Se realizó colonoscopia en todos los pacientes, para evaluar la actividad de la enfermedad endoscópicamente y detectar la localización de la enfermedad. La actividad endoscópica de la enfermedad fue evaluada por gastroenterólogos experimentados, utilizando colonoscopios de definición estándar (Olympus CV-190, sistema VP-4450HD y EC-590WL Fujinon, Fujifilm, Tokio, Japón). De acuerdo con el índice de actividad endoscópica Mayo (subíndice endoscópico Mayo), la apariencia mucosa endoscópica normal fue definida como Mayo0; la presencia de eritema en mucosa, patrón vascular disminuido y friabilidad leve, fue definida como Mayo1; la presencia de eritema marcado, ausencia de patrón vascular, y friabilidad y erosiones, fue definida como Mayo2, y la presencia de sangrado espontáneo y ulceración fue definida como Mayo313.
Análisis estadísticoLos datos fueron recolectados e ingresados en una computadora de escritorio. Se realizó el análisis estadístico utilizando el programa Statistical Package for Social Sciences (SPSS/versión 21). Los valores continuos fueron presentados como la media ±desviación estándar, o en el caso de los datos con distribución no normal, como la mediana y percentiles 25-75. Para las variables categóricas se utilizó la prueba chi cuadrado para comparar los diferentes grupos. La pruebaF (ANOVA) fue utilizada para las variables cuantitativas con distribución normal en la comparación de más de dos grupos, y para la comparación de pares se utilizó una prueba post hoc (Tukey, LSD). Para variables cuantitativas con distribución anormal se utilizó la prueba de Mann-Whitney en la comparación de dos grupos de estudio, para más de dos grupos de variables cuantitativas con distribución anormal se utilizó la prueba de Kruskal-Wallis. Para comparaciones de pares se utilizó una prueba post hoc (prueba de comparaciones múltiples de Dunn), para comparar la media de dos grupos de estudio y para evaluar si existía diferencia estadísticamente significativa en las medias de los dos juegos de datos se utilizó la prueba t de Student. La significancia estadística se estableció a un valor de p≤0.05. Los puntos de corte, la sensibilidad y la especificidad fueron calculados utilizando el análisis de la curva de la característica operativa del receptor (ROC por sus siglas en inglés). Se calculó el punto de corte en caso de que el valor del área bajo la curva ROC (AUC por sus siglas en inglés) estuviera por arriba de 0.89. De acuerdo con lo normalmente recomendado, la hipótesis nula (H0) fue rechazada si el valor de p correspondiente fuera menor a 0.05. Se requirió un tamaño de muestra mínimo de 200 pacientes para el presente estudio.
ResultadosUn total de 200 pacientes tuvieron CUCI clínicamente activa, de los cuales 135 (67.5%) fueron hombres y 65 (32.5%) fueron mujeres. La edad promedio de los participantes del estudio fue de 43.5±9.8 años. De acuerdo con el índice de gravedad de Truelove y Witts, 40 pacientes (20%) tenían actividad leve de la enfermedad, 82 (41%) tenían actividad moderada y 78 (39%) tenían actividad grave. Ninguno de los pacientes en el grupo de actividad grave presentó colitis fulminante. En la tabla 1 se muestran las características demográficas y la actividad endoscópica de la enfermedad de los pacientes.
Datos demográficos y clínicos básicos de los pacientes del estudio
| Parámetros | n=200 | |
|---|---|---|
| n | % porcentaje | |
| Edad (años) | ||
| <30 | 13 | 6.5 |
| 30-40 | 65 | 32.5 |
| 40-50 | 57 | 23.5 |
| 50+ | 65 | 32.5 |
| Rango | 28-60 | |
| Media±DE | 43.5±9.8 | |
| Sexo | ||
| Hombres | 135 | 67.5 |
| Mujeres | 65 | 32.5 |
| Gravedad de la enfermedad (índice de gravedad de Truelove) | ||
| Leve (10-34) | 40 | 20 |
| Moderado (35-64) | 82 | 41 |
| Grave (65 y más) | 78 | 39 |
| Localización de la enfermedad | ||
| Proctitis | 16 | 8 |
| Colitis izquierda | 72 | 36 |
| Colitis extendida | 112 | 56 |
| Índice de gravedad endoscópica (subíndice de Mayo) | ||
| 0 | 2 | 1 |
| 1 | 27 | 13.5 |
| 2 | 61 | 30.5 |
| 3 | 110 | 55 |
| Tratamiento | ||
| Mesalazina | 159 | 79.5 |
| Sulfasalazina | 41 | 20.5 |
| Azatioprina | 63 | 31.5 |
DE: desviación estándar; Media: media aritmética.
Existieron diferencias estadísticamente significativas en los niveles de IPA, PCR y albúmina, y la VSG en los pacientes con diferente actividad de la enfermedad. En la tabla 2 se muestra la comparación en las diferentes actividades clínicas de CUCI y los marcadores bioquímicos de los niveles de IPA, PCR y albúmina, y la VSG.
Comparación del IPA, la PCR y los niveles de albúmina y la VSG en los diferentes niveles de actividad de la colitis ulcerosa
| Marcadores de actividad clínica | LeveMedia±DE | ModeradaMedia±DE | GraveMedia±DE | Prueba ANOVA | p |
|---|---|---|---|---|---|
| PCR (mg/dl) | |||||
| Rango | 0.12-0.75 | 2.10-4.52 | 1.53-9.88 | ||
| Media±DE | 0.449±0.182 | 3.42±0.82 | 5.91±2.82 | 88.58 | 0.0001* |
| IPA | |||||
| Rango | 0.01-0.23 | 0.23-1.41 | 2.32-4.50 | 65.2 | 0.0001* |
| Media±DE | 0.13075±0.068 | 0.82±0.34 | 3.41±0.62 | ||
| Albúmina (g/dl) | |||||
| Rango | 3.6-4.8 | 3.00-4.00 | 2.40-3.46 | 58.2 | 0.0002* |
| Media±DE | 4.2475±0.386 | 3.56±0.37 | 2.94±0.32 | ||
| VSG (mm/h) | |||||
| Rango | 11-27.8 | 15.90-48.30 | 34.70-80.00 | 61.2 | 0.0001* |
| Media±DE | 19.635±4.894 | 36.30±10.33 | 59.01±13.89 | ||
DE: desviación estándar; IPA: índice PCR/albúmina; PCR: proteína C reactiva; VSG: velocidad de sedimentación globular.
Las diferencias en los valores de IPA, PCR y VSG fueron mayores, con significancia estadística, incluso entre pacientes con CUCI grave y pacientes sin CUCI grave, mientras que los niveles de albúmina en el grupo con actividad clínica grave fueron significativamente menores que en los demás grupos (p=0.01; p<0.05), como se muestra en la tabla 3.
El IPA, la PCR y los niveles de albúmina, y la VSG, en la CUCI no grave y en la CUCI grave
| Marcadores de actividad de clínica | CUCI no graveMedia±DE | CUCI graveMedia±DE | Prueba t de Student | p |
|---|---|---|---|---|
| PCR (mg/dl) | ||||
| Rango | 295.42-4.78 | 1.53-9.88 | 11.25 | 0.001* |
| Media±DE | 2.42±1.55 | 5.91±2.82 | ||
| IPA | ||||
| Rango | 70.66-1.41 | 2.32-4.50 | 12.89 | 0.001* |
| Media±DE | 0.58±0.42 | 3.41±0.62 | ||
| Albúmina (g/dl) | ||||
| Rango | 459.50-4.80 | 2.40-3.46 | 10.6 | 0.001* |
| Media±DE | 3.77±0.50 | 2.94±0.32 | ||
| VSG (mm/h) | ||||
| Rango | 3,588.40-48.40 | 34.70-80.00 | 16.2 | 0.001* |
| Media±DE | 29.66±11.57 | 59.01±13.89 | ||
CUCI: colitis ulcerosa crónica idiopática; DE: desviación estándar; IPA: índice PCR/albúmina; PCR: proteína C reactiva; VSG: velocidad de sedimentación globular.
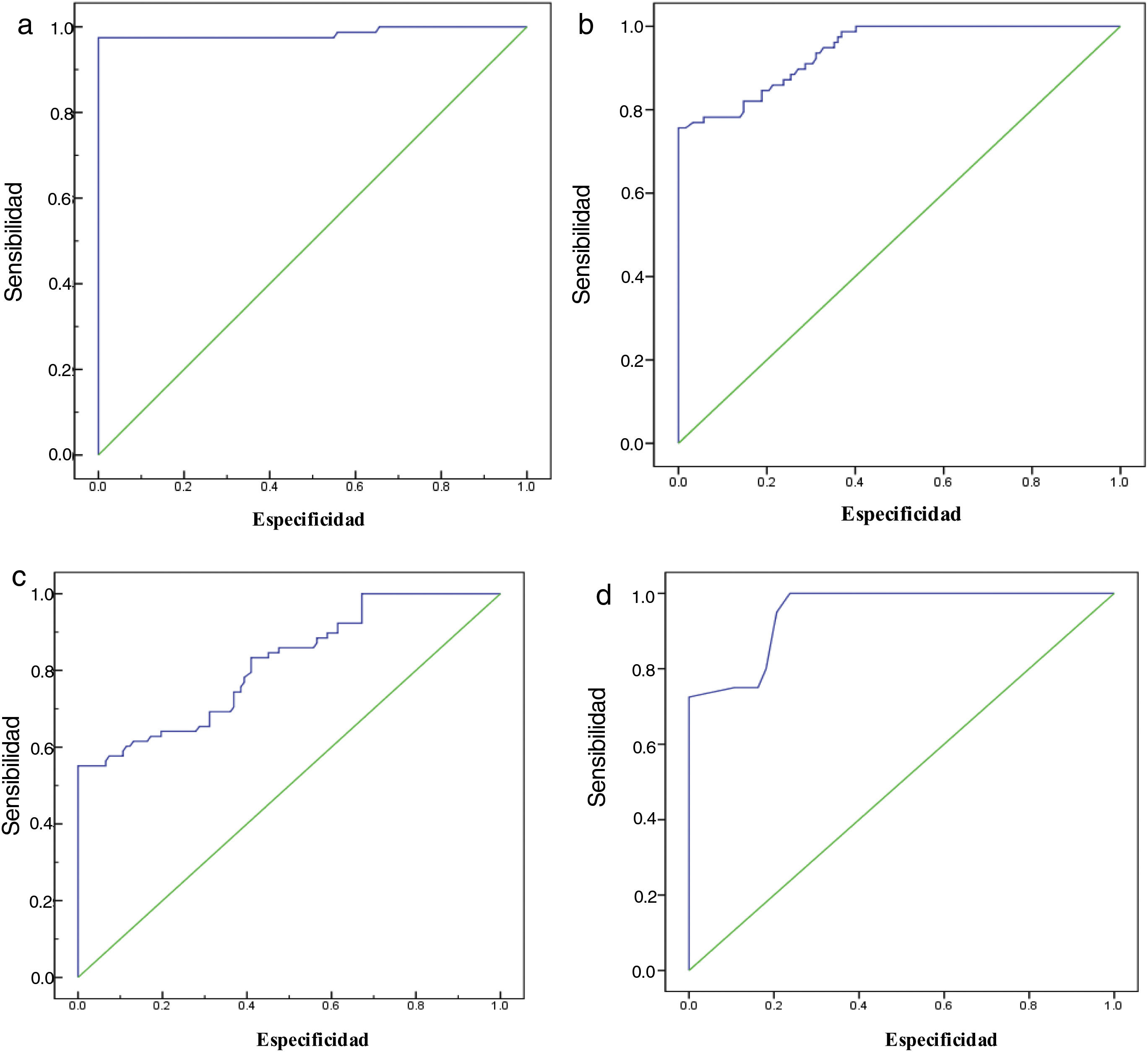
El punto de corte de 0.6 para el IPA demostró el mejor desempeño para definir pacientes con actividad grave, con un AUC de 0.985, 98% de sensibilidad, 100% de especificidad, valor predictivo positivo (VPP) del 100% y valor predictivo negativo (VPN) del 97%, p<0.001. Los valores AUC para el diagnóstico de enfermedad grave fueron 0.985, 0.88, 0.72 y 0.65 para el IPA, PCR, albúmina y VSG, respectivamente (tabla 4 y fig. 1).
Análisis ROC del IPA, la PCR, la albúmina y la VSG en el diagnóstico de enfermedad grave
| Parámetros | Punto de corte | AUC | p | Sensibilidad (%) | Especificidad (%) | VPP (%) | VPN (%) |
|---|---|---|---|---|---|---|---|
| IPA | 0.6 | 0.985 | 0.001* | 98.0 | 100.0 | 100.0 | 97.0 |
| PCR | 2 | 0.88 | 0.001* | 90.0 | 95.0 | 94.0 | 91.0 |
| Albúmina | 3.6 | 0.72 | 0.003* | 78.0 | 72.0 | 74.0 | 77.0 |
| VSG | 36 | 0.65 | 0.015* | 69.0 | 67.0 | 66.0 | 64.0 |
AUC: área bajo la curva de la característica operativa del receptor; IPA: índice PCR/albúmina; PCR: proteína C reactiva; VSG: velocidad de sedimentación globular; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
a)curva de la característica operativa del receptor para IPA mostrando el 100% de especificidad; b)curva de la característica operativa del receptor para PCR mostrando el 95% de especificidad; c)curva de la característica operativa del receptor para albúmina mostrando el 72% de especificidad; d)curva de la característica operativa del receptor para VSG mostrando el 67% de especificidad.
Los puntos de corte para IPA, PCR, albúmina y VSG fueron comparados con el número de pacientes con gravedad de enfermedad diferente, de acuerdo con el índice de gravedad de Truelove (tabla 5).
Comparación del número de pacientes clasificados de acuerdo con el índice de gravedad de Truelove, utilizando puntos de corte de los diferentes parámetros analizados
| Punto de corte | Actividad de la enfermedad (índice de gravedad de Truelove) | ||||||
|---|---|---|---|---|---|---|---|
| Parámetros | Leve (n=40) | Moderada (n=82 | Grave (n=78) | ||||
| n | % | n | % | n | % | ||
| IPA | > 0.6 | 8 | 20 | 82 | 99.1 | 78 | 100 |
| PCR | > 2 | 0 | 0 | 82 | 97.9 | 78 | 99.8 |
| Albúmina | < 3.6 | 2 | 5 | 49 | 59.8 | 78 | 98.6 |
| VSG | > 36 | 0 | 0 | 43 | 52.4 | 75 | 96.2 |
IPA: índice PCR/albúmina; PCR: proteína C reactiva; VSG: velocidad de sedimentación globular.
Cerca del 20-30% de los pacientes con CUCI presentan un riesgo de por vida de desarrollar un brote agudo en el curso de la enfermedad14. Además, la colonoscopia es un procedimiento invasivo que conlleva el riesgo de perforación en pacientes con CUCI grave15. Por lo tanto, existe una necesidad apremiante de marcadores predictivos no invasivos para pacientes con CUCI grave que sean confiables, dado que con el tiempo pueden desarrollar respuesta nula o incompleta a los corticoesteroides intravenosos, y en consecuencia requerir terapia de rescate16.
Se utilizan muchos marcadores de laboratorio para detectar la actividad de la enfermedad en pacientes con CUCI, como VSG, PCR, nivel de albúmina, calprotectina fecal y otros.
La PCR es uno de los indicadores inflamatorios no específicos de uso más común y tiene una media vida de aproximadamente 19h. Es un reactivo de fase aguda sintetizado por el hígado que se incrementa durante la actividad de la enfermedad debido a una respuesta de citocinas inflamatorias, como la TNF-alfa, la interleucina-6 (IL-6) y la interleucina-1 (IL-1)17.
A pesar de que la PCR es un reactivo de fase aguda, podría presentar una correlación falsa con el grado de actividad de la CUCI, ya que algunos pacientes endoscópicamente activos presentan niveles normales18-20.
El nivel sérico de albúmina es inversamente proporcional al grado de inflamación, debido a una disminución en la síntesis de albúmina por parte del hígado durante el proceso inflamatorio, y secundario a la síntesis de citocinas, como la TNF-alfa y la IL-621. Los niveles séricos de albúmina también se ven afectados por el estatus nutricional22.
La albúmina sérica baja y la PCR alta son asociadas con un grado de respuesta inflamatoria23. Karoui et al.24 encontraron una relación positiva entre actividad clínica y endoscópica, y niveles de PCR. Hindryckx et al.25 encontraron que la hipoalbuminemia estaba asociada con actividad de CUCI, ausencia de respuesta al tratamiento y mayor riesgo de colectomía en pacientes con CUCI grave.
En nuestro estudio retrospectivo, los datos fueron recolectados de una base de datos que incluía a 200 pacientes admitidos en la unidad de Gastroenterología de la Facultad de Medicina de Alejandría, a lo largo de un periodo de 8años, entre enero de 2012 y enero de 2020. Todos los pacientes tenían confirmación histológica de CUCI y fueron admitidos con CUCI activa.
Según la localización de la enfermedad, en nuestro estudio, 16 pacientes (8%) tenían proctitis, 72 pacientes (36%) tenían colitis de lado izquierdo y 112 pacientes (56%) tenían colitis extendida. La gravedad de la enfermedad de CUCI (subíndice Mayo) mostró que 171 pacientes tenían enfermedad moderada y grave (85.5%, subíndices Mayo2 y3). Los resultados de nuestro estudio mostraron diferencias estadísticamente significativas respecto al IPA, la PCR y la albúmina sérica, en fases diferentes de actividad CUCI (actividad leve, moderada y grave), de acuerdo con los criterios de Truelove y Witts. La PCR y el IPA mostraron un incremento estadísticamente significativo en diferentes fases de la CUCI.
Se evaluó el desempeño del IPA, de la PCR, de la albúmina sérica y de la VSG para evaluar la gravedad de la enfermedad, de acuerdo con su resultado de actividad clínica. El IPA presentó mayor sensibilidad (98% vs 90%, 78%, 69%), especificidad (100% vs 95%, 72%, 67%), VPP (100% vs 94%, 74%, 66%), VPN (97% vs 91%, 77%, 64%) y valor AUC (0.941 vs 0.931, 0.883, 0.888), para determinar la gravedad de la actividad, que los otros parámetros.
De manera similar a nuestro estudio, Sayar et al.26 encontraron una relación significativa entre el IPA y la actividad de la enfermedad, mostrando que el IPA tenía mayor especificidad y VPP que la PCR para predecir la colitis ulcerosa grave. Gibson et al.27 también encontraron que, al medir al tercer día de tratamiento, en pacientes con CUCI grave el IPA era un fuerte predictor de la falta de respuesta a la terapia con esteroides y que era superior a la PCR y a la albúmina. Chen et al.28 demostraron en su estudio que el IPA estaba fuertemente relacionado con la actividad de la enfermedad. En comparación con parámetros de conteo sanguíneo completo, el IPA tenía una mayor capacidad discriminatoria para la enfermedad inflamatoria intestinal (EII).
Nuestro estudio tuvo varias limitaciones. Primero, el pequeño tamaño de la muestra puede haber llevado a pérdida de significancia estadística en ciertos puntos y a un alto desempeño del IPA en los resultados. Segundo, la endoscopia no fue realizada en los pacientes en las diferentes etapas de actividad de la enfermedad y dependimos solamente de los criterios de Truelove y Witts, por lo que no pudimos emparejar o correlacionar el grado endoscópico de actividad con los criterios de Truelove y Witts. Tercero, nuestro estudio fue diseñado como un estudio retrospectivo de un solo centro, lo que evita sacar conclusiones firmes. Además, el estatus nutricional de los pacientes fue incierto debido a la naturaleza retrospectiva del estudio. Se requieren estudios prospectivos para proporcionar más información útil sobre este tema. Sin embargo, nuestro estudio sirve como base para futuros estudios mayores que obtengan el IPA en diferentes etapas de actividad de la enfermedad en pacientes con CUCI y para evaluar su nivel posterior a tratamiento.
En conclusión, nuestros resultados mostraron que el IPA fue un biomarcador útil para diferenciar la actividad de la CUCI, presentando mayor sensibilidad, especificidad y VPP que la PCR, al predecir la colitis ulcerosa grave. El IPA es un marcador económico, confiable y de fácil cálculo que puede ser utilizado para detectar actividad en pacientes CUCI grave.
Consideraciones éticasTodos los procedimientos en el estudio que involucraron participantes humanos fueron realizados de acuerdo con los estándares éticos del comité institucional de investigación (Comité de Ética de Investigación de la Facultad de Medicina de Alejandría, Egipto) y de la Declaración de Helsinki de 1964 y sus enmiendas posteriores o estándares éticos comparables.
Se obtuvo un consentimiento informado por escrito de cada uno de los pacientes participantes. En el caso de los pacientes menores de edad, se obtuvo el consentimiento informado por escrito de sus tutores legales. Los autores declaran que este artículo no contiene información personal que permita identificar a los pacientes.
FinanciaciónNo se recibieron apoyos específicos del sector público, del sector empresarial o de organizaciones no gubernamentales con relación al presente estudio.
Contribución de los autoresD.H. y A.E. diseñaron el estudio y realizaron la recolección de muestra y datos. D.H. y R.A. analizaron los datos. R.A., E.B. y M.E. realizaron el borrador del manuscrito. Todos los autores revisaron de manera crítica el manuscrito, aprobaron la versión final para publicación y acordaron responsabilidad por todos los aspectos del presente trabajo.
Conflicto de interesesLos autores declaran que no existe conflicto de intereses.
AgradecimientosLos autores desean agradecer al Dr. Doaa Header, al Dr. Ahmed El Lakany y al Dr. Reham Abo El Wafa por su apoyo con el análisis de datos, el concepto y diseño del estudio y la obtención de datos.