La infección por el virus de la hepatitis B (VHB) continúa siendo un problema de salud pública mundial, en México se estima que podría haber por lo menos tres millones de personas adultas que han adquirido la hepatitis B (anticuerpo anti-antígeno central del VHB [anti-HBc] positivo), de ellos cerca de 300,000 portadores activos (antígeno de superficie del VHB [HBsAg] positivo) podrían requerir tratamiento. Al ser prevenible por vacunación, debe enfatizarse la vacunación universal. Esta infección es un factor de riesgo mayor para el desarrollo de carcinoma hepatocelular, el estudio semestral con ultrasonido hepático y alfafetoproteína sérica favorece la detección temprana de esta neoplasia y debe realizarse en todo paciente con infección crónica por VHB, independientemente de la presencia de fibrosis avanzada o cirrosis. En la actualidad, la terapia de primera línea, son análogos nucleós(t)idos con alta barrera a la resistencia.
Hepatitis B virus (HBV) infection continues to be a worldwide public health problem. In Mexico, at least three million adults are estimated to have acquired hepatitis B (total hepatitis B core antibody [anti-HBc]-positive), and of those, 300,000 active carriers (hepatitis B surface antigen [HBsAg]-positive) could require treatment. Because HBV is preventable through vaccination, its universal application should be emphasized. HBV infection is a major risk factor for developing hepatocellular carcinoma. Semi-annual liver ultrasound and serum alpha-fetoprotein testing favor early detection of that cancer and should be carried out in all patients with chronic HBV infection, regardless of the presence of advanced fibrosis or cirrhosis. Currently, nucleoside/nucleotide analogues that have a high barrier to resistance are the first-line therapies.
A pesar de ser una enfermedad prevenible mediante una estrategia altamente eficaz como es la vacunación universal, hoy en día, la infección crónica por el virus de la hepatitis B (VHB), de acuerdo con la Organización Mundial de la Salud (OMS), continúa siendo un problema de salud pública a nivel mundial, que para el año 2015 afectaba ya a un estimado de 257 millones de personas1. Si bien México se considera una región geográfica de baja prevalencia (<2% de la población infectada), múltiples avances en cuanto a la fisiopatología de la enfermedad, herramientas de diagnóstico y grandes logros en cuanto a tratamientos más seguros y eficaces, han surgido desde que se elaboró el Primer Consenso Nacional de Hepatitis B Crónica en México en el año 20052; por este motivo la Asociación Mexicana de Hepatología A.C. (AMH) ha tomado la iniciativa de elaborar una Guía clínica actualizada sobre la hepatitis B, que permita integrar los nuevos conceptos sobre epidemiología, diagnóstico, tratamiento y seguimiento de los pacientes que padecen esta enfermedad. En la tabla 1 se muestra el resumen de las recomendaciones emitidas en esta guía clínica.
Resumen de las recomendaciones
| Recomendación | Grado de recomendación | Grado de evidencia |
|---|---|---|
| Grupos de riesgo y formas de transmisión | ||
| Recomendación 1: Toda persona con factores de riesgo mayores para adquirir o haber adquirido en el pasado infección por VHB, debe someterse a pruebas serológicas de escrutinio. | 1 | II-B |
| Recomendación 2: La estrategia más efectiva para lograr la eliminación de la transmisión del VHB, es la vacunación universal. | 1 | II-B |
| Escrutinio y vigilancia del desarrollo del CHC | ||
| Recomendación 3: El estudio semestral con ultrasonido hepático y AFP sérica favorece la detección temprana del CHC y debe realizarse en todo paciente con infección crónica por VHB, independientemente de la presencia de fibrosis avanzada o cirrosis. | 1 | II-B |
| Consejería respecto al consumo de alcohol, control de comorbilidades relacionadas al síndrome metabólico y necesidad de aplicar vacunas específicas | ||
| Recomendación 4: En todos los pacientes portadores de infección por VHB, y en todas las fases de la enfermedad, se recomienda la abstinencia en el consumo de alcohol. | 1 | II-B |
| Recomendación 5: En pacientes con infección crónica por VHB se deben tratar y controlar las comorbilidades relacionadas al síndrome metabólico. | 1 | II-B |
| Recomendación 6: A todos los pacientes con infección crónica por VHB sin inmunidad previa contra la hepatitis A, se les recomienda recibir vacunación contra la misma. | 1 | II-B |
| Estudios para realizar la evaluación inicial del paciente con infección crónica por VHB | ||
| Recomendación 7: Todo paciente con infección crónica por VHB requiere conocer su estatus respecto del HBeAg y del anti-HBe, además de la determinación del ADN-VHB (carga viral) con la finalidad de establecer un pronóstico y guiar el tratamiento. | 1 | I-A |
| Recomendación 8: Evaluar la severidad de la enfermedad hepática requiere además del examen físico, de pruebas bioquímicas, particularmente de ALT, y de ultrasonido hepático. | 1 | II-A |
| Recomendación 9: La presencia y el grado de fibrosis hepática puede determinarse por métodos no invasivos radiológicos. | 1 | II-B |
| Recomendación 10: La presencia y el grado de fibrosis hepática puede determinarse por métodos no invasivos serológicos. | 2 | II-B |
| Recomendación 11: La biopsia hepática será necesaria para establecer la presencia y el grado de fibrosis hepática cuando los métodos no invasivos no hayan resultado concluyentes. | 1 | II-B |
| Objetivos del tratamiento de la hepatitis B crónica | ||
| Recomendación 12: Los objetivos primordiales en el tratamiento de pacientes con HBC son prevención del desarrollo de cirrosis, descompensación hepática, CHC y muerte relacionada a causa hepática. | 1 | II-B |
| Recomendación 13: Un HBsAg indetectable en sangre y erradicación del ADN-VHB (ADNccc intrahepático y el ADN del VHB integrado) son necesarios para una curación completa. | 1 | III |
| Recomendación 14: La curación funcional del VHB debe definirse como la pérdida duradera del antígeno de superficie de la hepatitis B (HBsAg) con o sin seroconversión de HBsAg y ADN-VHB indetectable en sangre después de completar un curso de tratamiento. | 1 | II-B |
| Criterios de selección para iniciar terapia antiviral específica en pacientes con HBC | ||
| Recomendación 15: Se recomienda terapia antiviral en adultos con infección crónica por VHB en fase inmunoactiva (actualmente denominadas fases 2 y 4). | 1 | I-A |
| Recomendación 16: Los pacientes con HBC y cirrosis, ya sea compensada o descompensada, siempre deben recibir tratamiento antiviral específico ante cualquier concentración positiva del ADN-VHB, e independientemente de los niveles de ALT. | 1 | I-A |
| Seguimiento de pacientes con HBC que no ameritan iniciar tratamiento específico | ||
| Recomendación 17: La determinación de los niveles séricos del ADN-VHB, HBeAg y la edad son parámetros de consideración para realizar seguimiento en pacientes con infección crónica por VHB.En pacientes en fase inmunotolerante (fase 1), el seguimiento se recomienda cada 3 a 6 meses.En pacientes en fase de portador inactivo (fase 3), el seguimiento debe ser cada 3 meses en el primer año, y posteriormente cada 6 a 12 meses. | 1 | II-B |
| Recomendación 18: En pacientes con HBsAg+ se debe de considerar el riesgo de CHC, transmisión, reactivación y manifestaciones extrahepáticas, por lo cual se recomienda vigilancia estrecha. | 1 | II-B |
| Estrategias terapéuticas actuales, seguimiento y vigilancia de pacientes durante el tratamiento | ||
| Recomendación 19: El tratamiento antiviral de la hepatitis aguda por VHB solo está indicado en casos graves que cursan con datos de disfunción hepatocelular (hiperbilirrubinemia, coagulopatía) o criterios de insuficiencia hepática fulminante. | 1 | II-B |
| Recomendación 20: Los fármacos de primera elección en pacientes con HBC que cumplen criterios para iniciar tratamiento incluyen análogos nucleósidos (ETV) y análogos nucleótidos (TDF y TAF). | 1 | I-A |
| Recomendación 21: El tratamiento con IFNpeg alfa 2a puede ser una opción en un subgrupo de pacientes con la hepatitis crónica por VHB que cumplen criterios para iniciar tratamiento. | 2 | I-A |
| Coinfección VIH-VHB | ||
| Recomendación 22: En la actualidad, todas las personas con VIH y coinfección con VHB, deben recibir tratamiento antirretroviral estándar, que incluya de forma preferente en el esquema TDF o TAF+FTC o 3-TC. | 1 | I-A |
| Recomendación 23: En pacientes coinfectados VIH-VHB, en quienes no se puede usar TDF o TAF (tasa de filtración glomerular <50 o <30 ml/min, respectivamente), adicional al esquema antirretroviral, se recomienda el uso de ETV, siempre y cuando no hayan sido expuestos previamente a 3-TC o FTC en esquemas sin TDF o TAF. | 1 | I-A |
| Coinfección VHC-VHB | ||
| Recomendación 24: Pacientes con VHC que están coinfectados con VHB, tienen riesgo de reactivación del VHB al recibir tratamiento con AAD. | 1 | II-B |
| Recomendación 25: En pacientes coinfectados VHC-VHB que presentan HBsAg+, y que iniciarán tratamiento específico con AAD contra el VHC, debe considerarse también iniciar profilaxis con análogos nucleós(t)idos para prevenir la reactivación del VHB. | 2 | II-B |
| Recomendación 26: En pacientes HBsAg— y anti-HBc+ el riesgo de reactivación es bajo, por tanto, en estos pacientes se considera suficiente monitorizar las cifras de ALT durante y 12 semanas postratamiento con AAD. | 1 | II-B |
| Coinfección VHB-VHD | ||
| Recomendación 27: Se recomienda realizar determinación de anti-VHD en pacientes con HBsAg+ que presentan factores de riesgo para adquirir y padecer concomitantemente infección por VHD. | 1 | III |
| Recomendación 28: El tratamiento con IFNpeg alfa es el único tratamiento aprobado para tratar pacientes con coinfección VHB-VHD sin cirrosis y con cirrosis compensada, durante 48 semanas. | 1 | I-A |
| Cirrosis descompensada | ||
| Recomendación 29: Los pacientes con cirrosis descompensada y HBC deben recibir tratamiento con análogos nucleós(t)idos con alta barrera a la resistencia de forma prioritaria y por tiempo indefinido, independientemente de las cifras de ALT, del estatus del HBeAg y de la carga viral del ADN-VHB; además deben ser considerados para ser incluidos en un programa de trasplante hepático. | 1 | II-B |
| Recomendación 30: TAF puede utilizarse como una alternativa terapéutica contra el VHB en pacientes con cirrosis descompensada con alto riesgo de deterioro en la función renal o con alto riesgo de deterioro óseo. | 1 | III |
| Manejo postrasplante hepático, renal y de otros órganos sólidos | ||
| Recomendación 31: Los pacientes post trasplantados de hígado deben continuar el tratamiento con análogos nucleós(t)idos (TDF, TAF o ETV)+HBIG con el fin de evitar la recidiva de la HBC. | 1 | II-A |
| Recomendación 32: En pacientes post trasplantados de riñón u otro órgano sólido no hepático, la profilaxis o tratamiento del VHB debe individualizarse de acuerdo al estatus del HBsAg y del anti-HBc. | 1 | II-B |
| Riesgo de reactivación en pacientes bajo tratamiento inmunosupresor o citotóxico | ||
| Recomendación 33: Existe riesgo de reactivación del VHB en pacientes que se encuentran inmunocomprometidos o que reciben terapia citotóxica o inmunosupresora. | 1 | II-B |
| Recomendación 34: En pacientes con riesgo moderado a alto de reactivación del VHB debe indicarse profilaxis con análogos nucleós(t)idos con alta barrera a la resistencia. | 1 | II-B |
| Embarazo y lactancia | ||
| Recomendación 35: TDF es el único fármaco aprobado para tratar la hepatitis B en la mujer embarazada. | 1 | I-A |
| Recomendación 36: A todo recién nacido de madre portadora de infección activa por el VHB (HBsAg+), debe administrarse HBIG y vacuna anti-VHB antes de las primeras 12h posteriores al nacimiento. | 1 | I-A |
| Recomendación 37: La profilaxis antiviral con TDF debe comenzar en HBsAg+ mujeres embarazadas altamente virémicas a principios del tercer trimestre para evitar la transmisión vertical del VHB. | 1 | I-A |
| Recomendación 38: La lactancia materna no está contraindicada en mujeres con la hepatitis B. | 2 | III |
| Enfermedad renal y ósea | ||
| Recomendación 39: ETV se prefiere en pacientes con enfermedad renal u ósea establecida, o en aquellos que tienen factores de alto riesgo para deterioro de función renal u ósea. | 1 | II-B |
| Recomendación 40: TAF se prefiere en pacientes con enfermedad renal u ósea establecida, o en aquellos que tienen factores de alto riesgo para deterioro de función renal u ósea. | 1 | I-A |
AAD: agentes antivirales de acción directa; ADNccc: ácido desoxirribonucleico circular cerrado de forma covalente; ADN-VHB: ácido desoxirribonucleico del virus de la hepatitis B; anti-HBc: anticuerpos contra el antígeno del core; anti-HBe: anticuerpos contra el antígeno e; AFP: alfafetoproteína; ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; CHC: carcinoma hepatocelular; ETV: entecavir; FA: fosfatasa alcalina; FTC: emtricitabina; HBC: hepatitis B crónica; HBeAg: antígeno e del virus de la hepatitis B; HBIG: inmunoglobulina anti-hepatitis B; HBsAg: antígeno de superficie del virus de la hepatitis B; IFNpeg: interferón pegilado; TAF: tenofovir alafenamida; 3-TC: lamivudina; TDF: tenofovir disoproxil fumarato; VHB: virus de la hepatitis B; VHC: virus de la hepatitis C; VHD: virus de la hepatitis D; VIH: virus de inmunodeficiencia humana.
En noviembre de 2019, la AMH presidida por la Dra. Graciela Elia Castro Narro; y como Coordinador General de Consensos y Guías Clínicas de la AMH, el Dr. José Antonio Velarde Ruíz Velasco, tomó la iniciativa de designar a dos profesionales expertos (la Dra. Fátima Higuera-de-la-Tijera [FHT] y el Dr. Juan Francisco Sánchez Ávila [JFSA]) para fungir como coordinadores de la Guía Clínica de la Hepatitis B y cuyas funciones fueron: 1) Realizar una búsqueda exhaustiva de la literatura en las siguientes bases de datos: Pubmed, Embase, Medline, Trip Database, Clinical Evidence y Cochrane Library con el fin recopilar toda la información actualizada y relevante, y 2) Se conformó un panel de expertos, que fueron divididos según su área de mayor experiencia en una de 4 diferentes mesas de trabajo que se encargaron de elaborar los diferentes enunciados y recomendaciones; así como de calificar la evidencia existente mediante el sistema Grading of Recommendations Assessment, Development, and Evaluation (GRADE) (tabla 2)3.
Grado de recomendación y grado de evidencia (GRADE modificado)
| Grado de recomendación | |
| 1 | Fuerte a favor de la intervención: influyen en la fuerza de recomendación la calidad de la evidencia, de la cual derivan resultados importantes positivos para el paciente o para costos. |
| 2 | Débil a favor de la intervención: variabilidad en preferencias y valores, o incertidumbre. Poca evidencia o de baja calidad que demuestre beneficio al paciente, o requiere altos costos o consumo de recursos |
| Grado de evidencia | |
| I-A | Ensayos clínicos controlados, aleatorizados |
| II-A | Ensayos clínicos sin aleatorización |
| II-B | Estudios observacionales: cohortes o casos y controles |
| II-C | Estudios observacionales: series de casosExperimentos no controlados |
| III | Opinión de expertos |
Fuente: Manterola et al.3.
La seroprevalencia en México oscila entre el 0.47 y el 0.15% según un reporte del Centro Nacional de la Transfusión Sanguínea, en donde se evaluaron entre 2000 y 2012, respectivamente, un total de 19,096,294 reportes de sujetos que acudieron a donar sangre en diferentes regiones del país, siendo los estados con mayor prevalencia reportada Aguascalientes, Campeche, Chiapas, Ciudad de México, Durango, Estado de México, Hidalgo, Nayarit, Puebla, San Luis Potosí, Sinaloa, Sonora, Tabasco y Veracruz4. Se han descrito dentro del país zonas de alta endemicidad en comunidades indígenas. Estudios epidemiológicos en México han estimado que en el país podría haber por lo menos tres millones de personas adultas que han adquirido la hepatitis B (anticuerpo anti-antígeno central del VHB [anti-HBc] positivo), de ellos cerca de 300,000 portadores activos (antígeno de superficie del VHB [HBsAg] positivo) podrían requerir tratamiento. No obstante, si consideramos a la población indígena como zona de alta endemia, entonces el número de pacientes que se han infectado podría aumentar hasta 7 u 8 millones de mexicanos y a alrededor de un millón de portadores crónicos activos. Incluso se ha postulado que, de confirmarse esta situación, la infección por VHB podría afectar a un número mayor de personas, que el virus de la hepatitis C (VHC) en México5.
Según su divergencia genómica, el VHB se clasifica en 8 genotipos, designados con las letras A-H, información reciente sugiere la existencia de genotipos I y J. Una característica de la infección por el VHB es que existe heterogeneidad en la distribución geográfica de los genotipos del virus a nivel mundial. Los genotipos B y C están mayormente confinados al continente asiático, el A y D a Europa y EE. UU.. El genotipo H es predominante en México, mientras que el genotipo F prevalece en América Central y del Sur. La población mexicana nativa o mestiza muestra predominio del genotipo H, seguido de genotipos A, D y G6–9.
Es probable que se detecte el genotipo A en infecciones agudas asociada a altas cargas virales; por el contrario, el genotipo D se manifiesta a niveles muy bajos o indetectables. La progresión de la infección crónica ocurre principalmente entre mestizos adultos a través de transmisión horizontal y, en menor grado, en niños por transmisión vertical10.
Recientemente, en un análisis de grupos nativos mexicanos, se han informado diferencias en niveles de citocinas en el suero que pueden distinguir pacientes infectados con el genotipo H de pacientes que resolvieron la infección. El papel de los genotipos del VHB en la progresión de la infección no ha sido totalmente esclarecido. Sin embargo, se acepta que los genotipos A y D del VHB se asocian con bajo riesgo a desarrollar complicaciones por la infección, mientras que los B, C y F están estrechamente asociados con alto riesgo a desarrollar carcinoma hepatocelular (CHC). En general, la cirrosis hepática y el CHC asociado con la infección por VHB no ocurren con frecuencia en poblaciones nativas en México, incluso en comparación con el resto de América Latina, lo cual puede sugerir que los factores genéticos y ambientales también pueden modular el grado de adaptación a la infección por este virus. Finalmente, un aspecto importante a considerar es la utilidad de la detección de los genotipos virales con el objeto de evaluar el progreso y severidad de la infección, así como la respuesta al tratamiento10–12.
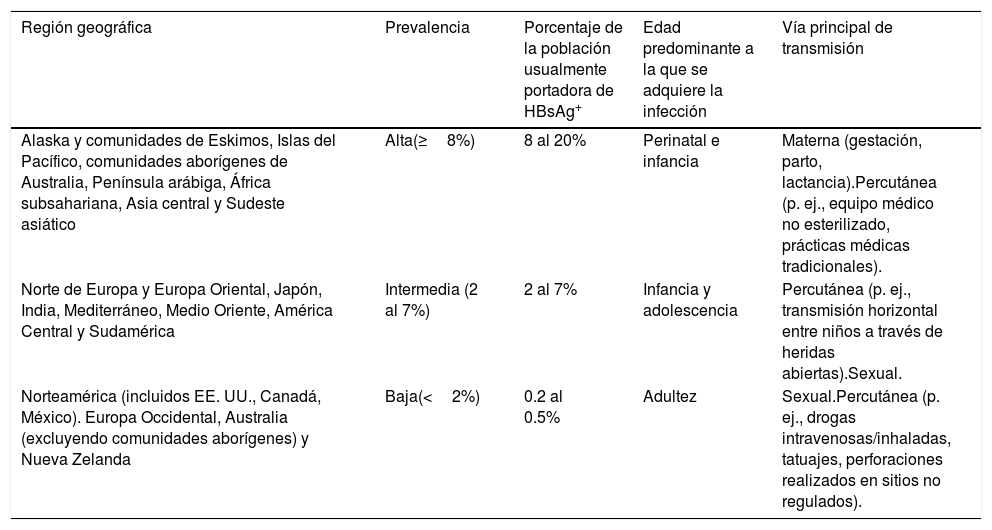
I. Grupos de riesgo y formas de transmisiónEl VHB se transmite principalmente por vía percutánea, contacto sexual o perinatal; la forma en la que se adquiere la infección por el VHB es determinante de la endemicidad de esta enfermedad crónica en una determinada población, siendo de mayor riesgo para determinar alta prevalencia cuando la infección se adquiere entre la comunidad en edades tempranas de la vida13 (tabla 3).
Variación geográfica en la prevalencia de la hepatitis B y vías principales de transmisión
| Región geográfica | Prevalencia | Porcentaje de la población usualmente portadora de HBsAg+ | Edad predominante a la que se adquiere la infección | Vía principal de transmisión |
|---|---|---|---|---|
| Alaska y comunidades de Eskimos, Islas del Pacífico, comunidades aborígenes de Australia, Península arábiga, África subsahariana, Asia central y Sudeste asiático | Alta(≥8%) | 8 al 20% | Perinatal e infancia | Materna (gestación, parto, lactancia).Percutánea (p. ej., equipo médico no esterilizado, prácticas médicas tradicionales). |
| Norte de Europa y Europa Oriental, Japón, India, Mediterráneo, Medio Oriente, América Central y Sudamérica | Intermedia (2 al 7%) | 2 al 7% | Infancia y adolescencia | Percutánea (p. ej., transmisión horizontal entre niños a través de heridas abiertas).Sexual. |
| Norteamérica (incluidos EE. UU., Canadá, México). Europa Occidental, Australia (excluyendo comunidades aborígenes) y Nueva Zelanda | Baja(<2%) | 0.2 al 0.5% | Adultez | Sexual.Percutánea (p. ej., drogas intravenosas/inhaladas, tatuajes, perforaciones realizados en sitios no regulados). |
HBsAg+: antígeno de superficie del virus de la hepatitis B positivo.
Fuente: Croagh et al.13.
Recomendación 1: Toda persona con factores de riesgo mayores para adquirir o haber adquirido en el pasado infección por el VHB, debe someterse a pruebas serológicas de escrutinio
- •
Grado de recomendación: 1; Grado de evidencia: II-B
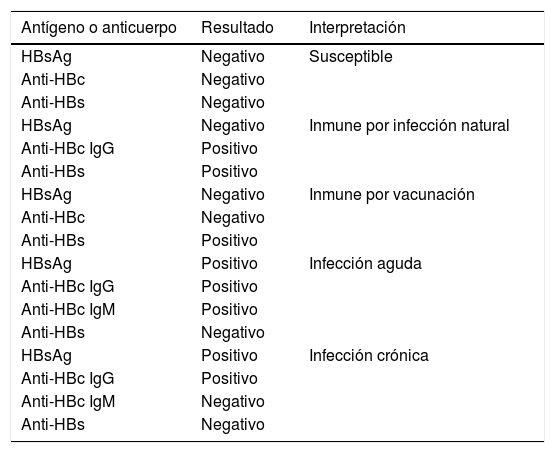
Se consideran grupos de riesgo: Personas inmigrantes provenientes de países con endemicidad intermedia a alta, usuarios activos o con historia de drogas intravenosas o inhaladas, hombres que tienen sexo con hombres, personas que viven con virus de inmunodeficiencia humana (VIH), pacientes con VHC, personas que van a recibir por cualquier motivo terapia inmunosupresora o citotóxica, terapia biológica, en protocolo de trasplante de órgano sólido o hematopoyético, pacientes con enfermedad renal crónica, pacientes en hemodiálisis o diálisis peritoneal, hemofílicos, donadores de sangre, semen o cualquier órgano o tejido, embarazadas, recién nacidos de madres portadoras del VHB, pacientes con elevación de alanina aminotransferasa (ALT) o aspartato aminotransferasa (AST) sin otra causa obvia, personas con enfermedad hepática crónica, parejas sexuales de personas portadoras del VHB, personas con múltiples parejas sexuales, personal de salud, personal de laboratorio o con riesgo ocupacional por exposición a sangre y fluidos, personas privadas de su libertad, antecedente de compartir punzocortantes, realización de tatuajes, perforaciones o procedimientos cosméticos desconociendo si se utilizaron agujas estériles, personas no vacunadas o que desconocen si alguna vez fueron vacunadas14. En estos grupos de alto riesgo, se debe efectuar escrutinio de infección por el VHB solicitando la determinación del HBsAg, que es el marcador de infección activa; anticuerpos contra el HBsAg (anti-HBs) y anti-HBc total, que en conjunto permiten discriminar entre un sujeto expuesto al VHB de aquel inmune por vacunación. La interpretación de la serología del VHB se muestra en la tabla 4. La presencia de HBsAg+ antes de 6 meses se considera infección aguda, cuando este persiste positivo más allá de 6 meses se dice que la infección por VHB es crónica, adicionalmente la presencia de anti-HBc de tipo inmunoglobulina M (IgM) apoya el diagnóstico de infección aguda15.
Interpretación de la serología del virus de la hepatitis B
| Antígeno o anticuerpo | Resultado | Interpretación |
|---|---|---|
| HBsAg | Negativo | Susceptible |
| Anti-HBc | Negativo | |
| Anti-HBs | Negativo | |
| HBsAg | Negativo | Inmune por infección natural |
| Anti-HBc IgG | Positivo | |
| Anti-HBs | Positivo | |
| HBsAg | Negativo | Inmune por vacunación |
| Anti-HBc | Negativo | |
| Anti-HBs | Positivo | |
| HBsAg | Positivo | Infección aguda |
| Anti-HBc IgG | Positivo | |
| Anti-HBc IgM | Positivo | |
| Anti-HBs | Negativo | |
| HBsAg | Positivo | Infección crónica |
| Anti-HBc IgG | Positivo | |
| Anti-HBc IgM | Negativo | |
| Anti-HBs | Negativo |
anti-HBc: anticuerpo contra el antígeno central del virus de la hepatitis B; anti-HBs: anticuerpo contra el antígeno de superficie del virus de la hepatitis B; HBsAg: antígeno de superficie del virus de la hepatitis B; IgG: inmunoglobulina G; IgM: inmunoglobulina M.
Recomendación 2: La estrategia más efectiva para lograr la eliminación de la transmisión del VHB, es la vacunación universal
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Desde 1991 la OMS recomendó la incorporación de las vacunas anti-VHB en los programas de salud. En México, desde 1999 se incorporó la vacuna anti-VHB al esquema de inmunizaciones16, y actualmente se recomienda la vacunación universal, estrategia que ha demostrado reducir dramáticamente la transmisión del VHB en diferentes poblaciones en las que se ha implementado. Todas las personas nacidas antes de 1999 que no han recibido la vacuna y todos aquellos que por cualquier motivo no fueron vacunados al nacimiento, deben también recibir el esquema de vacunación4,17.
II. Fases de la infección crónica- •
La infección crónica por el VHB es un proceso dinámico con fases replicativas y no replicativas, actividad que depende de una interacción entre el virus y el huésped
La interacción entre el virus y el huésped depende de muchos factores, como son la edad del paciente al adquirir la infección, los factores víricos (genotipo, mutaciones víricas y nivel de replicación), los factores del huésped (género, edad y estado inmunológico), los factores exógenos (consumo de alcohol) y la coinfección con otros virus hepatotropos o no hepatotropos; p. ej., el VHC o el VIH18,19.
En la infección aguda en vías de resolución existe aclaramiento viral con expresión de citocinas e inducción de linfocitos B productores de anticuerpos neutralizantes, los cuales erradican el virus del suero. Sin embargo, existe la posibilidad en pacientes con la hepatitis B resuelta de que ocurra reactivación. Esta reactivación puede ocurrir de manera espontánea, pero ocurre con mayor frecuencia en pacientes con inmunosupresión severa como puede ser aquellos que se encuentran recibiendo terapias inmunosupresoras, que padecen inmunodeficiencias adquiridas y aquellos postrasplantados19,20.
- •
La historia natural de la infección crónica por el VHB, se ha dividido en 5 fases las cuales toman en cuenta las características serológicas de la hepatitis B, la carga viral (ácido desoxirribonucleico del VHB [ADN-VHB]), la positividad o la negatividad del antígeno e del VHB (HBeAg), las cifras de ALT y los hallazgos histológicos en la biopsia hepática
Fase 1: Infección crónica por el VHB con HBeAg+(antes conocida como «fase inmunotolerante»). Se caracteriza por la presencia de HBeAg, niveles elevados de ADN-VHB, cifras de ALT normales con inflamación y fibrosis mínima o ausente en la biopsia hepática21,22.
Fase 2: Hepatitis B crónica (HBC) con HBeAg+(antes «fase inmunoactiva» con HBeAg+). Los pacientes en esta fase tienen HBeAg+, con niveles elevados de ADN-VHB, elevación de ALT y evidencia de inflamación y necrosis en la biopsia hepática con progresión acelerada de la fibrosis21,22.
Fase 3: Infección crónica por el VHB con HBeAg—(antes «portador inactivo»). En esta fase los pacientes tienen anticuerpos contra el HBeAg (anti-HBe) positivos, la carga viral del ADN-VHB generalmente es indetectable o baja (<2,000UI/ml) y la ALT se encuentra cercana a la normalidad (alrededor de 40UI/l). Las características histológicas típicas en esta fase son actividad necroinflamatoria leve con mínima fibrosis y el riesgo de progresión de la enfermedad es bajo. En esta fase se han reportado niveles bajos <1000UI/ml del HBsAg y puede ocurrir pérdida espontánea de dicho antígeno con seroconversión entre 1 a 3% de los casos anualmente21,22.
Fase 4: HBC con HBeAg—(antes «fase inmunoactiva» con HBeAg—). Estos pacientes se caracterizan por ausencia en suero de HBeAg, generalmente con anti-HBe+, pero con niveles elevados y fluctuantes del ADN-VHB y de ALT. La biopsia muestra actividad necroinflamatoria y fibrosis importantes. Estos pacientes poseen mutaciones en la región del precore o en la región del promotor basal del core que impiden la expresión del HBeAg21,22.
Fase 5: «Infección oculta». Los pacientes en esta fase tienen HBsAg—, con anti-HBc+, con o sin presencia de anti-HBs. Estos pacientes tienen ALT normal, y en la mayoría de los casos ADN-VHB indetectable. La pérdida del HBsAg antes del desarrollo de cirrosis es un factor de buen pronóstico22.
III. Escrutinio y vigilancia del desarrollo de carcinoma hepatocelularEl CHC es la neoplasia maligna más frecuente del hígado, es la cuarta causa de muerte relacionada a cáncer en todo el mundo, es el quinto cáncer más frecuente en los varones y el noveno cáncer más frecuente en las mujeres. De acuerdo al reporte del Fondo Mundial de Investigación del Cáncer, del Instituto Americano para la Investigación del Cáncer, en 2018 hubo más de 840,000 nuevos casos23. Dentro de los factores de riesgo para el desarrollo de CHC, la HBC representa el 44% del total mundial de casos, la mayoría de estos casos se presentan en Asia, donde la prevalencia de HBC es elevada24. Otros factores de riesgo incluyen al VHC, aflatoxinas, tabaco, alcohol, enfermedades metabólicas como deficiencia de alfa-1-antitripsina, hemocromatosis, cirrosis. La evidencia señala también que la obesidad puede ser factor de riesgo25. La diabetes puede aumentar el riesgo de CHC independientemente del riesgo conferido solo por la obesidad26,27.
Recomendación 3: El estudio semestral con ultrasonido hepático y alfafetoproteína (AFP) sérica favorece la detección temprana del carcinoma hepatocelular y debe realizarse en todo paciente con infección crónica por el VHB, independientemente de la presencia de fibrosis avanzada o cirrosis
- •
Grado de recomendación:1; Grado de evidencia: II-B
Estudios moleculares han mostrado que la integración del ADN-VHB en el genoma del huésped causa inestabilidad genómica, que puede conducir a hepatocarcinogénesis28–30. La positividad del HBeAg está fuertemente asociada con el aumento de riesgo de CHC31. El nivel de la carga viral es otro factor fuertemente asociado al riesgo de desarrollo de CHC; en un estudio de Chen CJ et al., el nivel de ADN-VHB en suero >10,000 copias/ml (equivalente a >2,000UI/ml) se asoció con aumento del riesgo de CHC de forma independiente del HBeAg, de las cifras de ALT, o de la presencia de cirrosis32. Adicionalmente, Tseng TC et al., encontraron que semejante a la carga viral del ADN-VHB, los niveles de HBsAg también se asociaron con el desarrollo de CHC, en donde el riesgo de esta neoplasia aumentó significativamente con cifras del HBsAg>1,000UI/ml en pacientes con HBeAg— y viremia baja33.
En el estudio REVEAL-HBV se observó que los sujetos que tenían una carga viral inicial inferior a 2,000UI/ml tenían un riesgo bajo de CHC y los que tenían >20,000UI/ml tenían mayor riesgo32.
Entre los 10 genotipos del VHB, los genotipos C, D y F están asociados con mayor riesgo de desarrollar CHC. En estudios longitudinales se ha observado que el subtipo Ce es un factor de riesgo independiente para el desarrollo de CHC31,33,34.
La inflamación persistente que provoca el VHB antes del tratamiento, representada clínicamente por niveles altos de aminotransferasas e histológicamente por actividad necroinflamatoria es un detonante principal en el desarrollo de CHC35.
La determinación de AFP con un punto de corte >20ng/ml para diagnóstico de CHC posee una sensibilidad entre el 41-65% y una especificidad entre el 80-95%; sin embargo, hasta el 50% de los pacientes con CHC tienen AFP<20ng/ml y se pueden encontrar resultados falsos positivos relacionados a otras alteraciones hepáticas. Los valores de AFP>400ng/ml son mucho más específicos, pero menos sensibles para el diagnóstico de CHC36. Valores de AFP>1,000ng/ml son de mal pronóstico tanto para la resección hepática como para el trasplante hepático y están relacionados con alto riesgo de recurrencia37,38.
Con relación al ultrasonido hepático para la detección de CHC, Coli A et al., reportaron una sensibilidad del 60.5% (44-76%) y una especificidad del 96.9% (95-98%), cociente de probabilidad positivo 17.7 (8.5-36.9) y cociente de probabilidad negativo de 0.5 (0.4-0.6). La combinación de AFP y ultrasonido hepático pueden aumentar las tasas de detección, pero también los costos y falsos positivos39.
Las lesiones de menos de 1cm se deben vigilar con ultrasonido a los 3 meses, si la lesión persiste del mismo tamaño se repite el ultrasonido a los 3 meses, si crece se deben practicar otros estudios, semejante a cuando la lesión encontrada es de más de 1cm, en donde se indica tomografía dinámica de hígado o resonancia magnética40.
IV. Consejería respecto al consumo de alcohol, control de comorbilidades relacionadas al síndrome metabólico y necesidad de aplicar vacunas específicasRecomendación 4: En todos los pacientes portadores de infección por VHB, y en todas las fases de la enfermedad, se recomienda abstinencia en el consumo de alcohol
- •
Grado de recomendación: 1; Grado de evidencia: II-B
El consumo de alcohol en cantidad >60g/día en pacientes con HBC acelera la progresión de la enfermedad hepática a cirrosis y desarrollo de CHC41. Un estudio demostró que el riesgo relativo (RR) para progresión de la enfermedad hepática entre pacientes con HBC y consumo de alcohol concomitante fue de 6.3 (intervalo de confianza al 95% [IC 95%]: 3.1-12.8); además, el consumo de alcohol en pacientes con HBC en un seguimiento a 20 años, se asoció también con un incremento de 6 veces en el riesgo de muerte por cirrosis y CHC42. Respecto a si la ingesta de alcohol en baja a moderada cantidad en pacientes con HBC incrementa también este riesgo, existe controversia41. Sin embargo, un estudio de revisión sistemática y metaanálisis demostró que no existe una cantidad que pueda considerarse segura en cuanto al consumo de alcohol, ya que incluso cantidades tradicionalmente consideradas no riesgosas, se relacionaron en este estudio con desarrollo de enfermedad hepática tanto en hombres como en mujeres, lo que implica variabilidad individual de susceptibilidad al daño aunada a múltiples factores que pueden interrelacionar para favorecer el daño hepático asociado al consumo de alcohol43. Por lo anterior, es recomendable mantener estricta abstinencia de alcohol en pacientes con infección por VHB en todas las fases de la enfermedad.
Recomendación 5: En pacientes con infección crónica por el VHB se deben tratar y controlar comorbilidades relacionadas al síndrome metabólico
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Aunque la HBC no parece incrementar el riesgo de padecer síndrome metabólico, aterosclerosis ni diabetes tipo 244; e incluso algunos estudios sugieren que la presencia de infección por el VHB se asocia con reducción en el riesgo de padecer síndrome metabólico45; se sabe que la HBC incrementa per se el riesgo de desarrollar cirrosis y CHC; así mismo, el síndrome metabólico, una condición cada vez más prevalente, también incrementa el riesgo de CHC de forma independiente de la presencia de cirrosis46. Por tanto, es recomendable, que en todo paciente con infección crónica por VHB, se establezca el tratamiento y control de comorbilidades propias del síndrome metabólico.
Recomendación 6: A todos los pacientes con infección crónica por el VHB sin inmunidad previa contra la hepatitis A, se les recomienda recibir vacunación contra la misma
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Los pacientes con HBC que adquieren la hepatitis A aguda tienen un curso clínico más severo y una tasa de mortalidad más alta en comparación con los individuos sanos que adquieren la infección por la hepatitis A; adicionalmente, estas diferencias son más pronunciadas en pacientes de edad avanzada y en aquellos con evidencia histológica de hepatitis crónica o cirrosis, en comparación con portadores de VHB sin dichas condiciones. Las vacunas disponibles contra la hepatitis A tienen alta eficacia y seguridad, por lo que a los pacientes con infección crónica por el VHB se les recomienda verificar su estatus serológico respecto a la hepatitis A, y en caso de no tener anticuerpos anti-hepatitis A se debe indicar la vacunación específica47.
V. Estudios para realizar la evaluación inicial del paciente con infección crónica por el virus de la hepatitis BRecomendación 7: Todo paciente con infección crónica por el VHB requiere conocer su estatus respecto del HBeAg y del anti-HBe, además de la determinación del ADN-VHB (carga viral) con la finalidad de establecer un pronóstico y guiar el tratamiento
- •
Grado de recomendación: 1; Grado de evidencia: I-A
El ADN-VHB en suero o plasma debe cuantificarse mediante tecnología de reacción en cadena de la polimerasa (PCR); por ejemplo, el ensayo «Abbott Real Time HBV» utiliza la tecnología de PCR junto con la detección de fluorescencia homogénea en tiempo real para la cuantificación del ADN-VHB. La selección de una región altamente conservada en el gen que codifica el HBsAg permite la detección de los genotipos A-H. La localización de la región diana en el tercio N terminal del gen de superficie garantiza que el ensayo no se vea afectado por los mutantes YMDD, los mutantes de escape del HBsAg o los mutantes resistentes a los fármacos, ya que esta región es imprescindible para la unión y secreción de partículas subvíricas y tolera solo cambios estructurales mayores. Los resultados pueden ser reportados en UI/ml o log UI/ml, o bien copias/ml o log copias/ml. El factor de conversión es 1UI: 3.41 copias. El intervalo lineal del análisis es de 10 a 1 billónUI/ml48.
La positividad del HBeAg generalmente indica replicación viral activa; este marcador, aunado a niveles séricos elevados de ADN-VHB, se relacionan con incremento en el riesgo de desarrollar cirrosis, descompensación y CHC31,32,49. Por tanto, la seroconversión al anticuerpo anti-antígeno e positivo (anti-HBe+) es uno de los objetivos del tratamiento, lo cual suele lograrse entre el 20 y el 30% de los pacientes HBeAg+50.
Dentro de las mutaciones más comunes en el VHB se encuentran las mutaciones en el precore y en el promotor del core basal específico, las cuales se asocian con reducción o abolición de la producción de HBeAg, respectivamente, estas mutaciones emergen de forma tardía en el curso de la historia natural de la enfermedad, en la fase inmunorreactiva de seroconversión del HBeAg51; al ser cambios tardíos en el curso de la HBC, estas mutaciones se relacionan con presencia establecida de fibrosis avanzada o cirrosis al momento del diagnóstico; así como, riesgo de flares de necroinflamación, descompensación y mayor riesgo de CHC52–55.
Los niveles séricos del HBsAg reflejan el ácido desoxirribonucleico circular covalentemente cerrado (ADNccc) activo, y tienen valor como marcador de eficacia durante el tratamiento56. Niveles séricos basales bajos de HBsAg (<1,000UI/ml); así como, una mayor disminución de los niveles séricos de HBsAg durante el tratamiento, tienen valor para predecir el seroaclaramiento del HBsAg57, particularmente en pacientes tratados con interferón pegilado (IFNpeg), ya que en pacientes tratados con análogos nucleós(t)idos (NA), el valor de cuantificar los niveles de HBsAg es incierto; por ello, en la práctica clínica, la cuantificación sérica del HBsAg no sustituye a la cuantificación del ADN-VHB58.
El VHB se caracteriza por una alta heterogeneidad genética ya que se replica a través de una transcriptasa inversa que carece de capacidad de corrección. Hasta ahora, se han descrito 10 genotipos (A-J). En general, el genotipo A se asocia con una mejor respuesta al tratamiento con INFpeg; el genotipo C, y en menor medida el B, generalmente representan un factor de riesgo de infección perinatal y se asocian con enfermedad hepática avanzada, cirrosis y CHC; el genotipo D está relacionado con respuesta deficiente al tratamiento con INFpeg. Por tanto, la determinación del genotipo puede jugar un papel pronóstico en pacientes que van a ser tratados con INFpeg, pero fuera de este escenario, la determinación del genotipo no se considera indispensable dentro del protocolo de estudio pre-tratamiento de los pacientes con HBC58.
Recomendación 8: Evaluar la severidad de la enfermedad hepática requiere además del examen físico, de pruebas bioquímicas, particularmente de ALT y de ultrasonido hepático
- •
Grado de recomendación: 1; Grado de evidencia: I-A
La elevación de ALT sérica es el marcador indirecto de necroinflamación más utilizado en pacientes con HBC, es uno de los parámetros más importantes a tener en cuenta para definir cuándo se requiere inicio del tratamiento; así como para la monitorización durante el mismo. Debido a la variabilidad que puede existir en los valores considerados como normales, se recomienda tomar como punto de corte para definir el límite superior normal (LSN) de ALT 30U/l en varones y 19U/l en mujeres59.
La realización de ultrasonido hepático basal es obligatoria, independientemente de la presencia y grado de fibrosis o cirrosis, pues permite evaluar la morfología hepática y forma parte del escrutinio de lesiones tempranas de CHC ante el riesgo elevado que representa la HBC para el desarrollo de esta neoplasia40.
Recomendación 9: La presencia y el grado de fibrosis hepática puede determinarse por métodos no invasivos radiológicos
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Los métodos radiológicos han demostrado mejor exactitud que los métodos serológicos para la clasificación del grado de fibrosis en pacientes con HBC, ya que no parecen modificarse de forma tan marcada como los serológicos en función de las cifras de transaminasas60.
Dentro de los métodos radiológicos, la elastografía de transición (ET) es el método más validado y, por tanto, el preferido61. Un estudio de metaanálisis demostró que este método presenta buena exactitud para clasificar el grado de fibrosis en pacientes con HBC; en comparación con la biopsia, la sensibilidad global de la ET para estadificar fibrosis significativa (≥F2), fibrosis avanzada (≥F3) y cirrosis (F4) fue 0.806 (IC 95%: 0.756-0.847), 0.819 (IC 95%: 0.748-0.874) y 0.863 (IC 95%: 0.818-0.898), respectivamente; la especificidad global fue 0.824 (IC 95%: 0.761-0.873), 0.866 (IC 95%: 0.824-0.899) y 0.875 (IC 95%: 0.840-0.903), respectivamente. Las áreas bajo la curva correspondientes fueron 0.88 (IC 95%: 0.85-0.91), 0.91 (IC 95%: 0.88-0.93) y 0.93 (IC 95%: 0.91-0.95), respectivamente62.
La elastografía bidimensional de onda de corte (2D-SWE) ha presentado exactitud semejante a la ET. El método más exacto de todos parece ser la elastografía por resonancia magnética (eRM), que ha resultado superior a la 2D-SWE23. Además de estadificar el grado de fibrosis con excelente exactitud (áreas bajo la curva para caracterizar fibrosis leve [≥F1], ≥F2, ≥F3 y F4, de 0.961, 0.986, 1.000 y 0.998, respectivamente); la eRM ha demostrado ser útil para estimar el grado de necroinflamación: leve (≥A1), moderada (≥A2) y severa (A3), con áreas bajo la curva de 0.806, 0.834, y 0.906, respectivamente; lo que permite una mejor caracterización del daño hepático, ya que la presencia y grado de necroinflamación es un factor relevante que sobrestima el grado de fibrosis63,64. Estos hallazgos requieren ser validados, ya que existen pocos estudios con eRM en el contexto de pacientes con HBC.
Recomendación 10: La presencia y el grado de fibrosis hepática puede determinarse por métodos no invasivos serológicos
- •
Grado de recomendación: 2; Grado de evidencia: II-B
Los marcadores serológicos han resultado ser inexactos en el contexto del paciente con HBC debido a que la elevación de las transaminasas es un factor que puede sobreestimar importantemente el grado de fibrosis al utilizar estos biomarcadores. Dentro de los marcadores serológicos más estudiados en pacientes con HBC se encuentran el AST to Platelet Ratio Index (APRI) y el Fibrosis-4 (FIB4), la mayoría de los estudios realizados concuerdan en que en pacientes con HBC son poco exactos. En un estudio donde se comparó el desempeño del APRI y del FIB4 versus el estadio de fibrosis de Ishak por biopsia; la mayoría (81-89%) de los pacientes con fibrosis avanzada o cirrosis no fueron detectados correctamente por ninguno de estos índices. Igualmente, el 71% de los pacientes sin fibrosis fueron incorrectamente clasificados como pacientes con fibrosis significativa o mayor. Además, tanto el APRI como el FIB4 aplicados a la semana 240 posterior al tratamiento infraestimaron el estadio de la fibrosis, lo que demuestra que la disminución de la necroinflamación asociada al tratamiento modifica estos índices, pero no hubo correlación entre ellos y el reporte de biopsia65.
El cociente GGT/plaquetas (GPR), el índice Lok, el índice de Forns, el sistema de puntuación de fibrosis hepática para HBC antígeno-e positivo (del inglés: e-antigen-positive CHB liver fibrosis [EPLF] scoring system) han sido comparados en diversos estudios con el APRI y el FIB4; sin embargo, no ha logrado demostrar de forma contundente ser más exactos para identificar la presencia y el grado de fibrosis en HBC66–69.
Wang J, et al. desarrollaron un nuevo modelo basado en el recuento plaquetario (PLT), la desviación estándar del ancho de distribución eritrocitaria (RDW-SD), la fosfatasa alcalina (FA) y la globulina sérica al que denominaron índice APRG, que son las siglas en inglés de cada componente del modelo. Las áreas bajo la curva del índice APRG para predecir ≥F2, ≥F3 y F4 fueron 0.757 (IC 95%: 0.699-0.816), 0.763 (IC 95%: 0.711-0.816) y 0.781 (IC 95%: 0.728-0.835), respectivamente. En este estudio, el índice APRG resultó superior a otros como el APRI, FIB4, GPR, cociente RDW/PLT, cociente AST/ALT, para predecir fibrosis significativa, avanzada y cirrosis. Sin embargo, no parece ser mejor que los métodos no invasivos radiológicos de acuerdo a las áreas bajo la curva reportadas en este estudio y, por tanto, por el momento no puede recomendarse70.
Respecto a los métodos serológicos comerciales, un metaanálisis evaluó el desempeño del FibroTest en comparación con la biopsia hepática para determinar el grado de fibrosis en pacientes con HBC, este estudio demostró que el FibroTest tiene mayor valor diagnóstico para excluir la presencia de cirrosis en pacientes con HBC, pero tiene una exactitud subóptima cuando se trata de detectar fibrosis significativa y cirrosis, en donde el área bajo la curva fue de 0.84 (IC 95%: 0.78-0.88)71.
Los métodos serológicos no invasivos se recomiendan solo como alternativa cuando no se dispone de métodos radiológicos para evaluar el grado de fibrosis en pacientes con HBC. Así mismo, los métodos serológicos pueden agregar valor diagnóstico al combinarse con un método no invasivo radiológico, pues esta estrategia incrementa la exactitud diagnóstica para determinar la presencia y el grado de fibrosis72.
Recomendación 11: La biopsia hepática será necesaria para establecer la presencia y el grado de fibrosis hepática cuando los métodos no invasivos no hayan resultado concluyentes
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Todos los métodos no invasivos son más precisos para descartar que para confirmar la presencia de fibrosis avanzada o cirrosis. En presencia de factores confusores, como en pacientes con HBC con niveles elevados de ALT, y en presencia de inflamación importante, el grado de fibrosis puede ser sobrestimado. Cuando los métodos no invasivos no son concluyentes debe recurrirse a la biopsia hepática como método para evaluar la presencia y el grado de fibrosis73.
La biopsia hepática sigue considerándose el estándar de oro para evaluar el grado de daño en pacientes con infección por VHB, es diversa y refleja la historia natural de la infección. El error de muestreo es el problema más importante que conduce a subestimar el grado de fibrosis. Una biopsia hepática adecuada debe contar con 11 tractos portales y una longitud de al menos 1.5 a 2.0cm, y no presentar fragmentación, las agujas de corte parecen superiores a las de succión al momento de realizar el procedimiento74.
VI. Objetivos del tratamiento de la hepatitis B crónicaRecomendación 12: Los objetivos primordiales en el tratamiento de pacientes con la hepatitis B crónica son la prevención del desarrollo de cirrosis, la descompensación hepática, el carcinoma hepatocelular y la muerte relacionada a causa hepática
- •
Grado de recomendación: 1; Grado de evidencia: II-B
La HBC es la principal causa de morbimortalidad relacionada con el hígado a nivel global75. No tratar esta enfermedad conlleva un riesgo elevado de progresión a cirrosis (>40%), descompensación (ascitis, hemorragia variceal, encefalopatía); así como, riesgo de desarrollo de CHC, al respecto un estudio demostró que hasta el 30% de los pacientes con cirrosis por HBC desarrollaron CHC durante un seguimiento a 10 años. Además, en pacientes con HBC también puede desarrollarse hepatocarcinoma en ausencia de cirrosis (10% de los casos en una cohorte que incluyó 8,539 pacientes)76. Un ADN-VHB elevado en suero está asociado de manera significativa con el desarrollo de insuficiencia hepática, cirrosis y CHC, haciendo que la terapia antiviral sea crucial para modificar la historia natural de la HBC75.
Recomendación 13: Un HBsAg indetectable en suero y erradicación del ADN-VHB (ADNccc intrahepático y el ADN del VHB integrado) son necesarios para una curación completa
- •
Grado de recomendación: 1; Grado de evidencia: III
El objetivo primordial del tratamiento de cualquier infección crónica es la erradicación del agente infeccioso, idealmente antes de que cause un daño irreversible. Si bien, hablando de HBC, en la actualidad no podemos lograr la erradicación viral, la supresión completa del virus sí se logra eventualmente con los tratamientos hoy en día disponibles77.
El desarrollo de nuevas terapias tiene por objetivo justamente el lograr la cura del VHB, es decir, la eliminación del virus, lo que permitiría en un futuro, detener el tratamiento sin riesgo de recaída virológica y sin riesgo de progresión de la enfermedad hepática. Sin embargo, una verdadera cura podría no ser factible porque el ADN-VHB está integrado en el genoma del huésped; incluso entre las personas que se han recuperado del VHB agudo, se puede detectar ADN circular cerrado de forma covalente viral (ADNccc) en el hígado, lo que explica la reactivación de la replicación del VHB cuando estas personas «recuperadas» están profundamente inmunodeprimidas78,79.
Recomendación 14: La curación funcional del VHB debe definirse como la pérdida duradera del antígeno de superficie de la hepatitis B (HBsAg) con o sin seroconversión de HBsAg y ADN-VHB indetectable en sangre después de completar un curso de tratamiento
- •
Grado de recomendación: 1; Grado de evidencia: II-B
En la actualidad se proponen 3 definiciones de cura en el contexto de infección por VHB:
- 1.
Curación completa: HBsAg indetectable en sangre y erradicación del ADN-VHB, incluido el ADNccc intrahepático y el ADN-VHB integrado.
- 2.
Curación funcional: ADN-VHB y HBsAg indetectables de manera sostenida en suero con o sin seroconversión al anti-HBs después de completar un curso finito de tratamiento, resolución de daño hepático residual y una disminución en el riesgo de CHC a lo largo del tiempo.
- 3.
Curación parcial: HBsAg detectable, pero ADN-VHB persistentemente indetectable en suero después de completar un curso finito de tratamiento78.
Recientemente se ha publicado un documento sobre los criterios de valoración del tratamiento para guiar los ensayos clínicos con el objetivo de «curar» el VHB. Este panel de expertos sugiere que el objetivo primario de los ensayos de fase 3 debe ser la cura funcional; esto es una pérdida de HBsAg en ≥30% de los pacientes involucrados en los estudios; y, por otro lado, la supresión virológica sostenida (ADN-VHB en suero indetectable) sin pérdida de HBsAg 6 meses después de la interrupción del tratamiento sería un objetivo intermedio. Finalmente, la mayoría de los participantes estuvo de acuerdo en que la «cura funcional del VHB» debe definirse como la pérdida duradera del antígeno de superficie de la hepatitis B (HBsAg) (basada en ensayos con límite inferior de detección (LLOD) ∼0.05UI/ml) con o sin seroconversión de HBsAg y ADN-VHB indetectable en suero después de completar un curso de tratamiento79.
La erradicación viral a corto plazo tiene como objetivo prevenir complicaciones de la enfermedad. Por esto, se ha sugerido la utilidad de algunos biomarcadores para evaluar el estatus de la enfermedad. Desafortunadamente, ninguno de los biomarcadores disponibles actualmente es una medida ideal de la eficacia del tratamiento por sí solo. Quizás por esta razón, la aprobación de nuevas terapias para la HBC por parte de las autoridades que otorgan licencias generalmente ha dependido de la demostración de mejoras significativas en 2 o más marcadores sustitutos de la progresión de la enfermedad con el tratamiento. Típicamente, los sustitutos son: 1) bioquímicos (niveles de aminotransferasas, en particular de ALT), 2) virológicos (niveles de ADN-VHB, HBeAg y HBsAg) y 3) histológicos (basados en sistemas de puntuación histológicos)77.
En la actualidad aún no es posible logar esta cura completa en pacientes con HBC; por tanto, las curas funcional o parcial son objetivos más realistas a alcanzar con las terapias disponibles. Adicionalmente, se debe buscar como otro importante objetivo la normalización de la ALT78–80.
Varios estudios en pacientes con HBC con HBeAg+ han demostrado que la pérdida del HBeAg inducida mediante el tratamiento y la seroconversión a anti-HBe, conducen a una fase en donde la replicación viral suele ser baja, lo que conlleva a una mejor supervivencia a largo plazo. Por lo tanto, inducir la pérdida del HBeAg y la seroconversión a anti-HBe adicionalmente a lograr una carga viral del ADN-VHB indetectable se considera un objetivo valioso80.
VII. Criterios de selección para iniciar terapia antiviral específica en pacientes con la hepatitis B crónicaRecomendación 15: Se recomienda terapia antiviral en adultos con infección crónica por virus de la hepatitis B en fase inmunoactiva (actualmente denominadas fases 2 y 4)
- •
Grado de recomendación: 1; Grado de evidencia: I-A
La indicación para iniciar el tratamiento se basa en 3 criterios: niveles séricos del ADN-VHB, niveles séricos de ALT y grado de enfermedad hepática determinado mediante métodos no invasivos o biopsia hepática80.
El objetivo del tratamiento es reducir el riesgo de progresión a cirrosis y evitar el riesgo de desarrollar CHC; es por ello que el tratamiento está indicado en la fase inmunoactiva de la infección crónica por VHB (actualmente también denominadas como fases 2 y 4), que es cuando existe riesgo de daño hepático y progresión de fibrosis hepática. El tratamiento antiviral se deberá iniciar en todo paciente, independientemente del grado de fibrosis, en quien existan datos de inflamación hepática (cifras de ALT≥2 veces sobre el LSN definido en esta guía) en combinación con replicación significativa del VHB, la cual se define de la siguiente manera77,80:
Si el HBeAg es negativo, considerar una carga del ADN-VHB>2,000UI/ml77,80.
Si el HBeAg es positivo, considerar una carga de ADN-VHB>20,000UI/ml77,80.
La inhibición persistente de la replicación del VHB y la normalización de las cifras de ALT correlacionan con la eliminación de la actividad necroinflamatoria y del riesgo de progresión de la fibrosis en los pacientes con HBC, esto a su vez se asocia con mejoría global en la sobrevida, la reducción en el riesgo de desarrollar CHC, y también la mejoría en la calidad de vida de los pacientes. Adicionalmente, la inhibición persistente de la replicación del VHB previene la transmisión80.
Recomendación 16: Los pacientes con hepatitis B crónica y cirrosis, ya sea compensada o descompensada, siempre deben recibir tratamiento antiviral específico ante cualquier concentración positiva del ADN-VHB, e independientemente de los niveles de ALT
- •
Grado de recomendación: 1; Grado de evidencia: I-A
En pacientes con cirrosis compensada, la terapia antiviral con NA con alta barrera a la resistencia (tenofovir disoproxil fumarato [TDF], tenofovir alafenamida [TAF] y entecavir [ETV]), y la supresión de la carga viral (ADN-VHB indetectable) que se logra con dicha terapia, ha demostrado disminuir significativamente el riesgo de progresión de la enfermedad. Así mismo, en pacientes con cirrosis descompensada la terapia antiviral con NA debe iniciarse a la brevedad posible ya que ha demostrado modificar significativamente la historia natural de la enfermedad, debido a que mejora la función hepática e incrementa la supervivencia81–83. Aunque estos pacientes deben adicionalmente evaluarse para trasplante hepático, la terapia con NA logra compensar a estos pacientes y se ha reportado que hasta el 35% de los pacientes tratados con NA logran salir de la lista de trasplante debido a que la enfermedad hepática se compensa84.
VIII. Seguimiento de pacientes con hepatitis B crónica que no ameritan iniciar tratamiento específicoRecomendación 17: La determinación de los niveles séricos del ADN-VHB, HBeAg y la edad son parámetros de consideración para realizar seguimiento en pacientes con infección crónica por VHB
En pacientes en fase inmunotolerante (fase 1), el seguimiento se recomienda cada 3 a 6 meses.
En pacientes en fase de portador inactivo (fase 3), el seguimiento debe ser cada 3 meses en el primer año, y posteriormente cada 6 a 12 meses.
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Pacientes en la fase inmunotolerante (fase 1) de la HBC; es decir, HBeAg+, con niveles normales o mínimamente elevados de ALT o AST, sin fibrosis ni actividad necroinflamatoria o en su caso inflamación leve o mínima, presentan un riesgo bajo de progresión de la enfermedad a pesar de que suelen presentar carga viral elevada, en ellos se recomienda vigilancia de las cifras de ALT cada 3 a 6 meses. El estatus del HBeAg debe verificarse cada 6 a 12 meses. En pacientes en quienes la carga viral se mantiene persistentemente elevada (ADN-VHB>20,000UI/ml), que presentan elevación de ALT<2 veces el LSN, se debe considerar la necesidad de evaluar el grado de fibrosis mediante ET (FIB4 o FibroTest como alternativas) o biopsia hepática, si existe fibrosis >F2, o ante presencia de actividad necroinflamatoria moderada a severa (A2, A3) se recomienda iniciar tratamiento antiviral específico80.
Los pacientes en fase de HBC inactiva (fase 3) (HBeAg−, anti-HBe+, ALT normal, ADN-VHB<2,000UI/ml) también se caracterizan por presentar mínima actividad necroinflamatoria y fibrosis; por tanto, pueden vigilarse con determinación trimestral de las cifras de ALT durante el primer año, y posteriormente cada 6 a 12 meses, adicionalmente de forma anual deben ser evaluados para verificar la pérdida del HBsAg85. En estos pacientes con HBC HBeAg−, si el ADN-VHB resulta >2,000UI/ml y ocurre elevación de ALT<2 veces el LSN, se debe considerar la necesidad de evaluar el grado de fibrosis mediante ET (FIB4 o FibroTest como alternativas) o biopsia hepática, si existe fibrosis >F2, o ante presencia de actividad necroinflamatoria moderada a severa (A2, A3) se recomienda iniciar tratamiento antiviral específico. En caso de que el ADN-VHB se mantenga <2,000UI/ml, pero exista incremento de ALT, siempre es recomendable evaluar posibles causas adicionales que expliquen este incremento, como consumo de alcohol, esteatohepatitis no alcohólica, hepatitis C, hepatitis D, enfermedad hepática autoinmune, daño hepático inducido por fármacos o herbolaria86.
En pacientes que logran de forma espontánea o mediante tratamiento el aclaramiento del HBsAg, ya no es necesario continuar la vigilancia mediante niveles de ALT y de ADN-VHB, debido a que se encuentran en etapa de «cura funcional» (HBsAg−, anti-HBs+)87.
Recomendación 18: En pacientes con HBsAg+se debe de considerar el riesgo de CHC, transmisión, reactivación y manifestaciones extrahepáticas, por lo cual se recomienda vigilancia estrecha y considerar inicio de tratamiento específico
- •
Grado de recomendación: 1; Grado de evidencia: II-B
En todo paciente con HBC y fibrosis avanzada o cirrosis se recomienda mantener el escrutinio de CHC mediante ultrasonido hepático y determinación de AFP sérica cada 6 meses. En aquellos con HBC e historia familiar de CHC, sujetos provenientes de regiones geográficas endémicas (p. ej., asiáticos), cuando el diagnóstico de HBC se estableció en edades tempranas de la vida (infancia o adolescencia) y son varones mayores de 40 años de edad o mujeres mayores de 50 años de edad se debe llevar a cabo el escrutinio semestral de CHC independientemente de la presencia y del grado de fibrosis88–90.
Adicionalmente, otro escenario clínico, ocasionalmente observado en pacientes coinfectados con VIH, VHC, inmunocomprometidos, embarazadas, en diálisis o en usuarios de drogas intravenosas, es la presencia de anti-HBc IgG+ de forma aislada (HBsAg—); en estos casos no se requiere vigilancia, salvo en casos de inmunosupresión, donde, aunque poco frecuente, debe considerarse riesgo de reactivación e inicio de profilaxis91–93.
Debe considerarse iniciar tratamiento en cualquier fase de la enfermedad en pacientes con alto riesgo de transmisión del VHB, como son pacientes usuarios de drogas inhaladas o intravenosas, hombres que tienen sexo con hombres, pacientes coinfectados con VIH; también en pacientes con manifestaciones extrahepáticas o pacientes inmunosuprimidos por cualquier causa90.
IX. Estrategias terapéuticas actuales, seguimiento y vigilancia de pacientes durante el tratamientoRecomendación 19: El tratamiento antiviral de la hepatitis aguda por VHB solo está indicado en casos graves que cursan con datos de disfunción hepatocelular (hiperbilirrubinemia, coagulopatía) o criterios de insuficiencia hepática fulminante
- •
Grado de recomendación: 1; Grado de evidencia: II-B
El diagnóstico de infección aguda por VHB se confirma por la presencia de anti-HBc de tipo IgM en un sujeto positivo a HBsAg. La mayoría de los pacientes inmunocompetentes que adquieren hepatitis B aguda se autolimitan y no requieren tratamiento94. Aunque es una condición infrecuente, la insuficiencia hepática fulminante (IHF) asociada al VHB es una condición potencialmente mortal (tan elevada como el 40-50%)95,96 caracterizada por necrosis masiva de hepatocitos que se traduce clínicamente en ictericia (bilirrubina total [BT]>3.0mg/dl o bilirrubina directa [BD]>1.5mg/dl), coagulopatía (INR≥1.5), encefalopatía o ascitis en ausencia de enfermedad hepática pre-existente96,97. El desarrollo de ascitis (hazard ratio [HR]: 10.5; IC 95%: 1.6-68.6; p=0.01) y un puntaje de MELD>25 (HR: 28.9; IC 95%: 4.7-177.3; p=0.0001) se han descrito como los factores predictivos más relevantes asociados con mortalidad o necesidad de trasplante98.
Aunque la mayoría de la evidencia se sustenta en estudios que han explorado la eficacia de lamivudina (3-TC) en la hepatitis B aguda99–106, en la actualidad se prefieren esquemas terapéuticos con ETV, TDF o TAF por su menor riesgo de desarrollo de resistencias. Estudios de casos y controles y estudios de cohortes han demostrado eficacia equiparable entre 3-TC, ETV y TDF, en donde el inicio temprano del tratamiento ha demostrado reducir el riesgo de progresión a IHF, de necesidad de trasplante y también ha mejorado la supervivencia98,107,108. En todo paciente con criterios de hepatitis aguda grave con riesgo de evolución a IHF debe indicarse tratamiento antiviral específico basado en ETV, TDF o TAF. La duración del tratamiento en general se recomienda hasta el aclaramiento del HBsAg, o si se ha llevado a cabo trasplante hepático se recomienda por tiempo indefinido109.
Recomendación 20: Los fármacos de primera elección en pacientes con hepatitis crónica por VHB que cumplen criterios para iniciar tratamiento incluyen análogos nucleósidos (ETV) y análogos nucleótidos (TDF y TAF)
- •
Grado de recomendación: 1; Grado de evidencia: I-A
Entecavir (0.5mg/día), TDF (300mg/día) y TAF (25mg/día) son inhibidores de la polimerasa del VHB con alta barrera a la resistencia, altamente potentes para lograr una supresión profunda de la replicación viral, y con excelente perfil de seguridad; características por las que actualmente se recomiendan como primera línea terapéutica en pacientes con infección por VHB. Los 3 son equiparables en eficacia en pacientes vírgenes a tratamiento110,111; sin embargo, ETV no se recomienda en pacientes con exposición previa a 3-TC, ya que aquellos pacientes que han desarrollado resistencia a 3-TC, suelen tener 2 o 3 mutaciones requeridas para desarrollar resistencia a ETV, por lo que hasta el 51% de estos pacientes presentarán resistencia a ETV en los siguientes 5 años. Tenofovir disoproxil fumarato y TAF son mejores opciones en pacientes con exposición previa a 3-TC112.
A 10 años de seguimiento, TDF y ETV han mostrado supresión efectiva de la carga viral del ADN-VHB entre el 94 al 99%, tanto en pacientes con HBeAg+, como en pacientes HBeAg—. La seroconversión del HBeAg en pacientes HBeAg+ con TDF o ETV se ha reportado entre el 49-53% de los casos. La normalización de ALT se ha logrado entre el 77-83% de los pacientes con HBC tratados con alguno de estos esquemas. Sin embargo, la frecuencia anual de seroconversión del HBsAg es poco común (<1% anualmente)113.
El tenofovir es un dianion a pH fisiológico con pobre permeabilidad membranal y baja disponibilidad tras su administración oral. Para mejorar su biodisponibilidad tras la administración oral, se debe administrar como profármaco (TDF o TAF)113–115.
Después de su administración oral, TDF es hidrolizado por esterasas intestinales y plasmáticas para convertirse en tenofovir difosfato, su metabolito activo; TAF por el contrario es estable en plasma, y es metabolizado principalmente en el medio intracelular por medio de la catepsina A para convertirse a su forma activa en tenofovir difosfato114. Tenofovir alafenamida está indicado a dosis de 25mg/día y al ser un profármaco con mayor estabilidad en plasma que TDF, presenta menor exposición en plasma del metabolito activo tenofovir difosfato; por tanto, es menor el riesgo de toxicidad renal y ósea derivada de la administración a largo plazo en comparación con TDF115. Los resultados de ensayos clínicos muestran que TAF es igualmente eficaz que TDF para lograr la supresión de la carga viral tanto en pacientes vírgenes a tratamiento, como en aquellos previamente experimentados, en pacientes HBeAg+ y en pacientes HBeAg— a 48, 96 y 144 semanas de tratamiento116. Lampertico P, et al., también demostraron que el cambio de TDF por TAF no compromete la eficacia terapéutica, y confirmaron también la menor toxicidad renal y ósea de TAF117. Los efectos adversos más frecuentes son semejantes a TDF (cefalea, dolor abdominal, fatiga, tos y náusea)116.
El seguimiento y la monitorización de los pacientes bajo tratamiento con NA se realiza con: Parámetros bioquímicos (biometría hemática [BH], pruebas funcionales hepáticas [PFH], química sanguínea [QS], depuración de creatinina), serológicos (HBsAg, anti-HBs, HBeAg, anti-HBe) y carga viral del ADN-VHB; todo lo anterior de manera basal, trimestral durante el primer año y semestral posteriormente113,118–120.
La respuesta al tratamiento con NA se define como118:
- a)
Virológica: Carga viral del ADN-VHB indetectable.
- b)
Bioquímica: Normalización de ALT sérica.
- c)
Histológica: Mejoría en el grado de necroinflamación hepática.
- d)
Serológica: Seroconversión del HBeAg e idealmente, aunque ocurre infrecuentemente del HBsAg (3 al 11%)119,120; por ello el tratamiento debe ser a largo plazo, generalmente de por vida, aunque en pacientes que han logrado la seroconversión del HBsAg puede plantearse la suspensión, sin dejar de monitorizar a los pacientes y continuar escrutinio semestral de CHC, particularmente en aquellos que logran la seroconversión en edad >50 años o en aquellos que son cirróticos118–120.
En la actualidad ya no se recomienda iniciar tratamiento con NA que tienen baja barrera a la resistencia; como 3-TC, adefovir (ADV) o telbivudina (TBV). En los pacientes con historia de tratamiento con 3-TC, ADV o TBV que han desarrollado resistencia, se recomienda cambiar de fármaco a TDF o TAF. En el caso de pacientes con resistencia a ADV pueden cambiar de fármaco a ETV, siempre y cuando no exista antecedente de exposición previa a 3-TC (la exposición previa a 3-TC confiere resistencia cruzada a ETV cuando están presentes las siguientes mutaciones: rtM204V/I, rtT184, rtS202, tM250)121–125. En pacientes con resistencia a ADV asociada a las mutaciones rA181T/V o rN236T, con carga viral elevada, la respuesta a TDF o TAF puede ser prolongada, en estos casos se recomienda agregar ETV126. Los pacientes con multirresistencia representan todo un reto, en la actualidad lo que se recomienda y se tiene disponible es tratar en forma conjunta con ETV más TDF o TAF127. Park ES, et al. reportaron 2 casos de mutirresistencia con respuesta parcial a TDF que fueron exitosamente tratados con un novel modulador del ensamblaje de la cápside (NVR 3-778), pero este tipo de fármacos aún no están disponibles en la práctica clínica128.
En pacientes bajo tratamiento con NA de alta barrera a la resistencia, se define como falla a tratamiento:
- a)
Respuesta parcial a la disminución >1log10UI/ml en la carga viral del ADN-VHB, pero persistiendo detectable después de al menos un año de tratamiento113.
- b)
Se define como rotura virológica al incremento >1log10 en la carga viral del ADN-VHB (o >100UI/ml en aquellos con carga viral previamente indetectable) durante el tratamiento113.
La mayoría de casos de estos 2 escenarios se deben a falta de adherencia al tratamiento. Sin embargo, cuando se ha descartado falta de adherencia, en casos de respuesta parcial o de rotura virológica se debe sospechar la urgencia de variantes asociadas a resistencia113.
En la práctica clínica la resistencia primaria a TDF o a TAF no se ha documentado en el seguimiento a largo plazo de pacientes con HBC, pero se sugiere la adición de ETV al esquema de TDF o TAF en el caso de que llegara a documentarse; a futuro una alternativa podría ser los moduladores del ensamblaje de la cápside (aún no disponibles)128. La resistencia primaria a ETV en pacientes vírgenes a terapias previas se estima en alrededor del 1.2%, en estos casos el cambio a TDF o TAF es efectivo113,129. La mayoría de los casos definidos en el inicio como respuesta parcial se relacionan con cargas virales excesivamente elevadas que con el paso del tiempo resuelve continuando en tratamiento sin cambios con el NA seleccionado de primera intención126,127,130.
Recomendación 21: El tratamiento con IFNpeg alfa 2a puede ser una opción en un subgrupo de pacientes con hepatitis crónica por VHB que cumplen criterios para iniciar tratamiento
- •
Grado de recomendación: 2; Grado de evidencia: I-A
El tratamiento con IFNpeg alfa 2a está definitivamente contraindicado en pacientes con cirrosis descompensada. Este tratamiento podría ser considerado en pacientes que presentan HBC idealmente sin cirrosis y criterios favorables para lograr la respuesta a este tratamiento, como son pacientes con HBeAg+, genotipo A o B (son los que han mostrado mejor respuesta en comparación con otros genotipos), jóvenes, sin comorbilidades, carga viral baja, ALT>2 veces en LSN131. En pacientes HBeAg— los predictores favorables de respuesta a IFNpeg son ser joven, mujer, carga viral baja y niveles elevados de ALT132.
El IFNpeg se administra semanalmente por vía subcutánea durante 48 semanas. La extensión a 72 o incluso a 96 semanas ha demostrado incrementar la tasa de éxito para alcanzar la respuesta viral sostenida (RVS); sin embargo, los múltiples efectos adversos del IFNpeg limitan el apego y la tolerabilidad de los pacientes133,134. La RVS a tratamiento se evalúa 24 semanas posteriores al fin de tratamiento, los criterios de respuesta son iguales a los descritos para NA, excepto por el criterio virológico, en este caso, se considera respuesta alcanzar una carga viral del ADN-VHB <2,000UI/ml (respuesta sostenida se alcanza en alrededor del 30% de los casos). La seroconversión del HBsAg (cura funcional) se alcanza en apenas el 10% de los casos118. Cabe además mencionar que en México ya no se comercializa desde que existen nuevos agentes de acción directa para tratar la hepatitis C.
Los criterios de falla al tratamiento con IFNpeg, en cuyo caso debe suspenderse el mismo, son:
HBeAg+: A la semana 12 de tratamiento suspender si no hay descenso en los niveles de HBsAg en caso de pacientes con genotipos A y D; mientras que en pacientes con genotipos B y C, el HBsAg>20,000UI/ml es criterio de suspensión del tratamiento. A la semana 24 de tratamiento todos los pacientes con niveles séricos de HBsAg>20,000UI/ml tienen escasas probabilidades de responder al tratamiento con IFNpeg y, por tanto, es criterio de suspensión cualquiera que sea el genotipo. En caso de falla se debe tratar con NA de primera línea135.
HBeAg—: Independientemente del genotipo, no lograr en el descenso en los niveles séricos del HBsAg y <2 log de descenso en la carga viral del ADN-VHB a la semana 12 se consideran criterios de falla al tratamiento136.
Recomendación 22: En la actualidad, todas las personas con VIH y coinfección con VHB, deben recibir tratamiento antirretroviral estándar, que incluya de forma preferente en el esquema TDF o TAF+emtricitabina (FTC) o lamivudina (3-TC)
- •
Grado de recomendación: 1; Grado de evidencia: I-A
La progresión a cirrosis, enfermedad hepática avanzada, descompensación o desarrollo de CHC, es más rápida en pacientes coinfectados VIH-VHB137; por ello, todo paciente con esta coinfección debe recibir tratamiento antirretroviral que incluya siempre 2 diferentes fármacos con actividad contra el VHB. Tanto el TDF, como el TAF, cualquiera de ellos en combinación con FTC o 3-TC, son fármacos aprobados para el tratamiento del VIH, que además poseen actividad contra el VHB con un bajo perfil de resistencia, por lo que en la actualidad se consideran de primera línea a incluir en el esquema antirretroviral de pacientes coinfectados VIH-VHB138–140.
No deben emplearse esquemas antirretrovirales que contengan un solo fármaco con actividad contra VHB; por ejemplo, 3-TC sola o FTC sola, ya que, por ejemplo, se ha demostrado que después de 2 a 4 años la resistencia del VHB a 3-TC en monoterapia ocurre entre el 40 y el 90% de los pacientes141. Los esquemas basados en TBV o ADV solos, o en combinación con 3-TC o FTC tampoco se recomiendan ya que presentan mayor riesgo de falla al tratamiento, selección de variantes resistentes respecto al VIH, y mayor frecuencia de toxicidad y efectos adversos como deterioro de función renal, miopatía o neuropatía, en comparación con TDF+FTC o TAF+FTC142–144.
Recomendación 23: En pacientes coinfectados VIH-VHB, en quienes no se puede usar TDF o TAF (tasa de filtración glomerular <50 o <30ml/min, respectivamente), adicional al esquema antirretroviral, se recomienda el uso de ETV, siempre y cuando no hayan sido expuestos previamente a 3-TC o FTC en esquemas sin TDF o TAF
- •
Grado de recomendación: 1; Grado de evidencia: I-A
Los esquemas a base de TDF+FTC y TAF+FTC en el paciente coinfectado VIH-VHB no están aprobados en pacientes con tasa de filtrado glomerular <50 y <30ml/min, respectivamente. Una alternativa para tratar la HBC en pacientes con deterioro de función renal y coinfectados VIH-VHB es ETV; sin embargo, siempre que se prescriba ETV en el paciente coinfectado VIH-VHB debe tenerse la certeza que el paciente se encuentra recibiendo terapia antirretroviral completamente supresiva (HAART), ya que se ha demostrado que en pacientes coinfectados VIH-VHB que no reciben esta terapia antirretroviral, el uso de ETV favorece la selección de la mutación M184V que confiere resistencia del VIH a 3-TC y FTC145. Siempre y cuando se administre en conjunto con HAART, el ETV ha demostrado ser una opción eficaz y segura en pacientes coinfectados VIH-VHB. Un estudio en este contexto, demostró que el tratamiento del VHB con ETV, en pacientes coinfectados con VIH que estaban recibiendo esquema HAART que incluía 3-TC en el mismo, demostró que a las 48 semanas de tratamiento con HAART y ETV se logró una reducción de −4.20log10 copias/ml respecto al ADN-VHB. No hubo efectos adversos significativos, ni cambios relevantes en cuanto a la viremia del VIH ni la cuenta de células CD4146.
Coinfección virus de la hepatitis C-virus de la hepatitis BRecomendación 24: Pacientes con VHC que están coinfectados con VHB, tienen riesgo de reactivación del VHB al recibir tratamiento con agentes antivirales de acción directa (AAD)
- •
Grado de recomendación: 1; Grado de evidencia: II-B
La reactivación del VHB se define como la pérdida del control inmune que ocasiona un abrupto incremento en la replicación viral, y puede ocurrir en 2 escenarios: 1) pacientes con infección crónica por VHB (HBsAg+ y anti-HBc+), y 2) pacientes previamente expuestos al VHB, pero que se habían recuperado (HBsAg—, anti-HBc+, anti-HBs generalmente positivo)147. La reactivación clínicamente significativa del VHB se caracteriza por elevación del ADN-VHB y de ALT148 en ambos escenarios; y específicamente en el segundo escenario también ocurre reversión de la seroconversión; es decir vuelve a haber positividad del HBsAg149 (ver definiciones técnicas de reactivación y «hepatitis flare» más adelante en el apartado específico sobre «Riesgo de reactivación en pacientes bajo tratamiento inmunosupresor o citotóxico»).
La prevalencia de HBsAg+ en pacientes con VHC se ha reportado entre el 1.4 al 5.8%149,150. Los pacientes coinfectados VHB-VHC, que reciben tratamiento específico con AAD contra en VHC se consideran en riesgo de reactivación del VHB. Entre noviembre de 2013 a octubre de 2016, la Food and Drug Administration (FDA) documentó 29 casos de reactivación del VHB en pacientes HBsAg+ que recibieron tratamiento con AAD por infección crónica por VHC concomitante, 2 de ellos fallecieron y un caso ameritó trasplante hepático151. Posteriormente otros estudios han demostrado alto riesgo de reactivación del VHB (>10%) en pacientes HBsAg+ durante y posterior al tratamiento con AAD contra el VHC. Por el contrario, en pacientes HBsAg— y anti-HBc+, el riesgo de reactivación se considera bajo (<1%)148,152–154.
Recomendación 25: En pacientes coinfectados VHC-VHB que presentan HBsAg+, y que iniciarán tratamiento específico con AAD contra el VHC, debe considerarse también iniciar profilaxis con análogos nucleós(t)idos para prevenir la reactivación del VHB
- •
Grado de recomendación: 2; Grado de evidencia: II-B
Con la finalidad de reducir el riesgo de reactivación, en todo paciente con VHC se debe, previo a iniciar el tratamiento con AAD, conocer el estatus respecto al VHB realizando un perfil serológico que incluya determinación de HBsAg, anti-HBs y anti-HBc151. Los pacientes con HBsAg+ tienen mayor riesgo de reactivación y riesgo de presentar flares (incremento de ALT>3 veces sobre el valor basal del paciente y >100U/l) durante el tratamiento con AAD, por ello en estos pacientes se debe además conocer el status basal de la carga viral del ADN-VHB y cifras de ALT, particularmente en aquellos con carga viral ADN-VHB detectable basalmente debe considerarse administrar profilaxis con NA durante la terapia con AAD y hasta 12 semanas posteriores al fin de tratamiento con los AAD (tabla 5). En quienes la carga viral del ADN-VHB basalmente se encuentra indetectable se puede optar por vigilar de forma estrecha, esto es, cada 4 semanas las cifras de ALT y de ADN-VHB, en caso de que la carga viral del ADN-VHB se haga detectable y exista elevación de ALT se sugiere considerar inicio de profilaxis148,152–155.
Profilaxis para evitar la reactivación de la infección por VHB en pacientes que están recibiendo AAD para tratar la hepatitis C o en pacientes que reciben inmunosupresión o agentes citotóxicos
| Fármaco y dosis | Comentario | Duración |
|---|---|---|
| TAF 25mg/día vía oral | Si la depuración de creatinina ≥15ml/minPreferente si hay exposición previa a lamivudina | a) Coinfección con VHC: Hasta la semana 12 posterior a concluir el tratamiento con AADb) Terapia inmunosupresora o agentes citotóxicos con riesgo moderado a alto de reactivación del VHB: continuar por >6 meses después de descontinuar la terapia de inmunosupresión o citotóxicac) Terapia inmunosupresora o agentes citotóxicos con riesgo muy alto de reactivación del VHB: (agentes depletantes de células-B; p. ej., rituximab): continuar por >12 meses después de descontinuar la terapia de inmunosupresión o citotóxica |
| TDF 300mg/día vía oral | Si la depuración de creatinina ≥50ml/minPreferente si hay exposición previa a lamivudina | |
| Entecavir 0.5mg/día vía oral | En pacientes sin exposición previa a lamivudina | |
| Entecavir 1mg/ día vía oral | En pacientes con exposición previa a lamivudina |
Recomendación 26: En pacientes HBsAg—y anti-HBc+el riesgo de reactivación es bajo, por tanto, en estos pacientes se considera suficiente monitorizar las cifras de ALT durante y 12 semanas postratamiento con AAD
- •
Grado de recomendación: 1; Grado de evidencia: II-B
En pacientes HBsAg— y anti-HBc+ el riesgo de reactivación es bajo, por tanto, en estos pacientes se considera suficiente monitorizar las cifras de ALT cada 4 semanas hasta la semana 12 postratamiento con AAD, si durante esta vigilancia ocurre elevación persistente de las cifras de ALT, se recomienda realizar adicionalmente una nueva determinación HBsAg y de la carga viral del ADN-VHB155.
La necesidad de iniciar tratamiento específico para la HBC en pacientes coinfectados VHC-VHB, se determina exactamente bajo los mismos criterios expuestos previamente en esta guía para pacientes monoinfectados con VHB80.
Coinfección virus de la hepatitis B-virus de la hepatitis DRecomendación 27: Se recomienda realizar determinación de anti-VHD en pacientes HBsAg+que presentan factores de riesgo para adquirir y padecer concomitantemente infección por VHD
- •
Grado de recomendación: 1; Grado de evidencia: III
Escasos estudios han evaluado la prevalencia de la infección por VHD en México, la frecuencia en pacientes con infección por VHB del VHD se ha informado entre el 2.3 al 4.0%156. La infección por VHD puede adquirirse en forma aguda y de manera simultánea con el VHB (coinfección). Este escenario suele caracterizarse por cuadro clínico en forma de hepatitis aguda grave y se asocia con elevada mortalidad y en pocas ocasiones evoluciona a la cronicidad. La infección por VHD puede también presentarse en forma de superinfección; es decir infección por VHD aguda en un paciente que padece previamente HBC, se manifiesta como exacerbación clínica en un paciente con HBC previamente estable, frecuentemente evoluciona a la cronicidad y conlleva mayor riesgo de CHC, y descompensación de la enfermedad hepática157.
De acuerdo con la OMS, al menos un 5% de las personas con infección crónica por el VHB también están infectadas por el VHD. El número mundial de infectados por el VHD ha disminuido desde la década de los 80, tendencia que se debe principalmente al programa mundial de vacunación contra el VHB. La coinfección VHB-VHD se considera la forma más grave de la hepatitis viral crónica, dada su progresión más rápida hacia el CHC y su mortalidad más elevada asociada a enfermedad hepática descompensada158.
Las vías de transmisión principales del VHD son sexual y parenteral, la transmisión vertical es posible, pero infrecuente. Los grupos de riesgo para adquirir la hepatitis D son los pacientes con diagnóstico de VIH; usuarios de drogas intravenosas; hombres que tienen sexo con hombres; personas con múltiples parejas sexuales sin protección; personas con historia de enfermedades de transmisión sexual; inmigrantes de regiones que reportan alta prevalencia como África (Central y Occidental), Asia (Central y Septentrional, Vietnam, Mongolia, Pakistán, Japón, China y Taipei Chino), islas del Pacífico (Kiribati, Nauru), Oriente Medio (todos los países), Europa Oriental (zonas del Mediterráneo Oriental y Turquía), Sudamérica (cuenca amazónica) y Groenlandia; pacientes con HBC con ADN-VHB indetectable o bajo y que a pesar de ello presentan niveles elevados de ALT o AST. En todos ellos se recomienda de forma basal realizar escrutinio de la hepatitis D, y en aquellos con factor de riesgo persistente es recomendable repetir el escrutinio periódicamente (cada 6 meses). La infección por VHD se diagnostica por la presencia de anticuerpos contra VHD (anti-VHD), y se confirma por la detección de ácido ribonucleico del VHD (ARN-VHD) en suero, que también es útil para evaluar la respuesta a tratamiento antiviral. La OMS recomienda la cuantificación del HBsAg para determinar la respuesta al tratamiento en caso de que no se disponga de pruebas para cuantificar el ARN-VHD. La reducción de los títulos de HBsAg suele predecir una pérdida de este antígeno y correlaciona con la depuración del VHD, aunque la pérdida del HBsAg es rara con el tratamiento158–163.
Recomendación 28: El tratamiento con IFNpeg alfa es el único tratamiento aprobado para tratar pacientes con coinfección VHB-VHD sin cirrosis y con cirrosis compensada, durante 48 semanas
- •
Grado de recomendación: 1; Grado de evidencia: 1A
Los NA orales que se emplean para tratar la HBC, no tienen actividad en contra del VHD, en pacientes coinfectados VHB-VHD, el tratamiento específico del VHB debe indicarse bajo las mismas reglas y criterios expuestos con anterioridad en pacientes monoinfectados163,164.
Al tratar pacientes con la hepatitis D, el principal objetivo es inhibir la replicación del VHD; es decir negativizar la carga viral del ARN-VHD, hecho que generalmente se acompaña de normalización de las cifras de ALT y disminución de la actividad necroinflamatoria en el parénquima hepático. Adicionalmente otro objetivo debe ser lograr también la negativización del HBsAg. Cuando el VHD se encuentra replicando activamente; es decir es detectable y cuantificable la carga viral del ARN-VHD, el tratamiento con IFNpeg alfa (2a o 2b) durante un mínimo de 48 semanas, independientemente de la respuesta observada durante el tratamiento, es el único tratamiento aprobado158. La tasa global de RVS es baja, alrededor del 25 al 30%164, y la tasa de recaída a largo plazo (alrededor de 4.3 años) es elevada (apenas el 12% permanecen en RVS)165. La RVS (carga viral indetectable 6 meses después de haber concluido el tratamiento) posterior a este tratamiento es un factor independientemente asociado a una menor probabilidad de progresión de la enfermedad hepática158. La respuesta viral temprana (carga viral indetectable a las 24 semanas durante el tratamiento) se considera un factor asociado con la RVS. La dosis habitualmente empleada de IFNpeg alfa 2b en los diferentes ensayos clínicos que han evaluado su eficacia en pacientes con VHD fue de 1.5μg/kg/semana por vía subcutánea166–168; y en el caso del IFNpeg alfa 2a fue de 180μg/semana igualmente por vía subcutánea; ambos han resultado semejantes en eficacia169,170. La adición de 3-TC171, ADV169 o ribavirina168 al esquema de IFNpeg alfa no ha resultado en mayor eficacia y, por tanto, no puede recomendarse el empleo de ninguno de estos fármacos adicionales. Cabe mencionar que un problema a considerar en México, al tratar pacientes con VHB-VHD, es que los IFNpeg alfa 2a y 2b ya no están disponibles en nuestro país desde que fueron descontinuados como terapia de primera línea contra el VHC.
Cirrosis descompensadaRecomendación 29: Los pacientes con cirrosis descompensada y HBC deben recibir tratamiento con análogos nucleós(t)idos con alta barrera a la resistencia de forma prioritaria y por tiempo indefinido, independientemente de las cifras de ALT, del estatus del HBeAg y de la carga viral del ADN-VHB; además deben ser considerados para ser incluidos en un programa de trasplante hepático
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Todos los pacientes con cirrosis y VHB deben recibir tratamiento para: a) limitar la progresión de la lesión hepática, b) mejorar la función hepática, c) disminuir el riesgo de desarrollo de CHC, d) previo al trasplante específicamente para reducir el riesgo de reinfección y prevenir el desarrollo de la hepatitis colestásica fibrosante en la etapa posterior al trasplante y e) reducir la mortalidad. El tratamiento debe ser por tiempo indefinido pues existe alto riesgo de recidiva tras suspender el mismo; e idealmente de debe alcanzar el objetivo de mantener una carga viral ADN-VHB indetectable, ya que esto se asocia a un mucho menor riesgo de infección del injerto posterior a llevar a cabo el trasplante hepático cuando este es necesario; aunque el tratamiento antiviral per se ha demostrado que hasta el 35% de los pacientes en lista de espera para recibir un trasplante hepático, pueden ser retirados de la misma debido a compensación de la enfermedad84,172. Tenofovir disoproxil fumarato y ETV (1mg/oral/al día en cirrosis descompensada) se consideran en la actualidad de primera elección en este grupo de pacientes, ya que son opciones eficaces, con alta barrera a la resistencia, y seguras; siendo ETV particularmente más seguro en aquellos con riesgo de osteopenia u osteoporosis, o con riesgo de deterioro de la función renal173–179.
El IFNpeg alfa está contraindicado en pacientes con cirrosis descompensada156, y en la actualidad otras terapias con baja barrera a la resistencia, que anteriormente fueron utilizados, ya no son recomendables pues al desarrollarse resistencia a las mismas favorecen progresión del grado de descompensación180.
A pesar de recibir tratamiento específico para la HBC, en estos pacientes persiste el alto riesgo de desarrollo de CHC, por tanto, debe continuarse el escrutinio semestral con ultrasonido hepático y determinación de AFP181.
Recomendación 30: Tenofovir alafenamida puede utilizarse como una alternativa terapéutica contra el VHB en pacientes con cirrosis descompensada con alto riesgo de deterioro en la función renal o con alto riesgo de deterioro óseo
- •
Grado de recomendación: 1; Grado de evidencia: III
Tanto la falla renal, como la enfermedad ósea, son condiciones frecuentes en el paciente con cirrosis descompensada. Se estima que hasta el 24% de los pacientes cirróticos ambulatorios desarrollan algún tipo de disfunción renal dentro del primer año a partir del primer episodio de ascitis182. La prevalencia de enfermedad ósea en el paciente con cirrosis se estima entre el 12 al 55%183. Aunque a la fecha, no existen estudios que hayan explorado específicamente el uso de TAF en pacientes con VHB y cirrosis descompensada, se sabe que TAF tiene la ventaja de tener menor toxicidad ósea y renal, incluso no precisa de ajuste en la dosis habitual de 25mg al día en pacientes con tasas de filtrado glomerular >15ml/min en el paciente monoinfectado con VHB22. Además, estudios en otras poblaciones como pacientes con VIH184–186, pacientes con HBC sin y con cirrosis compensada han demostrado no inferioridad con respecto a TDF, con mejor perfil de seguridad óseo y renal187–189. Es por ello que este panel considera que TAF puede ser utilizado como una alternativa segura y eficaz en pacientes cirróticos descompensados a la misma dosis de 25mg/día por vía oral que en pacientes compensados o en aquellos no cirróticos.
Manejo postrasplante hepático, renal y de otros órganos sólidosRecomendación 31: Los pacientes postrasplantados de hígado deben continuar el tratamiento con análogos nucleós(t)idos (TDF, TAF o ETV)+inmunoglobulina anti-hepatitis B (HBIG) con el fin de evitar la recidiva de la HBC
- •
Grado de recomendación: 1; Grado de evidencia: II-A
La combinación de un NA+HBIG en el paciente postrasplantado, con el fin de lograr la supresión de la carga viral del ADN-VHB y títulos de anticuerpos anti-HBs mayores a 100UI/l, ha demostrado evitar la infección del injerto entre el 90 y el 100% de los pacientes, y mejorar la tasa de supervivencia en el 80% a 5 años22,190,191.
Samuel D, et al.192 fueron los primeros en demostrar la utilidad de la HBIG para reducir el riesgo de infección del injerto utilizando dosis altas de HBIG (10,000UI al día por vía intravenosa) en la fase anhepática del transoperatorio; seguido de la misma dosis diaria por los siguientes 7 días, y posteriormente a largo plazo; es decir, a la misma dosis, pero a intervalos mensuales (durante más de 6 meses). Esta estrategia redujo la infección del injerto del 90% a tan solo entre el 20 al 40%, además de reducir significativamente la mortalidad de estos pacientes192–196. La principal limitante del uso de HBIG a dosis elevadas es su alto costo, y sus efectos secundarios como cefalea, rubor y dolor torácico, y más raramente reacciones alérgicas197. Estudios posteriores demostraron que la administración de HBIG en conjunto con terapia antiviral específica (TDF, TAF o ETV, drogas con una barrera alta a resistencia, en la actualidad considerados de primera línea) permite utilizar dosis menores de HBIG (por vía intravenosa, intramuscular o subcutánea)198–207, y en algunos casos incluso puede prescindirse de la administración de HBIG a largo plazo208; p. ej., en pacientes sin factores de mal pronóstico que impactan en el riesgo de infección del injerto; tales como, historia de CHC o CHC activo como causa prioritaria para llevar a cabo el trasplante, presencia de resistencia a fármacos previos, carga viral del ADN-VHB elevada al momento del trasplante, coinfección con VIH o con VHD, paciente con historia de pobre adherencia terapéutica209–220.
En combinación con tratamiento antiviral específico, el cual debe administrarse por tiempo indefinido; la dosis, la vía de administración y la duración respecto a la administración de HBIG es muy variable en los diferentes centros de trasplante alrededor del mundo, en general los diferentes ensayos clínicos que han demostrado eficacia, han evaluado dosis de entre 800 a 10,000UI, generalmente optando por dosis mayores en la fase anhepática del transoperatorio, continuando la administración diaria de dosis semejantes durante 5 a 7 días posteriores al trasplante, seguido de administración semanal de dosis entre 200 a 10,000UI durante el primer mes, y cuando se opta por dejar HBIG de mantenimiento, administrando dosis de entre 800 a 10,000UI una vez al mes de forma indefinida192–207,209–220. En términos generales, si se utilizan esquemas que incluyen HBIG en la profilaxis postrasplante en pacientes con VHB, para prevenir eficazmente la infección del injerto, se recomienda que los títulos de anti-HBs se mantengan >500UI/l durante los primeros 3 meses, >250UI/l a partir del tercer mes y hasta los 6 a 12 meses postrasplante, posteriormente es suficiente con mantenerlos entre 50 a 100UI/l197.
En casos seleccionados de bajo riesgo, donde el ADN-VHB es indetectable al momento del trasplante y no existe historia previa de resistencia a NA, un curso corto con duración de uno a 3 meses de administración de HBIG, acompañado de terapia con NA y posteriormente seguido de la monoterapia indefinida con ETV, TDF o TAF, ha demostrado prevenir de forma eficiente la recurrencia de la infección del VHB191.
Recomendación 32: En pacientes postrasplantados de riñón u otro órgano sólido no hepático, la profilaxis o tratamiento del VHB debe individualizarse de acuerdo al estatus del HBsAg y del anti-HBc
- •
Grado de recomendación: 1; Grado de evidencia: II-B
En estos casos, si el HBsAg es positivo se debe iniciar profilaxis o tratamiento preferentemente con TAF o ETV considerando su mejor perfil de seguridad respecto a la función renal. Si el HBsAg es negativo pero existe anti-HBc+ se recomienda vigilancia respecto al status del HBsAg durante el seguimiento de estos pacientes, si llega a ocurrir seroconversión al status HBsAg+ debe iniciarse de inmediato terapia con ETV o TAF independientemente de las cifras de ALT22.
Riesgo de reactivación en el paciente bajo tratamiento inmunosupresor o citotóxicoRecomendación 33: Existe riesgo de reactivación del VHB en pacientes que se encuentran inmunocomprometidos, o que reciben terapia citotóxica o inmunosupresora
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Definición de reactivación:
- a)
Pacientes con HBsAg+/anti-HBc+:
- 1.
Incremento >2log (100-veces) en la carga viral del ADN-VHB, en comparación con los niveles basales.
- 2.
ADN-VHB>3log (1,000)UI/ml en un paciente con carga viral previamente indetectable (dado que los niveles del ADN-VHB pueden fluctuar).
- 3.
ADN-VHB>4log (10,000)UI/ml si se desconoce el nivel basal de la carga viral.
- b)
Pacientes con HBsAg—/anti-HBc+:
- 1.
ADN-VHB detectable.
- 2.
Reaparición del HBsAg.
Un flare de hepatitis en ambos escenarios se define como el incremento en ALT>3 veces sobre los valores basales del paciente y >100U/l86.
El riesgo de reactivación está en relación a 3 factores principales: 1) el estatus respecto al propio VHB que presenta el paciente (tabla 6), 2) la enfermedad concomitante del paciente que motiva el inicio de terapia inmunosupresora o citotóxica (las enfermedades más comúnmente relacionadas son: cáncer, enfermedades inflamatorias crónicas, enfermedades autoinmunes), y 3) el agente inmunosupresor o citotóxico utilizado (tabla 7)221–223.
Riesgo de reactivación de acuerdo al estado serológico y la carga viral del VHB
| Riesgo de reactivación | Parámetros |
|---|---|
| Alto (>10%) | HBsAgHBeAg+ o −ADN-VHB>2000IU/ml |
| Moderado (1-10%) | HBsAg−Anti-HBs−Anti-HBc IgG+ |
| Bajo (<1%) | HBsAg−Anti-HBs+Anti-HBc IgG+ |
ADN-VHB: ácido desoxirribonucleico del virus de la hepatitis B (carga viral); anti-HBc IgG: anticuerpos anti-antígeno central del virus de la hepatitis B total o tipo inmunoglobulina G; anti-HBs: anticuerpo anti-antígeno de superficie del virus de la hepatitis B; HBeAg: antígeno e del virus de la hepatitis B; HBsAg: antígeno de superficie del virus de la hepatitis B; VHB: virus de la hepatitis B.
Fuente: Jang et al.84.
Fármacos inmunosupresores con potencial de reactivación del VHB y grado de riesgo
| Bajo riesgo (<1%) | Metotrexate.Azatioprina.6-Mercaptopurina.Corticosteroides durante <1 semana.Terapia intra-articular con corticosteroides. |
| Riesgo moderado (1-10%) | Inhibidores de calcineurina (tacrolimus, ciclosporina).Inhibidores de tirosina cinasa (imatinib, nilotinib). Riesgo moderado si HBsAg+ o HBsAg−/anti-HBc+.Inhibidores de TNF-alfa (infliximab, adalimumab, etanercept, certolizumab, golimumab). Riesgo moderado si HBsAg+ o HBsAg−/anti-HBc+.Otros inhibidores de citocinas (abatacept, ustekinumab, natalizumab, vedolizumab). Riesgo moderado si HBsAg+ o HBsAg−/anti-HBc+.Derivados de antraciclina (doxorrubicina, epirubicina). Riesgo moderado si HBsAg−/anti-HBc+.Prednisona: ≥10mg/día por ≥4 semanas (o corticosteroide equivalente). Riesgo moderado si HBsAg−/anti-HBc+.Prednisona: <10mg/día por >4 semanas (o corticosteroide equivalente). Riesgo moderado si HBsAg+. |
| Alto riesgo (>10%) | Quimioterapia sistémica.Agentes depletantes de células-B (rituximab, ofatumumab, obinutuzumab, ocrelizumab). Alto riesgo si HBsAg+ o HBsAg−/anti-HBc+.Derivados de antraciclina (doxorrubicina, epirubicina). Alto riesgo si HBsAg+.Prednisona: ≥10mg/día por ≥4 semanas (o corticosteroide equivalente). Riesgo alto si HBsAg+. |
HBsAg+: antígeno de superficie del virus de la hepatitis B positivo; HBsAg−: antígeno de superficie del virus de la hepatitis B negativo; anti-HBc+: anticuerpo anti-antígeno central del virus de la hepatitis B; TNF-alfa: factor de necrosis tumoral alfa; VHB: virus de la hepatitis B.
Recomendación 34: En pacientes con riesgo moderado a alto de reactivación del VHB debe indicarse profilaxis con análogos nucleós(t)idos con alta barrera a la resistencia
- •
Grado de recomendación: 1; Grado de evidencia: II-B
El efecto global estimado de 5 ensayos clínicos controlados que evaluaron la profilaxis antiviral en 139 pacientes HBsAg+ o anti-HBc+ versus 137 controles a quienes se ofreció tratamiento a demanda de rescate ante la presencia de reactivación del VHB, mostró que la profilaxis antiviral estuvo asociada al 87% reducción en el RR de reactivación (IC 95%: 70-94%) y también con una reducción del 84% (IC 95%: 58-94%) en el RR de flares de la hepatitis asociados al VHB. En un análisis por subgrupos, el mayor beneficio de recibir profilaxis antiviral se evidenció en los grupos clasificados con riesgo moderado y riesgo alto de reactivación, pero este beneficio no fue tan significativo en el grupo clasificado con bajo riesgo de reactivación223.
Pese a que la mayoría de los estudios respecto a profilaxis se han llevado a cabo con 3-TC, este fármaco ya no se recomienda, en su lugar en la actualidad se prefieren ETV, TDF o TAF por tener alta barrera a la resistencia. De estos 3, ETV es el que tiene mayor validación223,224.
En pacientes con bajo riesgo de reactivación no se recomienda inicio de profilaxis. En pacientes con criterios de moderado a alto riesgo de reactivación, la profilaxis con NA debe llevarse a cabo durante todo el tiempo que el paciente requiera el tratamiento inmunosupresor y continuarse por al menos 6 meses posteriores a la suspensión del agente inmunosupresor. Si se trata de agentes que inducen depleción de células B, se recomienda extender la profilaxis hasta por un mínimo de 12 meses posterior a la suspensión del inmunosupresor (tablas 6 y 7)155.
Embarazo y lactanciaRecomendación 35: Tenofovir disoproxil fumarato es el único fármaco aprobado para tratar la hepatitis B en la mujer embarazada
- •
Grado de recomendación: 1; Grado de evidencia: I-A
Las mujeres embarazadas que cumplen criterios estándar antes descritos para iniciar tratamiento contra el VHB, deben recibirlo, pero deben tenerse en cuanta ciertas precauciones. Entecavir e IFNpeg alfa están clasificados como categoría C en el embarazo, y por ello deben evitarse. Tenofovir alafenamida no tiene suficientes estudios que hayan evaluado su seguridad en el embarazo86. El tratamiento antiviral con TDF es seguro y efectivo en la mujer embarazada. En la mujer embarazada que previamente ya recibía tratamiento con NA se recomienda continuar con TDF, y en caso de haber estado previamente recibiendo ETV o cualquier otro NA, se debe cambiar de fármaco y prescribir TDF22.
Recomendación 36: A todo recién nacido de madre portadora de infección activa por el VHB (HBsAg+), debe administrarse inmunoglobulina anti-hepatitis B (HBIG) y vacuna anti-VHB antes de las primeras 12h posteriores al nacimiento
- •
Grado de recomendación: 1; Grado de evidencia: I-A
La transmisión perinatal del VHB ocurre principalmente durante el nacimiento, ya sea por vía vaginal o por cesárea. La inmunoprofilaxis estándar logra prevenir la transmisión en cerca del 95% de casos, y consiste en administrar HBIG (200UI/ml/vía intramuscular) y vacuna anti-VHB inmediatamente tras el nacimiento (<12h), seguido de 2 refuerzos de la vacuna aplicados dentro de los siguientes 6-12 meses225,226. Debido a menor inmunogenicidad de la vacuna anti-VHB en recién nacidos con bajo peso (<2,000g), se recomienda en ellos un refuerzo adicional, es decir 4 dosis totales de vacuna anti-VHB, comenzando la aplicación del primer refuerzo al mes de edad14.
Se recomienda confirmar la eficacia de la profilaxis realizando pruebas serológicas posteriores a la vacunación para anti-HBs y HBsAg después de completar la serie de vacunas, pero teniendo en cuanta nunca realizarlas antes de los 9 meses de edad para evitar la detección de anti-HB pasivos de la HBIG administrada al nacer y para maximizar la probabilidad de detectar la infección tardía por VHB. No se recomienda realizar pruebas anti-HBc de lactantes porque se podría detectar anti-HBc materno adquirido pasivamente en bebés nacidos de madres HBsAg+ hasta los 24 meses de edad. Los bebés HBsAg— con niveles anti-HB≥10mUI/ml están protegidos y no necesitan seguimiento. Los lactantes HBsAg— con anti-HBs<10mUI/ml deben ser revacunados con una sola dosis de la vacuna anti-VHB y realizar en ellos pruebas serológicas posvacunación 1-2 meses después. Solo los lactantes que permanezcan con <10mUI/ml después de la revacunación monodosis deberán recibir 2 dosis adicionales de la vacuna anti-VHB para completar la segunda serie, seguidas de las pruebas serológicas posteriores a la vacunación de uno a 2 meses después de la dosis final. Los lactantes HBsAg+ deben ser referidos para un seguimiento adecuado14,227,228.
Recomendación 37: La profilaxis antiviral con TDF debe comenzar en HBsAg+mujeres embarazadas altamente virémicas a principios del tercer trimestre para evitar la transmisión vertical del VHB
- •
Grado de recomendación: 1; Grado de evidencia: I-A
La inmunoprofilaxis estándar puede fallar para evitar la transmisión del VHB entre el 8-30% de los niños nacidos de madres altamente virémicas229. Por tanto, en embarazadas con carga viral elevada debe administrarse TDF. En un ensayo clínico multicéntrico, abierto, aleatorizado, de grupo paralelo, la terapia antiviral con TDF comenzando en las semanas 30 a 32 de gestación, demostró ser efectiva y segura para evitar la transmisión vertical en mujeres embarazadas sin una indicación estándar para comenzar tratamiento, pero que si presentaban HBsAg+ y una carga viral del ADN-VHB>200,000UI/ml o niveles de HBsAg>4log10UI/ml230. Otros autores recomiendan el inicio de TDF en este contexto clínico entre las semanas 24 a 28 de gestación22. La terapia antiviral con el fin de prevenir la transmisión vertical puede ser descontinuada 4 a 12 semanas después del parto, ya que prolongarla por más tiempo no ha demostrado beneficios adicionales86,230,231.
Recomendación 38: La lactancia no está contraindicada en mujeres con la hepatitis B
- •
Grado de recomendación: 2; Grado de evidencia: III
A pesar de que el HBsAg se ha detectado en leche materna, la lactancia no está contraindicada, incluso en mujeres HBsAg+ que no reciben tratamiento antiviral. En mujeres tratadas con TDF, se pueden encontrar pequeñas concentraciones de tenofovir en leche materna, pero su biodisponibilidad oral es limitada y, por tanto, tampoco se contraindica la lactancia materna. Sin embargo, la seguridad de otros NA durante la lactancia es incierta12. Ya que el VHB se transmite por contacto con sangre, algunos expertos recomiendan evitar temporalmente la lactancia en caso de grietas, escoriaciones o lesiones en los pezones14.
Enfermedad renal y óseaRecomendación 39: Entecavir se prefiere en pacientes con enfermedad renal u ósea establecida, o en aquellos que tienen factores de alto riesgo para deterioro de función renal u ósea
- •
Grado de recomendación: 1; Grado de evidencia: II-B
Múltiples factores están relacionados al deterioro de la función renal en pacientes con HBC. La infección crónica por el VHB per se, se asocia con glomerulonefritis membranosa232. Se consideran factores de alto riesgo para deterioro de la función renal los siguientes: presencia de cirrosis descompensada, tasa de filtración glomerular <60ml/min, hipertensión o diabetes no controladas, proteinuria, glomerulonefritis, uso concomitante de fármacos con potencial nefrotóxico y receptores de trasplante de órgano sólido22.
En una revisión sistemática y metaanálisis se evidenció que al comparar TDF versus ETV, el primero se asoció con mayor riesgo en el deterioro de la tasa de filtración glomerular (RR: 1.601; IC 95%: 1.035-2.478; p=0.0034) y mayor incidencia de hipofosfatemia (RR: 4.008; IC 95%: 1.485-10.820; p=0.006)233.
Así mismo, se sugiere cambiar de TDF a ETV o TAF (tomando en cuenta si existe exposición previa a 3-TC, en cuyo caso no se recomienda ETV). Un estudio retrospectivo que incluyó 103 pacientes tratados con TDF, en quienes se decidió cambio de esquema por ETV, por presentar tasa de filtrado glomerular <60ml/min, hipofosfatemia (fosfato <2.5mg/dl) o ambas condiciones, demostró que posterior a 46 semanas de tratamiento con ETV todos los parámetros de función renal mejoraron significativamente: creatinina de 1.3 a 1.1mg/dl (p<0.0001), tasa de filtrado glomerular de 54 a 65ml/min (p=0.002), fosfato de 2.2 a 2.6mg/dl (p<0.0001) y reabsorción tubular máxima de fosfato (TmPO4/eGFR) de 0.47 a 0.62mmol/l (p<0.0001). La supresión de la carga viral del VHB se mantuvo en la mayoría, excepto en el 5% de los pacientes, todos ellos presentaban resistencia a 3-TC. La probabilidad acumulada a 5 años de resistencia a ETV fue del 0% en pacientes vírgenes a 3-TC versus 11% en aquellos con exposición previa y resistentes a 3-TC (p=0.018)234.
Recomendación 40: Tenofovir alafenamida se prefiere en pacientes con enfermedad renal u ósea establecida, o en aquellos que tienen factores de alto riesgo para deterioro de función renal u ósea
- •
Grado de recomendación: 1; Grado de evidencia: I-A
Tenofovir alafenamida ha demostrado tener un mejor perfil de seguridad para la función renal en comparación con TDF. A 96 semanas de seguimiento, en 2 estudios fase 3, con un total de 1,298 pacientes, aquellos que recibieron TAF tuvieron menor deterioro en la tasa de filtración glomerular (−2.4ml/min) en comparación con quienes recibieron TDF (−6.7ml/min; p=0.008). Un menor porcentaje de pacientes, presentaron disminución en la tasa de filtración glomerular >25% cuando recibieron TAF versus TDF (10 versus 18%; p=0.002) o tuvieron una tasa de filtración glomerular <50ml/min (0 versus 2%; p=0.004)232.
Recientemente, Lampertico P, et al. realizaron un ensayo clínico de no inferioridad, multicéntrico, aleatorizado, doble ciego, fase 3, que incluyó 488 pacientes con HBC, 245 aleatorizados a continuar tratamiento con TDF y 243 aleatorizados a cambiar el esquema de TDF por TAF con un seguimiento a 48 semanas; en este estudio se demostró que TAF tiene mejor perfil de seguridad renal que TDF. Además, el grupo que cambió a TAF mostró incremento significativo en la densidad mineral ósea de cadera (0.66±2.08% versus −0.51±1.91%; diferencia de mínimos cuadrados 1.17% [IC 95%: 0.80 a 1.54; p<0.0001]) y columna (1.74±3.46% versus −0.11±3.23%; diferencia de mínimos cuadrados 1.85% [1.24 a 2.46; p<0.0001])117. Otro estudio por Buti M, et al. demostraron que a 48 semanas, el grupo tratado con TAF tuvo menor reducción en la tasa de filtración glomerular (mediana −1.8ml/min [IQR: −7.8 a 6.0] versus −4.8ml/min [−12.0 a 3.0]; p=0.004), tuvo menor deterioro en la densidad mineral ósea (cadera: −0.29% [IC 95%: −0.55 a −0.03] versus −2.16% [−2.53 a −1.79], diferencia ajustada del porcentaje 1.87% [IC 95%: 1.42 a 2.32; p<0.0001]; columna −0.88% [−1.22 a −0.54] versus −2.51% [−3.09 a −1.94], diferencia ajustada del porcentaje 1.64% [IC 95%: 1.01 a 2.27]; p<0.0001)116. Chan HL, et al. encontraron también menor deterioro en la función renal y en la densidad mineral ósea en el grupo tratado con TAF versus el grupo que recibió TDF187.
FinanciaciónEsta guía clínica se realizó con recursos propios de la Asociación Mexicana de Hepatología A.C.
Conflicto de interesesFátima Higuera-de la Tijera es ponente para Gilead, Medix, Abbott, Schwabe-Pharma, Scienty Med, Takeda. Graciela E. Castro-Narro es ponente para Gilead, Glaxo-Smith-Kline, Abbvie, Abbott, Eisai, Medix, CellPharma. José A. Velarde-Ruíz Velasco es ponente para Gilead, Abbott, Takeda. Eira Cerda-Reyes es ponente para Gilead, Abbvie, Takeda, Medix, Bayer, MSD, Sanfer. Rosalba Moreno-Alcántar es ponente para Gilead y Abbvie. Mauricio Castillo-Barradas es ponente para Gilead, Abbvie, Italmex. Laura E. Cisneros-Garza es ponente para Abbvie, Gilead, Bristol. Margarita Dehesa-Violante es ponente para Abbvie. Linda E. Muñóz-Espinosa es ponente para CellPharma. José L. Pérez-Hernández es ponente para Schwabe-Pharma, Scienty Med. Aldo Torre-Delgadillo es ponente para Gilead, Merz, Medix, CellPharma. Rocío Torres es ponente para Gilead, Abbvie. Enrique Wolpert-Barraza es ponente para Gilead y Abbvie. Ignacio Aiza-Haddad, Judith Flores-Calderón, Saraí González-Huezo, Ernesto Márquez-Guillén, Juan F. Sánchez-Ávila, Mayra V. Ramos-Gómez, Juan Sierra-Madero, Eduardo R. Marín-López y David Kershenobich no tienen conflictos de intereses que declarar.