El objetivo del Consenso Mexicano de Hipertensión Portal fue desarrollar un documento guía para facilitar la práctica clínica en eventos clave del paciente con hipertensión portal y sangrado variceal. El panel de expertos incluyó gastroenterólogos, hepatólogos y endoscopistas mexicanos distinguidos por su trayectoria profesional. El documento exploró temas de interés en los siguientes módulos: profilaxis preprimaria y primaria, hemorragia variceal aguda y profilaxis secundaria. El manejo del sangrado variceal ha mejorado notablemente en años recientes. La información actual indica que el manejo general del paciente cirrótico con sangrado variceal se debe realizar por un equipo multidisciplinario, lo que tiene un papel importante en el desenlace final. Se recomienda combinar la terapia farmacológica y endoscópica en el manejo inicial; los fármacos vasoactivos se deben iniciar cuanto antes ante la sospecha de sangrado de origen variceal y mantenerse durante 5 días. Después de estabilizar al paciente, se realizará la endoscopia diagnóstica de urgencia por un endoscopista calificado, y se dará el tratamiento endoscópico variceal correspondiente. La profilaxis con antibiótico se debe considerar como parte integral del tratamiento, iniciarse desde el ingreso hospitalario y mantenerse durante 5 días. En caso de falla terapéutica, las terapias de rescate se deben iniciar de inmediato; tomando en cuenta que las terapias de derivación mediante radiolgía de intervención son muy efectivas en el control del sangrado variceal refractario. Estas guías están basadas en la mejor evidencia disponible sobre hipertensión portal, y están dirigidas a lograr una mayor eficacia clínica.
The aim of the Mexican Consensus on Portal Hypertension was to develop documented guidelines to facilitate clinical practice when dealing with key events of the patient presenting with portal hypertension and variceal bleeding. The panel of experts was made up of Mexican gastroenterologists, hepatologists, and endoscopists, all distinguished professionals. The document analyzes themes of interest in the following modules: preprimary and primary prophylaxis, acute variceal hemorrhage, and secondary prophylaxis. The management of variceal bleeding has improved considerably in recent years. Current information indicates that the general management of the cirrhotic patient presenting with variceal bleeding should be carried out by a multidisciplinary team, with such an approach playing a major role in the final outcome. The combination of drug and endoscopic therapies is recommended for initial management; vasoactive drugs should be started as soon as variceal bleeding is suspected and maintained for 5 days. After the patient is stabilized, urgent diagnostic endoscopy should be carried out by a qualified endoscopist, who then performs the corresponding endoscopic variceal treatment. Antibiotic prophylaxis should be regarded as an integral part of treatment, started upon hospital admittance and continued for 5 days. If there is treatment failure, rescue therapies should be carried out immediately, taking into account that interventional radiology therapies are very effective in controlling refractory variceal bleeding. These guidelines have been developed for the purpose of achieving greater clinical efficacy and are based on the best evidence of portal hypertension that is presently available.
La hipertensión portal en la actualidad se define como el aumento en el gradiente de presión portosistémica en cualquier segmento del sistema venoso portal. Si bien la hipertensión portal puede resultar de alteraciones prehepáticas (trombosis de la vena porta o la vena esplénica), alteraciones posthepáticas (síndrome de Budd-Chiari) o por causas intrahepáticas no-cirróticas (esquistosomiasis, síndrome de obstrucción sinusoidal), es la cirrosis hepática la causa más común de hipertensión portal y, por lo tanto, es la más ampliamente investigada. Se ha documentado que un gradiente de presión venoso hepático (GPVH) de 10mmHg o mayor identifica a un grupo de pacientes con un curso clínico más agresivo como es el desarrollo de várices esofágicas y gástricas, descompensación clínica (desarrollo de ascitis, hemorragia variceal y encefalopatía), complicaciones posteriores a la resección hepática (descompensación o muerte) y el desarrollo de carcinoma hepatocelular.
El sangrado variceal en el paciente cirrótico es la complicación más directa de la hipertensión portal y conlleva una alta morbimortalidad, sin embargo datos recientes sugieren una mejoría en estos indicadores al instituir avances en la profilaxis y tratamiento, al compararse con los estudios previamente reportados1–5. No obstante, algunos estudios6 demuestran que los clínicos tienen un pobre apego a los lineamientos de manejo del paciente con sangrado variceal agudo. No se cuenta con datos en nuestro sistema de salud, pero se podrían esperar cifras similares o peores, esto parecería estar determinado por la falta de guías asequibles en nuestro idioma.
La información en esta área se ha desplazado en gran medida a través de conferencias de consenso entre expertos donde se han definido los eventos y desenlaces y se ha revisado cuidadosamente la evidencia existente, dando lugar a recomendaciones prácticas. La primera de estas conferencias tuvo lugar en 1986 en Groningen, Holanda, y desde entonces estas reuniones se han alternado entre Europa (conferencia de Baveno) y EE. UU. (American Association for the Study of Liver Diseases).
Por lo señalado, se considera que existe una creciente necesidad de un Consenso Mexicano con lineamientos basados en la mejor evidencia actual para el manejo de los pacientes con hipertensión portal. Este consenso en idioma castellano pretende favorecer una mejor práctica clínica de esta entidad en nuestro país.
MetodologíaEn una primera etapa, se integró un comité de trabajo que propuso la metodología del consenso y elaboró un cuestionario base que permitió ser el documento preliminar y que se transformó en el documento final de las «Guías sobre el tratamiento de la hipertensión portal».
Este comité incluía a especialistas de la República Mexicana dedicados a la gastroenterología, endoscopia y hepatología.
El comité de trabajo formuló un cuestionario base de enunciados que exploraba los siguientes 3 módulos de conocimiento: profilaxis preprimaria y primaria, hemorragia aguda y profilaxis secundaria.
Estos enunciados fueron revisados, discutidos y finalmente aprobados durante las reuniones de trabajo, con lo que se obtuvo la base para la redacción de las futuras guías de tratamiento.
Dinámica del consenso tipo panel DelphiLa respuesta a cada enunciado se manifestó de acuerdo a la dinámica tipo panel Delphi que incluye puntaje de grado de acuerdo/desacuerdo en una escala del 1 al 9 con la opción de agregar propuestas de cambio en la redacción del enunciado.
Las respuestas con un valor de 6 o mayor fueron consideradas como «de acuerdo» con el enunciado. Cada una de las respuestas fue sustentada en la evidencia encontrada en publicaciones nacionales y/o internacionales.
El comité organizador recibió las respuestas de los panelistas sobre los enunciados específicos; aquellos para los que no existió consenso (menos del 60% de acuerdo) fueron revalorados para la formulación de un nuevo enunciado sustentado en evidencia científica, el cual se propuso durante la «Reunión presencial de consenso».
Finalmente, se preparó un documento base denominado «Propuestas del consenso mexicano» que se entregó a cada panelista en la reunión-taller que se realizó en abril del 2010 en Hermosillo, Sonora, México. Un grupo de trabajo especial incorporó en el documento final las aportaciones generadas en el Consenso de Baveno V, que fue publicado en octubre de ese mismo año7, las cuales fueron aprobadas por todos los autores.
Durante dicha reunión, los coordinadores presentaron los enunciados a evaluar para el consenso final. Aquellos en los que no existió un consenso se definieron como «no acuerdo» en espera de mayor evidencia científica.
A todos los participantes se les pidieron sus niveles de acuerdo por escrito para la publicación de las guías finales en la Revista de Gastroenterología de México.
Primer módulo. Profilaxis preprimaria y primaria en hipertensión portalIntroducciónLa hipertensión portal, presión por arriba de 5mmHg, ocasiona el desarrollo de várices esofágicas (VE). Estas son consideradas una de las complicaciones más importantes, formando colaterales portosistémicas y siendo responsables del sangrado variceal8,9. Por este motivo, es una variable que define la progresión de cirrosis compensada a descompensada. Aun con los tratamientos actuales, la morbimortalidad asociada a esta condición es alta, lo cual enfatiza la necesidad de un tratamiento preventivo más efectivo3.
Al ser diagnosticada la cirrosis, las várices están presentes en un 30-40% de los pacientes compensados y en un 60% de los descompensados10–12. En aquellos cirróticos sin várices en su primera endoscopia la incidencia anual de VE es del 5 al 10%13–15.
FisiopatologíaLa formación de várices es consecuencia directa del incremento en la presión portal que, en cirrosis, es ocasionado por un aumento de la resistencia al flujo portal y por un incremento de la afluencia venosa portal. El aumento en la resistencia es tanto estructural (distorsión de la arquitectura vascular hepática por fibrosis y nódulos regenerativos) como dinámico (con contracción de miofibroblastos, activación de células estelares lo que ocasiona incremento en el tono vascular debido a disfunción endotelial y disminución de la biodisponibilidad del oxido nítrico e incremento en la actividad de vasoconstrictores endógenos como la endotelina, estímulo alfaadrenérgico, angiotensina, entro otros)16,17. Este incremento de la presión es el factor inicial que conduce a la apertura de canales vasculares embrionarios preexistentes, y adicionalmente, parecería existir una expresión incrementada de factores angiogénicos en la vasculatura esplácnica, como la expresión de VEGF18–20.
Cuando el GPVH se incrementa de manera significativa, se desarrollan colaterales en sitios de comunicación entre las circulaciones portal y sistémica10. Este proceso es modulado como se mencionó por factores angiogénicos21,22. Concomitantemente, el flujo venoso portal incrementado como resultado de la vasodilatación esplácnica e incremento del gasto cardiaco23 mantiene e incrementa la hipertensión portal.
El riesgo de sangrado se correlaciona de manera estrecha con el grado de presión portal. Las VE son las más frecuentes y clínicamente relevantes; se forman al excederse los 10mmHg de GPVH24. Un reducción de este gradiente de al menos un 20% del valor basal o a menos de 12mmHg, reduce de manera significativa el riesgo de sangrado25, por lo que las intervenciones que ayudan a disminuir esta presión han demostrado prevenir el sangrado.
Curso clínico y pronósticoEl sangrado variceal es el último paso de una serie de eventos que comienzan con un incremento de la presión portal, seguidos del desarrollo y la dilatación progresiva de las várices hasta que estas finalmente se rompen y sangran. La aparición de várices en pacientes compensados indica un cambio de estadio clínico, desde muy bajo de muerte a un año (1%) a un estadio de riesgo intermedio (3.4%). La aparición del sangrado variceal es un evento catastrófico, con un riesgo muy alto de muerte a un año (57%)26.
La clasificación endoscópica de las VE es un tanto subjetiva y presenta variabilidad interobservador27–29. De los sistemas de clasificación existentes, el desarrollado por el North Italian Endoscopy Club en 1988 dividía las várices en pequeñas, medianas y grandes, incluyendo además el grado Child-Pugh de la cirrosis y la presencia de manchas rojas de alto riesgo en las várices. Este sistema demostró tener alta especificidad para predecir sangrado variceal, pero no era sensible y tenía un bajo valor predictivo positivo30. A partir del consenso de Baveno I en 199231, se recomendó la clasificación de las várices en pequeñas (<5mm) o grandes (>5mm), se determinó como el mejor punto de corte para definir entre los 2 tamaños32 y se demostró que los pacientes Child-Pugh clase C, con várices grandes y manchas rojas tienen el riesgo más alto de sangrado dentro del año siguiente a la endoscopia33,34.
Una vez que se desarrollan, el ritmo de avance de várices pequeñas a grandes se sitúa en un 5 a un 18% (media 12%) por año15,35, particularmente en aquellos con enfermedad hepática progresiva. La escala Child-Pugh ha demostrado influir sistemáticamente con la progresión de las VE, sin embargo, el avance de la enfermedad hepática, y consecuentemente de la hipertensión portal, parecerían ser los factores de mayor importancia15,36,37.
La incidencia del primer sangrado es variable; en pacientes sin várices el riesgo es de aproximadamente un 2% por año, se incrementa a un 5% por año en aquellos con várices pequeñas y a un 15% por año en los que desarrollan várices medianas a grandes12. Por lo tanto, la probabilidad es variable, pero puede ser estimada de acuerdo a algunos indicadores de riesgo (tamaño variceal, clase de Child-Pugh, manchas rojo rubí).
En un estudio se encontró un GPVH significativamente más alto en aquellos pacientes que desarrollaron sangrado variceal (20.4±5.1 vs. 16±5.2; p<0,001)38. Todos los pacientes con várices, así como los pacientes con sangrado variceal tenían GPVH mayores a 12mmHg. Se demostró una correlación estrecha entre el gradiente de presión, la presencia de várices y la probabilidad de sangrado. De igual manera, se ha encontrado que los pacientes con un GPVH <10mmHg tienen una probabilidad del 90% de mantenerse compensados después de una mediana de seguimiento de 4 años39. Además, por cada 1mmHg de incremento en el GPVH, existe un aumento del 11% del riesgo de descompensación clínica. El aumento en el GPVH es por el momento un factor de riesgo muy importante para desarrollar várices.
La presión variceal está en función de la presión portal. Muchos estudios, como el previamente citado, han demostrado que el sangrado variceal no ocurre si el GPVH no alcanza el valor umbral de 12mmHg38,40,41. Por este motivo, si el GPVH se reduce sustancialmente existe una marcada disminución del riesgo de sangrado40,42. Esto es importante, debido a que la hipertensión portal es reversible con el tratamiento farmacológico que efectivamente disminuya la presión portal.
Medición del gradiente de presión portalEl método más comúnmente utilizado para medir la presión portal es mediante la determinación del GPVH, el cual es un método indirecto. El GPVH es la diferencia entre la presión venosa hepática en cuña y la presión venosa hepática libre. El GPVH ha sido usado para valorar la presencia de hipertensión portal desde su primera descripción en 195143, y está validado como el mejor predictor para el desarrollo de complicaciones de la hipertensión portal.
La medición del GPVH consiste en colocar un catéter con balón en una vena hepática grande bajo control radiológico; una vez asegurada esta posición se infla hasta ocluir el flujo obteniendo la presión en cuña, y al desinflar nos permite obtener la presión libre. Esta técnica de oclusión con balón forma una columna de fluido estancado desde la vena hepática hasta los sinusoides hepáticos de un segmento amplio de hígado; es un método fácil, rápido y se convirtió en la técnica habitual desde 197944. Además, en manos experimentadas, la medición del GPVH es altamente reproducible, exacta y segura.
La medición del GPVH ha sido propuesta para las siguientes indicaciones: 1) para monitorizar la presión portal en pacientes que están tomando fármacos usados para prevenir la hemorragia variceal; 2) como un marcador pronóstico39; y 3) en estudios que evalúan los agentes farmacológicos para el tratamiento de la hipertensión portal45.
Gastropatía portal hipertensivaEl diagnóstico endoscópico de la gastropatía portal hipertensiva (GPH) se basa en la presencia de un patrón característico tipo mosaico de la mucosa. Este patrón está caracterizado por áreas poligonales pequeñas con un borde deprimido. Superpuestas a este patrón puede haber lesiones rojas puntiformes que usualmente son mayores de 2mm de diámetro. La GPH es considerada leve cuando solo está presente el patrón de mosaico y grave cuando se superpone el puntilleo rojo46. La causa y la patogénesis de la GPH son poco entendidas. El desarrollo de la GPH se correlaciona con la duración de la cirrosis, pero no necesariamente al grado de disfunción hepática.
Tamizaje de las várices esofágicasAunque algunas pruebas no invasivas se han considerado útiles en la selección de pacientes con alto riesgo de tener VE, particularmente el recuento de plaquetas, la esplenomegalia47, datos obtenidos por ultrasonido abdominal (diámetro de la vena porta >13mm) y recientemente el fibroscan48; ninguna de ellas, solas o combinadas, es lo suficientemente exacta para descartar definitivamente la presencia de VE grandes49.
En un simposio de la American Association for the Study of Liver Diseases50 se sugirió que los pacientes cirróticos en clase Child-Pugh A deberían beneficiarse de una endoscopia cuando existieran datos de hipertensión portal (plaquetas<140 000, diámetro de vena porta >13mm y ultrasonido con evidencia de circulación colateral). Los pacientes en clase Child-Pugh B y C deberían tener una endoscopia al momento del diagnóstico. A los pacientes sin várices se les debe realizar una endoscopia superior cada 2 a 3 años si la función hepática es estable, y una vez por año en caso de signos de deterioro. Debido a que las VE se forman al incrementar la presión portal por encima de 10-12mmHg51 y a que el desarrollo a várices grandes es más rápido cuando están presentes en la endoscopia inicial, el intervalo deberá disminuirse a cada año en pacientes con várices pequeñas y con signos clínicos de deterioro (desarrollo de ascitis y/o encefalopatía hepática).
Recomendaciones:
- •
Todo paciente con cirrosis hepática deberá evaluarse por endoscopia superior; las várices deberán clasificarse en pequeñas (menores a 5mm) o grandes (≥5mm). (Nivel de acuerdo 9).
- •
Pacientes cirróticos sin várices deberán realizarse una endoscopia superior de control cada 2 a 3 años para evaluar la aparición y/o progresión en su tamaño. (Nivel de acuerdo 9).
- •
En pacientes cirróticos compensados con várices pequeñas se deberá realizar una endoscopia superior de control cada 2 años y cada año en aquellos con signos de deterioro para evaluar la progresión en su tamaño. (Nivel de acuerdo 9).
La profilaxis preprimaria es el término usado para la prevención en la formación de várices. Estudios experimentales han sugerido beneficio con el uso de betabloqueadores no selectivos (BBNS) al prevenir la formación de colaterales52,53. Los BBNS reducen la cifra total de la presión portal un 15 a 20%, independientemente de la función hepática y la gravedad de la hipertensión portal o los parámetros hemodinámicos sistémicos54.
Un estudio que incluyó a 213 pacientes cirróticos con hipertensión portal pero sin várices10, comparando timolol vs. placebo durante una mediana de 55 meses, no demostró beneficio con el uso de BBNS. No existió diferencia en el desarrollo de VE o sangrado de las mismas; de igual manera, presentaron la misma frecuencia de complicaciones (p. ej., ascitis, encefalopatía o muerte). Los eventos adversos fueron más frecuentes en el grupo con timolol. Por otro lado, en este estudio se demostró que un GPVH basal menor a 10mmHg, o una disminución mayor del 10% del basal o por debajo de los 10mmHg eran los únicos predictores independientes de mantenerse libre de VE. Esta reducción del GPVH fue obtenida con mayor frecuencia usando timolol, y esto sí fue estadísticamente significativo.
La baja efectividad de los BBNS en prevenir la formación de várices, y la alta frecuencia de efectos secundarios observada en pacientes compensados cuestionó el uso de BBNS sin el tamizaje endoscópico para búsqueda de várices10.
Un abordaje diferente disponible es prevenir la progresión de la cirrosis de acuerdo a su etiología específica y se deben referir a los pacientes a centros especializados.
Recomendación:
- •
Los BBNS no son útiles en la prevención de la formación de várices en pacientes con hipertensión portal. (Nivel de acuerdo 9).
En el pasado, el tratamiento profiláctico del sangrado variceal solo era considerado en pacientes con VE medianas a grandes. Esto se debía a que la mayoría de los estudios con bloqueadores betaadrenérgicos estaban hechos en este tipo de pacientes, mientras que el beneficio era menos claro en pacientes con várices pequeñas55. Sin embargo, está bien establecido que las várices pequeñas con signos rojos o en pacientes en clase Child-Pugh C tienen un riesgo de sangrado similar a las várices grandes33. Un estudio controlado evaluó el rol de los BBNS en la prevención del crecimiento y sangrado de las várices pequeñas. Este estudio14 incluyó a 161 pacientes cirróticos con várices pequeñas, demostrando una disminución en el ritmo de crecimiento de las várices en pacientes que recibieron nadolol comparado con placebo. Adicionalmente, el riesgo de sangrado al final del seguimiento fue significativamente más bajo en el grupo con nadolol (12%) comparado con el grupo placebo (22%). Basado en esto, el último consenso de la conferencia de Baveno concluyó que el tratamiento profiláctico con BBNS podría ser considerado en pacientes con VE pequeñas (sin factores de riesgo asociados de sangrado) con el fin primario de reducir el crecimiento variceal7. Pero, aun faltan más estudios para que esta sugerencia se pueda establecer como recomendación formal.
Recomendaciones:
- •
No existe evidencia concluyente sobre el beneficio del uso de BBNS en profilaxis primaria en presencia de várices pequeñas sin signos de riesgo e insuficiencia hepática inicial o en clase Child-Pugh A. (Nivel de acuerdo 9).
- •
Pacientes con várices pequeñas y signos endoscópicos de alto riesgo (puntos rojos) o con insuficiencia hepática avanzada en clase Child-Pugh B y C deben beneficiarse de utilizar BBNS. (Nivel de acuerdo 9).
La profilaxis farmacológica está orientada a prevenir el primer sangrado y mejorar la supervivencia al disminuir la mortalidad relacionada con el sangrado. La eficacia de los BBNS para prevenir el primer sangrado se ha comparado con placebo en 11 estudios controlados aleatorizados (ECA). El metaanálisis de estos estudios demostró que se reducía el riesgo de primer sangrado variceal (del 24% sin tratamiento al 15% con BBNS después de un seguimiento de 2 años)55. La mortalidad también fue menor en el grupo con BBNS y esta diferencia demostró ser estadísticamente significativa.
Recomendación:
- •
La profilaxis primaria en presencia de VE grandes en pacientes sin contraindicaciones deberá iniciarse con BBNS. (Nivel de acuerdo 9).
Es importante notar que los BBNS son de los medicamentos más baratos y seguros. Estos reducen la presión portal al disminuir el gasto cardiaco (efecto β-1) y al producir una vasoconstricción esplácnica reduciendo el flujo sanguíneo portal (efecto β-2)56. El propranolol y el nadolol son los 2 BBNS más usados55. El nadolol es más fácil de administrar debido a su vida media más larga, permitiendo administrarse una vez al día. Adicionalmente, tiene menor liposolubilidad, no cruza la barrera hematoencefálica y por esta razón tiene menores efectos secundarios en el sistema nervioso central57. El propranolol es comúnmente iniciado a una dosis de 20mg 2 veces al día, mientras que el nadolol se comienza a dosis de 40mg por día. Algunos estudios sugieren empezar con nadolol 20mg por día e incrementar la dosis hasta la máxima tolerada sin efectos secundarios o a los 240mg58. Como se mencionó, disminuir el GPVH a <12mmHg esencialmente elimina el riesgo de sangrado y mejora la supervivencia40, mientras que reducciones >20% del basal25 disminuyen significativamente el riesgo de primer sangrado variceal. Debido a que el GPVH no está ampliamente disponible, la dosis de BBNS debe titularse para disminuir la frecuencia cardiaca un 25% del basal o a 55lpm. Pero como la reducción en la frecuencia cardiaca no se correlaciona con la disminución en el GPVH56, la dosis de BBNS debe ajustarse a la máxima dosis tolerada o hasta alcanzar las metas previamente mencionadas (frecuencia cardiaca o latidos por minuto), lo que ocurra primero. La dosis se incrementará de manera escalonada hasta alcanzar el límite superior de 160mg 2 veces al día de propranolol o 240mg una vez al día con nadolol.
Los efectos colaterales más comunes son cefalea, fatiga, disnea, impotencia y alteraciones del sueño. Aunque usualmente no son graves, puede requerirse una disminución de la dosis u ocasionar poco apego al tratamiento. Alrededor del 10–15% de los efectos secundarios ocasionan discontinuación del tratamiento59. Además, aproximadamente el 15% de los pacientes tienen contraindicaciones para usar BBNS60. Las contraindicaciones absolutas incluyen insuficiencia cardiaca, enfermedad pulmonar obstructiva grave, bloqueo cardiaco de segundo o tercer grado, estenosis aórtica grave, o insuficiencia vascular periférica. Recientemente en un estudio prospectivo se comparó el beneficio de los BBNS entre pacientes con y sin ascitis refractaria61; incluían grupos sin diferencias significativas (incluyendo el GPVH 20±4.5 vs. 19.1±5), y sorprendentemente se observó una peor supervivencia en cirróticos con ascitis refractaria. Los pacientes con ascitis refractaria y BBNS tuvieron una mediana de supervivencia más corta (5 meses vs. 20 meses, p=<0.0001) y la supervivencia a uno y 2 años fue menor (19 vs. 64% y 9 vs. 45%, p=<0.0001, respectivamente). Los factores independientes que predecían mortalidad fueron carcinoma hepatocelular, Child-Pugh C, etiología de la ascitis refractaria (falla renal e hiponatremia) y uso de BBNS. Por todo ello, se sugiere evitar estos fármacos en ascitis refractaria. Finalmente, en pacientes con síndrome hepatorrenal se ha demostrado una reducción importante del gasto cardiaco, lo que indica una progresión de la disfunción circulatoria en cirrosis62, esto determinado por una precarga disminuida, función cronotrópica disminuida y, como se observó en otros estudios, una probable cardiomiopatía con disfunción de ventrículo izquierdo por cirrosis63–65. Esta insuficiencia cardiaca presente solo en etapas avanzadas de disfunción hepática, con alteración importante de la perfusión renal, ocasiona una enorme controversia sobre uso de BBNS en esta situación clínica66.
Cerca del 25% de los pacientes cirróticos con VE medianas o grandes tienen contraindicaciones para usar BBNS o no toleran estos fármacos, y el grado de protección alcanzado (aproximadamente el 40% de reducción del riesgo relativo [RR]) está lejos del ideal. Los nitratos disminuyen la presión portal principalmente a través de una reducción de las resistencias intrahepáticas y portosistémicas35, pero tienen un efecto de hipotensión sistémica y la disminución de la presión portal podría deberse más a hipotensión que a la disminución de las resistencias67. El mononitrato de isosorbide (MNIS) es el único en su clase evaluado para la prevención del sangrado variceal. Es ineficaz si es administrado solo60, y podría incrementar la morbilidad, especialmente en pacientes con cirrosis avanzada y ascitis68.
La combinación de BBNS y MNIS ha demostrado intensificar significativamente la respuesta a largo plazo de los BBNS en el GPVH69. En un estudio multicéntrico aleatorizado, el uso de nadolol más MNIS demostró ser significativamente más efectivo en disminuir el primer episodio de sangrado, comparado con el uso de nadolol solo a largo plazo (hasta 7 años) con solo pocos efectos colaterales70,71. Contrario a estos resultados, en otro estudio con 349 pacientes59 la probabilidad acumulada de primer sangrado variceal con el uso de propranolol más MNIS fue similar al grupo de propranolol más placebo.
Al estudiar esta combinación72, en 56 pacientes cirróticos con VE de alto riesgo (grandes con signos rojos), cuando se usaron BBNS solos a una dosis que disminuía la frecuencia cardiaca a 55lpm, la respuesta terapéutica en el GPVH fue del 38%. Cuando se agregó el MNIS a los BBNS en no-respondedores, la respuesta global en el GPVH se incremento al 48% de los pacientes. Esta aproximación basada en la vigilancia estrecha y temprana del GPVH, con adición secuencial de MNIS a los pacientes no-respondedores al BBNS, logró categorizar adecuadamente a los pacientes en su riesgo de sangrado. A 2 años, la probabilidad de primer sangrado variceal en respondedores era de un 4%, incrementándose en no-respondedores a un 22 a 24%. La adición de MNIS ocasionó efectos adversos en un 17% de los pacientes, pero estos eran solo leves y se eliminaban al disminuir la dosis, por lo que la combinación en este estudio se usó de manera segura. Esto sugiere que la combinación de BBNS y MNIS parece efectiva y segura en la profilaxis primaria; sin embargo, podría incrementar la morbilidad en pacientes con cirrosis avanzada. Aun no existe evidencia suficiente para recomendar la combinación, y se espera que nuevos ECA aclaren estos resultados contradictorios.
Un metaanálisis reciente sugiere que en pacientes cirróticos no apegados al uso de BBNS, con contraindicaciones o con pobre tolerancia a ellos, la ligadura endoscópica (LE) de las VE parece ser superior en prevenir el primer sangrado variceal73. En los 19 ECA la tasa de sangrado fue menor con LE (razón de momios: RM 0,48; intervalo de confianza de 95% [IC 95%] 0,36-0,65; p<0.0001); al considerar solo los estudios de alta calidad no se mantuvo este beneficio y no se redujo la mortalidad general o asociada al sangrado. Adicionalmente, los BBNS se asociaron a un mayor número de eventos adversos (RM 2.61; IC 95% 1.6-4.4; p<0.0001). La evidencia actual no podría recomendar la LE como terapéutica de primera línea sobre los BBNS; estos últimos continúan siendo válidos por su accesibilidad y costo. Sin embargo, la LE es una alternativa razonable en centros con experiencia y en pacientes con las características antes mencionadas.
Recomendaciones:
- •
La disminución del GPVH a valores inferiores a 12mmHg o un 20% de descenso con respecto al valor basal reduce el riesgo de hemorragia por VE. (Nivel de acuerdo 9).
- •
No existen datos que apoyen el empleo de MNIS como terapia única en profilaxis primaria. (Nivel de acuerdo 9).
- •
No hay evidencia suficiente para recomendar la combinación de BBNS más MNIS en profilaxis primaria. (Nivel de acuerdo 9).
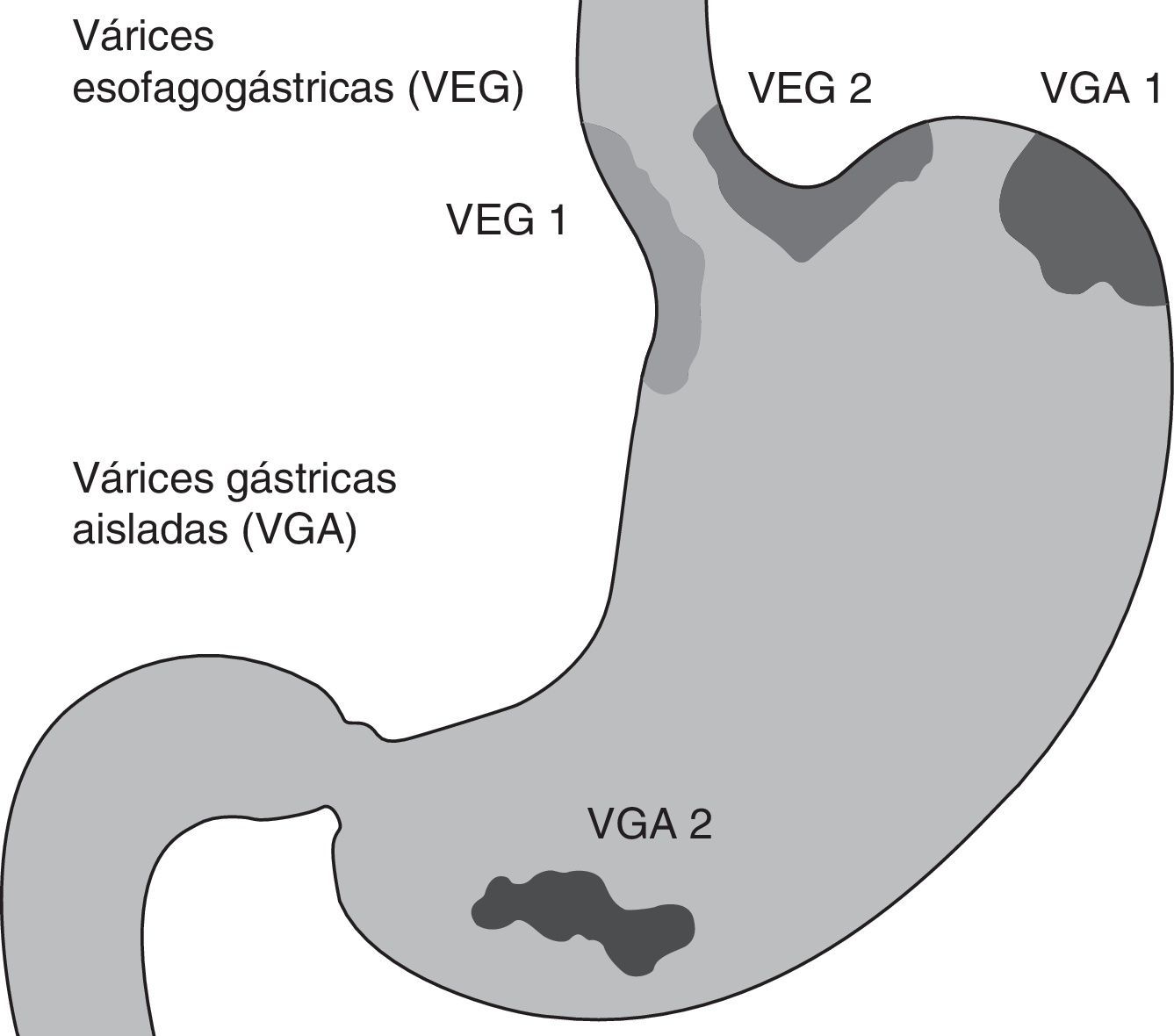
La prevalencia de las várices gástricas (VG) en pacientes con hipertensión portal varía del 18 al 70%74,75. La incidencia de sangrado por VG es relativamente poco frecuente, del 10 al 36%75, sin embargo, la mortalidad del primer sangrado por VG se mantiene en el 38 al 55% a las 6 semanas76,77. Habitualmente acompañan a las VE, pero pueden presentarse solas. Se han creado diferentes clasificaciones dependiendo de la localización de las várices76,78; los distintos subtipos tienen historias naturales y respuesta a tratamiento diferentes76,79. Las VG se subdividen en várices esofagogástricas (VEG) y VG aisladas (VGA), como fue descrito por Sarin75. Las VEG tipo 1 son continuación de las VE que se extienden 2 a 5cm debajo de la unión esofagogástrica, a lo largo de la curvatura menor del estómago, las VEG tipo 2 se extienden por debajo de la unión esofagogástrica hacia el fondo gástrico. Las VGA se dividen en VGA tipo 1, localizadas en el fondo, y VGA tipo 2, localizadas en cualquier otra parte del estómago (fig. 1). Las VEG tipo 1 son las más frecuentes y regularmente desaparecen espontáneamente con la obliteración de las VE. Las VEG tipo 2 son menos comunes, pero se asocian con una incidencia mayor de sangrado, y es menos probable que desaparezcan con la obliteración de las VE. Las VGA que no conectan con las VE usualmente ocurren en el fondo y son las más difíciles de tratar endoscópicamente80.
Clasificación de las várices gástricas. Clasificación descrita por Sarin, las VEG tipo 1 son continuación de las várices esofágicas extendiéndose hasta 5cm debajo de la unión esofagogástrica a lo largo de la curvatura menor del estómago, las VEG tipo 2 se extienden por debajo de la unión esofagogástrica hacia el fondo gástrico. Las VGA se dividen en VGA tipo 1, localizadas en el fondo, y VGA tipo 2, localizadas en cualquier otra parte del estómago. VGA: várices gástricas aisladas; VEG: várices esofagogástricas.
Las VGA en el fondo pueden resultar de la trombosis de la vena esplénica, lo cual se puede verificar por medio de estudios de imagen no invasivos. Estos pacientes frecuentemente requieren de esplenectomía para el control adecuado y la descompresión de las várices.
Las VG presentan dificultades únicas, a diferencia de las VE. Las terapias endoscópicas tradicionales con LE o con escleroterapia endoscópica (EE) han probado ser significativamente menos efectivas en el control agudo y profilaxis de las várices gástricas77,81. La gravedad incrementada de las VG se asocia con mayor probabilidad a su anatomía y fisiología distintivas, particularmente con las várices del fondo. Anatómicamente, las várices del fondo gástrico se asocian con venas de alto flujo originadas en cortocircuitos gastrorrenales, gastrofrénicos o cardiofrénicos, los cuales pueden tener un potencial de sangrado más grave82 y más frecuente a 2 años (55% VEG tipo 2 y 78% VGA tipo 1)76.
Hasta el momento no existe evidencia sobre la profilaxis preprimaria en VG y existe un solo estudio evaluando la profilaxis primaria del sangrado por VG. El rol del N-butil-2-cianoacrilato (NBC) fue valorado en un ECA abierto en 89 pacientes83, en donde se comparó NBC vs. BBNS o no tratamiento con seguimiento a 26 meses. Existió sangrado en solo un 10% de los pacientes con NBC comparado con un 38 y un 53% (BBNS y sin tratamiento respectivamente). Demostró diferencia significativa entre NBC y los otros 2 tratamientos (p=0,001, p=0,003), sin observar este efecto entre estos últimos (p=0,575). Se observó mayor eficacia con NBC en prevenir primer sangrado variceal de VG de alto riesgo (tamaño >20mm, MELD >17 y presencia de gastropatía portal hipertensiva) y reducción de mortalidad con NBC comparado con pacientes sin tratamiento (7 vs. 26%; p=0,048). El uso de BBNS en VG no redujo estos desenlaces a pesar de una reducción del GPVH. En este grupo de pacientes los factores que predecían mayor riesgo de sangrado por VG eran: tamaño>20mm, presencia de GPH y MELD>17. En conclusión, existe poca información sobre el tratamiento profiláctico en pacientes de alto riesgo con VG. Basados en este estudio, la atención se centraría en el uso de NBC con adecuada seguridad y efectividad. Sin embargo, ante la ausencia de evidencia específica sobre la profilaxis primaria en várices gástricas, se recomienda el uso de BBNS7.
Segundo módulo. Hemorragia variceal aguda: manejo inicial, transfusiones, antibióticos y tratamiento farmacológicoLa hemorragia variceal es una de las complicaciones más serias de los pacientes con cirrosis, particularmente en aquellos pacientes que han desarrollado descompensación clínica (ascitis, encefalopatía, episodio previo de hemorragia o ictericia). El sangrado en este escenario clínico es causado con mayor frecuencia por VE (65-70%) o por VG (10-15%)3,84. La mortalidad a las 6 semanas con cada episodio de hemorragia variceal es de un 15 a un 20%, que va de un 0% para pacientes en clase Child-Pugh A hasta un 30% en pacientes con clasificación Child-Pugh C85,86.
Historia natural y pronóstico de la hemorragia variceal agudaLos estudios clínicos muestran que el episodio de sangrado remite espontáneamente en un 40 a un 50% de los pacientes55. Con los tratamientos disponibles en la actualidad el sangrado se controla en más del 80% de los pacientes3.
La incidencia de resangrado es de un 30 a un 40% en las primeras 6 semanas; el mayor riesgo se presenta en los primeros 5 días, con una disminución al riesgo basal posterior a las 6 semanas1. Existen predictores de falla a tratamiento en los primeros 5 días como la presencia de infección bacteriana87,88, sangrado activo en la endoscopia de urgencia3,87,89, presencia de trombosis de la vena porta3, y GPVH>20mmHg medido al poco tiempo del ingreso89–91, algunos de los cuales han modificado el abordaje terapéutico gracias a lo cual se ha logrado reducir la tasa de resangrados en las primeras 6 semanas a un 20%3,91,92. Esto resulta de interés debido a que el resangrado temprano, al igual que la sepsis, son los 2 predictores más importantes de muerte por sangrado variceal93.
La muerte inmediata por sangrado no controlado oscila de un 4 a un 8%3,12. Aproximadamente un 60% de las muertes se relacionan con falla hepática, infección o síndrome hepatorrenal3. El consenso es que cualquier muerte que ocurra dentro de las siguientes 6 semanas de la hospitalización por sangrado variceal deberá considerarse una muerte relacionada con sangrado94.
Indicadores frecuentemente reportados que aumentan el riesgo de muerte son: la clasificación Child-Pugh, nitrógeno de la urea o creatinina, sangrado activo en la endoscopia, choque hipovolémico y carcinoma hepatocelular1,3,88,95.
El MELD predice significativamente la mortalidad en pacientes con cirrosis y sangrado variceal. En un estudio, la mortalidad a 6 semanas de los pacientes con MELD menor y mayor a 18, fue del 8 vs. 46%, respectivamente96. Más aun, los pacientes con un MELD alto (>18) y sangrado activo tenían un riesgo 10 veces mayor de morir dentro de las 6 semanas posteriores al sangrado variceal.
Por ello, el pronóstico de pacientes con sangrado variceal agudo está determinado por la presión portal90 y factores clínicos, como serían la gravedad de la enfermedad hepática, la magnitud del sangrado y el estatus bioquímico.
TratamientoEl manejo del sangrado variceal continúa siendo un reto clínico por su alta mortalidad. El sangrado variceal agudo debe manejarse en una unidad de terapia intensiva por un equipo médico experimentado, incluyendo enfermeras bien entrenadas, hepatólogos clínicos, gastroenterólogos, endoscopistas, radiólogos intervencionistas y cirujanos. La falta de estas instalaciones de manera específica deberá de ser suplida por la adecuada comunicación del equipo multidisciplinario de cada institución.
Manejo generalSe debe iniciar una corrección cautelosa del choque hipovolémico y encaminar parte importante de nuestro manejo a prevenir las complicaciones responsables de la gran mortalidad (infecciones bacterianas, descompensación hepática y falla renal).
Se debe comenzar con el ABC (por sus siglas en ingles: aireway, breathing, circulation) manteniendo una saturación de oxígeno, estado hemodinámico y hemoglobina adecuados. En el paciente encefalópata con sangrado importante (choque hipovolémico, hematemesis roja brillante) se debe asegurar inmediatamente la vía aérea; es un riesgo que potencialmente se puede exacerbar con la sedación durante el procedimiento endoscópico, por lo que se recomienda monitorizar con oximetría de pulso y considerar la intubación en el paciente con sangrado importante.
El manejo adecuado en la resucitación con líquidos, sangre o expansores de volumen se debe realizar de manera cuidadosa en estos pacientes. Se ha de evitar la hipotensión prolongada, para prevenir infección, falla renal y deterioro de la función hepática, los cuales se asocian a un riesgo incrementado de resangrado y muerte95. A pesar de que la expansión de volumen puede tener un incremento rebote de la presión portal y secundariamente del resangrado97,98, el uso de agentes vasoactivos disminuye la magnitud del incremento en la presión portal99,100. Se recomienda una hemoglobina de 7 a 8g/dL94, con cifras superiores en pacientes con cardiopatía o sangrado activo. La sobretransfusión se debe evitar debido a que puede resultar en un aumento de la presión portal con el consiguiente riesgo incrementado de resangrado temprano, al igual que la congestión pulmonar101,102.
La colocación de una sonda nasogástrica y la aspiración del contenido gástrico se practica frecuentemente, pero nunca se ha documentado una mejoría en la supervivencia o una disminución de las complicaciones, por lo que aun es controversial.
El tratamiento inicial para el sangrado variceal agudo está basado en la combinación de fármacos vasoactivos con la terapia endoscópica. La endoscopia diagnóstica debe realizarse tan pronto como sea posible después del ingreso (dentro de las primeras 12h), especialmente en pacientes con sangrado clínicamente importante. Esta recomendación basada en guías clínicas de diferentes países se adopta a partir de la opinión de expertos7,103,104. Una demora más prolongada (hasta 24h) puede ser aceptable en caso de sangrados menores (pacientes estables con presión sistólica >100mmHg y frecuencia cardiaca <125 lpm) con respuesta completa a los vasoconstrictores o en caso de no disponer de manera inmediata del equipo o de un endoscopista105,106.
Recomendaciones:
- •
En todos los pacientes cirróticos con hemorragia gastrointestinal superior de probable origen variceal (hematemesis y/o melena), se deberán iniciar medidas de resucitación (abordaje vascular y reposición de volumen), protección de vía aérea (considerar la intubación en el paciente con sangrado importante y encefalopatía) y administración de fármacos vasoactivos tan pronto como sea posible; aun antes de realizar el estudio endoscópico. (Nivel de acuerdo 8).
- •
Todos los pacientes cirróticos con sospecha de hemorragia variceal aguda deberán tener una endoscopia superior dentro de sus primeras 12h de ingreso hospitalario. (Nivel de acuerdo 9).
- •
En presencia de VE, y sin otras lesiones que expliquen la hemorragia, se considerará como sangrado de origen variceal y se ofrecerá la opción terapéutica correspondiente. (Nivel de acuerdo 9).
- •
No existe evidencia de la utilidad de la colocación de sonda nasogástrica. (Nivel de acuerdo 9).
Las infecciones bacterianas están presentes en un 20% de los pacientes cirróticos con sangrado gastrointestinal alto a su ingreso al hospital y otro 50% está en riesgo de infectarse107–111. Se debe buscar y descartar peritonitis bacteriana espontánea, infección de vías urinarias y neumonía, por su alta prevalencia. En este grupo de pacientes los antibióticos reducen resangrado109 y mortalidad111, y por tal motivo se recomienda su empleo desde el momento en que se sospeche y/o realice el diagnóstico de sangrado variceal agudo. Dos metaanálisis108,111 mostraron que el uso de profilaxis de corta duración con antibióticos tiene un efecto beneficioso sobre la mortalidad, con una disminución aproximada del 9%.
Las quinolonas son utilizadas frecuentemente debido a su fácil administración, buena absorción oral y bajo costo112. Se usan dosis de quinolonas (norfloxacino) de 400-500mg 2 veces al día, con una duración de 5 a 7 días. Se observó una reducción del RR para mortalidad en un 29% (IC 95%, 6–46%) y de un 58% (IC 95%, 48–66%) en la incidencia de infecciones, en pacientes que recbían antibiótico profiláctico comparado con placebo.
Recientemente, en pacientes de alto riesgo (con choque hipovolémico, ascitis, ictericia y malnutrición) la ceftriaxona intravenosa (1g por día) demostró ser superior al norfloxacino oral (400mg 2dos veces al día) para disminuir el desarrollo de infecciones (33 vs. 11%, p=0,03)110.
Por último, se debe evitar el uso de aminoglucósidos debido al alto riesgo de nefrotoxicidad113.
Recomendación:
- •
Los pacientes con hemorragia variceal aguda deben recibir antibióticos como norfloxacino oral 400mg cada 12h o ceftriaxona 1g parenteral por día en pacientes de alto riesgo (hipovolémico, con ascitis, ictericia y malnutrición) desde el momento en que ingresan en el hospital, con una duración de 5 días. (Nivel de acuerdo 9).
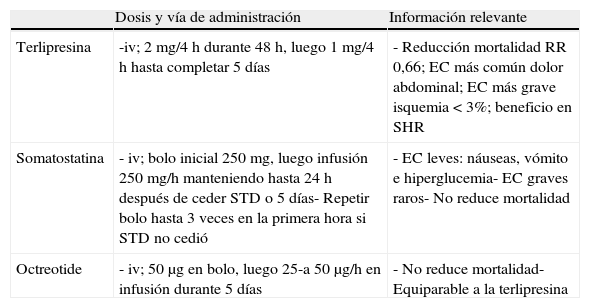
El objetivo del tratamiento farmacológico es reducir la presión portal, la cual se correlaciona estrechamente con la presión variceal. Esto fue observado en estudios iniciales90,114, los cuales demostraron que una presión portal mayor de 20mmHg se asociaba a peor pronóstico, y recientemente se confirmó en otro estudio utilizando somatostatina99 para reducir la presión portal durante el episodio de hemorragia variceal aguda, mejorando el desenlace. La selección del fármaco dependerá de los recursos locales. La terlipresina deberá ser la primera elección, debido a que es el único fármaco que ha demostrado mejorar la supervivencia55,115. Estos fármacos se administran con facilidad y son bastante seguros. El tratamiento se puede empezar incluso desde el traslado, lo que puede incrementar la supervivencia de los pacientes con sangrado masivo; más aun, pueden facilitar el procedimiento endoscópico115. Se utilizan 2 tipos distintos de medicamentos con mecanismos de acción diferente. Vasopresina y su análogo, la terlipresina, y la somatostatina o sus análogos (tabla 1).
Fármacos vasoactivos en sangrado variceal por hipertensión portal
| Dosis y vía de administración | Información relevante | |
| Terlipresina | -iv; 2mg/4h durante 48h, luego 1mg/4h hasta completar 5 días | - Reducción mortalidad RR 0,66; EC más común dolor abdominal; EC más grave isquemia<3%; beneficio en SHR |
| Somatostatina | - iv; bolo inicial 250mg, luego infusión 250mg/h manteniendo hasta 24h después de ceder STD o 5 días- Repetir bolo hasta 3 veces en la primera hora si STD no cedió | - EC leves: náuseas, vómito e hiperglucemia- EC graves raros- No reduce mortalidad |
| Octreotide | - iv; 50μg en bolo, luego 25-a 50μg/h en infusión durante 5 días | - No reduce mortalidad- Equiparable a la terlipresina |
EC: efectos colaterales; iv: intravenoso; RR: riesgo relativo; SHR: síndrome hepatorrenal; STD: sangrado de tubo digestivo.
Fármaco de larga acción derivado de la vasopresina, una triglicil lisina. Ocasiona un menor número de efectos colaterales, principalmente dolor abdominal. Efectos colaterales graves como isquemia periférica o miocárdica ocurren en menos del 3% de los pacientes116. La terlipresina disminuye el gasto cardiaco y aumenta la presión arterial y las resistencias vasculares sistémicas; esto conduce a la disminución de la afluencia vascular esplácnica. Esta disminución aunada a la vasoconstricción de la vasculatura esplácnica disminuye la presión portal aproximadamente un 20% después de la primera dosis117. El efecto se obtiene en los primeros 30min y permanece significativo hasta 4h después de la administración. Ante la sospecha de sangrado de origen variceal se recomienda iniciar a una dosis de 2mg cada 4h durante las primeras 48h y posteriormente disminuir a una dosis de 1mg cada 4h hasta 5 días116.
La terlipresina mejora significativamente el control del sangrado y la supervivencia118; es el único fármaco vasoactivo que ha demostrado mejorar el pronóstico del sangrado variceal en ECA55,118. Los metaanálisis recientes indican que la terlipresina se asocia con una reducción estadísticamente significativa en cualquier causa de muerte comparada con placebo (RR 0,66, IC 95%, 0,49–0,88). Por último, tiene una eficacia global en el control del sangrado del 75 al 80% a 48h115, del 67% a los 5 días116 y un efecto beneficioso en la función renal en pacientes con cirrosis descompensada95.
Somatostatina y sus análogosSomatostatina. A través de la experiencia de más de 3 décadas se conoce el efecto creciente de dosis más altas (500mg/h) en el GPVH, con mayor eficacia clínica en el subgrupo de pacientes con sangrado activo durante la endoscopia de urgencia119. Se debe iniciar con un bolo de 250mg seguido de una infusión a 250mg/h hasta lograr un periodo de 24h libre de sangrado, o mantener el tratamiento durante 5 días para prevenir resangrado120. El bolo inicial se puede repetir en la primera hora hasta 3 veces en caso de sangrado persistente. Los efectos secundarios son leves; hay náuseas, vómito e hiperglucemia en el 30% de los pacientes119–121. A pesar del efecto beneficioso en el control del sangrado, la somatostatina no tiene impacto sobre la mortalidad55.
Octeotride. Análogo de la somatostatina con vida media más larga, aunque sin efecto hemodinámico más prolongado122. Se recomienda administrar un bolo inicial de 50μg, seguido de una infusión a una dosis de 25 o 50μg/h123; igualmente se puede mantener durante 5 días para prevenir el resangrado temprano. Se ha demostrado un perfil de seguridad similar a la somatostatina y un efecto equiparable a la terlipresina, sin embargo, ningún estudio es doble ciego y carecen de poder55. La reducción estadísticamente significativa del resangrado temprano usando escleroterapia más octreotide podría deberse a la prevención del incremento posprandial de la presión portal123,124; de igual manera no modifica la mortalidad55,124.
Recomendaciones:
- •
En casos de hemorragia aguda de origen variceal, la administración de fármacos vasoactivos debe continuarse durante 3 a 5 días, para cubrir el periodo de máximo riesgo de resangrado. (Nivel de acuerdo 9).
- •
De las diversas opciones de manejo farmacológico durante el episodio agudo de hemorragia variceal, la terlipresina es el único agente vasoactivo que ha demostrado reducir la mortalidad. (Nivel de acuerdo 9).
La EE consiste en la inyección intravariceal o paravariceal de un agente esclerosante. Se realiza cada 10 a 14 días hasta erradicar las várices, lo cual lleva unas 5 a 6 sesiones. En la LE, se estrangulan las várices con la aplicación de bandas elásticas sobre la várice, habitualmente colocando 5 a 8 bandas por sesión. La LE de las VE se realiza cada 2 a 3 semanas hasta que se obliteran las várices o ya no pueden ser ligadas, usualmente en 3 a 4 sesiones. Sin embargo, debido a que la tasa de resangrado puede ser tan alta como un 50% después de la EE125, esta última ha sido reemplazada casi universalmente por la LE. Un metaanálisis con 7 estudios incluyendo 273 pacientes126 demostró una reducción significativa del 50% en resangrados con la LE, incluyendo resangrado variceal e inducido por úlceras.
La terapia endoscópica se recomienda ampliamente en todo paciente con sangrado variceal agudo. La EE ha demostrado ser efectiva en el control del sangrado agudo y en prevenir el resangrado comparada con el tratamiento médico con vasopresina o taponamiento con balón127. Sin embargo, el tratamiento endoscópico requiere un endoscopista calificado; y la EE en especial está frecuentemente asociada a eventos adversos126,128. La LE se ha comparado a la escleroterapia en varios ECA y un metaanálisis en la prevención del sangrado variceal a largo plazo, y fue encontrada superior a la escleroterapia126. En este metaanálisis, en comparación con la EE, la LE redujo la tasa de resangrado (RM 0,52; IC 95% 0,37-0,74), la mortalidad (RM 0,67; IC 95% 0,46-0,98) y la tasa de muerte asociada al sangrado (RM 0,49; IC 95% 0,24-0,99). Con un número limitado de LE se logra obtener un efecto positivo al evitar un episodio de resangrado (4 LE en lugar de EE evitan un episodio de resangrado) y un episodio de muerte (10 LE en lugar de EE para prevenir una muerte). La LE tiene menos complicaciones, no incrementa la presión portal (en comparación con la escleroterapia)129 y requiere menos procedimientos para la erradicación de las VE85,125,130. La LE, en caso de sangrado grave y profuso, puede ser técnicamente difícil debido a que el sangrado disminuye el campo visual; solo en estos casos el tratamiento inicial podría ser la escleroterapia. Por todos estos motivos, la LE debe ser el tratamiento endoscópico de elección en el sangrado variceal agudo.
Recomendaciones:
- •
Las opciones de manejo endoscópico (EE y/o LE) son útiles en el manejo del episodio agudo de hemorragia variceal. (Nivel de acuerdo 9).
- •
El manejo endoscópico de primera elección en el episodio de hemorragia aguda de VE es la LE. (Nivel de acuerdo 9).
- •
La LE variceal tiene menor tasa de complicaciones que la EE. (Nivel de acuerdo 9).
La recomendación actual es iniciar lo más tempranamente posible el tratamiento farmacológico (idealmente en el traslado al hospital, aunque solo se sospeche un origen variceal) y realizar la LE (o EE si la ligadura es técnicamente difícil) después de la resucitación inicial. Esto se basa en ECA donde se demuestra que el inicio temprano de fármacos vasoactivos facilita la endoscopia, y mejora el control del sangrado y del resangrado de los 5 días115,121,131,132. Al ser evaluada la combinación de tratamiento endoscópico y farmacológico contra la terapia endoscópica sola en el control del sangrado variceal agudo en un metaanálisis de 8 estudios aleatorizados133, se encontró mejoría en el control inicial del sangrado (RR 1.12; IC 95% 1.02-1.23) y la hemostasia de los 5 días iniciales (RR 1.28; IC 95% 1.18-1.39) con un número de pacientes a tratar de 8 y 5, respectivamente. Esta mejoría se obtuvo sin aumentar los eventos adversos; el beneficio se mantuvo significativo en los estudios con baja proporción de alcohólicos (<40%) o que excluían a cirróticos de alto riesgo (<35%). Sin embargo, la mortalidad no disminuyo significativamente (RR 0,73; IC 95% 0,45-1.18).
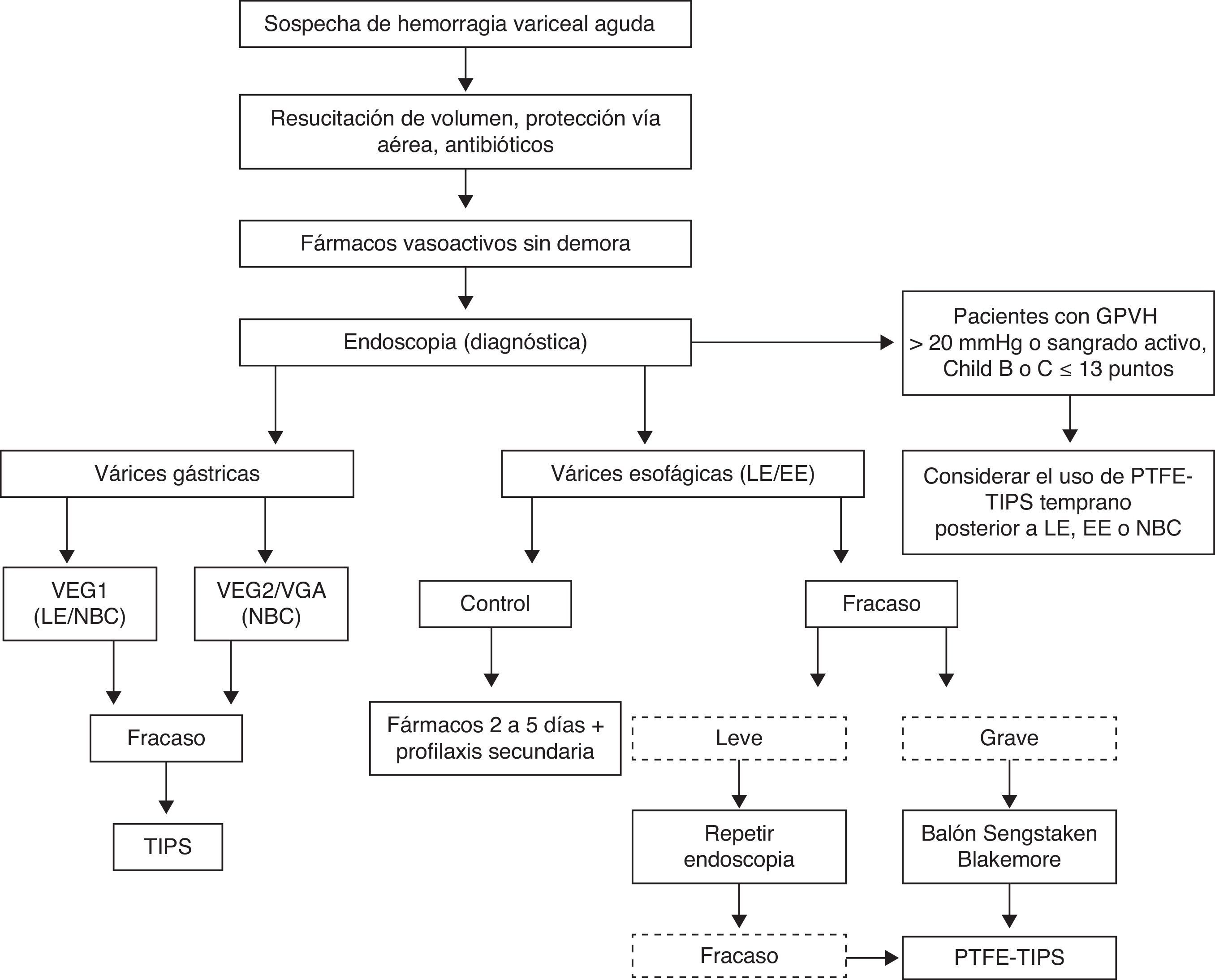
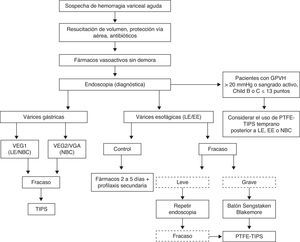
La terapia endoscópica y el tratamiento vasoactivo han demostrado tener una eficacia en el control del sangrado en el 80 a 85% de los pacientes. El tratamiento farmacológico mejora los resultados del tratamiento endoscópico si es iniciado justo después de la EE y la LE55,124, por lo que la recomendación actual es mantener los fármacos durante 2 a 5 días para cubrir el periodo de mayor resangrado7 (fig. 2).
Manejo de la hemorragia variceal aguda. Diagrama de flujo mostrando el manejo del sangrado variceal agudo. En pacientes de alto riesgo (Child-Pugh B o C≤13 puntos con GPVH>20mmHg) se deberá considerar un TIPS temprano. Ante pacientes con sospecha de hemorragia variceal aguda, se debe iniciar sin demora la resucitación de volumen cuidando mantener la hemoglobina alrededor de 8g/dL y con una reanimación juiciosa de cristaloides. Protección de vía aérea en pacientes con repercusión hemodinámica y encefalopatía. Se debe además hacer énfasis en medidas que aumentan la tasa de éxito y prevengan el resangrado como los antibióticos profilácticos, los fármacos vasoactivos y los métodos endoscópicos. Para várices esofágicas se prefiere la LE sobre la EE y en pacientes con fracaso en la hemostasia se tiene la opción de la sonda de balones como puente para una medida más eficaz y duradera como el TIPS. En pacientes con sangrado variceal de origen gástricos el tratamiento de primera elección será la aplicación de NBC, dejando la LE solo ante pacientes con sangrado activo en VEG tipo 1 en ausencia de NBC. En caso de tener una medición del GPVH>20mmHg o sangrado activo durante la endoscopia diagnóstica a pesar del uso correcto del fármaco vasoactivo en pacientes Child-Pugh B o C ≤13 puntos se debe considerar el empleo del TIPS temprano (72h) de PTFE posterior a la LE, EE o NBC. EE: escleroterapia endoscópica; Fracaso grave: paciente inestable con resangrado masivo; GPVH: gradiente de presión venoso hepático; LE: ligadura endoscópica; PTFE-TIPS: cortocircuito transyugular intrahepático portosistémico de politetrafluoroetileno; VEG: várices esofagogástricas; VGA: várices gástricas aisladas; NBC: N-butil-2-cianoacrilato.
Recomendación:
- •
El tratamiento combinado con LE variceal y fármacos vasoactivos es superior al tratamiento endoscópico aislado. (Nivel de acuerdo 9).
La administración de plaquetas y plasma fresco congelado no ha sido evaluada de manera adecuada en pacientes con sangrado variceal agudo134. Pero en aquellos pacientes con hemorragia variceal aguda y trombocitopenia parecería razonable mantener las plaquetas entre 40.000 y 50.000/mm3. Con relación a la transfusión de plasma, estudios recientes sugieren un estado hipercoagulable en pacientes con cirrosis causado por un desbalance entre factores procoagulantes y anticoagulantes (factor viii alto y proteína C baja)135, debido a que las pruebas de coagulación solamente evalúan la actividad procoagulante (INR), estas podrían tener limitaciones. A esto, se deberán agregar los inconvenientes que tiene la transfusión de plasma y concentrados plaquetarios como serían: el daño pulmonar agudo asociado a transfusiones, sobrecarga de volumen e infecciones, que nos hacen cuestionar su papel en el paciente con hemorragia variceal aguda. Por ello, su empleo se deja a consideración del médico tratante, en espera de estudios bien diseñados que demuestren su utilidad.
El uso de factor vii activado recombinante (rFVIIa), lo cual corrige el tiempo de protrombina en pacientes cirróticos,136 se ha evaluado en 2 ECA como un adjunto al tratamiento endoscópico y farmacológico137,138. En el primero de ellos no se observó ningún efecto en el control del sangrado agudo, resangrado y mortalidad. En el segundo estudio, el cual solo incluyó a pacientes cirróticos con un puntaje Child-Pugh <13, después de administrar rFVIIa se observó una mejoría significativa en el control del sangrado en las primeras 24h, del resangrado entre las 24h y los 5 días, y muerte en los primeros 5 días solo en el subgrupo de pacientes en clase Child-Pugh B y C con sangrado variceal (considerando al menos uno de los desenlaces anteriores: 15 fallas en 64 pacientes con placebo comparado con 5 fallas en 62 pacientes con rFVIIa [p=0,03]; específicamente en control del sangrado en las primeras 24h: 7 fallas en 63 pacientes con placebo comparado con 0 fallas en 62 pacientes con rFVIIa [p=0,01]). También demostraron que el uso del rFVIIa no aumentó el número de eventos trombóticos, por lo que parece seguro su uso en este escenario clínico. Se requieren más estudios para definir la población específica de pacientes que se beneficiarían del rFVIIa, así como la dosis mínima efectiva del fármaco. Por lo tanto, solo se debe considerar como terapia de rescate cuando todos los otros tratamientos han fallado.
Recomendaciones:
- •
Para el control de la hemorragia variceal aguda no se ha demostrado la utilidad de la administración de plasma y concentrados plaquetarios (si bien el plasma puede tener otra utilidad). (Nivel de acuerdo 8).
- •
No existe evidencia para sustentar el uso rutinario del factor vii (Nivel de acuerdo 8).
En la práctica clínica su mayor utilidad se relaciona con valorar la respuesta hemodinámica al tratamiento farmacológico, con el fin de evaluar la eficacia del tratamiento y para predecir el riesgo de resangrado de las VE. Sin embargo, la necesidad de un equipo apropiado, de operadores confiables y los altos costos, han desalentado su uso fuera de las unidades especializadas de hígado dedicadas al manejo de la hipertensión portal.
Estudios previos han demostrado que en pacientes cirróticos admitidos por sangrado variceal agudo, un GPVH mayor a 20mmHg está asociado a un incremento en la tasa de falla a tratamiento; hasta en un 50% de los pacientes90,91. Con esto se propuso la medición temprana del GPVH en pacientes con sangrado variceal para seleccionar a los que se beneficiarían de un manejo inicial más agresivo. En un estudio con 52 pacientes91, aquellos con GPVH inicial mayor de 20mmHg fueron aleatorizados a tratamiento convencional o a la colocación de un cortocircuito transyugular intrahepático portosistémico (TIPSLa tasa de falla en los pacientes con el tratamiento convencional fue de un 50%, comparado con un 12% de falla en pacientes con TIPS. En un segundo estudio86 se demostró que la falla a tratamiento en los primeros 5 días era 4 veces mayor en aquellos pacientes con GPVH mayor de 20mmHg (fig. 2).
Otro estudio de gran interés92 demostró mayor control del sangrado y disminución del resangrado con el uso de TIPS temprano, y la probabilidad de mantenerse libre de sangrado a un año fue significativamente mayor en el grupo de TIPS, 97% comparado con 50% (p<0,001); además se observó mayor supervivencia (86 vs. 61%) a un año sin aumentar el número de eventos adversos. Las diferencias principales con los estudios previos fueron el empleo del TIPS temprano (en las primeras 72h) en pacientes de alto riesgo (sangrado activo durante la endoscopia diagnóstica a pesar del uso del fármaco vasoactivo) y el uso de stents cubiertos de politetrafluoroetileno (PTFE). En este grupo de pacientes graves, los potenciales efectos adversos de los TIPS recubiertos parecerían equilibrarse con la alta eficacia en el control del sangrado, previniendo el deterioro clínico progresivo.
Es importante mencionar que estos excelentes resultados se corroboraron mediante un estudio de seguimiento y vigilancia, realizado en los mismos centros del ECA inicial139.
Por lo tanto, consideramos de gran utilidad recordar los 2 criterios principales para el empleo de TIPS temprano: el primero de ellos hemodinámico (de difícil acceso) basado en un GPVH mayor de 20mmHg, y el segundo, endoscópico (más accesible), que consiste en la presencia de sangrado activo durante la endoscopia diagnóstica a pesar del uso correcto del fármaco vasoactivo.
Recomendaciones:
- •
Se recomienda medir el GPVH en los pacientes cirróticos en los siguientes escenarios: hemorragia variceal no controlada, profilaxis secundaria con sangrado variceal recurrente. (Nivel de acuerdo 9).
- •
En el manejo de pacientes con hemorragia aguda variceal, la medición del GPVH con cifras superiores a 20mmHg identifica a pacientes con mayor riesgo de resangrado y mortalidad. (Nivel de acuerdo 9).
En un 10-20% de los pacientes, el sangrado variceal no responde al tratamiento endoscópico y/o farmacológico inicial. Si el sangrado es leve y el paciente se encuentra estable, se debe intentar un segundo procedimiento endoscópico. Si esto falla, o el sangrado es grave, se debe ofrecer un tratamiento derivativo previo a un deterioro mayor del estado clínico del paciente. Las terapias de rescate por falla a tratamiento incluyen el taponamiento con balón y las derivaciones portosistémicas. En casos de sangrado masivo no controlado, se debe considerar la colocación de un balón de Sengstaken-Blakemore.
La colocación de un balón en el esófago tiene como objetivo primordial detener mediante un método mecánico el sangrado de tubo digestivo de origen variceal; los balones más comúnmente utilizados son el de Linton Nachlas y el balón de Sengstaken-Blakemore. La colocación del balón logra detener el sangrado de manera temporal en un 40-90% de los pacientes11, sin embargo, el clínico debe tener presente que este método transitorio tiene una elevada recidiva de resangrado, cercana al 50%, y una elevada tasa de complicaciones como infección y/o perforación140,141. Por ello, se requiere una estrecha monitorización del paciente durante el uso de este método.
Otro método mecánico recientemente reportado en pacientes con hemorragia variceal de difícil control es el uso de stents metálicos autoexpandibles cubiertos142, con la ventaja sobre el taponamiento con balones de tener menos complicaciones inmediatas.
El TIPS consiste en la creación de un canal a través del parénquima hepático, conectando una rama de la vena portal con una vena hepática. Esta comunicación se logra por medio de técnicas de radiología intervencionista. El canal se mantiene permeable con un stent metálico autoexpandible idealmente cubierto143.
Este método, así como la derivación quirúrgica, es efectivo en controlar el sangrado variceal con una tasa cercana al 95%. Debido a que los TIPS han demostrado tener mejor eficacia, simplicidad y mejor costo-efectividad144, los cortocircuitos quirúrgicos han pasado a ser de segunda elección.
Recientemente, con el advenimiento de los stents recubiertos con PTFE, mejoró significativamente la persistencia de su permeabilidad a largo plazo, disminuyó el número de recaídas clínicas y el número de reintervenciones de un 44 a un 13% por año143 sin incrementar significativamente la encefalopatía (tabla 2).
Cortocircuito transyugular intrahepático portosistémico: indicaciones y contraindicaciones
| Indicaciones | Contraindicaciones |
| - Falla a tratamiento farmacológico y endoscópico | - Previo a un adecuado manejo farmacológico y endoscópico |
| - Hepatopatía crónica Child-Pugh A, B o C (puntaje Child-Pugh ≥5 pero ≤13)157 | - Hepatopatía crónica Child-Pugh C con puntaje ≥14157 |
| - Gradiente de presión venoso hepático>20mmHg91 | - Hipertensión portopulmonar, insuficiencia cardiaca |
| - Sangrado activo en endoscopia diagnóstica a pesar de fármaco vasoactivo92,139 | - Mal apego a tratamiento médico y seguimiento |
A pesar del excelente efecto hemostático, la colocación del TIPS no ha modificado la supervivencia de estos pacientes a largo plazo, con una mortalidad a 6 semanas del 38%, lo cual refleja la gravedad clínica de estos pacientes y la importancia de la enfermedad de base. Como fue mencionado, el reciente interés se centra en el uso temprano de este método en el subgrupo de pacientes con mayor morbimorbilidad por resangrado con un GPVH mayor de 20mmHg, obteniendo una reducción significativa de la falla al tratamiento y la mortalidad91 (fig. 2).
El uso de TIPS en el escenario de hemorragia aguda secundaria a hipertensión portal está confinado a la categoría de terapia de rescate, y como tal se debe intentar después de que han fallado los tratamientos farmacológicos y endoscópicos. La falla a la terapia endoscópica se define como la persistencia del sangrado después de 2 endoscopias terapéuticas en VE y una sesión para las VG145. En estos casos la inserción del TIPS no debe retrasarse.
A consecuencia de la disponibilidad de tratamientos no quirúrgicos efectivos, la cirugía de urgencia ha pasado a un segundo plano. Las opciones de derivación quirúrgica en situaciones de urgencia (definición heterogénea entre estudios, presencia de sangrado activo hasta 72h posterior al sangrado) más utilizadas en el pasado son los cortocircuitos no selectivos y los métodos de desvascularización. Sin embargo, es importante aclarar que la información proviene de series pequeñas y que estos métodos se comparan en su mayoría con escleroterapia146–148.
Los cortocircuitos no selectivos fueron los más utilizados como procedimientos de urgencia por su eficacia y rapidez en el control del sangrado, limitando el evento hemorrágico incoercible. Consisten en los cortocircuitos portocava (terminolateral y laterolateral) y mesocava con interposición de injerto protésico de 16 a 19mm. La desventajas son: el número incrementado de episodios de encefalopatía149 y la oclusión tardía que predispone a resangrado150. En pacientes candidatos a trasplante se sugiere realizar de primera elección un TIPS; en caso de no contar con este procedimiento o haber contraindicación para el mismo, se recomienda el cortocircuito mesocavo, ya que: 1) evita la disección del hilio hepático y 2) es fácilmente reversible mediante ligadura. En la mayoría de los estudios, que tenían un alto porcentaje de pacientes en clase Child-Pugh C, se presentaron tasas de mortalidad del 30 al 41%146,151–153; en uno de ellos la mortalidad resulto en un 19% al considerar solo pacientes en clase Child-Pugh A y B152.
La desvascularización gastroesofágica y transección esofágica (procedimiento modificado de Sugiura) fue utilizada ampliamente147,148,154,155; al compararse con la escleroterapia en caso de urgencia, tienen mortalidad temprana similar y en el control del resangrado algunos estudios favorecen a la transección147,154,155. Parecería tener menor control del sangrado, con tasas de resangrado superiores pero menor frecuencia de encefalopatía comparada con el cortocircuito no selectivo148. Resulta de importancia recordar que no se ha logrado reproducir la serie grande de Sugiura156, en la cual se obtuvo una mortalidad del 13% y un número bajo de resangrados del 5%.
Con relación a los pacientes con sangrado por várices gástricas, no se han utilizado métodos estadísticamente válidos para evaluar la eficacia de los métodos quirúrgicos como tratamientos de rescate. Algunos estudios lograron un excelente control del sangrado con los cortocircuitos, con alta incidencia de encefalopatía158. La desvasculatización rara vez fue utilizada y presenta una tasa notablemente alta de resangrado, de hasta el 40%.
Por estos motivos, el tratamiento quirúrgico se deberá considerar de rescate cuando hayan fallado los métodos endoscópicos, radiológicos y el tratamiento médico, en pacientes con mejor función hepática, recordando que la morbimortalidad postoperatoria se incrementa de manera directa con el tiempo de sangrado persistente. En centros donde no exista experiencia en los cortocircuitos y el TIPS, lo más apropiado sería realizar una transección esofágica. Los mejores candidatos a cirugía son pacientes cirróticos en clase Child-Pugh A. Por el contrario, para los pacientes en clase Child-Pugh C es importante enfatizar que el TIPS constituye la única terapia de rescate disponible, debido a su alta mortalidad quirúrgica.
Recomendaciones:
- •
El uso de la sonda de balones solo es una medida transitoria en el control del sangrado de tubo digestivo alto por hipertensión portal, al existir falla al tratamiento convencional, ya que si se utiliza durante más de 24h se asocia a diversas complicaciones potencialmente graves. (Nivel de acuerdo 9).
- •
Las terapias de rescate para el sangrado variceal son la colocación de TIPS o la derivación quirúrgica, si la condición clínica lo permite. (Nivel de acuerdo 9).
- •
En pacientes con hemorragia aguda de várices esofágicas con falla a tratamiento médico y endoscópico, deberá intentarse un segundo tratamiento endoscópico antes de buscar otra alternativa como TIPS o derivación quirúrgica. (Nivel de acuerdo 9).
- •
El uso de TIPS (preferentemente cubiertos con PTFE) se recomienda en pacientes con hemorragia por VE y/o gástricas que han fallado a otros tratamientos. (Nivel de acuerdo 9).
- •
La derivación quirúrgica se restringe a pacientes con reserva Child-Pugh A. (Nivel de acuerdo 9).
- •
En los pacientes que no son candidatos quirúrgicos debido al grado avanzado de insuficiencia hepática o a otras comorbilidades, el TIPS es la única alternativa disponible. (Nivel de acuerdo 9).
Del total de eventos de sangrado variceal agudo, las VG constituyen aproximadamente un 10 a 20% de los episodios en pacientes con hipertensión portal77,159. El sangrado por VG tiende a ser más grave, requiere mayor número de transfusiones y tiene una mortalidad superior al sangrado por VE81; después de controlar el episodio agudo, las VG tienen una alta tasa de resangrado, del 34 al 89%76.
En la mayoría de los estudios, los pacientes son tratados concomitantemente con terlipresina intravenosa, antibióticos de amplio espectro durante 3 a 5 días y la resucitación inicial, demostrando beneficio similar al observado en sangrado por VE. Con relación a la terapia específica para las várices gástricas, existen 2 opciones primarias: tratamiento endoscópico con la aplicación de adhesivos tisulares o la colocación radiológica del TIPS. El TIPS fue el tratamiento de primera línea en los países (p. ej., EE. UU.) donde existía una disposición limitada de adhesivos tisulares como el NBC, el cual se utiliza ampliamente en otras partes del mundo (fig. 2).
En 1986 se reportó por primera vez que el sangrado por VG podría ser controlado con el uso de la escleroterapia con un agente adhesivo tisular, el NBC160. El NBC es el agente más prometedor de todos los estudiados161–167; se polimeriza inmediatamente a un coagulo firme al hacer contacto con la sangre168,169, se inyecta estrictamente dentro de la várice y oblitera várices grandes. Tres a 4 días después ocurre necrosis de la pared variceal y el molde de NBC se desprende lentamente después de semanas o meses. La hemostasia primaria del sangrado agudo por VG con el uso del NBC oscila del 70 al 97%, con una tasa de resangrado temprano entre el 0 y el 28% dentro de las primeras 48h76,160,170. Como se puede observar, la tasa de resangrado continúa siendo alta, lo cual está lejos de ser ideal. Es posible que las venas de drenaje y tributarias de las VG, las cuales son de especial importancia para reducir el resangrado171,172, no se obliteren adecuadamente con la dosis convencional de NBC. También se ha demostrado la disminución del resangrado con inyecciones repetitivas hasta la obliteración completa (resangrado tardío, 18.5 vs. 44.7%), esto último se comprobó fácilmente al tocar la várice firme173. Esta terapia mejora y controla el resangrado, pero la mortalidad elevada refleja primariamente la enfermedad hepática avanzada, que no es modificada con el uso de NBC174,175.
El tromboembolismo se ha reportado en casos raros, es una complicación grave y catastrófica de la escleroterapia con NBC159,164,165,168,169,176–179. El riesgo parecería relacionarse con el tamaño de las várices, el flujo sanguíneo de estas, el volumen del NBC inyectado y la velocidad de inyección169,180. La fiebre se observa frecuentemente con dosis altas, está causada por una reacción de cuerpo extraño extensa, inflamación de la úlcera postescleroterapia o infección bacteriana. La bacteriemia se presenta hasta en el 33% de los pacientes con sangrado agudo por VG después de la aplicación de NBC181.
Diferentes dosis de NBC se han usado por distintos gastroenterólogos170,182, y la relación de dilución del esclerosante a agente lipoidal también es diferente173,183. Existe controversia en la dosis efectiva y la dilución de los agentes esclerosantes. La embolización puede ocurrir si se utiliza una cantidad excesiva de NBC por aplicación o si se sobrediluye el adhesivo con lipiodol. Por este motivo algunos autores recomiendan diluciones de 0,5:0,8 hasta 1:1, con lo que se retrasa el proceso de polimerización (más de 20s); una sobredilución incrementa el riesgo de embolización y la aplicación sin dilución ocasiona oclusión rápida del catéter inyector164,165,168,169,176,178,179,184. La cantidad máxima por aplicación para evitar esta complicación se debe limitar estrictamente a 1ml en las várices del fondo gástrico. Si se requieren dosis mayores por el tamaño de la várice, las inyecciones se deberán aplicar de manera secuencial.
Como ya fue mencionado, debido a la mayor tasa de hemostasia y menor tasa de resangrado, la obliteración con NBC de las VEG tipo 2 y VGA se utiliza como terapia de primera línea; esto se basa en el alto porcentaje de resangrado con la LE80,165,166,170,178,179.
Recomendaciones:
- •
La LE se recomienda para VEG tipo 1, pero no así para las VEG tipo 2 o las VGA tipo 1. (Nivel de acuerdo 9).
- •
Se recomienda la utilización de fármacos vasoactivos aunado con el tratamiento endoscópico, en el tratamiento de la hemorragia aguda por VG. (Nivel de acuerdo 9).
- •
La aplicación de NBC es efectiva para el tratamiento de la hemorragia por várices gástricas. (Nivel de acuerdo 9).
La GPH ocasiona menos del 10% de los sangrados agudos por hipertensión portal. Estudios pequeños han sugerido que el uso de octreotide puede ser útil en el control del sangrado agudo185. En el caso de sangrados importantes por GPH se ha utilizado el TIPS tratando de disminuir los requerimientos de transfusión186.
Recomendaciones:
- •
En aquellos pacientes con hemorragia aguda secundaria a GPH que fracasan al tratamiento convencional, deberán utilizarse otras alternativas como TIPS o derivación quirúrgica; esto en función de su reserva hepática. (Nivel de acuerdo 9).
- •
El tratamiento en pacientes con hemorragia aguda por GPH deberá ser con fármacos vasoactivos. (Nivel de acuerdo 9).
El riesgo del resangrado variceal en los primeros 2 años es del 60%, con una mortalidad del 35%55. Por esto, la prevención del resangrado es esencial en el manejo de pacientes con sangrado variceal para evitar resangrado y muerte. La profilaxis secundaria se inicia después de la recuperación del paciente del episodio agudo de hemorragia variceal, habitualmente en el sexto día7.
Recomendación:
- •
En el momento del egreso hospitalario de un paciente con sangrado variceal se debe de iniciar profilaxis secundaria con fármacos, erradicación endoscópica de várices o terapias de rescate (derivación quirúrgica o TIPS). (Nivel de acuerdo 9).
Se ha buscado evaluar el efecto de la terapia farmacológica en la reducción de la presión portal para prevenir el resangrado en hemorragia variceal. Los medicamentos estudiados son los BBNS solos o combinados. Además, se han tratado de utilizar otros medicamentos que no tienen efecto sobre la presión portal como los inhibidores de la bomba de protones (IBP) y el sucralfato.
Betabloqueadores no selectivos más mononitrato de isosorbideUn estudio comparó propranolol frente a propranolol más MNIS en la prevención del resangrado variceal, evidenciando una menor probabilidad de resangrado a 2 años de seguimiento en el grupo de terapia combinada (40.4 vs. 57.4%; p=0,09) pero sin alcanzar diferencia estadísticamente significativa187. De igual manera, otros estudios reportaron una tasa de resangrado menor, alrededor del 33-35% con la terapia combinada en comparación con BBNS solos, pero con mayores efectos adversos (fatiga, disnea, hipotensión postural, retención de líquidos y falla renal)9,55,187.
Otros medicamentos en los que se buscó utilidad para la prevención del resangrado variceal son los IBP y el sucralfato. Al evaluar el uso del sucralfato en la prevención de sangrado posterior a escleroterapia, diversos estudios demostraron una disminución del resangrado durante la erradicación de várices por medio de escleroterapia, encontrando este beneficio sobre la ulceración de la mucosa pero solo en pacientes en clase Child-Pugh A y B, sin incidir en la mortalidad188,189. Otro estudio prospectivo aleatorizado de 122 pacientes con sangrado variceal190 evaluó el uso de sucralfato más nadolol y LE vs. solo LE en la prevención del resangrado, encontrando que la terapia triple tenía un menor número de resangrado (23 vs. 47%; p=0,005) con una media de seguimiento de 21 meses; adicionalmente se obtuvo beneficio en las VEG (12 vs. 29%; p=0,001). Sin embargo, este beneficio con terapia triple podría estar dado en mayor medida por la LE y el nadolol.
En cuanto a los IBP, un estudio con pantoprazol 40mg cada 24h durante 10 días vs. placebo en pacientes sometidos a LE191 reportó el mismo número de úlceras posligadura en ambos grupos, pero la úlceras del grupo con pantoprazol fueron más pequeñas; además, 3 pacientes en el grupo placebo presentaron resangrado. Estos resultados parecerían estar a favor del uso de pantoprazol, pero se debe de tener en cuenta que fue un estudio pequeño y que los resultados no han sido reproducidos.
Recomendaciones:
- •
El uso combinado de BBNS más MNIS es efectivo, sin embargo, debe ser individualizado debido a los efectos colaterales y tolerabilidad. (Nivel de acuerdo 9).
- •
No hay suficiente evidencia para recomendar el uso de IBP ni de sucralfato para prevención de resangrado variceal. (Nivel de acuerdo 9).
Las opciones terapéuticas consisten en EE o LE.
Escleroterapia endoscópica versus ligadura endoscópicaMúltiples ECA comparando la LE con la EE demostraron que hay menor resangrado en el grupo de LE (RR 0,46; IC 95% 0,35-0,60), menos complicaciones y menor número de sesiones endoscópicas, sin diferencias en la recurrencia de várices y en la mortalidad127,192.
Globalmente el riesgo de resangrado en los pacientes sometidos a LE oscila alrededor del 32%9.
Tratamiento farmacológico y endoscópico combinadoEscleroterapia endoscópica más tratamiento farmacológicoLos BBNS solos se han comparado con la terapia combinada con EE en 3 ECA con un total de 277 pacientes, demostrando menor riesgo de resangrado con el tratamiento combinado; sin embargo, no se observaron diferencias en la mortalidad31,55,127,193.
Por otro lado, existen 10 ECA comparando BBNS vs. EE, incluyendo 862 pacientes, y demostraron que no hay diferencia en términos de resangrado y mortalidad (7 vs. 2%), sin embargo, los efectos colaterales son menores en el grupo de BBNS (2 vs. 22%)55,127.
Ligadura endoscópica más tratamiento farmacológicoDos ECA demuestran la superioridad de la terapia combinada de LE más BBNS cuando se compara con tratamiento farmacológico o LE sola190,194. La frecuencia de resangrado fue del 14% y 23% en el grupo de tratamiento combinado (LE más nadolol) comparado con el 38% y 47% en el grupo de procedimiento aislado. Ante esto, la combinación de LE con BBNS está ampliamente recomendada en la profilaxis secundaria de las várices esofágicas.
La combinación de BBNS más MNIS comparada con LE se ha evaluado en 3 ECA, siendo los resultados contradictorios. Un primer estudio mostró beneficio con la terapia farmacológica combinada195, otro con la LE196 y en un tercer estudio no hubo diferencia entre ambos tratamientos197. Estos resultados demuestran similitud entre ambas estrategias en la prevención de resangrado variceal, con rangos de 30% y 35%.
Recomendaciones:
- •
La LE es superior a la EE en la profilaxis secundaria del sangrado variceal. (Nivel de acuerdo 9).
- •
No se recomienda la EE como profilaxis secundaria (Nivel de acuerdo 9).
- •
El tratamiento con BBNS es superior a la EE en la profilaxis secundaria de sangrado variceal debido al menor porcentaje de efectos colaterales. (Nivel de acuerdo 9).
- •
El tratamiento combinado de BBNS más EL es la mejor opción en la actualidad para la profilaxis secundaria del sangrado variceal. (Nivel de acuerdo 9).
El procedimiento quirúrgico es muy efectivo en la prevención del resangrado. Las cirugías derivativas más comunes son la esplenorrenal distal (Warren), así como la desvascularización esogafogástrica (Sugiura). El inconveniente principal en dichos procedimientos es la mayor frecuencia de encefalopatía, pero sin impacto en la supervivencia, siendo los pacientes con cirrosis compensada el grupo que más se beneficia de la derivación quirúrgica, específicamente los Child-Pugh A11,198.
Cortocircuito transyugular intrahepático portosistémicoComo procedimiento derivativo, la realización de TIPS es efectiva para prevenir el resangrado, sin ser la terapia de primera línea, utilizándose en caso de falla al tratamiento médico o endoscópico199.
El TIPS se ha estudiado extensamente y comparado con otros tratamientos11,200,201; un metaanálisis demostró superioridad sobre la terapia endoscópica en la prevención a largo plazo del resangrado (19% vs. 47%), aunque esta ventaja no se tradujo en una mejor supervivencia (27% vs. 27%). El TIPS se asocia a una tasa significativamente más alta de encefalopatía portosistémica (34% vs. 19%). Resultados similares se obtuvieron cuando se comparó el TIPS con el tratamiento farmacológico, con una ventaja significativa del TIPS para alcanzar una tasa de resangrado más baja201. Por el contrario, la encefalopatía portosistémica en el grupo farmacológico es aproximadamente la mitad del presentado por el grupo con TIPS, mientras la tasa de supervivencia no demuestra diferencia entre los grupos.
El TIPS también se ha comparado con la cirugía en el escenario de la profilaxis secundaria202,203. Un ECA multicéntrico publicado recientemente por Henderson, con 140 pacientes cirróticos Child-Pugh clase A o B, con un seguimiento de 2 a 8 años, no se demostró ninguna diferencia en la tasa de resangrado, encefalopatía y supervivencia a 2 y 5 años, con una tasa más alta de trombosis, estenosis y necesidad de reintervención entre el grupo con TIPS (82%) comparado con el grupo con cortocircuito esplenorrenal distal (11%), por lo que se ha concluido que la opción de tratamiento se debe basar en la experiencia local de cada centro, la posibilidad de lograr un adecuado seguimiento y la logística de intervenir inmediatamente si fuera necesario202.
Recomendaciones:
- •
La derivación quirúrgica y el TIPS son las alternativas terapéuticas de elección ante la falla al tratamiento farmacológico y/o endoscópico en profilaxis secundaria, dependiendo de la reserva hepática. (Nivel de acuerdo 9).
- •
La derivación quirúrgica puede ser una opción viable en los pacientes cirróticos estables (Child-Pugh A). Para optar por esta maniobra, el centro donde se realice debe contar con la experiencia necesaria para la realización de cualquiera de las 2 cirugías. (Nivel de acuerdo 9).
- •
El TIPS se utiliza como terapia de rescate para prevenir el resangrado variceal. (Nivel de acuerdo 9).
La GPH ocasiona aproximadamente un 25% de todos los sangrados (agudos y crónicos) en pacientes con hipertensión portal. La presentación más común es de un sangrado crónico y anemia. La terapia farmacológica no se recomienda en la actualidad para prevenir sangrado agudo (profilaxis primaria) en pacientes con GPH. Sin embargo, los BBNS se han recomendado para prevenir sangrado crónico por GPH204,205.
Recomendación:
- •
En pacientes con sangrado crónico por GPH se recomienda como primera opción el uso de BBNS y suplementos de hierro. (Nivel de acuerdo 9).
El actual Consenso Mexicano de Hipertensión Portal contó con el apoyo de la Asociación Mexicana de Gastroenterología, Asociación Mexicana de Hepatología y Asociación Mexicana de Endoscopia Gastrointestinal, las cuales participaron en la organización de las reuniones, elaboración de los enunciados y proceso de votación.
Conflicto de interésesLos autores declaran no tener ningún conflicto de interés en la redacción del documento final.