La colitis ulcerosa crónica idiopática (CUCI) es una enfermedad que dura toda la vida y surge de la interacción entre factores genéticos y ambientales, observados principalmente en países desarrollados.
Se desconoce la etiología precisa, y por lo tanto no hay disponible terapia médica que cure la enfermedad. Dentro de Europa existe un gradiente norte–sur, sin embargo, en los últimos años parece haberse incrementado la incidencia en los países del sur y del este1,2. Los pacientes pueden vivir con una gran cantidad de sintomatología a pesar del tratamiento médico (el 66% describen interferencia con su trabajo y el 73% con sus actividades recreativas3) esperando que la etiología de la CUCI se revele muy pronto y surja una cura. Aunque es concebible que esto ocurra en la siguiente década, los médicos tienen que aconsejar a los pacientes basándose en la información actualmente disponible. A pesar de los estudios aleatorizados, siempre habrá muchas preguntas que únicamente pueden responderse mediante el ejercicio de juicio y opinión. Esto lleva a diferencias en la práctica entre médicos, que se demuestra claramente por las diversidades en el énfasis entre países.
Este Consenso intenta abordar estas diferencias. El Consenso no intenta que se reemplacen las guías de los diferentes países (como las del Reino Unido4 o Alemania5), que llegan básicamente a las mismas conclusiones, ya que, después de todo, se basan en la misma evidencia. Más bien, el objetivo del Consenso es promover una perspectiva europea en el manejo de la CUCI y sus problemas. Debido a que el desarrollo de las guías es un proceso caro y que requiere tiempo, esto puede ayudar a evitar la duplicación del esfuerzo en el futuro. Un Consenso europeo también se considera importante debido a un número cada vez mayor de estudios terapéuticos que reclutan pacientes en países de Europa Central y Oriental, donde todavía no se han publicado guías de práctica clínica.
Este documento es una actualización del Consenso Europeo anterior sobre el diagnóstico y manejo de la CUCI, y fue terminado por la Organización Europea para la Enfermedad de Crohn y la Colitis (ECCO) en una reunión celebrada en Dublín en febrero de 2011. La ECCO es un foro para especialistas de 31 países europeos en enfermedad inflamatoria intestinal (EII). Al igual que el Consenso inicial sobre el diagnóstico y manejo de la CUCI6–8, este Consenso actualizado se encuentra agrupado en 3 partes: definiciones y diagnóstico, manejo actual y manejo de situaciones especiales. Esta primera sección trata de los objetivos, métodos y definiciones del Consenso, así como de la clasificación, diagnóstico, imaginología y patología de la CUCI. La segunda sección trata sobre el manejo actual e incluye el tratamiento de la enfermedad activa, mantenimiento de la remisión inducida por medicamentos y la cirugía en CUCI. La tercera sección trata sobre situaciones especiales e incluye trastornos del reservorio ileoanal, vigilancia del cáncer, manifestaciones psicosomáticas y extraintestinales. Los capítulos incluidos anteriormente sobre embarazo y pediatría ya no se incluyen en estas guías, debido a que las Guías del Consenso de la ECCO sobre Reproducción y Embarazo y CUCI Pediátrica (junto con ESPGHAN) cubren extensamente estos temas9–11. Las terapias alternativas se incluyen ahora en la sección 2 bajo el título de manejo de la enfermedad activa y la terapia de mantenimiento en CUCI. La atención también se dirige a otras Guías del Consenso de ECCO sobre endoscopia del intestino delgado12, infecciones oportunistas13 y próximamente guías sobre cirugía, imaginología, endoscopia, patología y manejo de la anemia en la EII (www.ecco-ibd.eu).
La estrategia para lograr el Consenso implicó 5 pasos:
- 1.
Para el desarrollo de las primeras guías de ECCO publicadas en 20086–8, los presidentes y sus colaboradores formularon preguntas relevantes sobre cada uno de los 14 temas por separado con respecto al diagnóstico y tratamiento de la CUCI. Las preguntas se enfocaron en la práctica clínica actual y en los temas de controversia. A los participantes se les pidió responder a las preguntas basándose en su experiencia, así como en evidencia de la literatura (procedimiento Delphi)14. Para esta actualización, se realizó una llamada abierta a los participantes (ver el apartado de «Agradecimientos» y www.ecco-ibd). El Comité de las Guías de la ECCO (GuiCom) seleccionó a los participantes basándose en su historial de publicaciones y una declaración personal. Se establecieron los grupos de trabajo que revisaron las declaraciones del Consenso publicadas en 20086–8 y recomendaron si requerían revisión, basándose en los avances de la literatura publicada. Hubo un acuerdo de que no había necesidad de una revisión extensa de la sección de histopatología, ni de la sección sobre embarazo y CUCI pediátrica que no se incluirá en futuras guías de la CUCI, en vista de la existencia de guías específicas del Consenso de la ECCO que sirven como referencia para estas áreas9,10.
- 2.
De manera paralela, los grupos de trabajo realizaron una búsqueda sistemática de la literatura de los temas con las palabras clave apropiadas utilizando Medline/PubMed y la base de datos de Cochrane, así como sus propios archivos. El nivel de evidencia (NE) fue clasificado (tabla 1) de acuerdo con el Centro de Oxford para la Medicina Basada en Evidencia15.
Tabla 1.Niveles de evidencia y grados de recomendación basados en el Centro de Oxford para la Medicina Basada en Evidencia Para más detalles ver http://www.cebm.net/levels_of_evidence.asp#refs)a
Nivel Estudio diagnóstico Estudio terapéutico 1a Revisión sistemática (RS) con homogeneidad de los estudios de diagnóstico nivel 1 Revisión sistemática (RS) con homogeneidad de estudios aleatorizados controlados (RCT) 1b Estudio de cohorte de validación con buenos estándares de referencia RCT individual (con un intervalo de confianza estrecho) 1c La especificidad es tan alta que un resultado positivo rige el diagnóstico («SpPin») o la sensibilidad es tan alta que un resultado negativo descarta el diagnóstico («SnNout») Todo o nada 2a RS con homogeneidad de los estudios de diagnóstico de nivel>2 RS (con homogeneidad) de los estudios de cohorte 2b Estudio de cohorte exploratorio con buenos estándares de referencia Estudio de cohorte individual (incluyendo RCT de baja calidad; por ejemplo, <80% de seguimiento) 2c Investigación de «Resultados»; estudios ecológicos 3a RS con homogeneidad de 3b y mejores estudios RS con homogeneidad de los estudios de casos-controles 3b Estudio no consecutivo; o sin estándares de referencia consistentemente aplicados Estudio individual de casos-controles 4 Estudio de casos-controles, estándar de referencia poco favorable o no independiente Estudio de serie de casos (y estudios de cohorte de mala calidad y de casos-controles) 5 Opinión de expertos sin evaluación crítica explícita, o basada en la fisiología, investigación de laboratorio o «primeros principios» Opinión de expertos sin evaluación crítica explícita, o basada en la fisiología, investigación de laboratorio o «primeros principios» Grados de recomendación A Estudios de nivel 1 consistente B Estudios de nivel 2 o 3 consistente o extrapolaciones de los estudios de nivel 1 C Estudios de nivel 4 o extrapolaciones de estudios de nivel 2 o 3 D Evidencia de nivel 5 o estudios alarmantemente inconsistentes o inconclusos de cualquier nivel - 3.
Las declaraciones revisadas sobre los temas fueron redactadas por los presidentes, con base en las respuestas de su grupo de trabajo, así como la evidencia de la literatura, y primero se publicaron entre su grupo de trabajo y luego entre todos los participantes.
- 4.
Todos los grupos de trabajo se reunieron en Dublín en febrero de 2011 para acordar las declaraciones. Los participantes se reunieron bajo la Presidencia de A. Dignass y G. van Assche para llegar a un acuerdo sobre la versión final de cada declaración. Técnicamente, esto se hizo mediante la proyección de las declaraciones en una pantalla y revisándolas hasta lograr un consenso. Se definió consenso como un acuerdo por parte de más del 80% de los participantes, definiéndose como una Declaración de Consenso y numerado por conveniencia en el documento. Cada recomendación se clasificó (RG) de acuerdo con el Centro de Oxford para la Medicina Basada en Evidencia15, basados en el nivel de evidencia (tabla 1).
- 5.
El documento final de cada tema fue redactado por los presidentes junto con su equipo de trabajo. Las declaraciones del Consenso aparecen en recuadros con fondo gris y están seguidas de comentarios sobre la evidencia y la opinión. Las declaraciones están hechas para leerse en contexto con los comentarios calificativos y no para leerse de manera aislada. El texto final fue editado por A. Dignass, G. van Assche y J.O. Lindsay para dar consistencia de estilo antes de publicarlo y ser aprobado por los participantes. En algunas áreas el nivel de evidencia es generalmente bajo, lo que refleja la escasez de estudios aleatorizados controlados. Por consiguiente, se incluyó la opinión de expertos donde se consideró conveniente.
La ECCO llegó a un acuerdo común acerca de los términos frecuentemente utilizados. Aunque el significado de algunos términos (como «temprano» o «patrón de recaída») quedó indeterminado, dichos términos reflejan la toma de decisiones clínicas (como cuándo iniciar los inmunomoduladores) y como consecuencia se consideran útiles. Se reconoce la arbitrariedad de algunas de las definiciones, pero el Consenso considera que es útil llegar a un acuerdo en la terminología.
La CUCI es una condición inflamatoria crónica que causa inflamación continua de la mucosa colónica sin granulomas en la biopsia, que afecta al recto y en extensión variable al colon contiguo, que se caracteriza por tener un curso con recaídas y remisiones16.
EII no clasificada es el término más conveniente para la minoría de los casos donde no puede hacerse una distinción definitiva entre CUCI, enfermedad de Crohn u otra causa de colitis después de que se han tomado en cuenta los antecedentes, los hallazgos endoscópicos, la histopatología de múltiples biopsias de la mucosa y la radiología adecuada16,17.
Colitis indeterminada es un término reservado para que los patólogos describan una muestra de colectomía que tiene características tanto de CUCI como de enfermedad de Crohn17,18. Esto tiene diferentes factores pronósticos relacionados con una cirugía posterior.
Distribución de la enfermedadEl Consenso prefiere el uso de la clasificación Montreal (tabla 216) para definir la distribución de la enfermedad. Esta se utiliza para describir la extensión macroscópica máxima de la enfermedad en la colonoscopia, debido a que en el pasado la extensión de la enfermedad según lo visto por enema de bario se ha utilizado como indicador para el pronóstico a largo plazo de la CUCI. Todavía no se saben las implicaciones de una enfermedad microscópica más extensa. Se reconoce la mala correlación entre la extensión macroscópica y microscópica de la enfermedad (kappa=0.39)17. Esto también es válido para una clasificación basada en la extensión, dado que la esta varía con el tiempo, subrayando la naturaleza dinámica de la EII19.
Distribución de la colitis ulcerosa crónica idiopática16
| Término | Distribución | Descripción |
|---|---|---|
| E1 | Proctitis | Afectación limitada al recto (esto es, la extensión proximal de la inflamación es distal a la unión rectosigmoidea) |
| E2 | Colitis izquierda | Afectación limitada a la porción del colon distal a la flexura esplénica (análoga a «colitis distal») |
| E3 | Extensa | La afectación se extiende hasta la flexura esplénica, incluye pancolitis |
Existe cierta evidencia que sugiere que los pacientes con CUCI estratificados por edad (A1:<16; A2:16-40 y A3: >40 años) tienen diferentes cursos de la enfermedad. Se encontró que los pacientes diagnosticados antes de los 16 años tienen un curso inicial más agresivo, mientras que el diagnóstico en una edad más avanzada estuvo asociado con un menor riesgo de colectomía20,21. También existe cierta evidencia de que la CUCI diagnosticada en la infancia tiene una etiología y pronóstico diferentes. Esto se toma en consideración para la modificación de la clasificación de Montreal para edades pediátricas22.
Enfermedad activaPara los fines de este Consenso, la actividad clínica de la enfermedad se agrupó en remisión, leve, moderada y grave. Esto se refiere a la actividad biológica y no a la respuesta al tratamiento (ver la sección 1.2.8). Son necesarias definiciones precisas de la actividad de la enfermedad debido a que surge la confusión de si los términos se utilizan para referirse únicamente al tercio mínimo, intermedio o más grave de los casos que el médico pueda recordar en el momento. Entre 2006 participantes del Consenso, 31/59 consideraron los criterios de Truelove y Witts útiles en la práctica clínica (resumidos en la tabla 323), junto con la sigmoidoscopia para confirmar colitis activa.
Actividad de la enfermedad CUCI, adaptada de Truelove y Witts.23
| Leve | Moderada «entre leve y grave» | Grave | |
|---|---|---|---|
| Heces con sangre/día | <4 | 4 o más si | ≥6 y |
| Frecuencia cardiaca | <90lpm | ≤90lpm | >90lpm o |
| Temperatura | <37.5°C | ≤37.8°C | >37.8°C o |
| Hemoglobina | >11.5g/dL | ≥10.5g/dL | <10.5g/dL o |
| VSG | <20mm/h | ≤30mm/h | >30mm/h o |
| o PCR | Normal | ≤30vmg/L | >30mg/L |
El valor de los diferentes índices para fines de ensayos clínicos está más allá del alcance del Consenso, pero ha sido revisado en otro lugar24. La ECCO reconoce la necesidad de validar los sistemas de puntuación clínicos y endoscópicos.
Se prefiere el término CUCI grave (o «colitis aguda grave») a «colitis fulminante», debido a que el término «fulminante» es impreciso. Este término fue acuñado en 1950 y se refería a una exacerbación única que terminaba en muerte dentro del periodo de un año26, lo cual actualmente ya no tiene relevancia. La CUCI grave según lo definido por los criterios de Truelove y Witts (tabla 3 y sección 5.1) es fácil de aplicar en pacientes ambulatorios, ordena la hospitalización para un tratamiento intensivo y define un resultado (únicamente el 70% responde a terapia intensiva). Estos criterios son recomendados por el Colegio Americano de Gastroenterología (ACG)27 y la Asociación de Coloproctología de Gran Bretaña e Irlanda (ACPGBI)28, así como por la ECCO para identificar CUCI grave.
La CUCI moderada se ha vuelto necesaria para distinguir de la enfermedad levemente activa, porque la eficacia de algunos tratamientos puede diferir (sección 5). La medida clínica más simple para distinguir la CUCI moderada de la levemente activa es la presencia de friabilidad mucosa (sangrado al contacto ligero con la mucosa rectal en la sigmoidoscopia). La técnica de evaluación de la friabilidad mucosa con sigmoidoscopia flexible aún tiene que estandarizarse. Una estrategia es aplicar suficiente presión sobre la mucosa con la pinza de biopsia cerrada para crear una hendidura, mantener la presión durante 3seg y luego definir la friabilidad si ocurre sangrado desde el punto de presión. Esto aún tiene que validarse. Para la revisión de los diversos índices de actividad ver D’Haens et al.24.
Se reconoce una amplia variación en la interpretación endoscópica de la actividad de la enfermedad (sección 3.6.1).
RemisiónLa remisión se define como la resolución completa de síntomas y cicatrización endoscópica de la mucosa (sección 2.2.4). La combinación de las índices clínicos y endoscópicos es apropiada para ensayos clínicos24,29, pero las tasas de remisión reportadas varían hasta 2 veces más, dependiendo de la definición de remisión utilizada en el ensayo30. En la práctica clínica, los participantes estuvieron de acuerdo en que la «remisión» significaba una frecuencia de las deposiciones≤3/día sin sangrado y sin urgencia. La remisión definida por pacientes individuales tiene una sensibilidad del 86% y una especificidad del 76% para una remisión definida por las regulaciones (ausencia de sangre visible y ausencia de friabilidad de la mucosa), indicando que realizar una sigmoidoscopia para confirmar la cicatrización de la mucosa generalmente es innecesaria en la práctica31.
RespuestaLa respuesta se define como la mejoría clínica y endoscópica, dependiendo (para los fines de ensayos clínicos) del índice de actividad utilizado. En general, esto significa una disminución en el índice de actividad de>30%, además de una disminución del sangrado rectal y subpuntuaciones de la endoscopia, pero existen muchas variables24.
RecaídaEl término recaída se utiliza para definir la exacerbación de los síntomas en un paciente con CUCI establecida y que se encuentra en remisión clínica, sea de manera espontánea o después de tratamiento médico. En el Consenso, 47/59 consideraron el sangrado rectal como componente esencial de la recaída y 29/59 consideraron necesaria una combinación de sangrado rectal con un incremento en la frecuencia de las deposiciones y mucosa anormal en la sigmoidoscopia para definir la recaída. En los ensayos clínicos, los criterios para la recidiva deben predefinirse con la puntuación que se está utilizando para cada estudio individualmente24.
Recaída tempranaUn periodo arbitrario, pero clínicamente relevante de<3meses después de lograr la remisión con terapia previa define la recaída temprana. Necesita definirse su significado en la terapéutica.
Patrón de recaídaLa recaída puede ser poco frecuente (≤1/año), frecuente (≥2 recaídas/año) o continu (síntomas persistentes de CUCI activa sin un periodo de remisión)32. Aunque los términos son arbitrarios, se consideran clínicamente relevantes. Se ha propuesto un enfoque alternativo que defina la actividad de la enfermedad en un periodo de 5 años (sección 2.1.1), pero esto parece ser más útil para estudios epidemiológicos, debido a que lo que importa en la práctica clínica diaria es lo que probablemente ocurrirá en el siguiente año. Necesita definirse el significado que tiene para el pronóstico. Sin embargo, deberá tenerse cuidado para distinguir entre los términos que describen la actividad de la enfermedad en un momento en el tiempo y los que describen el patrón longitudinal (o «de comportamiento») de la enfermedad (secciones 1.2.3 y 2.2.1). El término «enfermedad activa crónica» se ha utilizado en el pasado para definir a un paciente que es dependiente, refractario o intolerante a esteroides, o a quien tenga actividad de la enfermedad a pesar de la terapia con inmunomoduladores. Dado que este término es ambiguo, es mejor evitar su uso. En su lugar, se prefieren las definiciones arbitrarias, pero más precisas, incluyendo refractario a esteroides o dependiente de esteroides.
Colitis ulcerosa crónica idiopática refractaria a esteroidesPacientes que tienen enfermedad activa a pesar de una dosis de prednisolona de hasta 0.75mg/kg/día en un periodo de 4 semanas. Esta definición coincide con la definición de enfermedad de Crohn refractaria a esteroides33, sin embargo, es probable que se modifique, con una reducción en la duración de la terapia con esteroides a medida que cambie el umbral para la terapia biológica.
Colitis ulcerosa crónica idiopática dependiente de esteroidesPacientes que sean
- i)
incapaces de reducir la dosis de esteroides por debajo del equivalente de prednisolona de 10mg/día dentro de los primeros 3 meses con tratamiento, sin enfermedad activa recurrente, o
- ii)
que tengan una recaída en los primeros 3 meses después de haber suspendido los esteroides.
Esto coincide con la definición para la enfermedad de Crohn dependiente de esteroides33, aunque se ha propuesto una definición alternativa de recaída dentro de los primeros 30 días después de completar el tratamiento de esteroides o esteroides en una dosis de 15-25mg/día durante al menos 6 meses23. Al igual que la definición de refractario a esteroides, es probable que la definición se modifique a medida que cambie el umbral para iniciar la terapia biológica.
La definición de la ECCO de dependencia de esteroides requiere que la duración total de la terapia con esteroides no exceda los 3 meses antes de que se alcance un umbral equivalente a una dosis de prednisolona de 10mg/día. Los pacientes aún se consideran dependientes de esteroides si tienen una recaída dentro de los primeros 3 meses después de la suspensión de los mismos. Aunque estos límites son arbitrarios, sirven como una guía para la práctica clínica y pueden utilizarse para uniformidad en los estudios clínicos. El objetivo debe ser suspender los esteroides por completo.
Colitis ulcerosa crónica idiopática refractaria a inmunomoduladoresSon pacientes con enfermedad activa o recaída a pesar de terapia con tiopurinas en una dosis adecuada durante al menos 3 meses (esto es, azatioprina 2-2.5mg/kg/día o 6-mercaptopurina 1-1.5mg/kg/día en ausencia de leucopenia). La definición es arbitraria, pero tiene una mayor relevancia clínica cuando se toma en cuenta para la decisión del inicio de terapia biológica o cirugía.
Colitis ulcerosa crónica idiopática distal refractariaDefinida como síntomas persistentes debido a inflamación colónica confinada al recto (proctitis) o al colon izquierdo, a pesar de tratamiento con esteroides orales y tópicos, y 5-ASA durante 4-8 semanas. Esto representa un problema clínico común, aunque no queda claro si es una entidad separada.
Paciente nuevoUn paciente con CUCI activa que se presenta al diagnóstico o poco después de que se realiza este, sin terapia previa para CUCI.
Terapia alternativaLa terapia que se utiliza en lugar de la medicina convencional.
Terapias complementariasTratamientos utilizados junto con la medicina convencional.
Opinión de expertosEl término «expertos» se utiliza aquí para referirse a la opinión de los especialistas en EII, que representan múltiples disciplinas de 31 países europeos y que contribuyeron al Consenso de ECCO. En algunas secciones se obtuvieron las opiniones de miembros individuales de otros equipos de expertos, incluyendo a miembros del grupo de trabajo de Enfermedades Digestivas de la Sociedad Europea de Patología (ESP), la Sociedad Europea de Radiología Gastrointestinal y Abdominal (ESGAR) y la Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátricas (ESPGHAN).
ClasificaciónClasificación de acuerdo a la extensión de la enfermedadDeclaración 2A de la ECCO
La extensión de la CUCI influye en el manejo del paciente. La extensión de la enfermedad influye en la modalidad del tratamiento y determina si se inicia la terapia oral y/o tópica (NE1b, RG B). La extensión de la enfermedad influye en el inicio y frecuencia de la vigilancia (NE2, RG B). Por lo tanto, se recomienda una clasificación de acuerdo con la extensión de la enfermedad (NE5, RG D).
La clasificación preferida es una clasificación endoscópica como se indica en la clasificación de Montreal: proctitis ulcerosa (limitada al recto), colitis izquierda (hasta la flexura esplénica) y colitis extensa, y por extensión máxima en el seguimiento (NE5, RG D).
Existen diversas razones por las que los pacientes con CUCI deben clasificarse de acuerdo a la extensión de la enfermedad. En primer lugar, la extensión de la inflamación influirá en el manejo del paciente y en la elección del sistema de administración de una terapia determinada. Por ejemplo, la terapia tópica en forma de supositorios (para proctitis) o enemas (para colitis distal) es generalmente el tratamiento de primera elección, mientras que la terapia oral —a menudo combinada con terapia tópica— es la adecuada para la colitis extensa (NE1b, RG B). En segundo lugar, la extensión de la colitis influye en el inicio y la frecuencia de vigilancia (NE2, RG B). En el estudio hecho en la población de Suecia34, la extensión de la enfermedad fue uno de los factores de riesgo para el desarrollo de cáncer colorrectal en 3,117 pacientes con CUCI seguido de 1 a 60 años después del diagnóstico. No se atribuyó ningún aumento del riesgo relativo a la enfermedad confinada al recto, mientras que el riesgo relativo para colitis distal y colitis extensa (previamente llamada pancolitis) fue de 2.8 (IC de 95% 1.6-4.4) y 14.8 (IC de 95% 11.4-18.9), respectivamente. Por lo tanto, a los pacientes con colitis distal y colitis extensa generalmente se les aconseja hacerse colonoscopia de vigilancia, mientras que los pacientes con proctitis no necesitan vigilancia (sección 2.2). La contribución de la extensión de la enfermedad en el momento del diagnóstico al riesgo de cáncer se ha confirmado más recientemente por el grupo de estudio de EC-IBD31.
El grupo del Consenso acordó que la clasificación preferida se basa en la endoscopia y divide la enfermedad en proctitis, colitis distal y colitis extensa (más allá de la flexura esplénica), según lo definido por el Grupo de Trabajo de Montreal en la Clasificación Molecular de EII16,17 (sección 1.1, tabla 2).
Clasificación de acuerdo a la gravedad de la enfermedadDeclaración 2B de la ECCO
La clasificación de CUCI basada en la gravedad de la enfermedad es útil en la práctica clínica y dicta el manejo del paciente (NE1b, RG B). La gravedad de la enfermedad influye en la modalidad del tratamiento y determina si se inicia o no terapia oral, intravenosa o quirúrgica. Los índices de gravedad de la enfermedad no se han validado adecuadamente. Los parámetros clínicos, bioquímicos, de imagen y endoscópicos, incluyendo la histopatología, ayudan a los médicos en el manejo de los pacientes (NE2, RG B). No hay definición de remisión completamente validada. La mejor manera de definir la remisión es una combinación de parámetros clínicos (esto es, frecuencia de deposición ≤3/día sin sangrado) y una mucosa normal en la endoscopia (NE5, RG D). La ausencia de un infiltrado inflamatorio agudo en la histología es útil.
En un estudio hecho en la población del Municipio de Copenhague, Langholz et al. demostraron que aproximadamente el 50% de los pacientes se encontrarán en remisión clínica en algún momento durante un año determinado35. Sin embargo, la probabilidad acumulativa de un curso de recaídas después de 25 años de seguimiento equivale al 90%. La actividad de la enfermedad en los primeros 2 años después del diagnóstico indicó (con un 70-80% de probabilidad) una probabilidad mayor de 5 años consecutivos de enfermedad activa, y por lo tanto se consideró como un buen parámetro para predecir el futuro patrón de actividad de la enfermedad.
El compromiso microscópico también parece ser importante. En los pacientes con CUCI inactiva estuvo presente un infiltrado inflamatorio crónico de células en todas las muestras. Un 52% de los pacientes con un infiltrado inflamatorio agudo de células tuvieron una recaída después de 12 meses de seguimiento, mientras que en ausencia del infiltrado solo el 25% tuvo recaída (p=0.02). De manera similar, las tasas de recaída fueron más altas en presencia de abscesos crípticos, depleción de mucina y fisuras en el epitelio superficial36. El grado de inflamación intestinal también es un factor de riesgo para cáncer colorrectal en pacientes con CUCI extensa de larga duración37.
Debe hacerse una distinción entre la actividad de la enfermedad en un punto en el tiempo (remisión, leve, moderada, grave) y la respuesta de la enfermedad al tratamiento (utilizando términos como respondedor a 5-ASA o a esteroides, refractaria a esteroides, dependiente de biológico, etc.). No deben confundirse los 2 por terminología inadecuada que describa enfermedad levemente activa que sea dependiente de esteroides como «grave». De hecho, las consecuencias (terapia biológica, colectomía) pueden considerarse «graves», pero la actividad de la enfermedad permanece como leve.
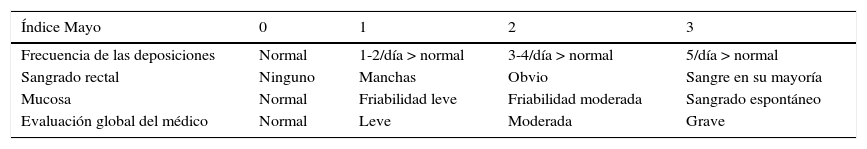
Elección del índiceEs importante una clasificación de la CUCI basada en la actividad y gravedad de la enfermedad porque influye en el manejo del paciente. La gravedad de la inflamación determinará si se inicia o no terapia oral, intravenosa o quirúrgica en un paciente determinado. Se han propuesto muchos índices o criterios de la actividad de la enfermedad (ver la sección 1.2.3 y D’Haens et al.24 para una revisión), pero ninguno se ha validado adecuadamente. El Consenso reconoce la necesidad de índices clínicos y endoscópicos validados que se relacionen con el resultado o las decisiones del tratamiento. Aunque las modificaciones de los criterios originales de Truelove y Witts (sección 1.2.3, tabla 3) se utilizan en la práctica diaria, la puntuación Mayo modificada (sección 1.2.3, tabla 4) se utiliza de manera más frecuente en los ensayos clínicos actuales23. Para la práctica clínica, el grupo del Consenso consideró que una combinación de características clínicas, hallazgos de laboratorio, modalidades de imaginología y parámetros endoscópicos, incluyendo histopatología, ayudarán a los médicos en el manejo de sus pacientes. La puntuación endoscópica se ilustra en la sección 3.5 y la tabla 6.
Puntuación Mayo24,25 ver www.gastrojournal.org para más detalles
| Índice Mayo | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
| Frecuencia de las deposiciones | Normal | 1-2/día > normal | 3-4/día > normal | 5/día > normal |
| Sangrado rectal | Ninguno | Manchas | Obvio | Sangre en su mayoría |
| Mucosa | Normal | Friabilidad leve | Friabilidad moderada | Sangrado espontáneo |
| Evaluación global del médico | Normal | Leve | Moderada | Grave |
La clasificación de Montreal (tabla 5)16,17 se basa principalmente en los criterios de Truelove y Witts, ya que estos reflejan la práctica clínica.
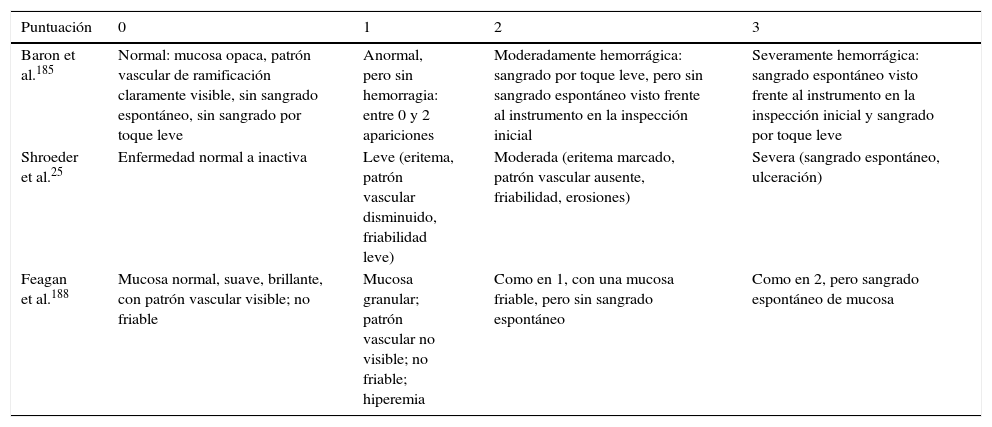
Puntuaciones endoscópicas para colitis ulcerosa crónica idiopática comúnmente utilizadas en estudios clínicos
| Puntuación | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
| Baron et al.185 | Normal: mucosa opaca, patrón vascular de ramificación claramente visible, sin sangrado espontáneo, sin sangrado por toque leve | Anormal, pero sin hemorragia: entre 0 y 2 apariciones | Moderadamente hemorrágica: sangrado por toque leve, pero sin sangrado espontáneo visto frente al instrumento en la inspección inicial | Severamente hemorrágica: sangrado espontáneo visto frente al instrumento en la inspección inicial y sangrado por toque leve |
| Shroeder et al.25 | Enfermedad normal a inactiva | Leve (eritema, patrón vascular disminuido, friabilidad leve) | Moderada (eritema marcado, patrón vascular ausente, friabilidad, erosiones) | Severa (sangrado espontáneo, ulceración) |
| Feagan et al.188 | Mucosa normal, suave, brillante, con patrón vascular visible; no friable | Mucosa granular; patrón vascular no visible; no friable; hiperemia | Como en 1, con una mucosa friable, pero sin sangrado espontáneo | Como en 2, pero sangrado espontáneo de mucosa |
Entre las características clínicas objetivas, la frecuencia de deposiciones con sangre, la temperatura corporal y la frecuencia cardiaca son buenos predictores de resultado. Los marcadores de laboratorio se han estudiado de manera intensiva con grados variables de éxito. La ampliamente utilizada proteína C reactiva de fase aguda (PCR) no es un marcador tan bueno para evaluar la actividad de la enfermedad en la CUCI como lo es en la enfermedad de Crohn, excepto para colitis aguda grave, donde tiene un valor establecido tanto en adultos como en niños38–40. Un aumento de la PCR>45mg/L en el día 3 después de la hospitalización por CUCI grave junto con 3-8 deposiciones al día es altamente predictiva de colectomía (sección 1.2.5). Se han estudiado otras proteínas de fase aguda positivas (velocidad de sedimentación globular [VSG], procalcitonina en suero41) o negativas (albúmina), pero ninguna ha demostrado una clara superioridad (para revisión ver Vermeire et al.42). Más recientemente, los marcadores fecales han demostrado resultados prometedores. Los marcadores más estudiados son calprotectina y lactoferrina fecal, pero la elastasa y el marcador más reciente S100A12 también han demostrado precisión en detectar inflamación del colon43–47. Estudios recientes enfatizan el valor de la calprotectina como una herramienta para el diagnóstico y la evaluación de la gravedad de la enfermedad (que se correlaciona con los índices endoscópicos, de recaída y de respuesta al tratamiento)48–51. Sin embargo, debe enfatizarse que ninguno de estos marcadores es específico de CUCI, ya que la mayoría representan inflamación del colon con una afluencia de neutrófilos en la mucosa intestinal, con la subsecuente liberación de gránulos citoplasmáticos a la luz intestinal.
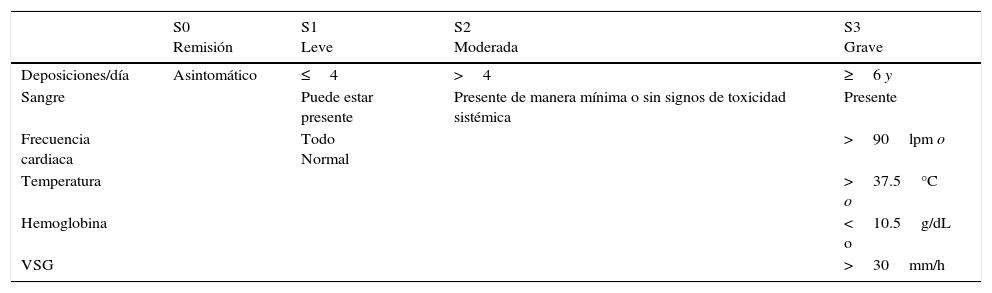
Clasificación de Montreal de actividad de la enfermedad en CUCI.16
| S0 Remisión | S1 Leve | S2 Moderada | S3 Grave | |
|---|---|---|---|---|
| Deposiciones/día | Asintomático | ≤4 | >4 | ≥6 y |
| Sangre | Puede estar presente | Presente de manera mínima o sin signos de toxicidad sistémica | Presente | |
| Frecuencia cardiaca | Todo Normal | >90lpm o | ||
| Temperatura | >37.5°C o | |||
| Hemoglobina | <10.5g/dL o | |||
| VSG | >30mm/h |
Al igual que ocurre con la definición de actividad de la enfermedad, tampoco existe una definición completamente validada de remisión. El grupo del Consenso acordó que la mejor manera de definir la remisión es una combinación de los parámetros clínicos (frecuencia de las deposiciones≤3/día sin sangrado) y mucosa normal o sin signos de actividad en la endoscopia30.
Clasificación de acuerdo a la edad al inicio o a colangitis esclerosante primaria concomitanteDeclaración 2C de la ECCO
Una clasificación de la CUCI de acuerdo con la edad al inicio resulta valiosa (NE2, RG B). La clasificación de la CUCI de acuerdo con la presencia concomitante de colangitis esclerosante primaria (CEP) es importante porque influye en el manejo de los pacientes (y la vigilancia) (NE2, RG C).
Una clasificación de acuerdo con la edad al inicio resulta valiosa. Los pacientes jóvenes con CUCI tienden a tener una enfermedad más agresiva y utilizan más inmunomoduladores, mientras que los pacientes diagnosticados con CUCI a mayor edad (A3) tienden a tener una enfermedad de curso más leve con menor necesidad de cirugía. Todas las terapias actualmente disponibles para la CUCI han demostrado una eficacia equivalente en niños y en adultos. El riesgo aparentemente mayor de cáncer colorrectal en pacientes con CUCI de inicio en la infancia seguramente refleja la duración de la enfermedad. Sin embargo, la CEP concomitante es una característica importante en pacientes con CUCI debido a un mayor riesgo asociado con cáncer colorrectal34,48. Esto influye en las decisiones sobre la vigilancia colonoscópica (sección 2.2).
Uso de marcadores molecularesSe han descrito varios (auto)anticuerpos en pacientes con CUCI, de los cuales los que mejor se conocen son los anticuerpos anticitoplásmaticos de neutrófilos perinucleares atípicos (pANCA). Se encuentra serología positiva para pANCA en aproximadamente el 50-60% de los pacientes, aunque existe gran variabilidad debido a diferencias en la metodología52,53. En general, los pANCA ha mostrado buena precisión para diferenciar la enfermedad de Crohn de la CUCI54–57, pero su sensibilidad no es lo suficientemente alta para justificar su uso en el diagnóstico. Estos anticuerpos tampoco son precisos en los pacientes con colitis aún por clasificar, donde los marcadores de diagnóstico serían de gran valor clínico. Otros anticuerpos antimicrobianos como anticuerpos anti-Saccharomyces cerevisiae, OmpC, I2, cBir antiflagelina, ALCA, ACCA, se encuentran principalmente en pacientes con enfermedad de Crohn58–61.
GenotipificaciónEl campo muy activo de genética de la EII ha llevado a la identificación de más de 160 variantes genéticas confirmadas, que están implicadas en una susceptibilidad a enfermedad de Crohn o CUCI. La región HLA es sin ninguna duda la región más asociada con CUCI62, sin embargo, el gen del receptor de interleucina 23 (IL23R) en el cromosoma 163, el gen DLG5 en el cromosoma 1064, la vía JAK/STAT, el gen de resistencia a multifármacos-1 y los genes del receptor tipo Toll (TLR) han demostrado una asociación con CUCI65–73. Recientemente, una amplia asociación del genoma identificó múltiples loci de susceptibilidad a CUCI, una de las cuales fue en 7q22 y 22q13 (IL17REL)74–76. Debido a que la CUCI es una enfermedad multifactorial compleja, las mutaciones asociadas a la enfermedad en estos genes nunca serán suficientes para causar la enfermedad, ni tampoco la ausencia de mutaciones es una garantía de permanecer libre de enfermedad. Por lo tanto, las pruebas para estas variantes genéticas no se recomiendan para propósitos clínicos.
Diagnóstico e imaginologíaIntroducciónLa CUCI se presenta principalmente en la adolescencia tardía y la etapa adulta temprana, aunque el diagnóstico puede hacerse en cualquier edad. Se ha demostrado un pequeño pico en la incidencia en algunas poblaciones después de la quinta década de vida77. La CUCI parece afectar a ambos sexos por igual. La inflamación característicamente comienza en el recto y se extiende proximalmente de forma continua, confluente y concéntrica para afectar una extensión variable del colon o toda su superficie mucosa. Las definiciones y clasificación de la extensión de la CUCI han sido detalladas en las secciones 1.1 y 2.1 (tabla 2)16. La extensión proximal de la inflamación puede avanzar o regresar con el tiempo, pero después de la regresión de la enfermedad la distribución de la inflamación tiende a volver a ser la misma que en episodios anteriores en el caso de una recaída. Sin embargo, reportes de una variante que respeta la región rectal y de una inflamación periapendicular en parches han desafiado la idea de que la CUCI representa una inflamación colónica continua78. Los síntomas dependen de la extensión y gravedad de la enfermedad, las manifestaciones extraintestinales y la terapia concomitante. Los patógenos entéricos también pueden alterar la presentación clínica.
Características clínicas y factores de riesgoCaracterísticas clínicas de la colitis ulcerosa crónica idiopáticaDeclaración 3A de la ECCO
Los síntomas de la CUCI dependen de la extensión y gravedad de la enfermedad, los más comunes incluyen diarrea con sangre, sangrado rectal y/o urgencia rectal. También se reporta con frecuencia defecación nocturna. Síntomas sistémicos como malestar general, anorexia o fiebre son características de un ataque grave (NE5, RG D).
El principal síntoma presente en CUCI es sangre visible en las heces y se reporta en más del 90% de los pacientes. Los síntomas asociados generalmente reflejan la gravedad endoscópica de la enfermedad como una medida de daño a la mucosa y puede diferir de acuerdo con la extensión de la enfermedad79–89. Una disminución en la consistencia de las heces durante más de 6 semanas diferencia a la CUCI de la mayoría de las diarreas infecciosas90. Los pacientes con CUCI extensa activa se presentan con diarrea crónica casi invariablemente asociada a sangrado rectal, o al menos sangre visible en las heces. Dichos pacientes también describen urgencia rectal, tenesmo, exudado mucopurulento, defecación nocturna y dolor abdominal tipo cólico o localizado en la fosa ilíaca izquierda antes de la defecación y aliviado con la misma. En contraste, los pacientes con proctitis generalmente presentan sangrado rectal, urgencia, tenesmo y ocasionalmente estreñimiento grave82,84. Las lesiones anales y perianales pequeñas pueden complicar la diarrea grave, pero aunque ocasionalmente puede haber fístulas simples en CUCI, una fístula perianal recurrente o compleja siempre debe despertar la sospecha de enfermedad de Crohn.
El inicio de la CUCI es generalmente insidioso y los síntomas frecuentemente se presentan semanas o incluso meses antes de que el paciente busque atención médica. La enfermedad puede presentarse con episodios intermitentes de síntomas o como un ataque grave (aproximadamente en el 15%) con síntomas sistémicos que incluyen pérdida de peso, fiebre y taquicardia, o incluso náuseas y vómito91. Las manifestaciones extraintestinales, especialmente una artropatía axial o periférica, epiescleritis y eritema nudoso pueden acompañar a la presentación en aproximadamente el 10% de los pacientes y raramente preceden a los síntomas intestinales92. La tromboembolia es más frecuente en los pacientes con CUCI que en la población general, pero generalmente se asocia con enfermedad activa y pancolitis93.
Factores de riesgo para colitis ulcerosa crónica idiopáticaEl uso de antiinflamatorios no esteroideos no selectivos se asocia con un mayor riesgo de exacerbación de CUCI (NE2b, RG B). Es probablemente seguro utilizar un tratamiento a corto plazo con inhibidores de la COX-2 (NE1b, RG B). Un antecedente familiar de enfermedad de Crohn o CUCI incrementa el riesgo de presentar CUCI en otro miembro de la familia (NE2b, RG B).
El fumar tabaco de manera activa tiene un efecto protector en el desarrollo y la gravedad de la CUCI94,95. En comparación, los exfumadores tienen aproximadamente un 70% más de riesgo de desarrollar la enfermedad, la cual con frecuencia es más extensa y refractario a tratamiento en comparación con quienes nunca han fumado. Las tasas de hospitalización y de colectomía también son más altas en exfumadores que en quienes nunca han fumado96,97. Se han reportado mejorías en los síntomas y un curso más leve de enfermedad en los exfumadores que vuelven a fumar97,98, pero el efecto es inconsistente. El fumar también puede evitar el desarrollo de CEP o pouchitis después de una colectomía y anastomosis ileoanal, pero esto también se ha cuestionado99–101.
Estudios de cohorte y de metaanálisis han mostrado que la apendicectomía realizada cuando es una apendicitis verdadera a una edad temprana puede proteger contra el inicio y subsecuente gravedad de la CUCI. Se ha reportado una disminución del riesgo del 69% con apendicectomía, aunque un estudio de cohorte danés no pudo confirmar esto77,102–106. El efecto protector de la apendicectomía es adicional al de fumar, pero no parece proteger contra el desarrollo de CEP107. Cuando se realiza la apendicectomía después del inicio de la CUCI, el efecto (si lo hay) en el curso de la enfermedad es mucho menos claro.
Los fármacos antiinflamatorios no esteroideos no selectivos parecen proporcionar un riesgo significativo para la exacerbación de CUCI. La magnitud de dicho riesgo nunca se ha determinado de manera adecuada y no queda claro si todos los pacientes se ven afectados en el mismo grado95–98,108–111. En contraste, una evidencia preliminar de ensayos clínicos abiertos y un ensayo clínico controlado doble ciego muestran que el tratamiento a corto plazo con inhibidores selectivos de COX-2 es seguro111,112. No obstante, es mejor evitar el uso prolongado debido a los efectos adversos sobre otros sistemas de órganos.
Los familiares de primer grado de los pacientes con CUCI tienen un riesgo de 10-15 veces más de desarrollar la enfermedad113. En un estudio de cohorte danés basado en la población, el riesgo relativo de desarrollar CUCI fue de 10 entre familiares con la enfermedad114. En otros términos, el riesgo de por vida de desarrollar CUCI para un familiar de primer grado es de alrededor del 2% o del 98% de no desarrollar la enfermedad, lo cual ayuda a tranquilizar a un paciente con CUCI preocupado por el riesgo de que sus hijos la desarrollen. En los casos de CUCI familiar existe un ligero predominio en mujeres y menor edad de inicio en comparación con los casos esporádicos113,115.
Historia clínica, exploración física y diagnósticoHistoria clínicaDeclaración 3C de la ECCO
Una historia clínica completa debe incluir un cuestionario detallado del inicio de los síntomas, en particular de los episodios recurrentes de sangrado rectal o diarrea con sangre, urgencia, tenesmo, dolor abdominal, incontinencia, diarrea nocturna y características de manifestaciones extraintestinales. Deberá preguntarse por viajes recientes, intolerancias alimenticias, contacto con enfermedades infecciosas entéricas, medicamentos (incluyendo antibióticos y antiinflamatorios no esteroideos), tabaquismo, prácticas sexuales, antecedentes familiares de EII, antecedentes familiares de cáncer colorrectal y apendicectomía previa (NE5, RG D).
El diagnóstico de CUCI se sospecha a partir de los síntomas clínicos (sección 3.2.1). Las formas de colitis infecciosa o inducida por fármacos deberán excluirse. Deberá hacerse un interrogatorio sobre los antecedentes familiares de EII y cáncer colorrectal, y se les deberá preguntar a los pacientes acerca de posibles manifestaciones oculares, orales, articulares o cutáneas116–121.
Exploración físicaDeclaración 3D de la ECCO
En pacientes con CUCI la exploración física deberá incluir el bienestar general, frecuencia cardiaca, temperatura corporal, presión arterial, peso y estatura, exploración abdominal para distención y dolor, inspección perianal, tacto rectal, inspección oral, y revisión de ojos, piel y/o afectación articular. La exploración física puede ser normal en pacientes con enfermedad leve o incluso con enfermedad moderada. (NE5, RG D).
Los hallazgos en la exploración física dependen de la extensión y gravedad de la CUCI. La exploración de pacientes con actividad leve o moderada generalmente es normal, aparte del hallazgo de sangre en la exploración rectal. Los pacientes con un ataque grave manifiestan fiebre, taquicardia, pérdida de peso, dolor en el marco cólico, distensión abdominal o disminución de la peristalsis122.
DiagnósticoDeclaración 3E de la ECCO
No existe un estándar de oro para el diagnóstico de CUCI. El diagnóstico debe establecerse mediante la combinación de la historia clínica, la evaluación clínica y los hallazgos endoscópicos e histológicos típicos. Debe excluirse una causa infecciosa. Cuando exista duda acerca del diagnóstico, es necesaria la confirmación endoscópica e histológica después de un intervalo de tiempo (NE5, RG D).
La historia natural de la CUCI se caracteriza por episodios de recaída y periodos de remisión, y de manera ocasional por un transcurso constante y continuo (aproximadamente un 5%). También puede ocurrir un episodio agudo único seguido de una remisión prolongada en aproximadamente el 5% de los pacientes35. En el estudio IBSEN aproximadamente el 60% de los pacientes experimentaron una disminución de los síntomas con el paso del tiempo123. La frecuencia de las recaídas (patrón de la enfermedad) generalmente se define en los primeros 3 años de enfermedad, y puede clasificarse como frecuente (≥2 recaídas/año) o poco frecuente (≤1 recaída/año32, secciones 1.2 y 2.2.1). Es de ayuda para los pacientes establecer rápidamente el diagnóstico, la extensión y la gravedad de la enfermedad, debido a que influye en las opciones de tratamiento y posiblemente en el progreso de la enfermedad89. Debido a que no hay un marcador patógeno único, el diagnóstico depende de la combinación de la historia clínica, los hallazgos endoscópicos, las características histológicas en múltiples biopsias de colon y pruebas negativas en heces para agentes infecciosos. Resulta poco razonable esperar que el patólogo realice por sí solo el diagnóstico (sección 4), pero las biopsias con mucosa normal excluyen definitivamente la actividad de CUCI como una causa de los síntomas. En el 10% de los pacientes el diagnóstico se cambiará a enfermedad de Crohn o el diagnóstico de EII se descartará durante los primeros 5 años después del inicio de los síntomas. La confirmación endoscópica e histológica del diagnóstico se considera esencial124. En una minoría de pacientes no es posible caracterizar la causa de colitis: ver sección 1.1 para el uso correcto de los términos «EII no clasificada» y «colitis indeterminada»16,18.
Estudios y procedimientos para establecer un diagnósticoEstudios inicialesDeclaración 3F de la ECCO
Los estudios de laboratorio iniciales deben incluir una biometría hemática completa, urea en suero, creatinina, electrolitos, enzimas hepáticas, perfil de hierro y PCR (NE5, RG D). La calprotectina fecal es un marcador preciso de inflamación de colon. La PCR y la VSG son marcadores útiles para vigilar la respuesta al tratamiento en CUCI grave (NE2b, RG B). Se recomiendan pruebas microbiológica para diarrea infecciosa, incluyendo toxina de Clostridium difficile (C. difficile) (NE2b, RG B). Es posible que sean necesarias pruebas adicionales en heces para pacientes que reporten un viaje reciente al extranjero (NE5, RG D). Deberán evaluarse los estados de inmunización del paciente para varias enfermedades virales y tuberculosis (NE5, RG D).
Al tiempo de diagnóstico, cada paciente debe tener una biometría hemática, marcadores de inflamación (PCR o VSG), electrolitos y pruebas de la función hepática, junto con una muestra de heces para pruebas de microbiología122. La calprotectina fecal es un marcador preciso de inflamación del colon. Los marcadores de laboratorio de la inflamación crónica pueden ser normales en pacientes con CUCI distal leve o moderada. La biometría hemática puede revelar trombocitosis como un resultado de la respuesta inflamatoria crónica, anemia que indica gravedad de la enfermedad o cronicidad y leucocitosis, planteando como posibilidad una complicación infecciosa.
En CUCI, excluyendo proctitis, la PCR se correlaciona ampliamente con la actividad clínica39,42,125–127. En pacientes con actividad clínica grave, una PCR elevada generalmente se asocia con una VSG elevada, anemia e hipoalbuminemia. Estos se han utilizado como biomarcadores de pronóstico para evaluar la necesidad de colectomía en colitis aguda grave40,128,129 (sección 5.2.5). Niveles de PCR>10mg/L después de un año con diagnóstico de colitis extensa, predicen un mayor índice de necesidad de cirugía126. Ni la PCR ni la VSG son lo suficientemente específicas para diferenciar la CUCI de causas infecciosas o por otras causas.
El diagnóstico inicial de CUCI requiere la eliminación de causas infecciosas de la colitis sintomática. Las muestras de heces deben cultivarse para patógenos comunes, incluyendo pruebas específicas para toxina A y B de C. difficile, Campylobacter spp. y Escherichia coli 0157:H7. Pueden realizarse pruebas adicionales relacionadas con lo encontrado en la historia clínica, como el análisis de heces en fresco para amibas u otros parásitos.
Estudios de microbiologíaNo se recomienda hacer una prueba para C. difficile de manera rutinaria en cada exacerbación de la enfermedad, debido a que es poco frecuente que se dé un resultado positivo130–132. Sin embargo, ya que la infección por C. difficile es un creciente problema de salud en pacientes hospitalizados por CUCI y está asociado con una mayor mortalidad y uso de recursos, se aconseja hacer pruebas en pacientes hospitalizados133, así como en aquellos con una historia previa de uso de antibióticos. En contraste, las pruebas microbiológicas de heces deben realizarse durante una recaída severa o refractaria a tratamiento134,135. La sigmoidoscopia flexible puede ser superior a la prueba de toxina de C. difficile en heces en pacientes con colitis seudomembranosa y es adecuada para pacientes con diarrea en los que la prueba de heces resulta negativa136.
Puede presentarse una reactivación de la infección por CMV en la CUCI, particularmente (pero no invariablemente) en pacientes inmunosuprimidos con CUCI grave137–139. La relevancia clínica de este hallazgo no es bien sabida, pero la infección por CMV puede causar recaída refractaria o grave. No se ha establecido un método óptimo para detectar infección por CMV clínicamente significativa en pacientes con CUCI. La técnica más comúnmente utilizada para el diagnóstico de infección y enfermedad por CMV es la detección de ADN de CMV a través de PCR. Los cuerpos de inclusión intranucleares ocasionales que coinciden con CMV en la histopatología no indican necesariamente una infección clínicamente significativa, pero las inclusiones intranucleares múltiples generalmente sí indican infección significativa140,141. El CMV debe considerarse en pacientes con CUCI refractaria o grave, y si se detecta, consultar al infectólogo acerca de la importancia clínica y de la terapia adecuada. Pueden consultarse más detalles en el Consenso de la ECCO sobre infecciones oportunistas en EII13.
BiomarcadoresLos marcadores más ampliamente estudiados son los pANCA y los anticuerpos anti-Saccharomyces cerevisiae. En la mayoría de las series clínicas se han encontraron pANCA positivos hasta en el 65% de los pacientes con CUCI y en menos del 10% de los pacientes con enfermedad de Crohn. Debe destacarse que la incidencia de pANCA en CUCI puede depender de la experiencia del laboratorio local y la latitud geográfica142,143. En vista de la actual sensibilidad limitada de estos marcadores, su uso rutinario para el diagnóstico de la CUCI y para tomar decisiones terapéuticas no está clínicamente justificado.
De los marcadores fecales de inflamación intestinal, se han evaluado en EII las proteínas derivadas de neutrófilos como calprotectina, elastasa, lisozima y lactoferrina144–147. La calprotectina fecal parece ser el biomarcador más sensible, no invasivo, que refleja la inflamación intestinal en la EII establecida148. Recientes estudios enfatizan el valor de la calprotectina en la selección de pacientes que requieren estudios de diagnóstico, evaluación, gravedad de la enfermedad (correlacionando con los índices endoscópicos), en el diagnóstico de recaída y la respuesta al tratamiento48,49,51,149,150. Sin embargo, como a todas las pruebas fecales, a la calprotectina le falta la especificidad para discriminar entre tipos de inflamación. Por lo tanto, su utilidad como una herramienta de diagnóstico en la CUCI está limitada, aunque aún pueda probar tener un valor como marcador con alto valor predictivo negativo en pacientes con una baja probabilidad de otra patología.
Procedimientos recomendados para establecer el diagnósticoDeclaración 3H de la ECCO
Cuando se sospecha CUCI, la colonoscopia, preferiblemente con ileonoscopia y biopsias de segmentos, incluyendo el recto, son los procedimientos de preferencia para establecer el diagnóstico y la extensión de la enfermedad (NE5, RG D). Los pacientes con un ataque grave deben tener una radiografía abdominal y enfermedad activa confirmada por sigmoidoscopia como un procedimiento de primera línea (NE5, RG D).
Se prefiere la colonoscopia con canulación del íleon terminal y biopsias segmentarias de la mucosa a la sigmoidoscopia para los pacientes con sospecha de CUCI. Es necesario considerar el contexto clínico y la disponibilidad: es mejor evitar la colonoscopia y la preparación del intestino en pacientes con colitis aguda grave para evitar retrasos de procedimiento y un mayor riesgo de perforación. La colonoscopia establece el diagnóstico y la extensión de la enfermedad en la mayoría de los casos. Parece ser más rentable que la sigmoidoscopia inicial64,151. Encontrar ulceraciones profundas en la colonoscopia predice un peor resultado y una mayor necesidad de cirugía152.
Una radiografía abdominal simple no es una prueba diagnóstica para CUCI, pero es valiosa en la evaluación inicial de los pacientes con sospecha CUCI grave (sección 3.5.3). La dilatación segmentaria del colon que supera los 5cm con bordes irregulares delineados por gas se correlaciona fuertemente con ulceración153. La distensión persistente en CUCI grave se correlaciona con una pobre respuesta al tratamiento, una mayor tasa de megacolon tóxico y de necesidad de cirugía154. Se recomiendan la esofagogastroduodenoscopia con biopsia de mucosa en pacientes con síntomas gastrointestinales superiores. La cápsula endoscópica representa un avance en la imaginología intestinal, pero son necesarios grandes ensayos prospectivos para confirmar la relevancia diagnóstica en la CUCI. La cápsula endoscópica es una técnica clínica potencialmente útil para categorizar a esos pacientes con colitis sin clasificar. Aunque los resultados normales de un estudio con cápsula endoscópica no excluyen enfermedad de Crohn, tienen un valor predictivo negativo muy alto155. Utilizando la cápsula endoscópica, Lopes et al. cambiaron el diagnóstico de EII no clasificada a enfermedad de Crohn en 7/14 pacientes, aunque esto no llevó a cambios en el manejo156.
Evaluación de la extensión, gravedad y actividadSignos de inflamación discontinua en colitis ulcerosa crónica idiopáticaConservación del recto y parche cecalSe ha descrito la conservación del recto macroscópica y microscópica antes de iniciar el tratamiento en niños que presentan CUCI157–160. En adultos, es más probable que una inflamación normal o en parches en el recto se deba a terapia tópica o sistémica para CUCI161,162. La inflamación en parche en el ciego se refiere al «parche cecal» y se observa en pacientes con colitis izquierda. Cuando hay conservación rectal macroscópica e histológica o la presencia de un parche cecal en la colitis recién diagnosticada, está indicada la evaluación del intestino delgado además de una ileonocolonoscopia. La historia natural de los pacientes con inflamación colónica derecha en parches parece ser similar a la de los que presentan CUCI del lado izquierdo141,142. Siempre que haya un patrón en parches de inflamación en colitis, está indicada una evaluación diagnóstica hasta el intestino delgado para excluir enfermedad de Crohn, además de una ileonocolonoscopia.
Lesiones apendiculares discontinuasSe reporta la afectación del apéndice como una lesión discontinua en hasta el 75% de los pacientes con CUCI111–113. La inflamación del apéndice ha sido asociada con un curso de mayor respuesta de la enfermedad y un mayor riesgo de pouchitis después de anastomosis del reservorio ileal163–166. Ambos hallazgos requieren confirmación.
Ileítis por reflujoLa extensión continua de la inflamación macroscópica o histológica desde el ciego hasta el íleon más distal se define como «ileítis por reflujo» (ver también la sección 4.2.3). Se observa hasta en el 20% de los pacientes con pancolitis. Raramente las erosiones ileales ocurren en pacientes sin involucramiento del ciego y esto desafía a la teoría patógena de que la ileítis por reflujo es ocasionada simplemente por el reflujo del contenido del ciego al íleon167–169. Se ha sugerido que existe un curso más refractario a tratamiento en pacientes con ileítis por reflujo168. Deberían considerarse estudios de imaginología adicionales del intestino delgado en los casos de ileítis macroscópica por reflujo, para diferenciar la CUCI de la enfermedad de Crohn.
Intestino delgadoNo se recomiendan de manera rutinaria los estudios radiológicos del intestino delgado por enteroclisis, movimiento complementario, enteroclisis por TC, enteroclisis por RM o cápsula endoscópica (revisados en el Consenso de ECCO sobre el diagnóstico en enfermedad de Crohn)33 y endoscopia de intestino delgado en EII12. Cuando hay una dificultad diagnóstica (conservación rectal, síntomas atípicos, ileítis macroscópica por reflujo) entonces son necesarios una serie de estudios para descartar enfermedad de Crohn además de una ileocolonoscopia.
Índices de actividad en colitis ulcerosa crónica idiopáticaDeclaración 3I de la ECCO
Se encuentran disponibles instrumentos para medir la actividad clínica y/o endoscópica en CUCI, pero ninguno se ha sometido a un proceso adecuado de validación. En la rutina diaria dichos índices son poco utilizados. Sería conveniente la incorporación de un sistema simple de puntuación clínica y/o endoscópica, pensado para mejorar la atención de los pacientes con CUCI y para obtener un sistema IT estandarizado para EII. La hospitalización inmediata es necesaria para todos los pacientes que cumplan con los criterios de Truelove y Witts para CUCI grave, para evitar retraso en la toma de decisiones, lo cual podría resultar en una mayor morbimortalidad perioperatoria (NE4, RG D).
Actualmente, el uso de puntuaciones de actividad de la enfermedad para CUCI está limitado a los ensayos clínicos. Sin embargo, con base en la necesidad de estandarizar la documentación de los pacientes con EII en Europa, es necesaria la incorporación de un sistema simple de puntuación con validez clínica y/o endoscópica en los archivos electrónicos de los pacientes. La clasificación original para CUCI grave fue propuesta por Truelove y Witts en 195520 y ha pasado la prueba del tiempo, porque es fácil de recordar y de aplicar. Esta clasificación aún se considera como el estándar de oro para la identificación rápida de pacientes ambulatorios que necesitan hospitalización inmediata y tratamiento intensivo153,170.
Estudios para colitis aguda grave en la admisiónLos pacientes deben tener una biometría hemática, marcadores inflamatorios (PCR o VSG), electrolitos y pruebas de función hepática además de una muestra de heces para cultivo y prueba para toxina C. difficile170.
Deberá realizarse una radiografía abdominal simple, no solamente para excluir la dilatación colónica (≥5cm) sino también para calcular la extensión de la enfermedad y buscar características que predigan la respuesta al tratamiento. La extensión proximal de la enfermedad se correlaciona ampliamente con la distribución distal de los residuos fecales; en 51 casos de CUCI grave, esta guía sobreestimó la extensión en el 18% y la subestimó en el 8% de los pacientes128. La presencia de islas de mucosa (pequeñas opacidades circulares que representan la mucosa residual aislada por ulceración circundante) o más de 2 asas de intestino delgado llenas de gas en la radiografía se asocian con una pobre respuesta al tratamiento171,172.
Una sigmoidoscopia flexible debe confirmar el diagnóstico de CUCI grave y ayudar a descartar infección, particularmente por CMV137,138,173. Si se tiene una fuerte sospecha de que el CMV podría ser el responsable del deterioro (como en un paciente con inmunomoduladores asociado a fiebre alta), es adecuado solicitar histopatología urgente. Una respuesta puede estar disponible en 4h. La preparación del enema de fosfato antes de la sigmoidoscopia flexible se considera segura, pero probablemente es mejor evitarla en pacientes con dilatación del colon. No se recomienda colonoscopia completa en pacientes con colitis aguda grave, debido a que la preparación purgante puede provocar dilatación y la perforación colónica es un verdadero riesgo de la colonoscopia durante la enfermedad activa. Los criterios endoscópicos para CUCI grave incluyen hemorragia de la mucosa con ulceración profunda, desprendimiento de la mucosa en el borde de estas ulceraciones y ulceración en pozo152,174, todos los cuales pueden evaluarse con sigmoidoscopia flexible.
Reevaluación de la extensión y gravedad de la colitis ulcerosa crónica idiopáticaA pesar de la importancia de la ubicación de la enfermedad para determinar el pronóstico, el riesgo de cáncer y la elección de la terapia, nunca se ha estudiado la conveniencia de la nueva estadificación periódica después de la colonoscopia inicial. En un estudio de cohorte hecho en población de Noruega, la cicatrización de la mucosa después de un año de tratamiento estuvo asociada con un riesgo menor para colectomía (el 1.6% de los pacientes con cicatrización de la mucosa comparado con el 7% de los pacientes sin cicatrización de la mucosa)175. El 40% de los pacientes que lograron la remisión endoscópica (definida como una falta de inflamación significativa en la endoscopia y en la biopsia rectal) permanecieron asintomáticos durante un año de seguimiento en comparación con el 18% de los pacientes que no lograron la remisión176. En un estudio prospectivo multicéntrico, 78 pacientes con CUCI activa leve a moderada recibieron mesalamina oral y rectal; aquellos en remisión clínica con puntuaciones endoscópicas menos graves (definidas como mucosa de apariencia normal, únicamente con enrojecimiento leve y/o friabilidad) tuvieron una menor probabilidad de recaída en un año en comparación con los pacientes que únicamente se encontraban en remisión clínica177.
La colonoscopia es más sensible que los estudios de bario para calcular la extensión de la enfermedad, pero el riesgo de cáncer está basado históricamente en los estudios de contraste y la colonoscopia define una extensión diferente a la histopatología78,178–180. La cromoendoscopia se correlaciona mejor con la extensión de la enfermedad determinada por histopatología, pero el procedimiento requiere de tiempo y de un nivel de experiencia que no está universalmente disponible181. La remisión clínica inducida por fármaco puede no estar asociada con remisión endoscópica o histológica, pero las implicaciones pronósticas de la reevaluación endoscópica en enfermedad inactiva aún están por determinarse78. Esta área requiere estudio sistemático.
Endoscopia, ultrasonido y colonografíaCaracterísticas endoscópicas de la colitis ulcerosa crónica idiopáticaDeclaración 3K de la ECCO
Ninguna característica endoscópica es específica para CUCI. Las características endoscópicas más útiles para CUCI son la afectación colónica continua y confluente con una clara delimitación de la inflamación y la afectación rectal (NE2b, RG B). La gravedad de la CUCI por endoscopia está reflejada de mejor manera por la presencia de friabilidad de la mucosa, sangrado espontáneo y ulceraciones profundas (NE2b, RG B).
Los cambios endoscópicos comienzan de manera característica proximales al borde anal y se extienden proximalmente de manera continua, confluente y concéntrica. La delimitación entre las áreas con inflamación y las normales generalmente es clara y puede presentarse abruptamente en milímetros, especialmente en la enfermedad distal.
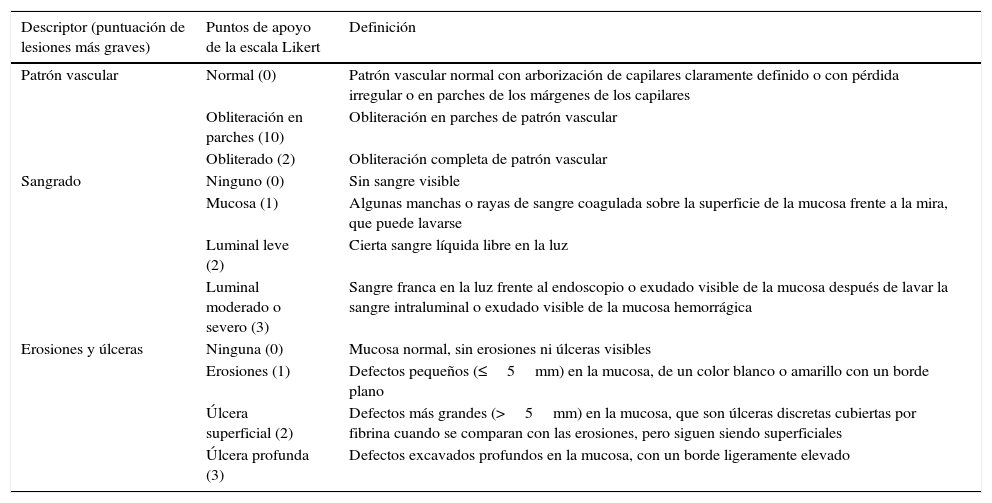
Es bien reconocida una amplia variación en la interpretación endoscópica de la actividad de la enfermedad182. Aunque se han reportado granularidad, patrón vascular, ulceraciones y friabilidad con sangrado para predecir la evaluación global de la gravedad en la endoscopia183, el índice endoscópico de gravedad de la colitis ulcerosa (UCEIS) utiliza el patrón vascular, sangrado y ulceración, cada uno con 3 o 4 niveles de gravedad, para capturar el rango completo de gravedad a la endoscopia y un 88% de varianza entre los endoscopistas (tabla 7)184. Este es el primer índice endoscópico validado de gravedad en CUCI.
Índice endoscópico de gravedad de colitis ulcerosa (UCEIS)184
| Descriptor (puntuación de lesiones más graves) | Puntos de apoyo de la escala Likert | Definición |
|---|---|---|
| Patrón vascular | Normal (0) | Patrón vascular normal con arborización de capilares claramente definido o con pérdida irregular o en parches de los márgenes de los capilares |
| Obliteración en parches (10) | Obliteración en parches de patrón vascular | |
| Obliterado (2) | Obliteración completa de patrón vascular | |
| Sangrado | Ninguno (0) | Sin sangre visible |
| Mucosa (1) | Algunas manchas o rayas de sangre coagulada sobre la superficie de la mucosa frente a la mira, que puede lavarse | |
| Luminal leve (2) | Cierta sangre líquida libre en la luz | |
| Luminal moderado o severo (3) | Sangre franca en la luz frente al endoscopio o exudado visible de la mucosa después de lavar la sangre intraluminal o exudado visible de la mucosa hemorrágica | |
| Erosiones y úlceras | Ninguna (0) | Mucosa normal, sin erosiones ni úlceras visibles |
| Erosiones (1) | Defectos pequeños (≤5mm) en la mucosa, de un color blanco o amarillo con un borde plano | |
| Úlcera superficial (2) | Defectos más grandes (>5mm) en la mucosa, que son úlceras discretas cubiertas por fibrina cuando se comparan con las erosiones, pero siguen siendo superficiales | |
| Úlcera profunda (3) | Defectos excavados profundos en la mucosa, con un borde ligeramente elevado |
Las características endoscópicas de inflamación leve son eritema, congestión vascular de la mucosa y pérdida del patrón vascular. La colitis moderadamente activa se caracteriza por una pérdida completa del patrón vascular, sangre adherida a la superficie de la mucosa y erosiones, frecuentemente con una apariencia granular rugosa y friabilidad de la mucosa (sangrado al contacto leve). La CUCI grave se caracteriza por sangrado espontáneo y ulceración (tabla 6)78,180,182,184,185. La elección de la puntuación endoscópica es compleja y se ha analizado23,182,186. A diferencia de la enfermedad de Crohn, las úlceras en la CUCI grave siempre se encuentran dentro de la mucosa inflamada. La presencia de ulceración profunda es un signo de mal pronóstico180. En enfermedad de larga duración, la atrofia de la mucosa puede resultar en pérdida de las haustras, estenosis de la luz intestinal y («seudo») pólipos postinflamatorios. El significado de «cicatrización de la mucosa» en CUCI ha sido objeto de análisis detallado187.
La puntuación total es la suma de los 3 descriptores en el área más afectada del colon visible en sigmoidoscopia. Aunque la versión original del UCEIS dio una puntuación de 1 a la apariencia normal de un descriptor, se tomó la decisión de hacer un cambio en la numeración de los niveles, con normalidad con una puntuación de 0, de manera que la suma más simple del UCEIS vaya de 0 al 8184.
Ultrasonido abdominal y gammagrafía en colitis ulcerosa crónica idiopáticaEl ultrasonido abdominal puede utilizarse para buscar inflamación del intestino delgado o del colon con una sensibilidad del 80-90%. El ultrasonido tiene la ventaja de ser de bajo costo, fácil de realizar sin preparación previa y no es invasivo, pero la precisión depende mucho de la habilidad del operador y hay una especificidad baja para diferenciar la CUCI de otras causas de inflamación colónica25,188–191. Sin embargo, el ultrasonido abdominal parece ser útil en la monitorización del éxito del tratamiento y hay datos iniciales de que el ultrasonido podría ayudar a pronosticar el curso de la enfermedad192.
El ultrasonido hidrocolónico (ultrasonografía abdominal junto con instilación retrógrada de agua en el colon) tiene una alta sensibilidad para identificar la colitis activa, pero el método también es muy difícil para la práctica clínica diaria193. El ultrasonido doppler de las arterias mesentéricas superiores e inferiores se ha utilizado para evaluar la actividad de la enfermedad y el riesgo de recaída. Deberá considerarse como una técnica complementaria para evaluar la actividad de la enfermedad en manos expertas194,195. Para que este método sea viable, se necesitan más estudios multicéntricos prospectivos.
La gammagrafía de leucocitos es segura, no invasiva y permite potencialmente la evaluación de la presencia, extensión y actividad de la inflamación. Sin embargo, le falta especificidad al método196,197, y por lo tanto actualmente no puede recomendarse como una herramienta de diagnóstico estándar para la CUCI. Este método es poco confiable si los pacientes están tomando esteroides. Se están desarrollando nuevos marcadores para detectar la inflamación que no están asociados a la exposición a la radiación.
Colonografía virtual en colitis ulcerosa crónica idiopáticaPocos estudios con un número limitado de pacientes han investigado la colonografía por RM o colonografía por TC en CUCI. Los resultados son contradictorios y los cambios sutiles de la mucosa como las erosiones o pólipos planos no se ven suficientemente198,199. Debido a estas limitaciones, actualmente la colonoscopia virtual no es alternativa a la colonoscopia estándar en pacientes con CUCI.
Estenosis del colon en colitis ulcerosa crónica idiopáticaDeclaración 3N de la ECCO
Cada estenosis del colon en la CUCI debe levantar la sospecha de carcinoma colorrectal. Deben tomarse múltiples biopsias y buscarse una opción quirúrgica. Cuando la canulación endoscópica del colon no es posible, pueden emplearse procedimientos de imaginología, como enema de bario de doble contraste, colonografía por TC y/o por RM (NE5, RG D).
En la CUCI de larga duración, una estenosis del colon señala un aumento en el riesgo de carcinoma colorrectal y requiere una evaluación histológica cuidadosa37. Si la colonoscopia es incompleta debido a la estenosis, puede utilizarse un enema de bario con doble contraste o incluso con contraste simple para evaluar la estenosis y el colon proximal200. Sin embargo, con la colonografía por TC se puede evaluar el patrón de la mucosa proximal a la estenosis, así como la patología extraintestinal, y por lo tanto se ha convertido en el estudio de elección en esta situación201.
HistopatologíaGeneralEn la CUCI, la histopatología se utiliza para el diagnóstico, evaluación de la actividad de la enfermedad e identificación de neoplasias intraepiteliales (displasia). Esto último se tratará por separado.
ConsideracionesDiversos factores han influido en la exactitud del diagnóstico histopatológico de la CUCI, al igual que en la enfermedad de Crohn. El uso de la colonoscopia como procedimiento diagnóstico de elección ha permitido el análisis de múltiples biopsias de diferentes segmentos del colon. Se obtienen biopsias con mayor frecuencia de manera temprana en la evolución de la enfermedad. Además, las biopsias pueden obtenerse en niños pequeños que presentan diarrea con sangre. Asimismo, la introducción de las nuevas terapias que inducen la cicatrización de la mucosa ha hecho que los patólogos estén alertas al impacto del tratamiento en cuanto a las características microscópicas. Esto ha cambiado el enfoque del diagnóstico histopatológico en la última década.
Evaluación de la literaturaSe buscaron artículos que reportan investigación original en la reproducibilidad, sensibilidad, especificidad y valor de predicción de las características individuales útiles para el diagnóstico histopatológico de la CUCI en la literatura, utilizado Medline y PubMed. Únicamente se consideraron las características que lograron reproducibilidad moderada juzgadas por los métodos estadísticos kappa o hallazgos confirmados por varios estudios. Además, hemos revisado los estudios que describen y definen las características microscópicas de diagnóstico. La literatura puede dividirse en grupos dependiendo del número (uno o múltiples) de biopsias examinadas o la duración de la enfermedad. En 10 estudios se examinaron múltiples biopsias (incluyendo 2 que comparaban el valor diagnóstico de la toma de una única biopsias en comparación con la toma de múltiples biospias)159,202–210. La literatura sobre la duración de la enfermedad también puede dividirse. El primer grupo está compuesto de estudios con biopsias obtenidas en pacientes con un diagnóstico establecido de CUCI, con base en el seguimiento clínico extendido. La duración de la enfermedad varía entre 6±3 semanas y 12 años. Un segundo grupo está compuesto de estudios retrospectivos sin información clara sobre la duración de la enfermedad. Estos estudios pueden integrarse a los del primer grupo, debido a que el diagnóstico queda nuevamente establecido durante el periodo de seguimiento. Un tercer grupo reúne los estudios sobre las biopsias obtenidas de manera temprana después del inicio de la enfermedad, antes del tratamiento157,159,208,209,211. Para la enfermedad de inicio temprano, la duración de la misma varía entre 4 y 14días (3.69±0.52 días después de la aparición del sangrado rectal, o 10 días después de los síntomas iniciales)203,211,212. En estos estudios, el diagnóstico se confirmó de manera subsecuente en el seguimiento de los pacientes y son estudios prospectivos. Los niños se incluyen principalmente en el tercer grupo.
Si bien puede parecer evidente para los médicos experimentados, se deberá tener cuidado para evitar la confusión entre el uso de histopatología para confirmar un diagnóstico de CUCI y el uso de histopatología para confirmar la presencia de enfermedad activa. Esto es particularmente relevante para los ensayos clínicos de CUCI activa (sección 4.4).
Características microscópicas—definicionesSe han evaluado un gran número de características microscópicas. Estas pueden clasificarse en:
- •
características de la arquitectura
- •
anomalías epiteliales y
- •
características inflamatorias.
Las características de la arquitectura incluyen ramificación de las criptas, distorsión de la cripta, atrofia de cripta e irregularidad de la superficie. Las anomalías de las células epiteliales son depleción de mucina y metaplasia de las células de Paneth. Las características inflamatorias incluyen mayor celularidad de la lámina propia, plasmocitosis basal, agregados linfoides basales y eosinófilos en la lámina propia.
Anomalías de la arquitectura de la criptaRamificación de las criptas: 2 o más criptas ramificadas (bifurcadas) en una sección bien orientada, ya sea que la ramificación sea en el eje vertical u horizontal208,211,213–215. Cuando se aplica a una sola cripta, la característica es menos específica214. La patogénesis puede explicarse por la regeneración que sigue a un daño previo o destrucción (criptólisis).
Distorsión de la mucosa (de la cripta): irregularidades en el tamaño de la cripta (esto es, diámetro variable), espaciado, orientación (esto es, pérdida de paralelismo) o de la forma (incluyendo ramificación con una configuración quística)159,203–205,208,209,211,215. En algunos estudios esto incluye separación de la muscular de la mucosa subyacente204,211. Las muestras de la zona de transición anal o manguito columnar (algunas veces erróneamente llamadas «biopsias rectales bajas») no son convenientes para la evaluación de la ramificación de la cripta o distorsión de la mucosa.
Atrofia de la mucosa (de la cripta) y densidad de la cripta: una combinación de la reducción de la cripta (criptas adelgazadas, generalmente reconocidas por una distancia de más de un diámetro de cripta entre criptas) y un incremento en la distancia entre la capa muscular de la mucosa y la base de las criptas211,215,216. Algunos autores enfatizan el uso ya sea la reducción de la cripta203 o una mayor distancia entre la capa muscular de la mucosa y la base de las criptas208 en lugar de ambas características. Un incremento en el espacio intercriptal y la distancia de la cripta–muscular de la mucosa puede ser normal en el ciego y el recto distal215. La distancia entre la capa muscular de la mucosa y la base de la cripta no debe evaluarse en la cercanía de los folículos linfoides. La patogénesis puede explicarse como una consecuencia de la muerte de la cripta debida a la enfermedad y se ha estudiado en modelos experimentales en animales. Si todas las células de la cripta mueren, las criptas no pueden regenerarse y desaparecer en 48h. Sin embargo, si una o más células clonogénicas sobreviven al daño, la proliferación rápida regenera la cripta en 72-96h. Subsecuentemente la mucosa cicatriza por una expansión clonal y el número de criptas que sobreviven para regenerarse después de un daño citotóxico se correlaciona con la severidad del síntoma. Varios factores de crecimiento afectan la regeneración de la cripta en estos modelos murinos217. No obstante, queda poco claro qué tamaño de biopsia (intacto) es el conveniente para la evaluación adecuada y cuántos niveles de la biopsia necesitan examinarse para evaluar adecuadamente la atrofia.
Irregularidad de la superficie: irregularidad de la superficie (los sinónimos incluyen superficie vellosa, superficie con vellosidad o mucosa con vellosidad)203,214 significa entradas amplias de la cripta, que dan a la superficie de la mucosa la apariencia de un dedo211. La impresión se debe a la separación de criptas216 y se ha propuesto una distinción semántica entre la «superficie irregular» y la «superficie vellosa», de acuerdo con la proporción vellosidad-cripta204.
Anomalías de células epitelialesMetaplasia de células de Paneth: las células de Paneth normalmente son muy poco comunes en el colon distal a la flexión esplénica, encontrándose presentes solamente en el 0-1.9% de pacientes controles que no tienen EII218. La presencia de células de Paneth en el colon distal puede denominarse metaplasia de células de Paneth. La patogénesis está relacionada con la regeneración y reparación epitelial218.
Depleción de mucina: definida como una reducción en el número de células caliciformes o disminución de la cantidad de mucina dentro de las células215.
Características inflamatoriasPlasmocitosis basal: definida como la presencia de células plasmáticas ya sea alrededor (profundidad de 1/5 de la lámina propia) o por debajo de las criptas, junto a o penetrando la capa muscular de la mucosa. La plasmocitosis basal también se puede referir a células plasmáticas debajo de la cripta203, plasmocitosis con extensión a la base de la mucosa159, o a la acumulación de células plasmáticas entre la base de las criptas y la capa muscular de la mucosa208. La anomalía puede ser focal o difusa y no siempre está presente la ubicación de las células debajo de las criptas203,211.
Celularidad de la lámina propia: evaluada de acuerdo a la densidad, composición y distribución. Un incremento en el número total de las células plasmáticas, linfocitos, histiocitos y eosinófilos es una característica de todos los tipos de inflamación colorrectal215 y tiene un valor discriminante limitado. En la CUCI el infiltrado celular es difuso y transmucoso.
Un aumento en la densidad se ha descrito como un infiltrado «subjetivamente anormal»214, un aumento «prominente» (evaluado por la ampliación del espacio intercriptal debido al infiltrado inflamatorio216 o simple «hipercelularidad»)203. El incremento es difícil de cuantificar. La celularidad aumentada de la lámina propia puede estar ausente en enfermedad inactiva, después de tratamiento o en el transcurso natural de la enfermedad181,219. Además, el incremento de la celularidad de la lámina propia puede persistir en la colitis infecciosa220 y es una característica normal de biopsias del ciego.
Se ha examinado la composición para resolver estos problemas. Algunos autores discriminan entre un incremento solo en los neutrófilos y un incremento tanto en las células redondas como en los neutrófilos. Los neutrófilos pueden estar presentes en la lámina propia o entre las células epiteliales, se reconocen fácilmente y son una característica reproducible de la inflamación216. Más de 3 neutrófilos en la lámina propia fuera de los capilares puede ser anormal204, pero el número exacto no se ha acordado. Los neutrófilos son una característica de la criptitis con migración de los neutrófilos a través del epitelio de la cripta, induciendo a alteración de la cripta y abscesos de la misma, lo cual puede ser responsable del daño o la alteración de la superficie celular. Sin embargo, el valor diagnóstico de los neutrófilos en CUCI está limitado debido a que también están presentes en colitis infecciosa y otras formas de colitis203,216. En comparación, los eosinófilos en la lámina propia son altamente variables. Se ha observado un aumento en la CUCI y se ha propuesto un potencial valor diagnóstico, pero los datos se obtuvieron de ensayos de pacientes con enfermedad de larga duración205,213.
La distribución del infiltrado inflamatorio celular de lámina propia se ha dividido en: focal (celularidad normal en el fondo con áreas de celularidad incrementada), en parches (celularidad anormal en el fondo con intensidad variable) y difusa (celularidad anormal en el fondo con un incremento total en la densidad). Se prefieren estos términos. La confusión viene cuando el término «discontinuo» se utiliza para describir los cambios focales y en parches en algunos estudios215, o se utiliza como sinónimo de focal en otros205. Un incremento difuso puede ser superficial (confinado a los tercios superficiales y medios de la lámina propia) o transmucoso (generalmente hasta el tercio más bajo). La distribución puede evaluarse en una muestra única o entre múltiples muestras del mismo sitio. Para evitar un error de diagnóstico, los criterios de inflamación transmucosa difusa para diagnóstico de CUCI no deben utilizarse en las biopsias de enfermedad de inicio temprano en niños159, o después de tratamiento y cuando la enfermedad está en etapa de resolución o inactiva. En estas circunstancias la biopsia puede ser normal o mostrar cambios focales161,207,221.
Agregados linfoides basales: colecciones nodulares de linfocitos entre la base de la cripta y la capa muscular de la mucosa214, sin centros germinales204,214,215,222. Al menos se necesitan 2 agregados para que esta característica se considere anormal204,215,216.
Cambios estromales: se ha observado aumento difuso en el espesor de la muscular de la mucosa o una capa doble de muscular de la mucosa (lo cual es inusual, pero es característico cuando se presenta) en CUCI activa de larga duración y en CUCI inactiva223.
Ileítis por reflujo: la inflamación ileal en CUCI se denomina ileítis por reflujo, a pesar del hecho de que la patogénesis de reflujo nunca se ha establecido. La «ileítis por reflujo» debe estar en continuidad con la inflamación colónica (ver también 3.5.1) y las lesiones en el ciego deben mostrar un grado similar o mayor de inflamación activa. Las lesiones ileales en la «ileítis por reflujo» se caracterizan por inflamación activa en las vellosidades y la lámina propia, junto con el acortamiento y la atrofia de las vellosidades. Las erosiones ileales focales y aisladas, la metaplasia de glándula mucosa o el edema irregular con la inflamación activa leve son características que sugieren enfermedad de Crohn167,169.
Declaración 4B de la ECCO
Las biopsias deben acompañarse de información clínica, incluyendo la edad del paciente, la duración de la enfermedad y la duración y tipo de tratamiento (NE1b, RG B). Las biopsias de diferentes regiones deben manejarse de tal manera que la región de origen pueda identificarse (NE1c, RG A). Esto puede hacerse utilizando diferentes contenedores, caja de cartuchos multiwell o una tira de acetato (NE5, RGD). Todas las muestras de tejido deben fijarse de inmediato por inmersión en formalina amortiguada o una solución equivalente antes de transportarlas. Se recomienda que se examinen múltiples secciones de cada muestra (NE5, RG D).
Se ha propuesto que un incremento no específico en el infiltrado inflamatorio en la lámina propia en combinación con ausencia en la distorsión de la arquitectura de la cripta, indica un diagnóstico de colitis aguda infecciosa203,216 más que de CUCI. Sin embargo, este hallazgo no está confirmado en ensayos con pacientes con inicio temprano de la enfermedad (dentro de los primeros 10 días de síntomas)212,224.
Declaración 4C de ECCO
La plasmocitosis basal en la aparición inicial de la enfermedad tiene un alto valor predictivo para el diagnóstico de EII (NE3, RG C). Repetir las biopsias después de un intervalo de tiempo puede ayudar a resolver los problemas de diagnóstico diferencial y establecer un diagnóstico definitivo, especialmente en adultos, mostrando características adicionales (NE5, RG D).
La plasmocitosis basal se observa en las biopsias obtenidas en el inicio temprano en el 38–100% de los pacientes adultos203,211 y puede ayudar a diferenciar entre CUCI y colitis infecciosa211. Particularmente esta es una característica en niños pequeños; en esos casos está principalmente presente en biopsias rectales y disminuye proximalmente. Se trata de una característica temprana, algunas veces es la primera lesión que aparece159,203,208,209,211 y es un buen marcador predictivo.
Las anomalías glandulares pueden identificarse con un buen acuerdo interobservador (83-90%)204,222,225. De acuerdo con la mayoría de los estudios, la irregularidad difusa de la arquitectura de la cripta y disminución en el número de criptas o atrofia indican CUCI213,215. Sin embargo, estas características pueden no estar presentes en las biopsias obtenidas de los pacientes con CUCI en una etapa temprana211. Se observaron cambios arquitectónicos de la cripta en biopsias obtenidas entre 16 y 30 días después del inicio211, pero no en biopsias en etapas más tempranas. En otro estudio203 se encontró arquitectura anormal en todas las biopsias obtenidas dentro de los primeros días del inicio, pero en este estudio, el comienzo de la enfermedad se definió por pérdida de sangre y no por otro síntoma. La distorsión de la cripta y la atrofia de la mucosa pueden regresar a la normalidad o permanecer inalteradas después de la resolución de los síntomas161,221.
Pueden no encontrarse características diagnósticas confiables en las biopsias obtenidas en la enfermedad de inicio temprano, en colitis aguda grave o en pacientes con una respuesta inmunológica atípica (como niños pequeños o pacientes con CEP). No se recomienda actualmente el uso rutinario de técnicas adicionales como la inmunohistoquímica.
Enfermedad establecidaDeclaración 4E de la ECCO
Un diagnóstico de CUCI establecida se basa en la combinación de: plasmocitosis basal (definida como la presencia de células plasmáticas alrededor (parte profunda de la lámina propia) o debajo de las criptas (subcríptica)), aumento importante y difuso de células en la lámina propia transmucosa, y distorsión arquitectónica difusa de la mucosa o de las criptas (NE1a, RG A).
No se ha establecido el número exacto de características necesarias para el diagnóstico. Se logra un diagnóstico correcto de CUCI en aproximadamente el 75% de los casos cuando 2 o 3 de las 4 características, distorsión grave de la arquitectura de la cripta, disminución grave de la densidad de la cripta, superficie irregular e inflamación importante difusa de la transmucosa, están presentes, en ausencia de granulomas genuinos204,209.
En la CUCI establecida está presente una superficie vellosa en el 17–63% de los casos (en comparación con el 0-24% en enfermedad de Crohn y el 0-7% en colitis infecciosa)215. Esta lesión se observa aproximadamente en un tercio de las biopsias iniciales de los niños con CUCI208. En adultos, esta característica estuvo presente en aproximadamente el 23% de los pacientes que se presentaron 16-30 días después de los síntomas iniciales, pero no en biopsias anteriores211.
Declaración 4G de la ECCO
La plasmocitosis basal es una buena característica diagnóstica en CUCI establecida (NE2, RG B). Un aumento importante y difuso de células en la lámina propia transmucosa es una buena característica de diagnóstico en enfermedad activa establecida (NE2, RG B). La distribución de la inflamación en el colon, con un gradiente menor de inflamación de distal a proximal hace pensar un diagnóstico de CUCI en un paciente que no ha recibido tratamiento (NE5, RG D).
El valor diagnóstico de la plasmocitosis basal está confirmado por estudios de biopsias obtenidas en enfermedad establecida, estando presente en hasta el 63% de los casos204. La característica es rara en colitis que no es de EII214, pero también es común en enfermedad de Crohn. La plasmocitosis basal disminuye y puede desaparecer durante el tratamiento.
Un infiltrado importante y difuso de células en lámina propia transmucosa favorece el diagnóstico de CUCI215, pero la inflamación en parches puede observarse ocasionalmente en CUCI213 o, cuando se analizan múltiples biopsias, puede que solo una pieza tenga evidencia de colitis crónica y las otras tengan mucosa normal208,221,226. El incremento importante y difuso de células en la lámina propia transmucosa puede estar ausente en niños pequeños (<12 años). Puede disminuir en intensidad y volverse irregular durante la evolución natural de la enfermedad o posterior al tratamiento. Esta característica por lo tanto se utiliza principalmente para el diagnóstico en enfermedad establecida. Su ausencia no excluye un diagnóstico de CUCI.
Declaración 4H de la ECCO
La presencia extendida de neutrófilos en el epitelio de la cripta (criptitis y abscesos de cripta) favorece el diagnóstico de CUCI. Sin embargo, estas lesiones pueden presentarse en colitis infecciosa y otros tipos de colitis (NE2b, RG B). Los neutrófilos en la lámina propia e intraepiteliales están ausentes en enfermedad inactiva. (NE2b, RG B).
La presencia extendida de neutrófilos en el epitelio de la cripta favorece el diagnóstico de CUCI, pero los abscesos en la cripta y la criptitis también pueden presentarse en colitis infecciosa, aunque son menos prominentes26. Los neutrófilos están ausentes durante la enfermedad inactiva.
Los agregados linfoides basales favorecen un diagnóstico de CUCI establecida, pero pueden presentarse en enfermedad de Crohn214,216 y no son útiles en el inicio temprano de la enfermedad.
Declaración 4I de la ECCO
La metaplasia de células de Paneth distal a la flexión esplénica no es una característica específica. Es sugestiva de un diagnóstico de CUCI en enfermedad establecida (NE3, RG C). La depleción grave y extensa de mucina es útil para el diagnóstico de CUCI en enfermedad activa (NE3, RG C).
La metaplasia de células de Paneth favorece un diagnóstico de CUCI205. El valor predictivo es alto pero la sensibilidad baja214. No se observa en biopsias obtenidas de manera temprana en la enfermedad211,216 y parece estar relacionada con la enfermedad establecida218. La disminución de mucina también favorece un diagnóstico de CUCI. Se correlaciona con actividad de la enfermedad, de manera que es útil, pero no una característica diagnóstica fundamental159. Sin embargo, la preservación de la mucina en asociación con enfermedad activa puede favorecer un diagnóstico de enfermedad de Crohn más que de CUCI206.
Características microscópicas—actividad de la enfermedadSe ha observado desaparición de la inflamación de la mucosa después del tratamiento161, de manera que las biopsias también se utilizan para distinguir entre enfermedad inactiva y activa, así como para diferenciar grados de actividad. Se han introducido sistemas de puntuación para la evaluación de la actividad de la enfermedad, particularmente para las pruebas terapéuticas. El valor potencial de la histopatología para predecir la recaída y evaluar el control adecuado de la inflamación tiene implicaciones para el manejo terapéutico y la reducción del riesgo de neoplasia. El daño epitelial en asociación con presencia de neutrófilos y plasmocitosis basal se han propuesto como marcadores de la actividad de la enfermedad y la predicción de la recaída36,227–229.
El valor de la histopatología como confirmación independiente de la actividad de la enfermedad en estudios clínicos para el tratamiento de CUCI leve o moderadamente activa frecuentemente es ignorado. Una falta de inflamación microscópica en una biopsia de mucosa excluye de manera definitiva la CUCI activa y esta es una medida importante para la validación de la enfermedad activa al reclutar a pacientes para los ensayos clínicos, debido a que puede evaluarse de manera independiente a partir de la endoscopia. El problema es prevalente: en un estudio fase 3 de un nuevo agente para tratar la CUCI leve a moderadamente activa, fueron excluidos 77/511 (15%) pacientes que tenían CUCI inactiva al ingresar al estudio, a pesar de los criterios clínicos y endoscópicos que indicaban enfermedad activa230. Claramente esto produce cuestiones complejas. Existen limitaciones logísticas con el tiempo para el análisis histológico, especialmente por un lector central, que impide que se utilice como un criterio de inclusión, y se emplea para excluir retrospectivamente a aquellos pacientes con enfermedad inactiva. Sin embargo, la Agencia Europea de Medicamentos en sus guías para los ensayos clínicos de nuevos agentes para la CUCI establece que la ausencia de evidencia histológica de inflamación activa excluye de manera definitiva la enfermedad activa (CHMP/EWG/ 18463/2006, adoptada el 28 de enero de 2008).
Declaración 4K de la ECCO
El término «colitis indeterminada» debe restringirse a las muestras de patología. Cuando los pacientes tienen colitis que no se ha podido clasificar después de haber tenido en cuenta todos los estudios clínicos, radiológicos, endoscópicos e histológicos, entonces el término preferible es EII no clasificada (NE5, RG D).
La evolución de las características microscópicas que son útiles para el diagnóstico de CUCI es un proceso dependiente de la duración y la actividad de la enfermedad. Esta noción se confirma mediante estudios experimentales. En enfermedad de inicio temprano, pueden estar presenten pocas o ninguna de las características relevantes. En la enfermedad establecida el diagnóstico puede basarse en una combinación de plasmocitosis basal, anomalías en la arquitectura de las criptas, infiltrado inflamatorio transmucoso difuso e irregularidad de superficie epitelial. La evolución natural de enfermedad activa a enfermedad inactiva y el tratamiento también tiene un impacto sobre las características microscópicas. En la enfermedad inactiva, pocas características pueden persistir, los neutrófilos se encuentran notablemente ausentes y las biopsias pueden ser normales.
Es importante distinguir entre diferentes situaciones para el diagnóstico de CUCI:
- •
Biopsias obtenidas durante la fase inicial de la enfermedad (en las primeras 2 semanas de la aparición de los síntomas, incluyendo a niños pequeños y sin tratamiento)
- •
Biopsias obtenidas de pacientes con enfermedad establecida antes del tratamiento (síntomas durante más de 4-6 semanas)
- •
Biopsias obtenidas de pacientes con enfermedad establecida después de tratamiento (sería conveniente el análisis de biopsias previas)
En cada paciente, incluyendo a los niños, el resultado diagnóstico puede incrementarse cuando se analizan múltiples biopsias de diferentes segmentos del colon, incluyendo el recto y el íleon, aunque estas deben etiquetarse cuidadosamente para su adecuada evaluación209,210,231,232.
FinanciamientoNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.
Por toda su dedicación y empeño al Dr. Jesús K. Yamamoto-Furusho (presidente de la Pan American Crohn's and Colitis Organisation) como encargado de la publicación de las guías ECCO en español.
Estamos particularmente agradecidos a las Sras. Sylke Weidmann y Anna Saelter, Frankfurt por su asistencia secretarial y a las Sras. Julia Gabriel y Nicole Eichinger de la oficina de ECCO por la contribución sustancial en la coordinación e incorporación del Consenso. Agradecemos a todos aquellos que mostraron interés y compromiso con el proceso del Consenso de ECCO (procedimientos estándar en www.ecco-ibd.eu).
Miembros de las partes colaboradoras en la actualización 2011/2012:
Definiciones, clasificación, diagnóstico e imaginología (incluyendo, endoscopia) e histopatología
Rami Eliakim (IS), Presidente
Fernando Magro (PT)
Christian Maaser (DE)
Yehuda Chowers (IS)
Los colaboradores en el consenso fueron:
M. Allez, Hôpital Saint-Louis, París, Francia
L. Beaugerie, Hôpital Saint-Antoine, París, Francia
B. Bokemeyer, Gastroenterologische Gemeinschaftspraxis, Minden, Alemania
Y. Chowers, Rambam Health Care Center, Haifa, Israel
J.-F. Colombel, Hospital Huriez, Lille, Francia
S. Danese, Istituto Clinico Humanitas, Rozanno, Milán, Italia
G. D¿Haens, Academic Medical Centre, Amsterdam, Países Bajos
A. D¿Hoore, University Hospital Gasthuisberg, Leuven, Bélgica
A. Dignass, Agaplesion Markus Krankenhaus, Frankfurt, Alemania
R. Eliakim, Sheba Medical Center, Tel Hashomer, Israel
P. Gionchetti, Universita di Bologna, Bolonia, Italia
F. Gomollón García, Hospital Clínico Universitario, Zaragoza, España
W. Häuser, Klinikum Saarbrücken, Saarbrücken, Alemania
K. Herrlinger, Asklepios Klinik Nord–Heidberg, Hamburgo, Alemania
J. Lindsay, Barts and the Londres NHS Trust, Londres, Reino Unido
C. Maaser, Klinikum Lüneburg, Lüneburg, Alemania
F. Magro, Sao Joao Hospital, Porto, Portugal
G. Mantzaris, Evangelismos Hospital, Atenas, Grecia
G. Moser, University Hospital Vienna, Viena, Austria
G. Novacek, Medical University of Vienna, Viena, Austria
B. Oldenburg, University Medical Centre UMC Utrecht, Utrecht, Países Bajos
T. Øresland, Akershus University Hospital, Lorenskog, Noruega
J. Panes, Hospital Clinic Barcelona, Barcelona, España
F. Portela, Coimbra University Hospital, Coimbra, Portugal
W. Reinisch, University Hospital Vienna, Viena, Austria
G. Rogler, University Hospital Zurich, Zúrich, Suiza
M. Sans, Centro Médico Teknon, Barcelona, España
E. Stange, Robert Bosch Krankenhaus, Stuttgart, Alemania
J. M. Stein, Crohn Colitis Center, Frankfurt, Alemania
A. Sturm, Krankenhaus Waldfriede, Berlín, Alemania
H. Tilg, Bezirkskrankenhaus Hall in Tirol, Hall in Tirol, Austria
S. Travis, John Radcliffe Hospital, Oxford, Reino Unido
G. van Assche, University Hospital Gasthuisberg, Leuven, Bélgica
S. Vermeire, University Hospital Gasthuisberg, Leuven, Bélgica
A. Windsor, University College Londres Hospital, Londres, Reino Unido
Los colaboradores de la reunión del consenso por país fueron:
Austria: Moser, Novacek, Reinisch, Tilg
Bélgica: D’Haens, D’Hoore, Franchimont, van Assche, Vermeire
Bulgaria: Kotzev, Spassova
Croacia: Cukovic Cavka, Vucelic
República Checa: Bortlik, Douda
Dinamarca: Dahlerup, Kjeldsen
Finlandia: Färkkilä
Francia: Allez, Beaugerie, Carbonnel, Colombel
Alemania: Bokemeyer, Dignass, Häuser, Herrlinger, Maaser, Stange, Stein, Sturm
Grecia: Karagiannis, Mantzaris, Tsianos
Hungría: Lakatos,
Irlanda: Egan, O¿Morain
Israel: Eliakim, Odes
Italia: Danese, Gionchetti, Cottone, Kohn
Lituania: Kriukas, Kupcinskas
Noruega: Berset, Øresland, Jahnsen
Polonia: Rydzewska
Portugal: Magro, Portela
Rumania: Cijevschi Prelipcean, Diculescu
Rusia: Belousova, Potapov
Serbia: Tarabar
Eslovaquia: Gregus, Huorka
Eslovenia: Stabuc
España: Casellas Jorda, Gomollón Garcia, Panes, Sans
Suecia: Hertervig
Suiza: Rogler, Michetti, Seibold
Países Bajos: Fidder, Weersma
Turquía: Ferhat Celik, Törüner
Ucrania: Dorofeyev, Zviagintseva
Reino Unido: Lindsay, Travis, Windsor
Este artículo es una traducción del artículo publicado en Journal of Crohn's and Colitis, Vol. 6, Dignass A, et al. Second European evidence-based Consensus on the diagnosis and management of ulcerative colitis Part 1: Definitions and diagnosis, 965–990 © 2012 European Crohn's and Colitis Organisation. Publicado por Elsevier B.V. Todos los derechos reservados.
http://dx.doi.org/10.1016/j.crohns.2012.09.003
Citar este artículo como: Dignass A, et al., Second EUROPEAN evidence-based Consensus on the diagnosis and management of ulcerative colitis: Definitions and diagnosis, Journal of Crohn's and Colitis (2012), http://dx.doi.org/10.1016/j.crohns.2012.09.003