La estadificación en el carcinoma hepatocelular (CHC) otorga pronóstico y orientación terapéutica. La resección y el trasplante hepático son opciones curativas y las terapias de ablación se aplican a pacientes que no reciben tratamiento curativo. La sobrevida tras la resección hepática o terapias de ablación es variada.
ObjetivoDescribir la presentación, la estadificación, el manejo y la evolución de los pacientes con CHC en nuestro centro.
Pacientes y métodosCuarenta y dos pacientes fueron seguidos prospectivamente durante 7 años. La sobrevida se calculó mediante Kaplan-Meier y log-rank entre los sistemas de estadificación (Okuda, BCLC y CLIP) y tipos de tratamiento (resección hepática, ablación por radiofrecuencia y ningún tratamiento quirúrgico).
ResultadosLa edad media ± desviación estándar de los pacientes fue 68,9 ± 9,5 años; el 57% fueron mujeres y el 54% cirróticos. El 31% tenía infección por VHC. El tamaño medio del tumor fue 6.48 ± 2.52cm. Los estadios CLIP 0, Okuda I y BCLC A tuvieron mejor sobrevida que otros estadios (p<0.05). La resección tuvo mejor sobrevida (mediana: 32 meses y sobrevida a 1, 3 y 5 años del 83, el 39 y 19.7%) que ablación por radiofrecuencia (25 meses, y el 90 y el 17.2% a 1 y 3 años) y que ningún tratamiento quirúrgico (1 año<5%) (p<0.05).
ConclusiónLos pacientes con CHC en nuestro centro al igual que otra población en México son diagnosticados tardíamente. El pronóstico usando CLIP y BCLC es similar a la literatura. Los mejores resultados se observaron en estadios tempranos y los que tuvieron resección quirúrgica del CHC.
Hepatocellular carcinoma (HCC) staging provides a basis for calculating disease prognosis and therapeutic guidance. Liver resection and transplantation are curative options, and ablation therapies are applied to patients that are not candidates for curative treatment. Survival after liver resection or ablation therapies varies.
AimsTo describe the presentation, staging, management, and outcome in patients with HCC in our center.
Patients and methodsForty-two patients had a 7-year prospective follow-up. Survival was calculated with the Kaplan-Meier analysis and the log-rank test was used for its comparison between the staging systems (Okuda, BCLC, and CLIP) and types of treatment (liver resection, radiofrequency ablation, and no surgical treatment).
ResultsThe mean age of the patients was 68.9 ± 9.5 years; 57% were women. A total of 54% of the patients presented with cirrhosis and 31% were infected with hepatitis C virus (HCV). The mean tumor size was 6.48 ± 2.52cm. The CLIP 0, Okuda I, and BCLC A stages had better survival rates than the other stages (P<0.05). Survival with resection was superior (median of 32 months and survival at 1, 3, and 5 years of 83, 39, and 19.7%, respectively) to that of both radiofrequency ablation (median of 25 months and survival at 1 and 3 years of 90 and 17.2%, respectively) and no surgical treatment (1 year < 5%) (P<0.05).
ConclusionThe patients at our center were diagnosed at late stages of HCC, as is the case in other Mexican populations. Outcome in relation to CLIP and BCLC was similar to the prognoses reported in the literature. The best results were observed in the patients with early stage disease and those that underwent HCC resection surgery.
El carcinoma hepatocelular (CHC) es un problema de salud mundial muy importante. El CHC es el quinto cáncer más común en todo el mundo y la neoplasia hepática primaria más frecuente1,2. El CHC tiene una incidencia estimada de 0.5 a un millón de nuevos casos por año1-4. Si bien los factores de riesgo reconocidos incluyen la hemocromatosis y ciertas toxinas ambientales, la hepatitis B (VHB) y la hepatitis C (VHC) son los factores causales más predominantes en el desarrollo de CHC en el mundo. La cirrosis hepática está presente en el 50-80% de los pacientes que desarrollan CHC5. En México, la cirrosis hepática tiene un impacto crítico, ya que representa la tercera causa de muerte en nuestra población. El CHC representa > 90% de los tumores hepáticos primarios en nuestro país y, al igual que en otros países, la mortalidad por CHC en México ha mostrado una alza del 14% del año 2000 al año 20066,7.
Los sistemas de estadificación del CHC son importantes para predecir el pronóstico del paciente y orientar el enfoque terapéutico. Los sistemas convencionales para CHC, como la clasificación Okuda, tienen algunas limitaciones. Actualmente, se han propuesto y validado nuevos sistemas de estadificación, como el de la Clínica de Cáncer de Hígado de Barcelona (BCLC), que vincula el estadio de la enfermedad con una estrategia de tratamiento, y la calificación del Programa Italiano del Cáncer de Hígado (CLIP), que se utiliza en pacientes con enfermedad avanzada8.
El pronóstico del CHC sigue siendo muy pobre, con una sobrevida a 5 años <5% sin ningún tipo de tratamiento1. Hasta el momento, la resección y el trasplante hepático son las principales opciones curativas para el CHC. El trasplante hepático ofrece una cura potencial para el CHC atendiendo también la cirrosis subyacente. Sin embargo, menos del 20% de los pacientes reciben una resección hepática (RH) de índole curativa y un menor número de pacientes recibe un trasplante hepático9-11. El potencial de las terapias de ablación permite terapias locorregionales en pacientes con CHC que de otra manera no son candidatos a un tratamiento quirúrgico curativo. Las opciones de terapia de ablación para el CHC incluyen la inyección de etanol percutánea, la crioterapia, la ablación por radiofrecuencia (ARF) y la quimioembolización intraarterial, sola o combinada con ARF9,11,12. En algunos casos, estas terapias locorregionales se utilizan como terapias puente para llevar al paciente a un trasplante hepático11. La sobrevida tras la resección o las terapias de ablación en el CHC tiene una amplia gama de porcentaje debido a las diferencias en las etapas de CHC entre todos los estudios10,12-17. Las opciones de tratamiento sistémico para el CHC irresecable son limitadas. Recientemente, el sorafenib ha recibido aprobación de la Food and Drug Administration para el tratamiento sistémico del CHC18. A su vez, pocos estudios han investigado la presentación del CHC y sus resultados en México, siendo la mayoría procedentes de centros médicos de la ciudad de México durante diferentes intervalos19-25.
ObjetivoNuestro estudio tiene como objetivo describir la presentación, la estadificación, el manejo y los resultados de los pacientes con CHC de nuestro centro.
Pacientes y métodosEntre julio del 2005 y marzo del 2012, 42 pacientes con diagnóstico de CHC se evaluaron en el Centro Médico Nacional «Adolfo Ruiz Cortines» del Instituto Mexicano del Seguro Social en Veracruz, México, para tratamiento quirúrgico. Los pacientes fueron seguidos de manera prospectiva desde su evaluación inicial. El estudio fue aprobado por el comité de ética local institucional. Los factores examinados incluyen demografía (edad, sexo e índice de masa corporal), presencia de cirrosis, detección de hepatitis viral y valores de laboratorio. Los pacientes se clasificaron por Child-Pugh26 y modelo para la enfermedad hepática terminal (MELD)27.
El diagnóstico de CHC se realizó durante la evaluación o antes de la remisión a nuestro centro. Los valores de laboratorio incluidos en el estudio fueron de coagulación (tiempo de protrombina e índice internacional normalizado), pruebas de función hepática (bilirrubina total y albúmina sérica), creatinina sérica, detección de hepatitis viral, alfafetoproteína (AFP) y estudios radiológicos como tomografía computarizada (TAC) y resonancia magnética (RMN) con el fin de determinar el número de lesiones tumorales y tamaño del tumor. Todos los pacientes sometidos a RH o ARF tuvieron cuentas plaquetarias superiores a 100×103cél/mm3. Todos los pacientes fueron evaluados para descartar la presencia de metástasis extrahepáticas con TAC de toráx y gammagrama óseo. El diagnóstico se consideró tomando en cuenta criterios establecidos8,9,11para lesiones de 2cm en pacientes cirróticos: lesiones hipervascularizadas arterialmente en 2 estudios (TAC y RMN) o en uno solo cuando la AFP > 400 ng/ml. En pacientes no cirróticos, se solicitaron medios histopatológicos convencionales con biopsia por aspiración de aguja fina.
Los pacientes fueron clasificados según el sistema Okuda y las clasificaciones BCLC y CLIP. Se agrupó a los pacientes en 3 categorías para fines del manuscrito: tratamiento no quirúrgico (NT), la RH y la ARF. Todas las ARF se realizaron por laparotomía exploradora o laparoscopia cuando esta estuvo disponible para el paciente (n=2). Se otorgaron 2 ciclos de ARF cuando las lesiones eran inferiores a 5cm, y 3 a 4 ciclos cuando las lesiones eran superiores a 5cm. Los pacientes fueron seguidos a través de la consulta externa con pruebas de función hepática y niveles séricos de AFP cada mes, ultrasonografía hepática cada 2 meses y TAC toracoabdominal cada 6 meses o antes en sospecha de recurrencia. La recurrencia del tumor se definió por el aumento de AFP y la aparición de nuevas lesiones tumorales radiológicas en pacientes que se sometieron a RH. Se registró el uso de sorafenib cuando estuvo disponible en nuestra unidad. La sobrevida global fue el objetivo principal del estudio. La sobrevida se calculó a partir del momento de la evaluación hasta la muerte o la pérdida del seguimiento. Los pacientes fueron evaluados por modalidad de tratamiento y sistema de clasificación/estadificación.
Análisis estadísticoLos datos fueron analizados mediante el software SPSS 21 (SPSS, 2012, Chicago, EE. UU.). Se utilizaron la media ± desviación estándar y el rango para describir variables continuas, y la frecuencia y los porcentajes para variables categóricas. Se utilizó el análisis de varianza (ANOVA) para las variables continuas con distribución normal entre los grupos de tratamiento y la chi al cuadrado (χ2) para las variables categóricas. La sobrevida se calculó mediante prueba de Kaplan-Meier y la prueba de log-rank (Mantel-Cox) se utilizó para comparar la sobrevida entre los grupos. La mediana de sobrevida se registró en meses. Un valor de p <0.05 se consideró estadísticamente significativo.
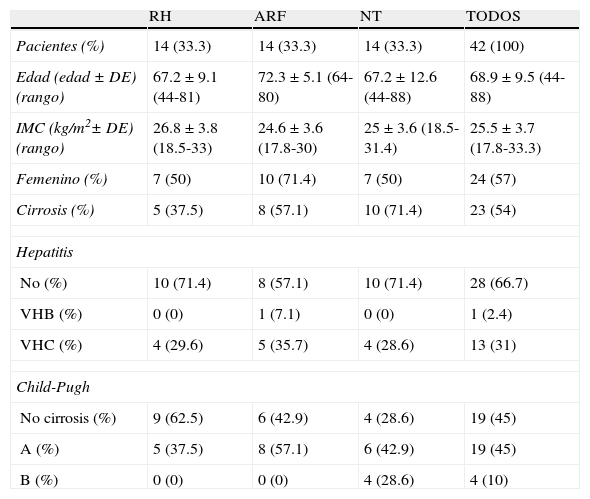
ResultadosLa edad media de todos los pacientes fue de 68.9 ± 9.5 años. La mayoría de los pacientes (57%) eran mujeres y más de la mitad de los pacientes eran cirróticos (54%). El VHC fue la hepatitis viral más común presente en nuestra población (31%) y ninguno de los pacientes se clasificó como Child-Pugh C. Los datos demográficos de los pacientes, la presencia de cirrosis, hepatitis viral y la clasificación Child-Pugh para todos los pacientes y por modalidad de tratamiento se encuentran en la tabla 1. De manera coincidente, fue el mismo número de pacientes el que recibió tratamiento quirúrgico (ya sea RH o ARF) y los pacientes que no recibieron tratamiento quirúrgico (NT) (n=14). A un paciente se le realizó una ARF y una RH durante el mismo procedimiento.
Características clínicas de los pacientes por grupoa
| RH | ARF | NT | TODOS | |
| Pacientes (%) | 14 (33.3) | 14 (33.3) | 14 (33.3) | 42 (100) |
| Edad (edad ± DE) (rango) | 67.2 ± 9.1 (44-81) | 72.3 ± 5.1 (64-80) | 67.2 ± 12.6 (44-88) | 68.9 ± 9.5 (44-88) |
| IMC (kg/m2± DE) (rango) | 26.8 ± 3.8 (18.5-33) | 24.6 ± 3.6 (17.8-30) | 25 ± 3.6 (18.5-31.4) | 25.5 ± 3.7 (17.8-33.3) |
| Femenino (%) | 7 (50) | 10 (71.4) | 7 (50) | 24 (57) |
| Cirrosis (%) | 5 (37.5) | 8 (57.1) | 10 (71.4) | 23 (54) |
| Hepatitis | ||||
| No (%) | 10 (71.4) | 8 (57.1) | 10 (71.4) | 28 (66.7) |
| VHB (%) | 0 (0) | 1 (7.1) | 0 (0) | 1 (2.4) |
| VHC (%) | 4 (29.6) | 5 (35.7) | 4 (28.6) | 13 (31) |
| Child-Pugh | ||||
| No cirrosis (%) | 9 (62.5) | 6 (42.9) | 4 (28.6) | 19 (45) |
| A (%) | 5 (37.5) | 8 (57.1) | 6 (42.9) | 19 (45) |
| B (%) | 0 (0) | 0 (0) | 4 (28.6) | 4 (10) |
ARF: ablación por radiofrecuencia; IMC: índice de masa corporal; NT: no tratamiento quirúrgico; RH: resección hepática; VHB: virus de la hepatitis B; VHC: virus de la hepatitis C.
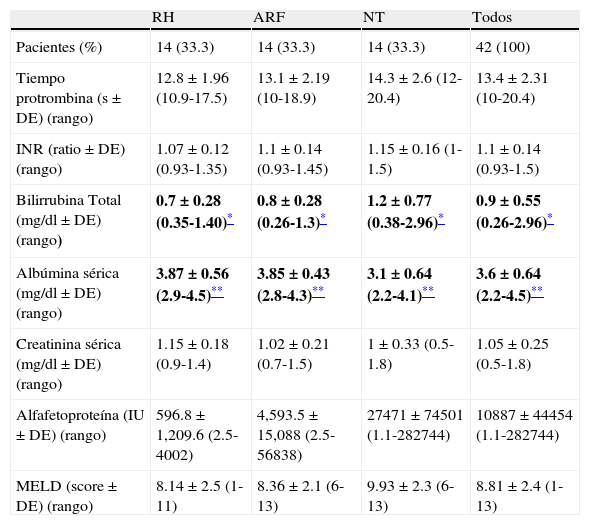
Los pacientes de NT tenían peores pruebas de función hepática que los pacientes con tratamiento quirúrgico (sea RH o ARF). Los valores de bilirrubina total y la albúmina sérica tuvieron una diferencia estadísticamente significativa entre los pacientes con RH, ARF o NT. Del mismo modo, los pacientes NT tenían niveles de AFP superiores y MELD que los pacientes con RH o los sometidos a ARF, aunque estas diferencias no tuvieron significación estadística. La creatinina sérica fue similar en todos los pacientes. Todos los valores de laboratorio se detallan en la tabla 2.
Valores de laboratorio de los pacientes por modalidad de tratamiento
| RH | ARF | NT | Todos | |
| Pacientes (%) | 14 (33.3) | 14 (33.3) | 14 (33.3) | 42 (100) |
| Tiempo protrombina (s ± DE) (rango) | 12.8 ± 1.96 (10.9-17.5) | 13.1 ± 2.19 (10-18.9) | 14.3 ± 2.6 (12-20.4) | 13.4 ± 2.31 (10-20.4) |
| INR (ratio ± DE) (rango) | 1.07 ± 0.12 (0.93-1.35) | 1.1 ± 0.14 (0.93-1.45) | 1.15 ± 0.16 (1-1.5) | 1.1 ± 0.14 (0.93-1.5) |
| Bilirrubina Total (mg/dl ± DE) (rango) | 0.7 ± 0.28 (0.35-1.40)* | 0.8 ± 0.28 (0.26-1.3)* | 1.2 ± 0.77 (0.38-2.96)* | 0.9 ± 0.55 (0.26-2.96)* |
| Albúmina sérica (mg/dl ± DE) (rango) | 3.87 ± 0.56 (2.9-4.5)** | 3.85 ± 0.43 (2.8-4.3)** | 3.1 ± 0.64 (2.2-4.1)** | 3.6 ± 0.64 (2.2-4.5)** |
| Creatinina sérica (mg/dl ± DE) (rango) | 1.15 ± 0.18 (0.9-1.4) | 1.02 ± 0.21 (0.7-1.5) | 1 ± 0.33 (0.5-1.8) | 1.05 ± 0.25 (0.5-1.8) |
| Alfafetoproteína (IU ± DE) (rango) | 596.8 ± 1,209.6 (2.5-4002) | 4,593.5 ± 15,088 (2.5-56838) | 27471 ± 74501 (1.1-282744) | 10887 ± 44454 (1.1-282744) |
| MELD (score ± DE) (rango) | 8.14 ± 2.5 (1-11) | 8.36 ± 2.1 (6-13) | 9.93 ± 2.3 (6-13) | 8.81 ± 2.4 (1-13) |
ARF: ablación por radiofrecuencia; MELD: Model for End Stage Liver Disease; NT: no tratamiento quirúrgico; RH: resección hepática.
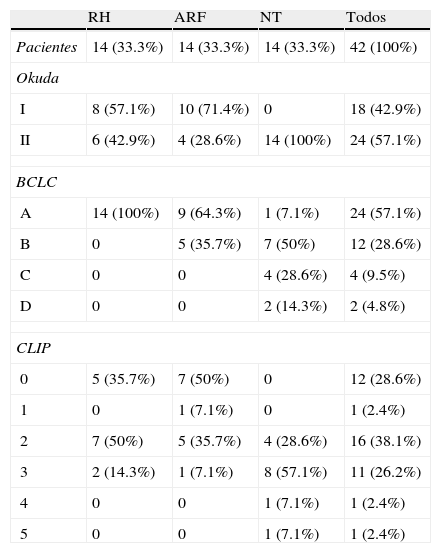
El tamaño promedio de las lesiones tumorales fue de 6.48 ± 2.52cm (rango 2-13cm). La mediana de tamaño fue de 6cm. Veintitrés pacientes (54.8%) tenían tumores mayores a 5cm. Los pacientes de NT tenían lesiones más grandes (7.36 ± 2.37cm, rango 5-13cm) que los pacientes sometidos a ARF (6.07 ± 2.9cm, rango 3-13cm) y los pacientes con RH (6 ± 2.48cm, rango 2-9cm), aunque esta diferencia no fue estadísticamente significativa. Trece pacientes (92.9%) con RH tuvieron un tumor único y solo un paciente (7.1%) tenía 3 tumores. Del mismo modo, los pacientes sometidos a ARF, 12 pacientes (85.7%), tenían un tumor y el resto de los pacientes en el grupo (n=2, 14.3%) tenía 2 tumores. Tres pacientes NT (21.4%) tenía 3 tumores y 10 (71.4%) tenían únicamente un tumor en ese grupo. En todos los pacientes con más de un tumor, el tamaño de este fue superior a 5cm. Catorce pacientes (33.3%) tuvieron biopsia preoperatoria con diagnóstico histopatológico de CHC (5 pacientes sometidos a RH, 5 pacientes sometidos a ARF y 4 pacientes con NT). La tabla 3 muestra la estadificación de los paciente según Okuda, BCLC y CLIP. La mayoría de los pacientes fueron clasificados como Okuda estadio ii (57.1%). Todos los pacientes que se sometieron a RH se clasificaron como estadio inicial de BCLC (A). La mayoría de los pacientes NT (78.6%) estaban en estadios BCLC intermedios y avanzados (etapas B y C). Las puntuaciones de CLIP también fueron superiores en los pacientes NT.
Estadificación de los pacientes por tipo de tratamiento
| RH | ARF | NT | Todos | |
| Pacientes | 14 (33.3%) | 14 (33.3%) | 14 (33.3%) | 42 (100%) |
| Okuda | ||||
| I | 8 (57.1%) | 10 (71.4%) | 0 | 18 (42.9%) |
| II | 6 (42.9%) | 4 (28.6%) | 14 (100%) | 24 (57.1%) |
| BCLC | ||||
| A | 14 (100%) | 9 (64.3%) | 1 (7.1%) | 24 (57.1%) |
| B | 0 | 5 (35.7%) | 7 (50%) | 12 (28.6%) |
| C | 0 | 0 | 4 (28.6%) | 4 (9.5%) |
| D | 0 | 0 | 2 (14.3%) | 2 (4.8%) |
| CLIP | ||||
| 0 | 5 (35.7%) | 7 (50%) | 0 | 12 (28.6%) |
| 1 | 0 | 1 (7.1%) | 0 | 1 (2.4%) |
| 2 | 7 (50%) | 5 (35.7%) | 4 (28.6%) | 16 (38.1%) |
| 3 | 2 (14.3%) | 1 (7.1%) | 8 (57.1%) | 11 (26.2%) |
| 4 | 0 | 0 | 1 (7.1%) | 1 (2.4%) |
| 5 | 0 | 0 | 1 (7.1%) | 1 (2.4%) |
ARF: ablación por radiofrecuencia; BCLC: Clínica de Cáncer de Hígado de Barcelona; CLIP: Programa Italiano de Cáncer de Hígado; NT: no tratamiento quirúrgico; RH: resección hepática.
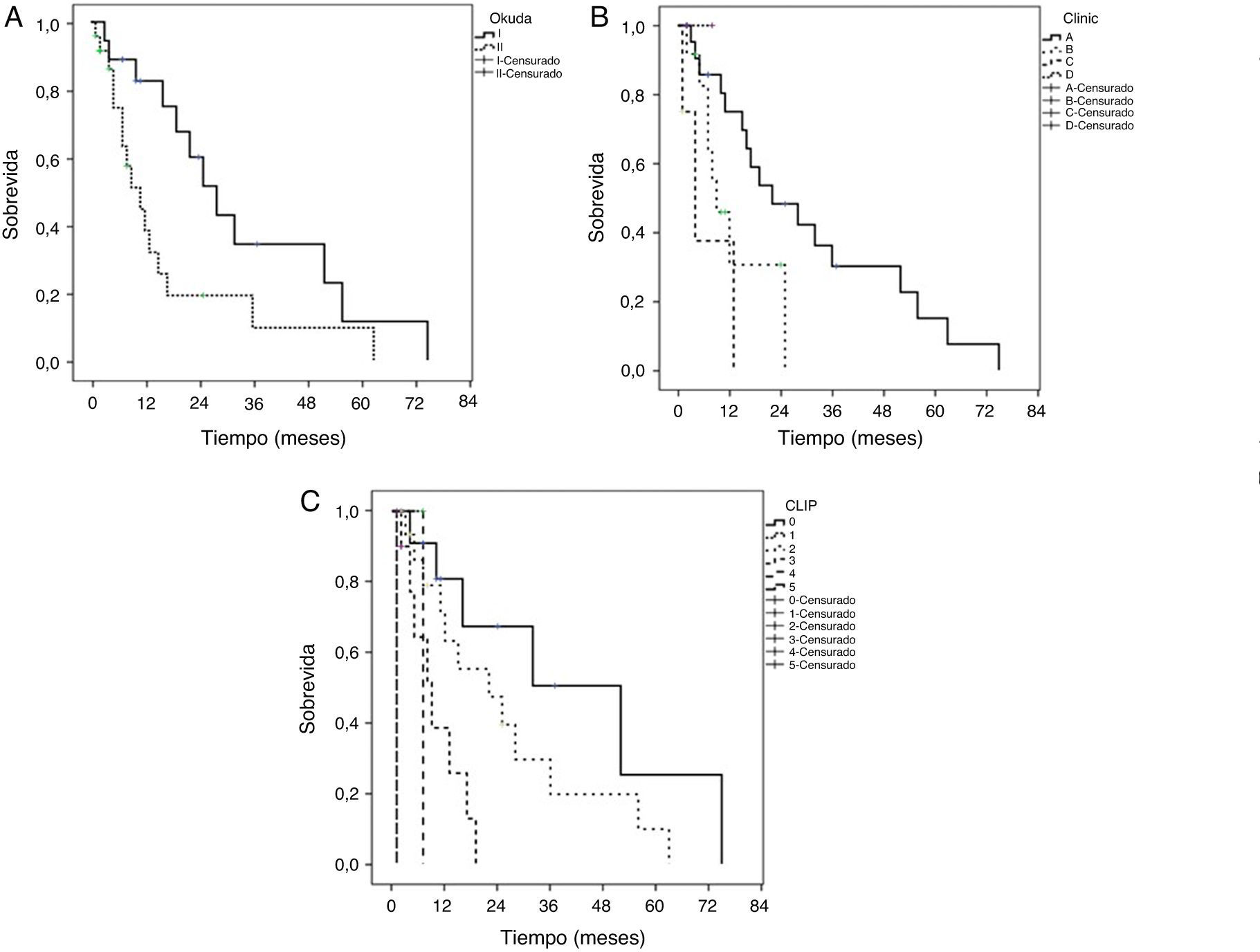
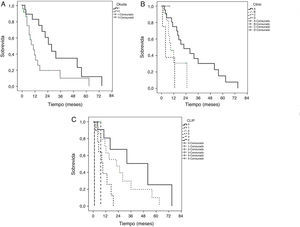
La mediana de sobrevida fue de 16 ± 3.8 meses (IC del 95%, 8.5-23.4) en todos los pacientes, siendo superior en los pacientes sometidos a RH, con baja puntuación CLIP y estadios tempranos de acuerdo a BCLC. La sobrevida actuarial (Kaplan-Meier) se realizó en los sistemas Okuda, BCLC y CLIP (fig. 1). Las diferencias en la puntuación CLIP fueron estadísticamente más significativa entre ellas (p=0.0001). Los pacientes con una puntuación CLIP de 0 tuvieron una sobrevida del 80.1, el 50.6 y 25.1% a 1, 3 y 5 años, respectivamente. Los pacientes con una puntuación CLIP de 2 tuvieron una sobrevida a 1, 3 y 5 años del 63.2, el 19.7 y el 10.1%, respectivamente. Los pacientes con una puntuación CLIP de 3 tuvieron una sobrevida a un año del 38.5%, con una sobrevida máxima de 19 meses. La sobrevida máxima de las puntuaciones CLIP 4 y 5 fueron 6.8 y 1.1 meses, respectivamente. Solo un paciente tuvo una puntuación CLIP de 1, cuya sobrevida máxima fue de 6.8 meses. Los pacientes clasificados como fase temprana (estadio A) de BCLC tuvieron la mejor sobrevida actuarial (el 75.2, el 30.1 y el 15. 3% para 1, 3 y 5 años, respectivamente). Los pacientes en etapa intermedia (B) y etapa avanzada (C) tuvieron una sobrevida a un año del 30 y el 37%, respectivamente. Estas diferencias fueron estadísticamente significativas entre las etapas (p=0.01). Ninguno de los pacientes clasificados como estadio avanzado (D) sobrevivió más allá de 12 meses. Del mismo modo, no hubo sobrevivientes en las etapas B y C durante 3 años. Los pacientes en estadio Okuda i tuvieron mejor sobrevida a 1, 3 y 5 años (el 88.9, el 34.2 y el 11.5%) que el estadio Okuda ii (el 82.6, el 19.1 y el 9.6%). Estas diferencias fueron estadísticamente significativas (p=0.023).
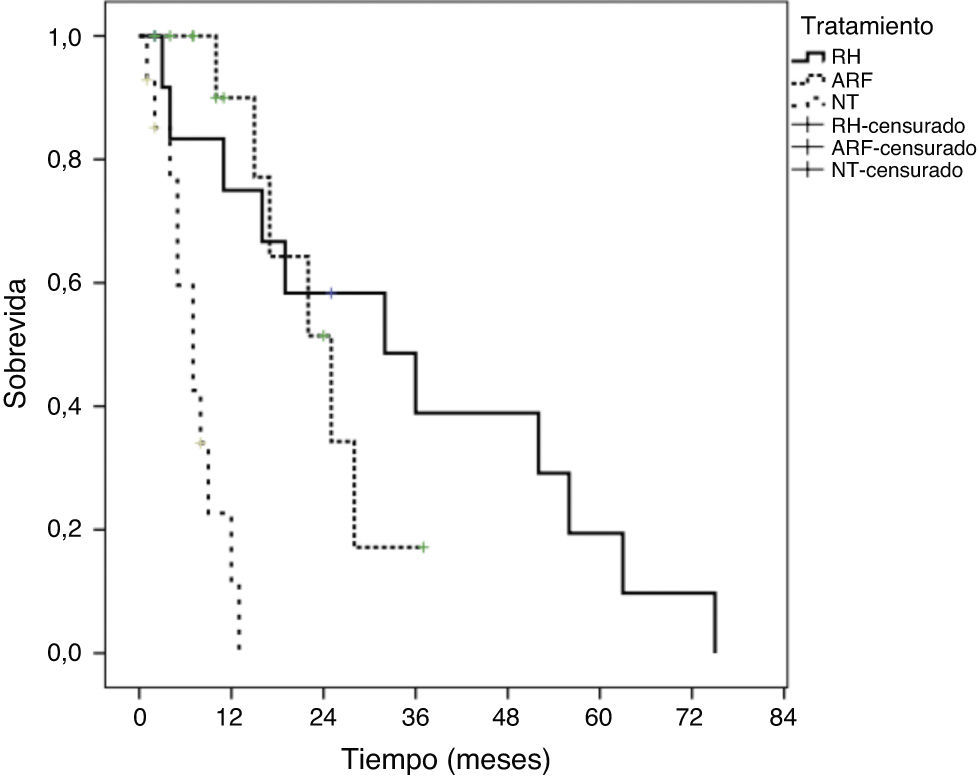
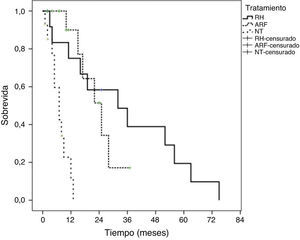
La sobrevida de acuerdo con la modalidad de tratamiento mostró que los pacientes que se sometieron a RH tuvieron mejor sobrevida que los pacientes sometidos a ARF o NT (p=0,0001). Las medianas de supervivencia de los pacientes con RH fue de 32 ± 12.9 meses (IC del 95%, 6.6-57.3). La mediana de sobrevida de los pacientes sometidos a ARF fue de 25 ± 4.8 meses (IC del 95%, 15.4 a 34.5) y 7 ± 1.6 meses (IC del 05%, 8.5 a 23.4) para los pacientes NT. La sobrevida actuarial a 1, 3 y 5 años de los pacientes con RH fue del el 83, el 39.1 y el 19.7%. Los pacientes que fueron sometidos a ARF tuvieron una sobrevida a un año del 90 y el 17.2% a 3 años. La sobrevida a un año de los pacientes que no recibieron tratamiento quirúrgico alguno (NT) fue inferior al 5%. La figura 2 muestra las curvas de sobrevida mediante Kaplan-Meier para todas las modalidades de tratamiento.
Por último, la recurrencia del tumor en los pacientes con RH fue del 21.4% (n=3) a los 18, 40 y 50 meses, todas en el borde quirúrgico y en pacientes con resecciones anatómicas. De estos pacientes, 2 recibieron sorafenib y otro ningún tratamiento. Siete pacientes recibieron sorafenib: 2 pacientes posterior a la RH y 2 pacientes NT y 3 pacientes sometidos a ARF.
DiscusiónExisten similitudes en las características clínicas de nuestros pacientes con CHC cuando se comparan las poblaciones mundial y mexicana. El CHC suele aparecer en pacientes mayores de 55 años de edad, como se ha visto en nuestro estudio, independientemente de la distribución geográfica (EE. UU. y los países de Oriente)13,14,16,19,24. Desde 1999, Tsukuma, et al.5 mostraron que la cirrosis estaba presente en el 50-80% de los pacientes que finalmente desarrollaron CHC. En 1999, Fong et al.13 tuvieron una incidencia del 70% en la cirrosis hepática en los pacientes con CHC. Los estudios mexicanos del mismo año tienen una incidencia de cirrosis de un 56% en la población19 y estas cifras elevadas se mantienen en nuestro país con mayores porcentajes, cercanos o superiores a un 50%: 38% en el estudio de Meza-Junco et al.22 y 72% en los empleados federales en la Ciudad de México24. Aunque el VHB es más común en los países orientales, donde la infección por VHC llega a ser tan alta como un 75%5,12, la asociación de VHB y VHC con CHC también está bien descrita en la población norteamericana1,6,7. En México, el VHC es la segunda causa de la cirrosis hepática, la cual está íntimamente relacionada con el CHC6,7, y estudios de instituciones mexicanas mostraron que el VHC está presente en hasta un 60% de los pacientes con CHC21. Nuestro centro tiene características similares, ya que la mitad de nuestros pacientes tienen cirrosis hepática (54%) y el VHC está presente en casi un tercio de nuestra población.
Actualmente, no hay un sistema de clasificación aceptado en todo el mundo utilizado para el CHC. Los sistemas de clasificación tradicionales, como Okuda o Child-Pugh, no incluyen diferentes variables pronósticas, tales como el grado de hipertensión portal, la AFP, el tamaño del tumor y el estado funcional del paciente, por lo que estos deben utilizarse de forma concomitante con otros sistemas8. La clasificación BCLC y la puntuación CLIP incluyen la clasificación de Child-Pugh y se utilizan con diferentes capacidades de predicción del pronóstico y tratamiento del paciente8,9. La clasificación de Okuda tiene una capacidad pronóstica inferior a los demás8 y la puntuación CLIP tiene un poder pronóstico mejor en la población occidental8. La clasificación BCLC también sirve como guía para el tratamiento de CHC en sus primeras etapas9. Los estudios mexicanos sobre CHC utilizan en su mayoría un solo sistema de estadificación como Okuda19-22 o BCLC24. Nuestro estudio demuestra capacidad predictiva en todos los sistemas, desde los estadios avanzados tienen peor pronóstico estadísticamente significativo que las etapas tempranas e intermedias. Por otra parte, la puntuación CLIP y el sistema BCLC tuvieron mejor validez significativa que el sistema Okuda.
El trasplante hepático ofrece la mejor sobrevida a 5 años en pacientes con CHC; sin embargo, menos del 20% de los pacientes cumplen los criterios de Milán para trasplante (un solo CHC menor a 5cm o menos de 3 nódulos menores a 3cm)9-11. Los resultados de trasplante hepático en México para CHC son limitados28–32y no existen publicaciones mexicanas que detallen experiencias completas con todo tipo de terapias para CHC. En los Estados Unidos de Norteamérica, experiencias de instituciones individuales se han publicado examinando los resultados del tratamiento en pacientes con CHC, donde el 75% tenían tumores > 5cm, con mediana de sobrevida de 39 meses y sobrevida actuarial a 1, 3 y 5 años del 81, el 54 y el 37%, respectivamente13. Las terapias de ablación (no ARF) tuvieron una mediana de sobrevida de 15 meses13. Un subanálisis del mismo centro de los tumores >10cm describió una mediana de sobrevida de 32 meses y un 33% de sobrevida actuarial a 5 años, sin diferencias significativas entre los tumores pequeños (< 10cm) y grandes (> 10cm)14. Otro centro occidental10 encontró que solo el 30% de los pacientes con CHC evaluados fueron intervenidos quirúrgicamente (trasplante 13%, 12% RH y 5% ARF). La mejor mediana de sobrevida fue para los pacientes trasplantados (100.3 meses), seguidos de la RH (44.5 meses) y la ARF (31.6 meses) (p < 0.05). La sobrevida al año de RH y ARF fue del 81 y el 86%, respectivamente; la sobrevida a 3 años fue de cerca del 50% en ambos (RH 57% y 47% ARF) y la sobrevida a los 5 años fue del 47% en los pacientes sometidos a RH y el 36% en pacientes de ARF. Recientemente, la relación entre las modalidades de terapia CHC y la sobrevida global ha sido analizada utilizando la base de datos SEER desde 1973 hasta el 200317. El tamaño tumoral medio fue de 5cm y el 52% tenía lesión única. La RH se realizó en el 16% de los pacientes con una sobrevida a los 5 años del 35%. La ARF se utilizó en el 25%, con un 20% de sobrevida a 5 años17. Un subanálisis del SEER en pacientes con CHC menor de 5cm mostró una sobrevida media de 45 meses y un 39% de sobrevida a 5 años después de una RH. Los estudios de China tienen mejores sobrevidas medias y actuariales comparados con los estudios de Occidente, tanto en RH16 como también en ARF12. Nuestro centro tiene ciertas similitudes con los estudios occidentales, como la media del tamaño tumoral, el número de lesiones únicas y una buena sobrevida actuarial a un año en RH y ARF; sin embargo, nuestra sobrevida media es ligeramente menor para la RH y ARF, y la sobrevida a 5 años es menor en comparación con los centros antes mencionados. Se debe destacar que, aunque nuestra mediana de sobrevida es adecuada, el IC del 95% es muy amplio en nuestra serie, lo cual puede modificar la estimación de nuestra sobrevida actuarial a 5 años. Algunos otros factores pudieron influir en esta misma sobrevida, como la edad, las comorbilidades de los pacientes y los aspectos relacionados a la RH misma; sin embargo, estos no fueron tomados en nuestro análisis estadístico. La comparación entre todas las modalidades de tratamiento no es factible en nuestro estudio, ya que nosotros no realizamos trasplante hepático; sin embargo, se debe destacar que el 42.8% (n=18) no sería considerado candidato a trasplante hepático según BCLC9 y el 69% (n=29) estaba fuera de los criterios de Milán para el trasplante9-11. Nuestro hospital tiene un centro de referencia institucional para trasplante hepático, el cual tiene como criterio de referencia para edad a pacientes menores de 65 años y en el caso de CHC utilizan los criterios de Milán para la misma, por lo cual la referencia de nuestros pacientes hubiera sido muy limitada sobre la base de estos 2 criterios.
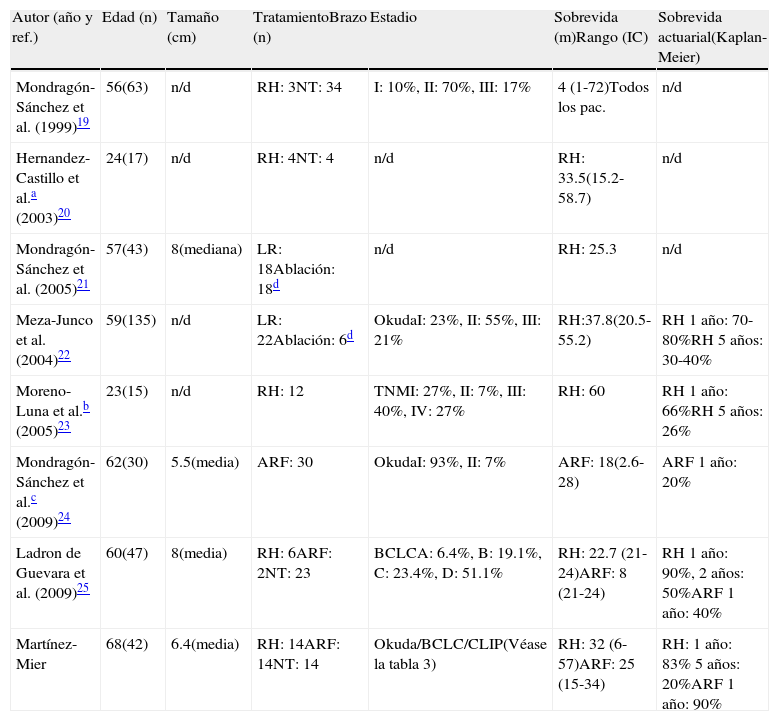
Pocos estudios mexicanos han sido publicados evaluando las diferentes modalidades de tratamiento del CHC (tabla 4). Podemos notar ciertas diferencias entre estos estudios y nuestros resultados: a) sin tener en cuenta los estudios de CHC en pacientes <40 años de edad20 y los pacientes con CHC fibrolamelar23, los pacientes en nuestro centro son mayores que otros; b) nuestros estudio tiene un número similar de RH y de ARF; c) solo 2 estudios, además del nuestro, incluyen la ARF como terapia para el CHC y uno de estos incluye todo tipo de tumores hepáticos24; d) nuestro estudio incluye varios sistemas de estadificación para el CHC, y e) la mediana de sobrevida de los pacientes sometidos a ARF es mayor al resto de ellos, con una sobrevida en RH similar o superior. A pesar de que estas diferencias fortalecen nuestro estudio, tenemos que reconocer algunas salvedades además de la falta de resultados de trasplante hepático: nuestro centro no realiza quimioembolización transhepática arterial23,25, como ha sido sugerido para pacientes estadio B de BCLC, lo que ha llevado a ser más liberales en el uso de la ARF desde que empezamos a utilizarlo en 200533, pudiendo así modificar nuestros resultados y, además, el uso de sorafenib en nuestro centro es irregular, lo que no nos permite hacer un análisis estadístico del uso del sorafenib.
Estudios mexicanos sobre la presentación de HCC y sus resultados
| Autor (año y ref.) | Edad (n) | Tamaño (cm) | TratamientoBrazo (n) | Estadio | Sobrevida (m)Rango (IC) | Sobrevida actuarial(Kaplan-Meier) |
| Mondragón-Sánchez et al. (1999)19 | 56(63) | n/d | RH: 3NT: 34 | I: 10%, II: 70%, III: 17% | 4 (1-72)Todos los pac. | n/d |
| Hernandez-Castillo et al.a (2003)20 | 24(17) | n/d | RH: 4NT: 4 | n/d | RH: 33.5(15.2-58.7) | n/d |
| Mondragón-Sánchez et al. (2005)21 | 57(43) | 8(mediana) | LR: 18Ablación: 18d | n/d | RH: 25.3 | n/d |
| Meza-Junco et al. (2004)22 | 59(135) | n/d | LR: 22Ablación: 6d | OkudaI: 23%, II: 55%, III: 21% | RH:37.8(20.5-55.2) | RH 1año: 70-80%RH 5años: 30-40% |
| Moreno-Luna et al.b (2005)23 | 23(15) | n/d | RH: 12 | TNMI: 27%, II: 7%, III: 40%, IV: 27% | RH: 60 | RH 1año: 66%RH 5años: 26% |
| Mondragón-Sánchez et al.c (2009)24 | 62(30) | 5.5(media) | ARF: 30 | OkudaI: 93%, II: 7% | ARF: 18(2.6-28) | ARF 1año: 20% |
| Ladron de Guevara et al. (2009)25 | 60(47) | 8(media) | RH: 6ARF: 2NT: 23 | BCLCA: 6.4%, B: 19.1%, C: 23.4%, D: 51.1% | RH: 22.7 (21-24)ARF: 8 (21-24) | RH 1año: 90%, 2años: 50%ARF 1año: 40% |
| Martínez-Mier | 68(42) | 6.4(media) | RH: 14ARF: 14NT: 14 | Okuda/BCLC/CLIP(Véase la tabla 3) | RH: 32 (6-57)ARF: 25 (15-34) | RH: 1año: 83% 5años: 20%ARF 1año: 90% |
ARF: ablación por radiofrecuencia; BLCL: Barcelona Clinic Liver Cancer Center; CLIP: Cancer Liver Italian Program; n/d: no determinado; NT: no tratamiento quirúrgico; RH: resección hepática; TNM: tumor nódulo metástasis.
En conclusión, los pacientes con CHC en nuestro centro tienen características similares a otra población en México, siendo diagnosticados en estadios tardíos. El pronóstico en nuestros pacientes usando CLIP y BCLC es similar a lo reportado en la literatura. Los mejores resultados se observaron en estadios tempranos y aquellos que tuvieron resección quirúrgica del CHC. Se deberá hacer un diagnóstico y una referencia oportuna a centros especializados para determinar su manejo o envío a otros centros donde exista la opción de tratamiento que corresponda al paciente según su estatificación
FinanciamientoNinguno.
Conflicto de interesesNinguno que declarar.