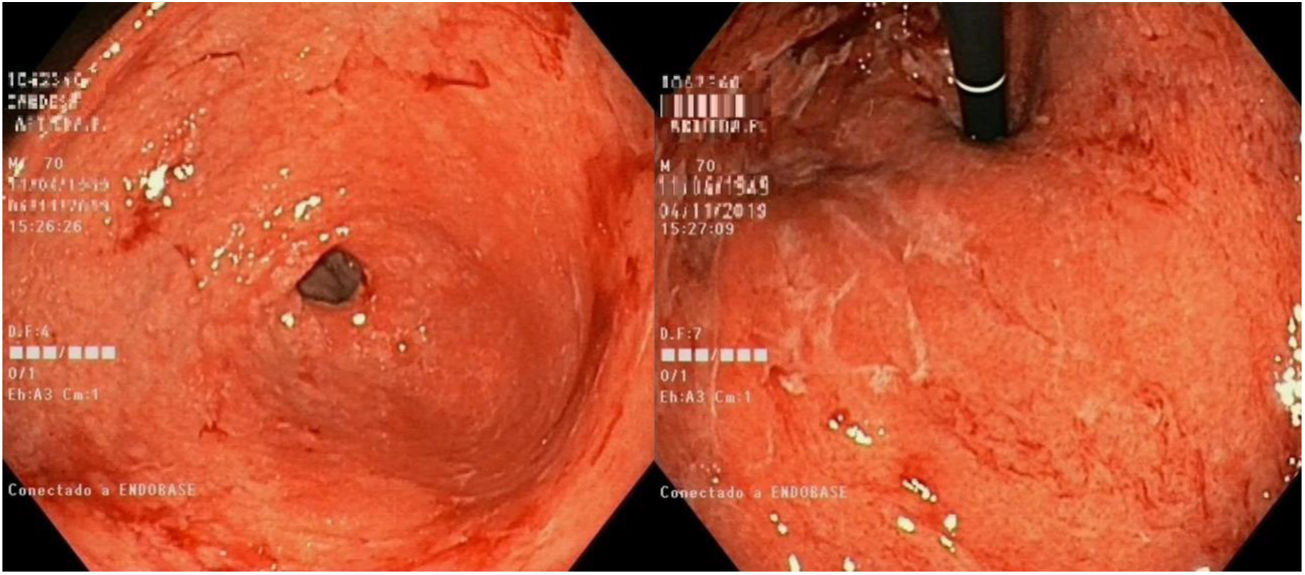
Un hombre de 70 años con melanoma metastásico (T3bN2M1) tratado con nivolumab (62 ciclos, 3mg/kg cada 14 días) durante 2.5 años fue internado en el hospital con dolor epigástrico, hiporexia y vómitos de un mes de progreso. Los datos de laboratorio y la tomografía computarizada abdominal no mostraron hallazgos significativos. Se realizó una esofagogastroduodenoscopía, que reveló mucosa engrosada, congestión difusa, edema, eritema y friabilidad de la mucosa gástrica (fig. 1). Las biopsias gástricas mostraron infiltración celular inflamatoria en la lámina propia, abscesos de cripta y destrucción glandular (fig. 2), lo cual fue indicativo de posible evento adverso relacionado con la terapia con nivolumab. No existió evidencia de infección por Helicobacterpylori (H. pylori). El nivolumab fue descontinuado y el paciente recibió terapia con inhibidor de bomba de protones (PPI, por sus siglas en inglés). El paciente fue dado de alta después de 3semanas de hospitalización y permanece asintomático 6 meses posterior al retiro del nivolumab. Los inhibidores de puestos de control inmunitarios, como el nivolumab, se asocian frecuentemente con eventos gastrointestinales adversos. La diarrea y la enterocolitis son las presentaciones más comunes y la gastritis y la esofagitis son raras. La gastritis inducida por nivolumab puede mejorar con la detención de la terapia, el uso de PPI y terapia con corticoides. Es necesario hacer prueba para infección por H. pylori, ya que dicha bacteria puede empeorar el curso clínico.
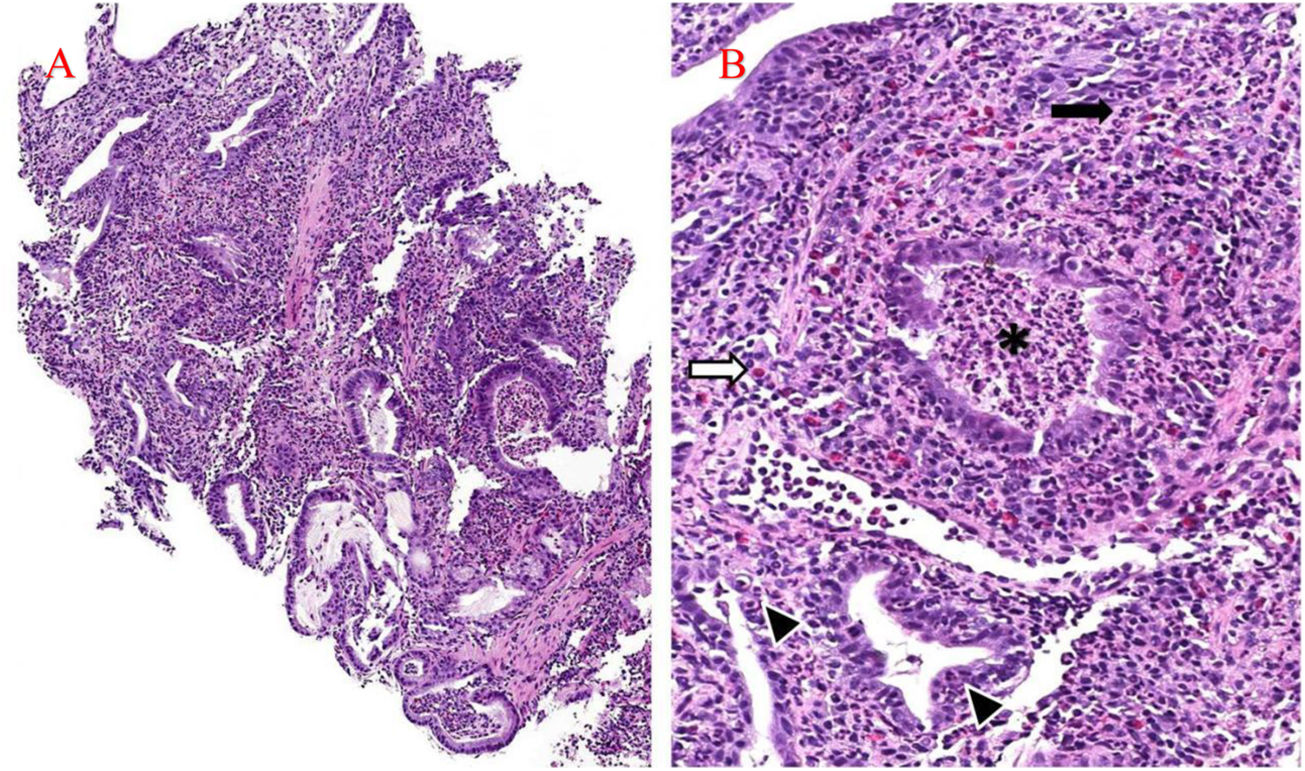
A) La biopsia gástrica muestra marcada distorsión arquitectónica secundaria a la presencia de infiltración inflamatoria densa dentro de la lámina propia (H&E×100). B) La infiltración inflamatoria se compone principalmente de neutrófilos (flecha negra) pero también hay presentes eosinófilos (flecha blanca). La criptitis (puntas de flecha) y los abscesos de cripta (asterisco) son prominentes (H&E×200).
El paciente proporcionó su consentimiento informado para recibir el tratamiento y participar en la presente investigación, lo cual cumple con las regulaciones actuales de la investigación bioética y fue autorizado por el comité institucional de ética.
Los autores declaran que el presente artículo no contiene información personal que pudiera identificar al paciente.
FinanciaciónNo se recibió financiamiento alguno con relación a este estudio/artículo.
Conflicto de interesesLos autores declaran que no existió conflicto de intereses.