Durante el curso clínico de la enfermedad inflamatoria intestinal (EII) diversas causas pueden comprometer la función renal, hepática y medular e incrementar el riesgo de osteoporosis, infecciones y neoplasias. El objetivo de este estudio es describir el seguimiento que llevan los pacientes mexicanos con EII respecto a su esquema de vacunación, riesgos asociados a tratamiento y cáncer.
Material y métodosEstudio transversal, retrospectivo. Se encuestó a 100 pacientes con diagnóstico histopatológico de EII entre febrero y junio de 2017 acerca del seguimiento de esquema de vacunación, riesgos asociados al tratamiento y cáncer. Se realizó el análisis estadístico en SPSS v. 24.
ResultadosSe estudiaron 100 pacientes con EII (el 90% con colitis ulcerosa crónica idiopática, y el 10% con enfermedad de Crohn; el 60% eran mujeres y el 40%, hombres): el 75% negaron poseer un carnet de vacunación; el 71.4% de las mujeres se habían realizado al menos una citometría cervical en su vida, el 28.6% no se la realizan de forma anual; el 24% utilizan protector solar diariamente; el 18.2% con más de 10 años de evolución de una colitis ulcerosa crónica idiopática tiene una colonoscopia anual; anualmente se registra función renal en el 57.1%, biometría hemática en el 92.9%, función hepática en el 78.6% y el 34.8% no tienen densitometría ósea en el expediente.
ConclusionesEstos resultados son un foco rojo que indica la necesidad de reforzar el papel del primer nivel de atención respecto al seguimiento vacunal y la necesidad de mejorar la educación al paciente con relación a la EII.
During the clinical course of inflammatory bowel disease, different causes can compromise kidney, liver, and bone marrow function and increase the risk for osteoporosis, infections, and neoplasias. The aim of the present study was to describe the follow-up of Mexican patients with inflammatory bowel disease in relation to their vaccination regimen, treatment-associated risks, and cancer screening.
Materials and methodsA retrospective cross-sectional study was conducted within the time frame of February and June 2017. One hundred patients that had a histopathologic diagnosis of inflammatory bowel disease were surveyed about their follow-up vaccination regimen, treatment-associated risks, and cancer screening. SPSS v24 software was employed for the statistical analysis.
ResultsOne hundred patients with inflammatory bowel disease were studied (90% with ulcerative colitis and 10% with Crohn's disease; 60% women, 40% men): 75% stated that they had no vaccination regimen. A total of 71.4% of the women had at least one Pap smear in their lives and 28.6% did not have them done annually. Twenty-four percent of the patients wore sun block daily. A total of 18.2% of the patients with more than a 10-year progression of ulcerative colitis had an annual colonoscopy. Yearly kidney function was registered in 57.1% of the patients, 92.9% had a yearly complete blood count, and 78.6% had yearly liver function tests. A total of 34.8% of patients had no bone densitometry in their case records.
ConclusionsThese results are a red flag suggesting the need to reinforce the role of the primary healthcare providers in relation to vaccination follow-up and the need to improve the education of the patient in relation to inflammatory bowel disease.
La colitis ulcerosa crónica idiopática (CUCI) y la enfermedad de Crohn (EC) representan los 2tipos principales de enfermedad inflamatoria intestinal (EII)1. Su etiología sigue siendo desconocida, sin embargo, se considera una enfermedad multifactorial, en la que las interacciones recíprocas entre la genética del huésped, los factores ambientales, la microbiota y las respuestas inmunitarias, que normalmente mediarían en la homeostasis de la mucosa, parecen desreguladas e inducen o perpetúan una inflamación crónica2,3. Los pacientes con diagnóstico de EII requieren el uso de fármacos que implican diversos riesgos, dentro de los cuales la primera línea de tratamiento son los 5-aminosalicilatos4,5. Además, en algún momento, el 80% de los pacientes requerirán tratamiento con corticosteroides, el 40% con tiopurinas y alrededor del 20% con fármacos biológicos. Es por eso por lo que, debido a los medicamentos que reciben y a factores intrínsecos de la enfermedad, los pacientes con EII tienen un riesgo aumentado de adquisición de infecciones6,7, de enfermedades prevenibles por vacunación8 y de desarrollo o recurrencia de cáncer9,10.
El perfil de seguridad de los aminosalicilatos, especialmente mesalazina, es similar al placebo; sin embargo, estos fármacos no están excentos de riesgos como nefrotoxicidad, nefritis intersticial o alergia11, por lo que se recomienda realizar un control anual de la función renal12. Con relación al uso de tiopurinas, existen algunos efectos adversos independientes de la dosis, ante los cuales solo podemos predecir la predisposición con estudios genéticos y evitar su uso en casos seleccionados, como el desarrollo de pancreatitis. Otros son dosis dependientes, como la mielotoxicidad y la toxicidad hepática, los cuales debemos vigilar mediante un recuento sanguíneo completo y pruebas de función hepática antes del tratamiento y con seguimiento durante dicho tratamiento13. Así mismo, el uso de tiopurinas incrementa el riesgo de infecciones oportunistas y malignidad14,15.
Uno de los riesgos más importantes que conlleva la EII, no solo por el uso de esteroides sino también por el efecto de la inflamación en el hueso, la malabsorción de calcio y vitamina D y otros factores como el bajo índice de masa corporal16, es la alteración en la densidad mineral ósea, cuya prevalencia oscila entre el 22 y el 77% para osteopenia y entre el 17 y el 41% para osteoporosis17. Además, otros riesgos que se pueden presentar con el uso de estos fármacos, aunque con menor frecuencia, son el glaucoma y las cataratas16. Finalmente, el tratamiento biológico conlleva, entre otras cosas, un riesgo incrementado de reactivación de tuberculosis latente, por lo que es necesario realizar prueba de tuberculina o ensayo de liberación de interferón-γ antes del tratamiento y anualmente durante él6.
De igual forma, el uso de este tipo de fármacos y factores intrínsecos de la EII incrementan el riesgo de cáncer de piel, por lo que se debe aconsejar a los pacientes que usen protector solar de amplio espectro18, así como el de cáncer de colon con relación a CUCI, por lo que se requiere un control colonoscópico anual a partir de los 8 años de evolución de la enfermedad19. Las mujeres, en particular, corren un mayor riesgo de resultados anormales de la prueba de Papanicolaou asociados con el virus del papiloma humano20 y de cáncer cervical, por lo que el seguimiento estrecho mediante citología cervical anual es particularmente importante21. Respecto a los riesgos infecciosos, algunos de ellos son prevenibles con vacunas16; sin embargo, parece que solo el 14% de los gastroenterólogos informa de manera adecuada sobre la vacunación de sus pacientes con EII para prevenir estas infecciones22.
No existen estudios que nos permitan conocer cómo se lleva el seguimiento de estos aspectos en los pacientes mexicanos con EII. Es por eso por lo que este estudio tiene como objetivo describir el seguimiento que llevan los pacientes mexicanos con EII de su esquema de vacunación, riesgos asociados a tratamiento y cáncer.
Material y métodosEstudio transversal y retrospectivo realizado entre febrero y junio de 2017. Se interrogó a 100 pacientes con diagnóstico definitivo de EII de la Clínica de EII del Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán. Otros datos clínicos, sociodemográficos y de laboratorio se recopilaron retrospectivamente a partir del expediente clínico para su posterior concentración y análisis en SPSS v. 24.
Durante la consulta de los pacientes que acuden de manera constante en la clínica de EII se les hizo una serie de preguntas. Se les preguntó si conservaban su cartilla de vacunación como un documento importante en casa; si se aplicaron o recuerdan haberse aplicado las siguientes vacunas y la fecha de aplicación: varicela, herpes zóster, triple viral, difteria y pertussis, tétanos, influenza, virus del papiloma humano, hepatitis A, hepatitis B, meningocócica, neumocócica; en el caso de las mujeres, si alguna vez se habían realizado una citometría cervical, la fecha de la última citología cervical, si conocen el resultado, la frecuencia con la que acuden a toma de citometría cervical (cada año, cada 2años, cada 3años, cada 5años, o con intervalos mayores a 5años); si asisten a consulta del servicio de dermatología (alguna vez en su vida, una vez al año o una vez cada 2años o ninguna); si utilizan protector solar todos los días; si tienen hábito tabáquico positivo o negativo, los años que habían fumado y el número de cigarros consumidos al día con el fin de calcular el índice tabáquico (calculado por el número de cigarrillos al día por el número de años de fumador, dividido entre 20).
Otros datos clínicos y sociodemográficos se recolectaron de los expedientes clínicos; estos incluían edad, sexo, diagnóstico histopatológico de CUCI o EC, patrón clínico de EC (inflamatorio, estenosante o fistulizante), así como la extensión de CUCI (proctitis, proctosigmoiditis, colitis izquierda o pancolitis), número de años de evolución, historia familiar de cáncer de colon, cervical y de piel; historia personal de diabetes, dislipidemias, cataratas y glaucoma; la presencia de manifestaciones extraintestinales como artritis, artralgias, sacroilitis, espondilitis anquilosante, pioderma gangrenoso, eritema nudoso, colangitis esclerosante primaria o uveítis, prueba de tuberculina o derivado proteico purificado (PPD) registrada en el expediente, así como la fecha y resultado (positivo >10mm o negativo <10mm) y, finalmente, si tenían seguimiento por el servicio de oftalmología o dermatología (al menos una nota en el expediente, una vez al año, una vez cada 2años o ninguna). También se preguntó por el registro de diagnóstico de cataratas, glaucoma o necrosis avascular de la cabeza del fémur como consecuencia del uso de esteroides.
Respecto al seguimiento de laboratorio, se registró el intervalo con el que se tiene información (una vez al año, una vez cada 3años, o cada 5 años o más) de la biometría hemática, función renal (uea, creatinina) y pruebas de funcionamiento hepático (bilirrubina total, directa e indirecta y transaminasas). Se registraron también los resultados de la densitometría de cadera y columna lumbar (clasificando el resultado como normal, osteopenia, osteoporosis o sin registro) así como la fecha e informe de la última colonoscopia y el intervalo con el que se tiene el registro (máximo cada año, máximo cada 3años, o cada 5 años o más, o sin registro), así como la historia o presencia de cáncer de colon registrada en el expediente.
Finalmente, se recolectaron datos sobre el tratamiento farmacológico de EII, tales como el tratamiento actual y los previos utilizados en su historia clínica (aminosalicilatos, esteroides, inmunomoduladores o agentes biológicos), incluyendo dosis promedio, años de tratamiento y cálculo de la dosis acumulada de cada uno (número de días de tratamiento multiplicada por la dosis promedio).
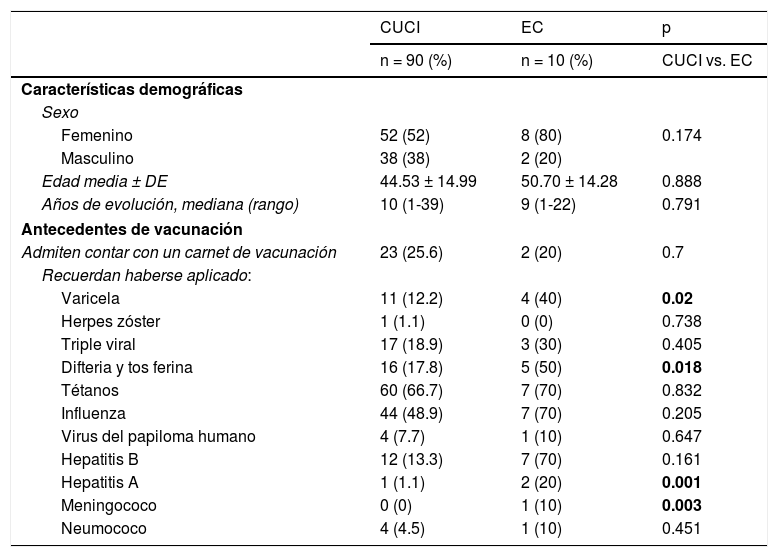
ResultadosSe interrogó a 100 pacientes con EII, de los cuales el 90% tenían CUCI y el 10% EC; el 60% eran mujeres y el 40%, hombres. Respecto al seguimiento del esquema de vacunación, destaca que el 75% de los pacientes negaron poseer un carnet de vacunación. Las características demográficas de la población y los antecedentes de vacunación se detallan en la tabla 1.
Características demográficas y recordatorio de seguimiento del esquema de vacunación de pacientes mexicanos con enfermedad inflamatoria intestinal
| CUCI | EC | p | |
|---|---|---|---|
| n = 90 (%) | n = 10 (%) | CUCI vs. EC | |
| Características demográficas | |||
| Sexo | |||
| Femenino | 52 (52) | 8 (80) | 0.174 |
| Masculino | 38 (38) | 2 (20) | |
| Edad media ± DE | 44.53 ± 14.99 | 50.70 ± 14.28 | 0.888 |
| Años de evolución, mediana (rango) | 10 (1-39) | 9 (1-22) | 0.791 |
| Antecedentes de vacunación | |||
| Admiten contar con un carnet de vacunación | 23 (25.6) | 2 (20) | 0.7 |
| Recuerdan haberse aplicado: | |||
| Varicela | 11 (12.2) | 4 (40) | 0.02 |
| Herpes zóster | 1 (1.1) | 0 (0) | 0.738 |
| Triple viral | 17 (18.9) | 3 (30) | 0.405 |
| Difteria y tos ferina | 16 (17.8) | 5 (50) | 0.018 |
| Tétanos | 60 (66.7) | 7 (70) | 0.832 |
| Influenza | 44 (48.9) | 7 (70) | 0.205 |
| Virus del papiloma humano | 4 (7.7) | 1 (10) | 0.647 |
| Hepatitis B | 12 (13.3) | 7 (70) | 0.161 |
| Hepatitis A | 1 (1.1) | 2 (20) | 0.001 |
| Meningococo | 0 (0) | 1 (10) | 0.003 |
| Neumococo | 4 (4.5) | 1 (10) | 0.451 |
En negrita, valores de p con de P es menor a 0.05 o sea con significancia estadística (p < 0.05).
Con relación a la vigilancia de los riesgos asociados al consumo de medicamentos que se mencionan en la tabla 2, el 84% tenían tratamiento con 5-aminosalicilatos; de ellos, el 57.1% tenía medición de pruebas de función renal anual, el 38.1% cada 3 años y el 4.8% cada 5 años o más; el 46% con esteroides. De estos, ningún paciente tenía cataratas, glaucoma ni necrosis avascular de la cabeza femoral, el 4.3% de ellos tenía al menos una nota al año del servicio de oftalmología. El 34.8% no tenían densitometría ósea en el expediente, el 15.2% tenían una cada año y el 32.6% una cada 5 años o más. El 28% tenía tratamiento con tiopurinas; de ellos, el 92.9% tenía al menos una biometría hemática anual, el 78.6% tenía pruebas de función hepática anuales. El 3% de los pacientes tenían tratamiento con biológico y todos tenían registro de PPD negativo.
Vigilancia de riesgos asociados al consumo de medicamentos en pacientes mexicanos con enfermedad inflamatoria intestinal
| 5-aminosalicilatos N = 84 (%) | Sin 5-aminosalicilatos N =15 (%) | p | |
|---|---|---|---|
| Intervalo PFR | 0.224 | ||
| Cada año | 48 (57.1) | 12 (80) | |
| Cada 3años | 32 (38.1) | 3 (20) | |
| Cada 5 años | 4 (4.8) | 0 (0) |
| Esteroides N = 46 (%) | Sin esteroides N = 54 (%) | p | |
|---|---|---|---|
| Seguimiento por Oftalmología | 0.082 | ||
| Nunca | 44 (95.7) | 46 (85.2) | |
| Una nota de Oftalmología | 2 (4.3) | 8 (14.8) | |
| Densitometría | 0.592 | ||
| Normal | 13 (43.3) | 13 (50) | |
| Osteopenia | 12 (40) | 11 (42.3) | |
| Osteoporosis | 5 (16.7) | 2 (7.7) | |
| Intervalo de densitometría | 0.223 | ||
| Nunca | 16 (34.8) | 28 (51.9) | |
| Cada año | 7 (15.2) | 7 (13) | |
| Cada 3años | 8 (17.4) | 5 (9.3) | |
| Cada 5 años | 15 (32.6) | 14 (25.9) | |
| Tiopurinas N = 28 (%) | Sin tiopurinas N = 72 (%) | p | |
|---|---|---|---|
| Intervalo de BH | 0.130 | ||
| Cada año | 26 (92.9) | 71 (98.6) | |
| Cada 3años | 2 (7.1) | 1 (1.4) | |
| Intervalo de PFH | 0.821 | ||
| Cada año | 22 (78.6) | 56 (77.8) | |
| Cada 3años | 6 (21.4) | 15 (20.8) | |
| Biológico N = 3 (%) | Sin biológico N = 97 (%) | p | |
|---|---|---|---|
| PPD | 3 (100) | 24 (24.7) | 0.735 |
BH: biometría hemática; PFH: pruebas de función hepática; PFR: pruebas de función renal; PPD: derivado proteico purificado.
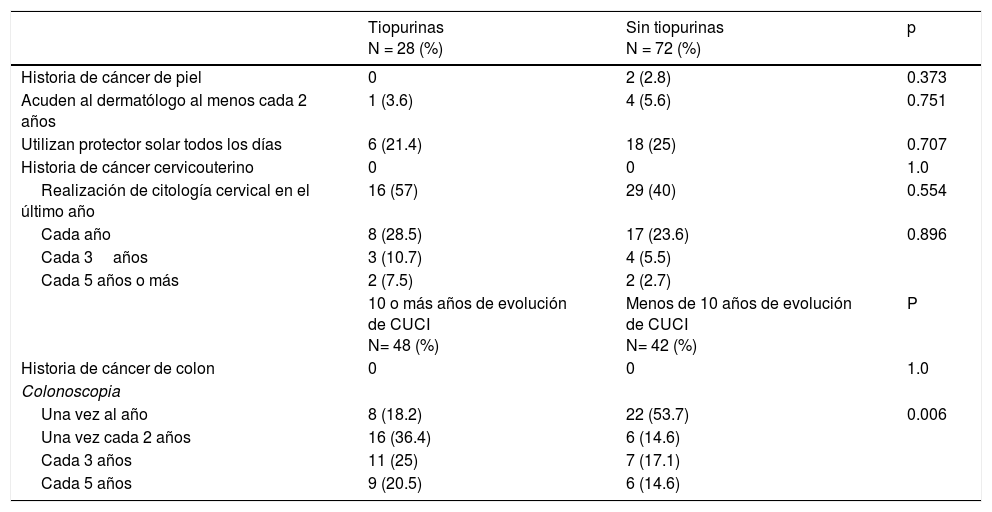
Respecto a la vigilancia y prevención del desarrollo de cáncer, detallados en la tabla 3, el 71.4% de las mujeres admitieron haberse realizado al menos una citometría cervical en su vida: el 28.6% de ellas no se la realizan de forma anual, el 14.3% lo hace cada 3 años. Sin embargo, ninguna de ellas reportó positividad para infección por virus del papiloma humano. El 17% de los pacientes respondieron que acuden al dermatólogo al menos una vez al año, el 24% reconocen utilizar protector solar diariamente, el 18% de los pacientes reportaron hábito tabáquico positivo. Al analizar estas variables con relación al consumo de tiopurinas, se encontró que el 3.6% de los pacientes que consumen estos medicamentos acuden al dermatólogo al menos cada 2 años y que el 21.4% utilizan protector solar todos los días. Así mismo, el 28.5% se realiza una citología cervical anual. El 18.2% de los pacientes con más de 10 años de evolución de la enfermedad tiene una colonoscopia anual; ninguno de ellos tenía antecedente personal de cáncer de colon.
Vigilancia del desarrollo de cáncer en pacientes mexicanos con enfermedad inflamatoria intestinal
| Tiopurinas N = 28 (%) | Sin tiopurinas N = 72 (%) | p | |
|---|---|---|---|
| Historia de cáncer de piel | 0 | 2 (2.8) | 0.373 |
| Acuden al dermatólogo al menos cada 2 años | 1 (3.6) | 4 (5.6) | 0.751 |
| Utilizan protector solar todos los días | 6 (21.4) | 18 (25) | 0.707 |
| Historia de cáncer cervicouterino | 0 | 0 | 1.0 |
| Realización de citología cervical en el último año | 16 (57) | 29 (40) | 0.554 |
| Cada año | 8 (28.5) | 17 (23.6) | 0.896 |
| Cada 3años | 3 (10.7) | 4 (5.5) | |
| Cada 5 años o más | 2 (7.5) | 2 (2.7) | |
| 10 o más años de evolución de CUCI N= 48 (%) | Menos de 10 años de evolución de CUCI N= 42 (%) | P | |
| Historia de cáncer de colon | 0 | 0 | 1.0 |
| Colonoscopia | |||
| Una vez al año | 8 (18.2) | 22 (53.7) | 0.006 |
| Una vez cada 2 años | 16 (36.4) | 6 (14.6) | |
| Cada 3 años | 11 (25) | 7 (17.1) | |
| Cada 5 años | 9 (20.5) | 6 (14.6) |
El 75% de los pacientes mexicanos con EII no poseen un carnet de vacunación, el 28.6% de las mujeres no se realizan una citología cervical anual; el 16.3% de los pacientes con más de 10 años de evolución de la enfermedad tiene una colonoscopia anual. Estos resultados indican la necesidad de reforzar el papel del primer nivel de atención y del médico gastroenterólogo con relación al seguimiento vacunal de la educación del paciente respecto a su enfermedad, con el fin de mejorar su compromiso con el seguimiento de la EII y facilitar así su camino a la remisión. Lo anterior no es responsabilidad única del médico subespecialista, ya que la vigilancia y seguimiento de estos aspectos se encuentran también al alcance del primer nivel de atención en salud16.
En este estudio, se observó que el 75% de los pacientes con EII niegan contar con un carnet de vacunación y que las vacunas que con mayor frecuencia refieren aplicarse son tétanos e influenza (66.7 y 70% respectivamente). Se sabe que las bajas tasas de vacunación se ven agravadas por la falta de conciencia sobre la vacunación del paciente con EII, lo cual coloca un riesgo sustancial en esta población para desarrollar infecciones, potenciado por el uso de los medicamentos propios de la pirámide terapéutica de esta enfermedad23.
Existen numerosas barreras que limitan el aumento de las tasas de vacunación, tales como la apatía general, los temores y preocupaciones sobre los efectos secundarios de la vacunación e incluso barreras logísticas como la ubicación de los centros proveedores y el tiempo de espera para ver a un médico24. Una de las limitantes en este estudio para conocer de manera objetiva el esquema de vacunación de cada paciente fue que la mayoría no contaba con él, por lo que resulta importante hacerles hincapié a los pacientes sobre la importancia de este documento25. Una de las estrategias para lograr que los pacientes adopten este interés es educarlos con información sencilla y práctica sobre las infecciones oportunistas que pueden adquirir, tales como varicela, herpes zóster, influenza, neumonía neumocócica, difteria y tétanos, hepatitis B, infecciones meningocócicas, para las que casos fatales han sido reportados en pacientes con EII25-29.
Respecto a la vigilancia de efectos adversos de los medicamentos utilizados, en este estudio parece que, en general, se tiene un buen seguimiento laboratorial con relación a la biometría hemática, pruebas de función hepática y renal anual. Sin embargo, los pacientes con EII también tienen un riesgo incrementado de desarrollar cáncer de piel, uveítis y epiescleritis, glaucoma o cataratas30-32, por lo que resaltamos la importancia de su seguimiento por parte de los servicios de dermatología y oftalmología, ya que en este estudio se observó que menos del 10% acuden a estos servicios.
En este estudio se observó que el 30% de los pacientes se han realizado una densitometría ósea en algún momento de la enfermedad, lo cual consideramos alarmante, ya que tienen un riesgo incrementado de desarrollar osteoporosis y osteopenia no solo debido al uso de esteroides, sino también al mayor riesgo que presentan de deficiencia de vitamina D y calcio, además de los factores intrínsecos de la enfermedad y la inflamación crónica que conllevan33,34. Por ello, proponemos a los gastroenterólogos que refuercen la realización de densitometría ósea de manera rutinaria, es decir, anual.
En casos específicos, en quienes está indicado el uso de terapia farmacológica con biológico, antes de iniciar el tratamiento se propone la realización de PPD para descartar tuberculosis latente35,36 y brindar antes del biológico el tratamiento farmacológico adecuado35,37. En esta muestra de pacientes con EII todos los pacientes con biológico tienen registro de PPD y tele de tórax, por lo que la vigilancia en este rubro es adecuada.
Por otra parte, en este estudio se reporta que el 81% de las mujeres se realiza citología cervical de manera anual; sin embargo, el 19% restante que no lo hace es, sin duda, un área de oportunidad y mejora.
En nuestro estudio se observó que únicamente el 18.2% de los pacientes con más de 10 años de evolución de CUCI se realizan una colonoscopia anual para vigilar la displasia. La importancia de este dato radica en el riesgo incrementado de cáncer colorrectal que tiene este grupo de pacientes. El cáncer es la segunda causa más común de muerte en pacientes con EII, aunque las tasas de cáncer colorrectal han ido disminuyendo. Se recomienda que los pacientes con EII se haga una colonoscopia de vigilancia 8-10 años después del inicio de los síntomas. Las colonoscopias de vigilancia deben realizarse a intervalos de 1 a 3 años, en función de si el riesgo es bajo, intermedio o alto para el desarrollo de cáncer colorrectal. La colonoscopia debe ser realizada cuando los pacientes están en remisión clínica y la vigilancia debe ser anual en pacientes con enfermedad activa persistente a nivel endoscópico, con antecedentes de displasia, con antecedentes familiares de cáncer de colon en un pariente de primer grado o con colangitis esclerosante primaria38-40. Es por eso por lo que proponemos a los médicos que atienden a pacientes con CUCI que refuercen estas medidas.
Por último, es importante recalcar el papel que tiene cada nivel de atención respecto a la EII, así como la responsabilidad de cada paciente para el cumplimiento de las recomendaciones que se le brindan para el seguimiento y vigilancia de su enfermedad, y la vigilancia de las comorbilidades que puede presentar durante el curso clínico6. Este estudio resalta la importancia de reforzar la atención en los diferentes niveles para cumplir con el papel con el que cuenta cada uno con relación a la vigilancia y seguimiento de todos los pacientes, particularmente los pacientes con EII que están inmunocomprometidos. En cada uno de los pacientes se debe obtener una historia clínica completa, en la que se profundice en los antecedentes heredofamiliares, sobre todo, en antecedentes de cáncer de primera línea, en la evaluación del esquema de vacunación de manera objetiva con cartilla y en llevar un adecuado seguimiento y vigilancia de los efectos adversos de medicamentos y riesgos propios de la enfermedad, así como en un manejo multidisciplinario por parte de dermatología y oftalmología6,16.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciamientoLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades, sin ánimo de lucro.
Conflicto de interesesEl Dr. Jesús Kazuo Yamamoto Furusho es conferencista, líder de opinión y miembro de los comités de advisory board para los laboratorios Abbvie, Ferring, Hospira, Janssen, Pfizer y Takeda a nivel nacional e internacional. Ha sido o es conferencista para los laboratorios Almirall, Danone, Farmasa, Grunenthal y UCB. Ha sido o es investigador principal en proyectos a nivel mundial con los laboratorios Abbvie, Allergan, Bristol, Ferring, Pfizer, Roche, Shire y Takeda. Actualmente es presidente de la Pan American Crohn's and Colitis Organisation (PANCCO).
Los autores A. Sarmiento-Aguilar, N.N. Parra-Holguín, K.E. Bozada-Gutiérrez declaran no tener ningún conflicto de intereses.