La infección por Helicobacter pylori (H. pylori) representa el factor etiológico más importante en numerosas enfermedades gastroduodenales. A pesar de haberse utilizado múltiples esquemas antibióticos para modificar su morbimortalidad asociada, la prevalencia de esta infección bacteriana continúa siendo desproporcionadamente alta en todo el mundo, debido principalmente a la resistencia antibiótica. A los efectos de evaluar la eficacia no inferior y la seguridad de 2regímenes de triple terapia durante 10 días para la erradicación de H. pylori comparamos claritromicina 500mg, lansoprazol 30mg y amoxicilina 1g, 2 veces al día (terapia triple estándar o CLA, grupo 1) vs. pantoprazol 80mg, levofloxacina 500mg y 500mg de azitromicina, 1 vez al día (PLA, grupo 2). Los 2regímenes fueron comparados en pacientes previamente no tratados.
Material y métodosEntre junio del 2012 y marzo del 2014 se llevó a cabo un estudio abierto de fase iiib aleatorizado y de no inferioridad que comparó CLA versus PLA en un periodo de 10 días. La erradicación se verificó con pruebas de aliento con 13C-urea. Las biopsias gástricas se analizaron para resistencia a claritromicina por hibridación fluorescente in situ, anterior a la administración de cualquier antibiótico. Los resultados de eficacia y seguridad fueron analizados siguiendo la metodología de no inferioridad.
ResultadosDe los 227 sujetos positivos a H. pylori que fueron aleatorizados, finalmente se analizaron 194 por protocolo solamente. La tasa de erradicación del grupo 2 fue del 63%, no inferior a la tasa de erradicación del grupo 1 del 58.5% (límite superior IC 95%=0.11608; margen de no inferioridad=0.1200). La resistencia a la claritromicina evaluada fue del 28.2%. Los eventos adversos fueron significativamente mayores en el grupo 1 que en el grupo 2 (86% vs. 65.4%, p=0.001).
ConclusionesLa erradicación de H. pylori en primera línea con terapia combinada de pantoprazol/levofloxacina/azitromicina resulta tan efectiva como con la terapia triple estándar, aunque con mejor tolerabilidad y una dosificación más fácil. La resistencia a la claritromicina debe considerarse en los tratamientos de erradicación del H. pylori.
ClinicalTrials.gov identificación: NCT02726269.
Helicobacter pylori (H. pylori) infection remains the leading cause of several gastroduodenal diseases. Despite the fact that multiple antibiotic regimens have been used to change its associated morbidity and mortality, the prevalence of this bacterial infection continues to be disproportionately high worldwide, mainly due to antibiotic resistance. To assess the noninferiority efficacy and safety of 210-day triple regimens on H. pylori eradication, we evaluated clarithromycin 500mg, lansoprazole 30mg, and amoxicillin 1g, all bid (standard triple therapy or CLA, Group 1) vs. pantoprazole 80mg, levofloxacin 500mg and azithromycin 500mg, all od (PLA, Group 2). Both regimens were compared in treatment-naïve patients.
Materials and methodsAn open label phase IIIb randomized and noninferiority trial comparing CLA vs. PLA was carried out for a 10-day period, within the time frame of June 2012 and March 2014. Eradication was verified with 13C-urea breath testing. Gastric biopsies were tested for fluorescence in situ hybridization (FISH)-clarithromycin resistance prior to any antibiotic administration. Efficacy and safety results were analyzed according to the noninferiority methodological approach.
ResultsFrom the 227 H. pylori positive subjects that were randomized, 194 were finally analyzed as per-protocol. The group 2 eradication rate was 63% and was noninferior to the group 1 eradication rate of 58.5% (upper limit 95% CI: 0.11608; below the noninferiority margin: 0.1200). FISH clarithromycin-resistance was found in 28.2% of the cases. Adverse events, all minor and self-limited, were significantly higher in group 1 than in group 2 (86 vs. 65.4%; p=0.001).
ConclusionsFirst-line H. pylori eradication with pantoprazole/levofloxacin/azithromycin combination therapy is as effective as the standard triple therapy, with better tolerability and easier dosing. Clarithromycin resistance should be considered when selecting antibiotics in Helicobacter pylori eradication treatments.
ClinicalTrials.gov identifier NCT02726269.
La infección gástrica con Helicobacter pylori (H. pylori) es la causa principal de la gastritis, la úlcera duodenal y el cáncer gástrico. En México, la media nacional de seroprevalencia de H. pylori reportada en la población general es del 66%1,2. Además, la tasa de mortalidad de cáncer gástrico era de 4.5 por cada 100,000 en 1980 y se ha incrementado a 6.5 por cada 100,000 en un periodo de 10 años2.
Las recomendaciones de esquemas de erradicación de H. pylori son ampliamente disponibles3. Los mejores resultados han sido obtenidos con la llamada terapia triple, la cual incluye 2antibióticos y un inhibidor de bomba de protones (IBP). En México la combinación de claritromicina, amoxicilina y un IBP ha sido la opción recomendada, ya que la resistencia al metronidazol está entre las más altas del mundo (hasta 80%)4. En un estudio reciente que comparó esquemas secuenciales y tradicionales en 7 países latinoamericanos (Chile, Colombia, Costa Rica, Honduras, Nicaragua y México [2 sitios]), las tasas de erradicación fueron del 66 al 77% para los sujetos mexicanos5. El Consenso de Maastritch IV estipula que la combinación de antibióticos debe ser seleccionada de acuerdo con la resistencia identificada3. Sin embargo, en México hay poca información actual respecto a la resistencia identificada, solamente unos cuantos estudios recientes sugieren que la resistencia a la claritromicina puede estar a la alza6. Sin embargo, esos estudios enfatizan que la resistencia del H. pylori a la claritromicina está entre el 17.8 y el 24%, según las series de casos analizadas4,7. Así, es necesaria la búsqueda de alternativas terapéuticas para mejorar esos inaceptables niveles de resistencia al antibiótico, los cuales guardan una alta correlación con importantes fallos terapéuticos en la erradicación de H. pylori.
La levofloxacina es una quinolona de amplio espectro que ha sido utilizada como tratamiento de segunda línea para erradicar H. pylori y en pacientes con alergia a la penicilina3,8. Los datos indican que la levofloxacina en conjunto con un macrólido podría ser tan efectiva como la tradicional terapia triple. Los estudios clínicos realizados con terapias triples basadas en quinolonas han reportado tasas de erradicación del 80 al 90.4% después de 10 días, dependiendo de la terapia evaluada9. Aunque es cierto que también hay una tendencia a la alza en la resistencia a las quinolonas en Latinoamérica, esa tendencia no ha llegado aún al nivel de resistencia a los macrólidos, especialmente a la claritromicina10,11. En consecuencia, los esquemas basados en quinolonas siguen representando un escenario prometedor para la erradicación de H. pylori en México12.
Los objetivos del presente estudio fueron comparar el esquema triple con el esquema alternativo de levofloxacina+azitromicina+un IBP y determinar la frecuencia de resistencia a la claritromicina en la población de zonas metropolitanas en México.
Materiales y métodosSujetosEl presente estudio de fase iiib fue de no inferioridad, controlado, prospectivo, abierto, aleatorizado y de grupo paralelo. Se llevó a cabo entre junio del 2012 y enero del 2014 en 4clínicas en 2ciudades ubicadas en el centro del país: la Ciudad de México y la ciudad de Toluca.
Se incluyó a 230 pacientes previamente no tratados, de un rango de edad de 18 a 65 años, con infección de H. pylori demostrada por medio de biopsia endoscópica. Los pacientes firmaron las cartas de consentimiento informado. Los criterios de exclusión incluyeron comorbilidad severa, embarazo, lactancia y alergia a los fármacos del estudio. Se aleatorizó a los pacientes por medio de un procedimiento de bloques permutados para asegurar el equilibrio en el número de pacientes asignados a cada sitio clínico. El procedimiento utilizó números aleatorios generados por ordenador y fue realizado por la organización de investigación clínica (OIC) responsable de la realización del estudio1. Dado que los pacientes fueron reclutados de forma competitiva, se asignaron tantos bloques como fueron necesarios a cada sitio clínico hasta que el tamaño de muestra previamente calculado fue alcanzado.
Régimen de tratamientoLos pacientes fueron asignados aleatoriamente a uno de 2grupos: el grupo 1 recibió 2veces al día claritromicina 500mg, lansoprazol 30mg y amoxicilina 1g (Pylopac®, Medix SA de CV, México); el grupo 2 recibió una vez al día pantoprazol 80mg (Zoltum®, Laboratorio Monte Verde SA, Argentina), levofloxacina 500mg (Laboratorios Asofarma de México SA de CV, México) y azitromicina 500mg (Truxa®, Laboratorios Monte Verde SA, Argentina). Ambos grupos recibieron el tratamiento durante 10 días. Los antibióticos fueron prescritos después de las comidas, mientras que el IBP fue tomado en condiciones de ayuno. No se permitió otro tipo de medicamento hasta el final del tratamiento. Los medicamentos fueron amablemente proporcionados por ASOFARMA de México.
EvaluacionesSe obtuvieron muestras de sangre para el análisis de seguridad en el laboratorio central después de haber obtenido el consentimiento informado de los pacientes y antes del tratamiento. Los pacientes fueron evaluados utilizando la prueba de aliento con 13C-urea (13C-UBT por sus siglas en inglés) 4semanas después del tratamiento de erradicación de H. pylori. Se tomó una muestra de sangre adicional para comparar con los resultados iniciales. La erradicación de H. pylori fue definida como una 13C-UBT negativa.
La adherencia al tratamiento y los eventos adversos (EA) relacionados con el tratamiento fueron evaluados al final del tratamiento. Para evaluar la adherencia con el tratamiento asignado todos los pacientes recibieron un diario impreso para registrar las tomas de medicamento (fecha, hora de administración y frecuencia diaria) y los EA. Los EA fueron clasificados como ligeros si no interfirieron con las actividades diarias, moderados si interfirieron con las actividades diarias en alguna medida, y severos si se requirió de hospitalización o de la suspensión del tratamiento, o si el EA resultó en la muerte del paciente. Debido a que la población objetivo para el análisis de eficacia primaria fue por protocolo, solo aquellos pacientes que según los datos reportados en el diario impreso cumplieron con el 100% de la administración del tratamiento asignado fueron considerados válidos para dicho análisis.
Evaluación histológica y microbiológicaTodas las biopsias fueron revisadas por un patólogo central (LB). Las biopsias endoscópicas fueron inmediatamente fijadas en 10% buffer formalina, impregnadas en parafina, seccionadas (rebanadas de 4mm de grosor) y deshidratadas en una serie de concentraciones gradualmente mayores de etanol/xileno. Cada sección fue teñida con hematoxilina y eosina (H&E). El diagnóstico de gastritis fue establecido de acuerdo con el sistema Sydney actualizado13.
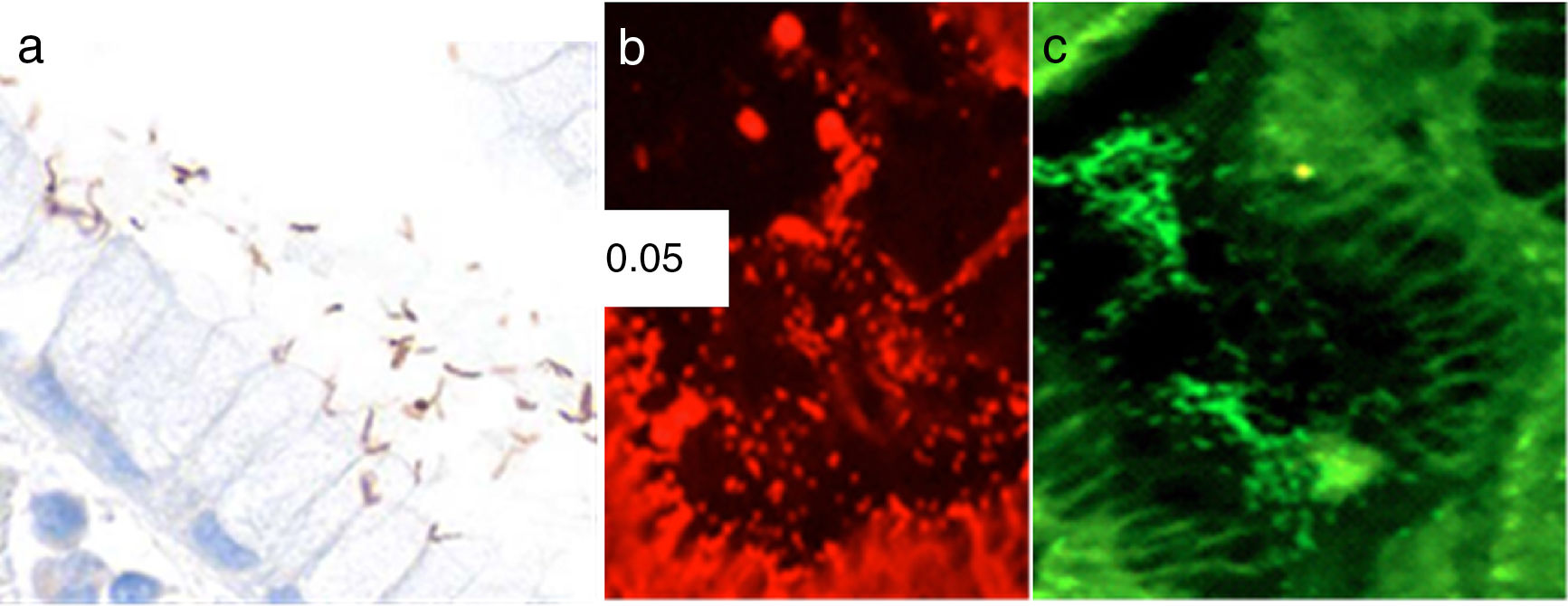
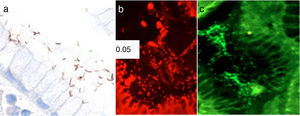
Identificación de H. pylori y determinación de la resistencia al macrólido utilizando hibridación fluorescente in situLa identificación de H. pylori fue realizada con tinciones de H&E. En aquellos casos con características morfológicas indicativas de una infección en los que no fue posible la identificación del germen con las tinciones de H&E se realizó inmunohistoquímica para H. pylori (anti-Helicobacter pylori; 1:500; Thermo Scientific, Fremont, CA, EE. UU.). La hibridación fluorescente in situ (FISH) se realizó de acuerdo con un protocolo previamente descrito14. Las secciones de tejido de 4mm, fijadas en formalina e impregnadas en parafina, fueron colocadas en láminas cubiertas con poli-L-lisina y brevemente procesadas con hexano y etanol. La hibridación fue realizada utilizando BACTfish H pylori combi kit (Izinta Trading Co. Ltd., Hungría). La sonda para identificar H. pylori (Hpy 1) (5’CACACCTGACTGACTATCCCG-3’) fue etiquetada con isotiocianato de fluoresceína (FITC por sus siglas en inglés), el cual proporciona una señal verde. Y las sondas para detectar las 3mutaciones más prevalentes de resistencia a la claritromicina ClaR1 (A2143G) 5’CGGGGTCTTCCCGTCTt-3’, ClaR2 (A2144G) 5’CGGGGCTCTCCGTCTT-3’ y ClaR3 (A21443C) 5-CGGGGTCTTGCCGTCTT-3’ fueron etiquetadas con fluorocromo rojo (Cy3) (fig. 1). Posterior a la hibridación de 90 min a 46° C, las secciones fueron lavadas mediante baño con buffer en 2ocasiones a 46° C durante 15 min14. Las secciones secadas con aire fueron teñidas con 4’, 6’ diamino-2-fenilindol (DAPI por sus siglas en inglés). Las láminas fueron evaluadas utilizando un microscopio de fluorescencia Nikon Eclipse 80i. Las imágenes fueron tomadas utilizando una cámara Nikon DS-Fi1 y procesadas con el software NIS-Elements 2.1 (Nikon Corporation, Shinagawa Intercity Tower, Tokio, Japón).
Fotomicrografías de mucosa gástrica. a) Identificación de H. pylori a través de immunohistoquímica. b) FISH positiva (cepa H. pylori resistente): presencia de resistencia a mutaciones de claritromicina (puntos rojos). c) FISH negativa (cepa H. pylori sensible): no resistencia a las mutaciones de claritromicina.
De acuerdo con los lineamientos de estadística actuales sobre el análisis estadístico en estudios de no inferioridad, son más deseables los análisis sin intención de tratar (non-ITT por sus siglas en inglés), como el abordaje en tratamiento o por protocolo (PP), que los análisis por intención de tratar, dado que en los estudios de no inferioridad, un análisis por intención de tratar a menudo resultará en un incremento del riesgo de concluir no inferioridad (error tipo i)15. En consecuencia, el análisis de eficacia estuvo basado en la tasa de erradicación de H. pylori en sujetos que terminaron el tratamiento como PP. El abordaje por intención de tratar modificado (mITT), en el cual los pacientes recibieron al menos una dosis del tratamiento asignado y completaron el 13C-UBT, fue llevado a cabo por razones de mayor soporte y para el análisis de seguridad.
Cálculo del margen de no inferioridadConsiderando un abordaje de no inferioridad16, se definió un margen de no inferioridad (δ) preestablecido para el efecto del tratamiento en el resultado de eficacia primaria. Bochenek et al.17 compararon la eficacia de 2regímenes de tratamiento triple versus 2regímenes de terapia dual para erradicación de H. pylori en pacientes con úlcera péptica de corto plazo (7 días). Se obtuvo un porcentaje de erradicación del 65% para una de las combinaciones triples (pantoprazol+amoxicilina+claritromicina o PAC) y el 43% para una de las combinaciones dobles (pantoprazol+claritromicina o PC). Dado que fueron diseños de superioridad, los resultados fueron analizados en poblaciones por intención de tratar. Los intervalos de confianza del 95% (IC 95%) fueron 56-73% y 36-53% para PAC y PC, respectivamente.
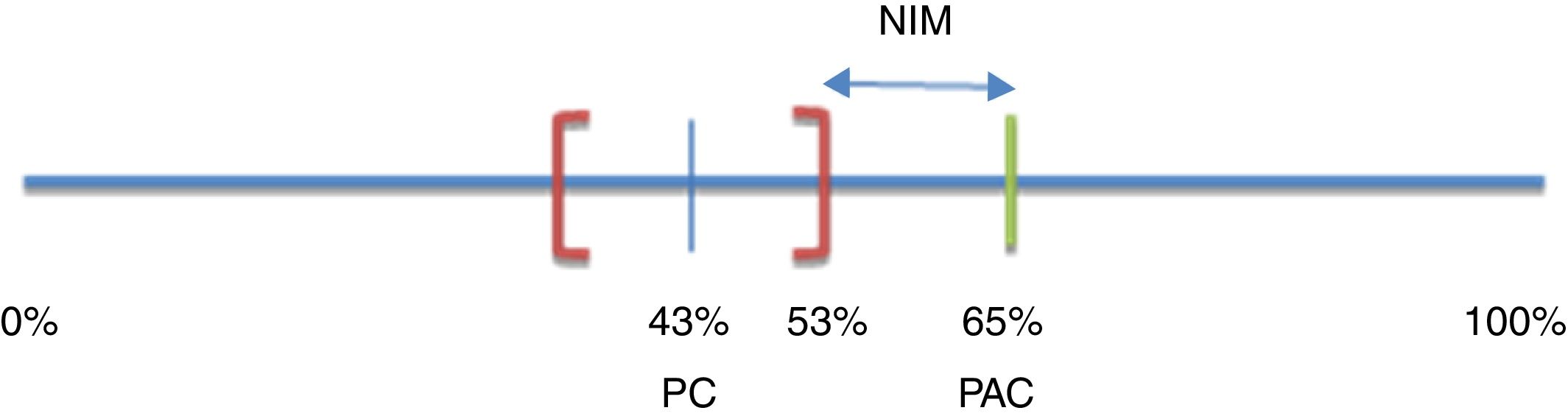
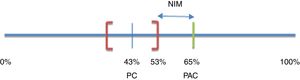
El margen de no inferioridad (δ) para el presente estudio fue estimado considerando que cualquier tratamiento con 3ingredientes activos (PAC) debería ser superior a cualquier otro tratamiento con solo 2ingredientes activos (PC). Así, se esperó que el porcentaje de erradicación de H. pylori con PAC fuera mayor que el límite superior del IC del 95% calculado para la tasa de erradicación observada con PC (53%). La disminución máxima de eficacia aceptable con relación a lo observado con el tratamiento triple (PAC) fue entonces definida como δ. En consecuencia, δ fue la diferencia entre el porcentaje de erradicación de H. pylori logrado con el tratamiento triple (PAC) y el límite superior del IC calculado para el tratamiento doble (PC): δ=65-53%=12%15,16 (fig. 2).
Margen de eficacia de no inferioridad.
NIM: margen de no inferioridad; PAC: pantoprazol + amoxicillina + claritromicina; PC: pantoprazol + claritromicina.
Basado en Bochenek et al.17.
Bajo esta premisa, en nuestro estudio, el grupo 2 (PLA) fue considerado no inferior al grupo 1 (CLA) cuando el límite superior del IC del 95% para la diferencia entre la tasa de erradicación entre ambos grupos fue más bajo que el margen de no inferioridad preestablecido (δ=0.12 o 12%).
Los pacientes a quienes no se les pudo dar seguimiento o quienes no completaron el tratamiento debido a EA severos fueron considerados fallas del tratamiento y fueron excluidos del análisis por protocolo. Las variables continuas fueron descritas utilizando la media y la desviación estándar. Las pruebas de la chi al cuadrado y t de Student fueron utilizadas para comparar las diferencias entre los 2grupos respecto a la línea base y los EA; un valor de p<0.05 fue considerado estadísticamente significativo. La prueba de la t de Student por pares fue utilizada para comparar los resultados bioquímicos para el análisis de seguridad. Se utilizó el programa de IBM SPSS 21 para realizar el análisis estadístico.
El estudio fue aprobado por un comité de ética independiente2 y por la COFEPRIS (autoridad de Salud de México) y fue realizado de acuerdo con la Declaración de Helsinki para la protección de sujetos humanos, en adherencia a los lineamientos de la buena práctica clínica.
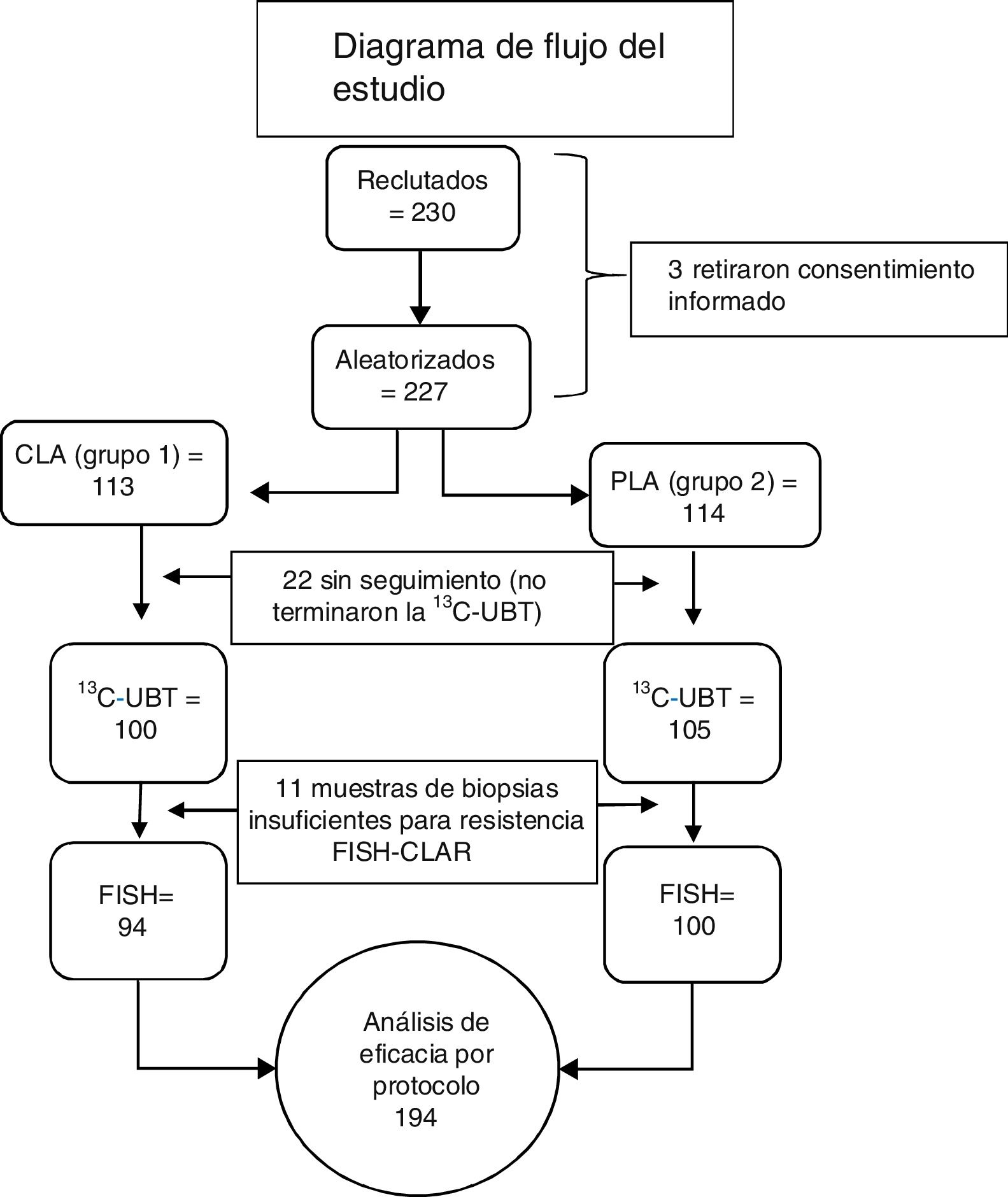
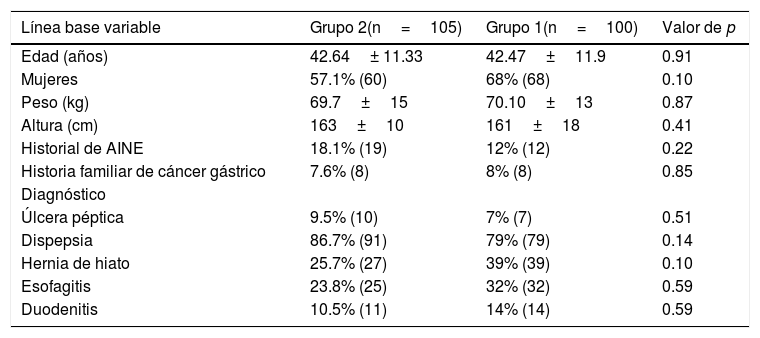
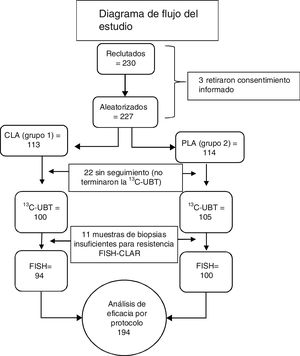
ResultadosCaracterísticas de grupoEl estudio incluyó a 230 sujetos. Tres sujetos retiraron su consentimiento informado antes del comienzo del tratamiento. Veintidós de los 227 sujetos aleatorizados fueron bajas en el seguimiento y no completaron la 13C-UBT. Dado que las biopsias de 11 sujetos no proporcionaron suficiente tejido para realizar la prueba de resistencia a la claritromicina, de los 205 pacientes elegibles, solo 194 sujetos fueron incluidos en el análisis de eficacia primaria PP (fig. 3). No se encontraron diferencias en sexo, edad, peso, altura o diagnóstico endoscópico entre los 205 participantes elegibles (tabla 1). La ingesta de fármacos antiinflamatorios esteroideos y una historia familiar de cáncer gástrico no mostraron diferencia significativa. La principal comorbilidad fue la enfermedad cardiovascular (3.9%), seguida de osteoartropatía degenerativa (2%). Un sujeto presentaba diabetes mellitus tipo 2, otro fue positivo para el virus de inmunodeficiencia humana y uno más tenía cirrosis compensada (0.5% cada uno). Para propósitos del análisis PP(eficacia primaria de no inferioridad), solo aquellos pacientes que cursaron todos los procedimientos incluidos en el protocolo (población por protocolo, 194 sujetos con 100% de adherencia) fueron considerados.
Características demográficas de los sujetos por grupo de tratamiento
| Línea base variable | Grupo 2(n=105) | Grupo 1(n=100) | Valor de p |
|---|---|---|---|
| Edad (años) | 42.64± 11.33 | 42.47±11.9 | 0.91 |
| Mujeres | 57.1% (60) | 68% (68) | 0.10 |
| Peso (kg) | 69.7±15 | 70.10±13 | 0.87 |
| Altura (cm) | 163±10 | 161±18 | 0.41 |
| Historial de AINE | 18.1% (19) | 12% (12) | 0.22 |
| Historia familiar de cáncer gástrico | 7.6% (8) | 8% (8) | 0.85 |
| Diagnóstico | |||
| Úlcera péptica | 9.5% (10) | 7% (7) | 0.51 |
| Dispepsia | 86.7% (91) | 79% (79) | 0.14 |
| Hernia de hiato | 25.7% (27) | 39% (39) | 0.10 |
| Esofagitis | 23.8% (25) | 32% (32) | 0.59 |
| Duodenitis | 10.5% (11) | 14% (14) | 0.59 |
AINE: antiinflamatorios no esteroideos.
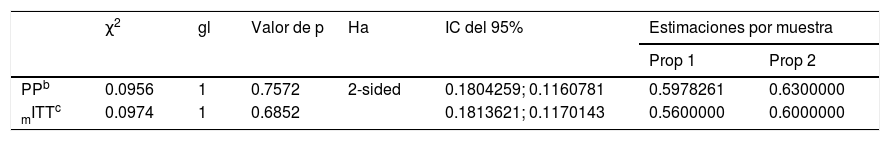
La tasa de erradicación fue del 59% (55/94) en el grupo 1 y el 63% (63/100) en el grupo 2. En la población PP (n=194), el límite superior del IC del 95% para la diferencia en las tasas de erradicación entre el grupo 1 y el grupo 2 fue más bajo que el margen de no inferioridad preestablecido de 0.12 (IC del 95%: –0.18043, 0.11608; p <0.0001). Así, la tasa de éxito de erradicación de H. pylori con ambos tratamientos resultó estadísticamente comparable, apoyando la no inferioridad del grupo PLA con relación a la terapia tradicional. Tanto el análisis primario llevado a cabo en la población PP como el análisis secundario realizado en la población por intención de tratar modificada apoyan la misma conclusión de no inferioridad entre los tratamientos probados (tabla 2).
Prueba de 2muestras para igualdad de proporciones con corrección de continuidada
| χ2 | gl | Valor de p | Ha | IC del 95% | Estimaciones por muestra | ||
|---|---|---|---|---|---|---|---|
| Prop 1 | Prop 2 | ||||||
| PPb | 0.0956 | 1 | 0.7572 | 2-sided | 0.1804259; 0.1160781 | 0.5978261 | 0.6300000 |
| mITTc | 0.0974 | 1 | 0.6852 | 0.1813621; 0.1170143 | 0.5600000 | 0.6000000 | |
gl: grados de libertad; IC: intervalo de confianza; mITT: población modificada por intención de tratar; PP: población por protocolo.
Se encontró resistencia a la claritromicina en el 28.9% (56/194) de los sujetos de la población PP (tabla 3), distribuida aleatoriamente entre ambos grupos y en todos los sitios clínicos. En un subanálisis por sitio (tabla 3) se mostró que la resistencia al H. pylori era mayor en Toluca que en la Ciudad de México: 50% (19/37) vs. 23.5% (37/157), respectivamente (p=0.002 en la comparación global). Estos resultados indican que pueden existir diferencias regionales en el patrón de resistencia dentro del país.
Resistencia a la claritromicina diagnosticada con FISH (población PP=194)
| Sitio | Pacientes reclutados | FISH (+) | % CLAR | Valor de p |
|---|---|---|---|---|
| Toluca (1) | 37 | 19 | 50% | |
| Ciudad de México (3) | 157 | 37 | 23.5% | 0.002a |
| Total | 194 | 56 | 28.9% |
Toluca: 1 sitio; Ciudad de México: 3 sitios.
CLAR: resistencia a la claritromicina; FISH: hibridación fluorescente in situ.
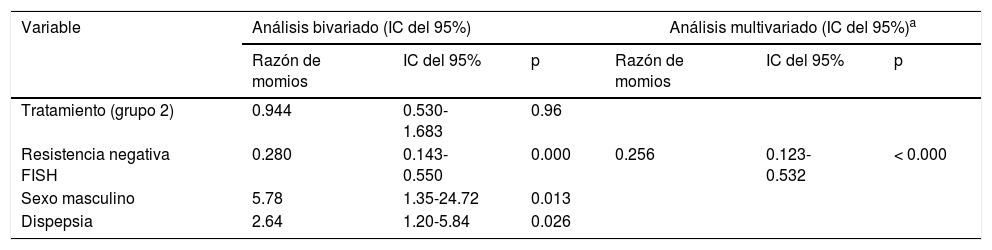
La tabla 4 muestra los resultados del análisis de regresión bivariado y multivariado para identificar los factores de influencia independientes que ayudan a una tasa de erradicación de H. pylori exitosa, con la persistencia del H. pylori como la variable dependiente. Al comparar sujetos con o sin H. pylori persistente, el análisis bivariado mostró que las probabilidades de tener una tasa de erradicación de H. pylori exitosa estaba bajo la influencia de variables como sexo, dispepsia y ausencia de resistencia a la claritromicina. Sin embargo, en el análisis multivariado, solo la ausencia de resistencia a la claritromicina estuvo asociada significativamente con un resultado de tratamiento exitoso.
Razón de momios estimada por análisis de regresión logística en la población por protocolo (= 194) Comparación de sujetos con o sin H. pylori persistente
| Variable | Análisis bivariado (IC del 95%) | Análisis multivariado (IC del 95%)a | ||||
|---|---|---|---|---|---|---|
| Razón de momios | IC del 95% | p | Razón de momios | IC del 95% | p | |
| Tratamiento (grupo 2) | 0.944 | 0.530-1.683 | 0.96 | |||
| Resistencia negativa FISH | 0.280 | 0.143-0.550 | 0.000 | 0.256 | 0.123-0.532 | < 0.000 |
| Sexo masculino | 5.78 | 1.35-24.72 | 0.013 | |||
| Dispepsia | 2.64 | 1.20-5.84 | 0.026 | |||
Finalmente, se obtuvieron resultados positivos con 13C-UBT en pacientes con resistencia negativa FISH en 17.2% de los sujetos, independientemente del tratamiento que recibieron, lo cual podría indicar resistencia a la amoxicilina o levofloxacina.
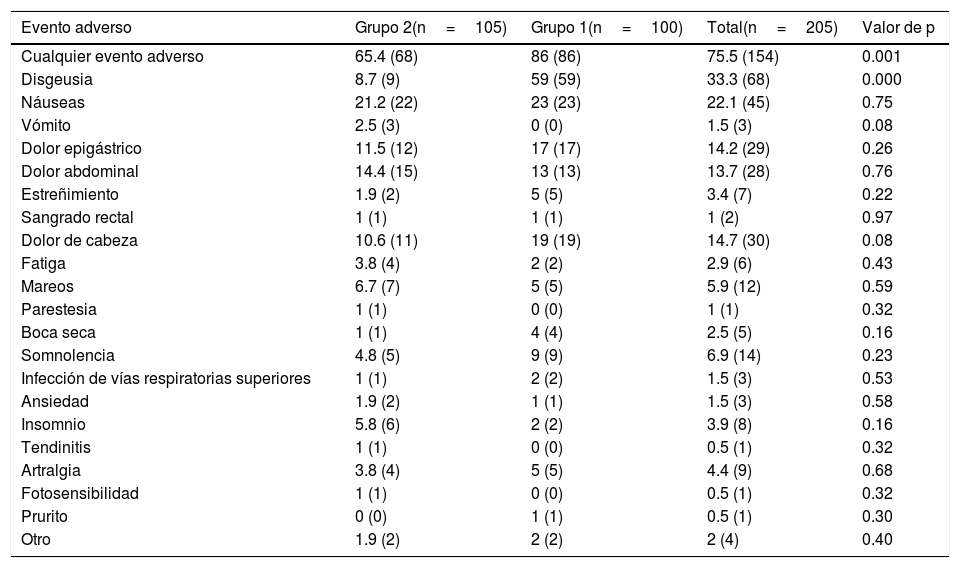
SeguridadLos 205 sujetos aleatorizados a tratamiento fueron incluidos en el análisis de seguridad (tabla 5). Respecto a los EA, en el grupo se reportaron en un 86% en el grupo 1 y en 65.4% en el grupo 2 (p=0.001). El EA más frecuente fue disgeusia (33.3%), seguido de heces blandas (24.3%), náuseas (22.1%), dolor de cabeza (14.7%), dolor epigástrico (14.2%), incomodidad abdominal (13.7%), somnolencia (6.9%), mareo (5.9%), artralgia (3.9%) e insomnio (3.9%). La disgeusia fue reportada por el 59% de los sujetos en el grupo 1 y por solo 8.7% en el grupo 2 (p=<0.000). No existió diferencia entre los grupos respecto a la frecuencia de cualquier otro EA. No existieron diferencias en los parámetros bioquímicos evaluados antes y después de cada tratamiento, ni entre los tratamientos asignados (p=0.89).
Eventos adversos por tratamiento
| Evento adverso | Grupo 2(n=105) | Grupo 1(n=100) | Total(n=205) | Valor de p |
|---|---|---|---|---|
| Cualquier evento adverso | 65.4 (68) | 86 (86) | 75.5 (154) | 0.001 |
| Disgeusia | 8.7 (9) | 59 (59) | 33.3 (68) | 0.000 |
| Náuseas | 21.2 (22) | 23 (23) | 22.1 (45) | 0.75 |
| Vómito | 2.5 (3) | 0 (0) | 1.5 (3) | 0.08 |
| Dolor epigástrico | 11.5 (12) | 17 (17) | 14.2 (29) | 0.26 |
| Dolor abdominal | 14.4 (15) | 13 (13) | 13.7 (28) | 0.76 |
| Estreñimiento | 1.9 (2) | 5 (5) | 3.4 (7) | 0.22 |
| Sangrado rectal | 1 (1) | 1 (1) | 1 (2) | 0.97 |
| Dolor de cabeza | 10.6 (11) | 19 (19) | 14.7 (30) | 0.08 |
| Fatiga | 3.8 (4) | 2 (2) | 2.9 (6) | 0.43 |
| Mareos | 6.7 (7) | 5 (5) | 5.9 (12) | 0.59 |
| Parestesia | 1 (1) | 0 (0) | 1 (1) | 0.32 |
| Boca seca | 1 (1) | 4 (4) | 2.5 (5) | 0.16 |
| Somnolencia | 4.8 (5) | 9 (9) | 6.9 (14) | 0.23 |
| Infección de vías respiratorias superiores | 1 (1) | 2 (2) | 1.5 (3) | 0.53 |
| Ansiedad | 1.9 (2) | 1 (1) | 1.5 (3) | 0.58 |
| Insomnio | 5.8 (6) | 2 (2) | 3.9 (8) | 0.16 |
| Tendinitis | 1 (1) | 0 (0) | 0.5 (1) | 0.32 |
| Artralgia | 3.8 (4) | 5 (5) | 4.4 (9) | 0.68 |
| Fotosensibilidad | 1 (1) | 0 (0) | 0.5 (1) | 0.32 |
| Prurito | 0 (0) | 1 (1) | 0.5 (1) | 0.30 |
| Otro | 1.9 (2) | 2 (2) | 2 (4) | 0.40 |
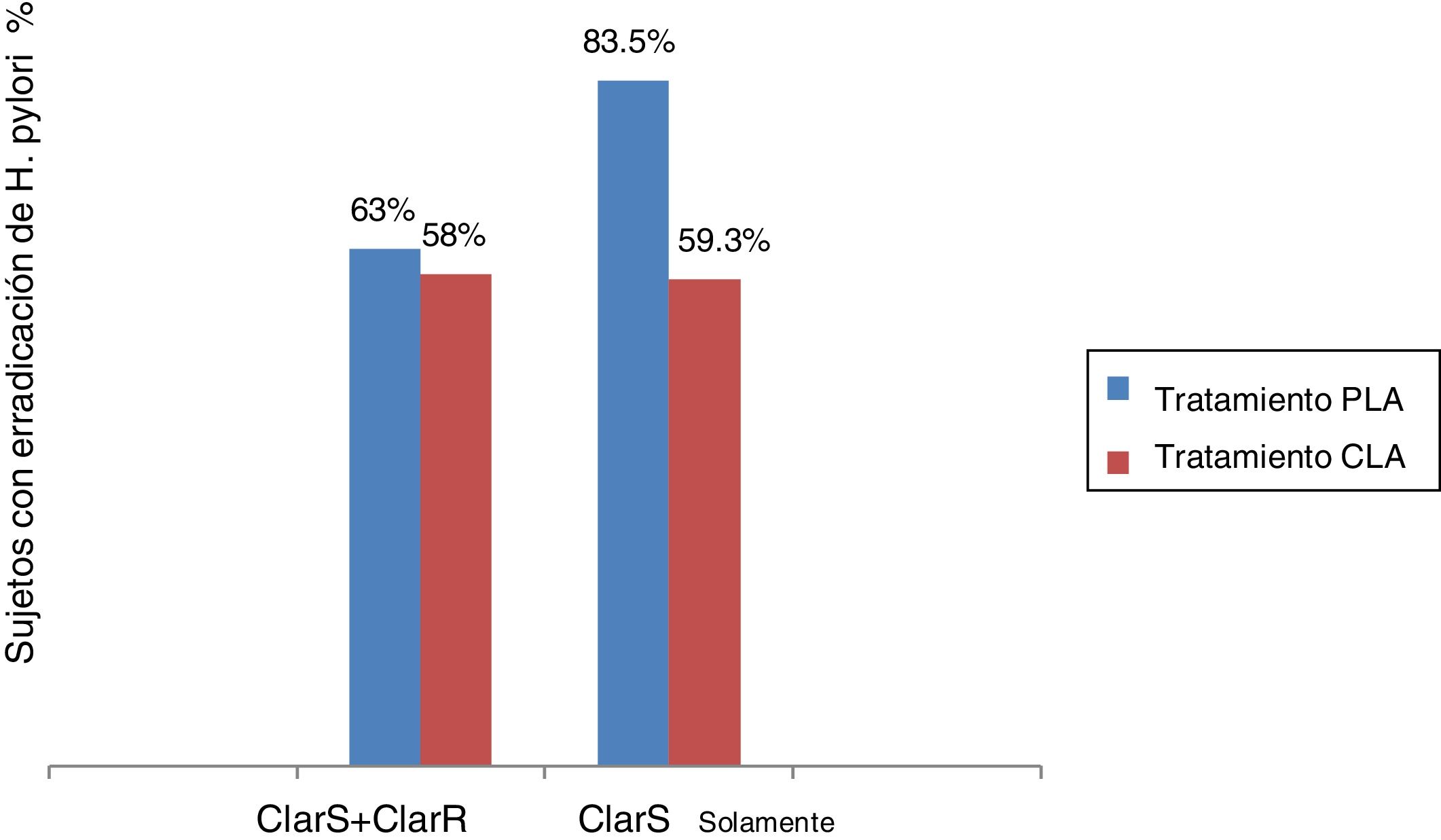
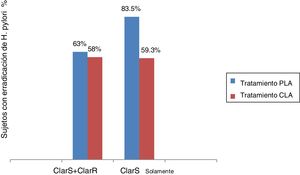
Debido a que las tasas de erradicación de H. pylori en el mundo han bajado en la última década, la efectividad empírica de las terapias ha sido cuestionada y la resistencia a los antibióticos, principalmente relacionada con el abuso y la automedicación, se ha convertido en una prioridad de la investigación18,19. En el presente estudio clínico, el tratamiento de prueba (grupo 2) fue no inferior al tratamiento estándar (grupo 1), pero cuando se implementó el tratamiento guiado por la resistencia, se hizo evidente que la combinación administrada al grupo 2 era superior al tratamiento triple (combinación del grupo 1) en una infección sensible a la claritromicina (fig. 4).
Tasas de erradicación por tratamiento, con base en resistencia a claritromicina.
ClarS: sensibilidad a claritromicina; ClarR: resistencia a claritromicina.
ClarS + ClarR: tasa de erradicación de H. pylori no inferior (PLA vs. CLA, p = 0.757).
ClarS solamente: tasa de erradicación de H. pylori superior (PLA vs. CLA, p = 0.013).
Se ha demostrado que la duración del tratamiento es un aspecto importante: metaanálisis de reportes sobre tratamientos de 7 días versus 10 días han señalado que en comparación con los tratamientos de 7 días, el curso de 10 días mejora la tasa de erradicación en un 4%. En consecuencia, el tratamiento de 10 días permite un tiempo de exposición adecuado para un tratamiento efectivo3. En un metaanálisis reciente, se comparó a terapias de primera línea con levofloxacina con el tratamiento triple estándar. No se encontraron diferencias al comparar levofloxacina+amoxicilina+un IBP versus claritromicina+amoxicilina+un IBP. Sin embargo, la combinación de levofloxacina+claritromicina resultó en una mejor erradicación20.
Con relación a la azitromicina, no se ha observado que incremente los riesgos asociados con este macrólido, particularmente de eventos cardiovasculares, en esquemas terapéuticos de 10 días. Los estudios observacionales que evaluaron el aumento de riesgo de eventos cardiovasculares por el uso de azitromicina asociaron el aumento con concentraciones en suero obtenidas después de la administración oral en dosis múltiples diarias. Ese riesgo disminuyó dramáticamente cuando las concentraciones en plasma cayeron después de finalizado el tratamiento, independientemente de la concentración del macrólido en tejido21.
El esquema propuesto implicaba una sola dosis de azitromicina por día, suficiente para lograr concentraciones en tejido gástrico persistentemente altas. Además, el nivel máximo de azitromicina en suero después de una dosis oral de 500mg es 5veces más bajo que el obtenido después de una dosis equivalente de claritromicina, el cual tiene una mayor asociación con el riesgo de arritmias ventriculares severas. En consecuencia, no es probable que la azitromicina haya incrementado dichos riesgos en el esquema propuesto de 10 días.
Nuestros resultados confirman que la resistencia a la claritromicina en México es alta (28.8% total). Este porcentaje es sorprendentemente más alto que los datos reportados en otras series, en las cuales la frecuencia de resistencia a la claritromicina va del 4 al 25%, dependiendo del área geográfica y el método de laboratorio empleado para evaluar la resistencia al antibiótico. La frecuencia diferencial encontrada entre las 2ciudades evaluadas también es sorprendente: en Toluca se observó casi el doble de la frecuencia observada en la Ciudad de México. Aunque menos de un tercio del total de la población del estudio fue reclutado en Toluca, la diferencia es igualmente notable. Mientras que el uso indiscriminado de antibióticos es común en México y favorece las mutaciones aleatorias de cepas de H. pylori, lo cual crea resistencia a la claritromicina, las diferencias regionales en los patrones de resistencia podrían deberse a otros factores. En consecuencia, se requiere de más estudios clínicos y epidemiológicos para aclarar esta suposición.
También nuestros hallazgos indican que la claritromicina y la azitromicina tienen en común la mutación del punto 23S del ácido ribonucleico ribosómico (rRNA por sus siglas en inglés), la cual podría ser considerada un marcador de resistencia al macrólido. Dado que dicho marcador de resistencia es posiblemente común en el fenotipo de ambos macrólidos, no se puede descartar un efecto de resistencia cruzada que subyace al efecto diferencial significativo del tratamiento basado en levofloxacina, al considerar solamente a la población sensible a la claritromicina o a la totalidad de la población. Esto no es un evento menor: determinaría el cambio en la eficacia de un tratamiento potencialmente superior para la erradicación de H. pylori a uno no inferior o clínicamente equivalente. De esta manera, el factor de la resistencia del antibiótico a macrólidos (resistencia directa a la claritromicina y resistencia cruzada a la azitromicina) podría explicar por qué las tasas de erradicación de H. pylori totales obtenidas en los 2tratamientos comparados aquí no fueron mayores del 65%, pero cuando las subpoblaciones fueron analizadas por separado, controlando por sensibilidad a la claritromicina (ClarS), el porcentaje de erradicación de H. pylori por el tratamiento con PLA se incrementó significativamente (p=0.013) (fig. 4).
Métodos de biología molecular como la FISH y la reacción en cadena de la polimerasa (PCR por sus siglas en inglés) son técnicas de uso amplio para determinar la susceptibilidad al antibiótico de H. pylori. Se ha demostrado que la FISH es un método rápido, exacto y con buena relación de costo-efectividad para detectar H. pylori y para determinar la resistencia a macrólidos en colonias de cultivo de H. pylori, al igual que en las muestras histopatológicas22. Presumiblemente, la tasa de resistencia de H. pylori a la levofloxacina es más baja que a los macrólidos. Además, la correlación entre resistencia genotípica (medida por la detección de mutaciones a través de métodos de biología molecular como la FISH) y resistencia fenotípica (medida a través de las concentraciones inhibitorias mínimas de antibióticos y desenlaces clínicos) es alta para ambos antibióticos. Los estudios indican que la relación entre resistencia genotípica y desenlaces clínicos es incluso mejor después de la terapia de erradicación basada en claritromicina. Así, la detección de mutaciones de resistencia a este antibiótico parece ser un método apropiado para predecir probables fallas terapéuticas23. Sin embargo, no se llevaron a cabo pruebas en el presente estudio que soporten lo anterior.
En nuestro estudio, la mayoría de los EA fueron relacionados con el tratamiento (85.1%), pero fueron ligeros y autocontenidos y no fueron motivo para interrumpir el tratamiento. Las tasas fueron significativamente más altas en el grupo de claritromicina (86%) que en el grupo de levofloxacina (65.4%), lo cual coincide con algunos estudios que comparan la terapia triple estándar con la terapia basada en levofloxacina20. La 13C-UBT ha sido considerada el estándar de oro para verificar los resultados de erradicación del tratamiento24. En el presente estudio, el 90.33% de los sujetos completaron la prueba. Los pacientes que no regresaron al laboratorio para las pruebas (9.67%, 22 sujetos) representan el mismo porcentaje de falla descrito en la literatura con relación a la efectividad de los métodos de monitoreo25,26. Existen estudios que muestran que en México se observa atrofia en el 22% de las biopsias gástricas27, lo cual podría explicar el alto porcentaje de sujetos en nuestro estudio (17.2%) que tuvieron resistencia FISH negativa y 13C-UBT positiva.
Una de las desventajas del presente estudio fue la realización de pruebas de resistencia de un solo antibiótico, pero los resultados fueron claramente dependientes de la resistencia a la claritromicina. Es importante que en investigaciones futuras sobre los resultados de otros tratamientos de erradicación se incluyan las tasas de resistencia de todos los antibióticos para mejorar el perfil epidemiológico. Finalmente, debemos tener precaución respecto a la generalización de los resultados de resistencia al antibiótico de nuestro estudio, ya que deberían ser apreciados como una variación local en las terapias aplicadas en la erradicación de H. pylori.
En conclusión, la combinación de azitromicina-levofloxacina-pantoprazol fue no inferior al tratamiento triple y estuvo asociado con menos EA que las terapias con claritromicina. La levofloxacina puede ser un antibiótico adecuado y seguro en esquemas de erradicación de H. pylori. Sin embargo, su utilización como un tratamiento de primera línea o de segunda línea está aún por ser establecida, dependiendo del patrón local de resistencia. Nuestros hallazgos coinciden con los de muchos otros países en apoyo del hecho de que la terapia triple con claritromicina no está logrando la tasa de erradicación esperada y se deben buscar otras alternativas. El conocimiento de los patrones de resistencia obtenidos de programas de vigilancia antimicrobiana locales y regionales o la experiencia clínica local a través de técnicas de biología molecular, como la FISH, es un apoyo importante para decidir el tratamiento que tendrá la tasa de éxito más alta posible. Si ningún régimen disponible puede lograr ≥ 90% de erradicación, entonces los clínicos deberán utilizar los regímenes localmente disponibles más efectivos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos fueron realizados de acuerdo con los reglamentos del comité de ética de investigación clínica relevante y con los del Código de Ética de la Asociación Médica Mundial (Declaración de Helsinki).
Confidencialidad de los datosLos autores declaran que siguieron los protocolos de sus centros de trabajo respecto a la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores obtuvieron el consentimiento informado de los pacientes mencionados en este artículo. El autor en correspondencia está en posesión de dicho documento.
FinanciaciónEl presente estudio se realizó con fondos de Asofarma de México SA de CV.
AutoríaConcepto y diseño del estudio: LLG, FC; recolección de datos: LLG, LBQ, BCR, MDS; análisis e interpretación de datos: LLG, LBQ, FC; análisis estadístico: LLG, LBQ, FC; borrador de manuscrito: LLG, LBQ, BCR; revisión crítica del manuscrito: LLG, LBQ, SGH, MDS, FC; obtención de fondos: FC; apoyo administrativo, técnico y material y supervisión del estudio: FC.
Conflicto de interesesEl presente estudio se realizó con fondos de Asofarma de México SA de CV. Durante el desarrollo de la investigación la Dra. Laura L. de Guevara, Dra. Leticia Bornstein-Quevedo, Dra. Saraí González-Huezo, Dr. Mauricio Di Silvio y la Dra. Beatriz Castañeda recibieron patrocinio de parte de Asofarma de México SA de CV. El Dr. Fernando G. Costa es Asesor Médico Corporativo de Estudios Clínicos para Asofarma S.A.I. y C. (Argentina).
Véase contenido relacionado en DOI: http://doi.org/10.1016/j.rgmx.2018.10.005, Escobedo-Belloc M y Bosques-Padilla F. El incremento en la resistencia de Helicobacter pylori a los antibióticos en México: ¿son la azitromicina más levofloxacina la respuesta? Rev Gastroenterol Mex.2018:84:271-73.
Infinite Clinical Research (ICR) fue la OIC contratada para realizar el estudio.
Comité de Ética del Centro de Investigación Médico Biológica y Terapia Avanzada SC (CImByTA), Guadalajara, Jalisco (MX). Fecha de aprobación: 22 de junio del 2012 (referencia: protocolo ASO HP 01, versión 2.0).