Alrededor de una quinta parte de las lesiones subepiteliales (LS) gástricas se corresponden con leiomiomas1. Las de ubicación cardial o próximas a la unión esófago-gástrica (UEG) son quirúrgicamente exigentes, asociándose a riesgos de estenosis, fugas o alteraciones fisiológicas postoperatorias. En la actualidad, gran parte de estas lesiones pueden ser resecadas empleando disección endoscópica submucosa (DES), técnica iniciada en Asia y posteriormente difundida al resto del mundo. En Latinoamérica la experiencia con este procedimiento continúa en desarrollo. La morbilidad asociada a la resección de LS empleando DES va del 6.7 a 55.4%, incluyendo hemorragias, perforaciones, enfisema subcutáneo, neumomediastino y fístulas secundarias a falla en el cierre de los planos incididos2. De igual forma, la manipulación de lesiones mayores a 40̊mm puede resultar compleja y terminar en resecciones incompletas3,4. La combinación de la videoendoscopia flexible (VEF) y la laparoscopia transgástrica intraluminal (LTGI) plantea una alternativa terapéutica y una estrategia de especial interés para su tratamiento.
Describimos la técnica empleada y evaluamos los resultados de la resección de LS cardiales, en tres pacientes intervenidos entre junio 2012 y octubre 2017. Expresamos las variables en valores absolutos y calculamos la media aritmética y el rango de las variables continuas. Describimos las variables categóricas en frecuencia. Incluimos evaluación clínica preoperatoria, videoendoscopia digestiva, TC-Abdominal trifásica, ultrasonido endoscópico y citología por punción, esta última compatible con leiomiomas en los casos 2 y 3. Las características de cada paciente se detallan en la tabla 1. Otros factores puntuales que motivaron la indicación quirúrgica, fueron la duda diagnóstica en la citología por punción, sin posibilidad de costear los gastos de su repetición (caso 1) y ante la posibilidad de crecimiento, la insistencia de los pacientes en la resección de una lesión «tumoral» de localización «difícil», decisión respaldada por el gastroenterólogo tratante.
Serie de pacientes con resección laparoscópica-endoscópica de lesiones subepiteliales cardiales. Características clínicas, hallazgos en estudios de extensión y resultados postoperatorios
| Paciente | Sexo/edad | IMC(kg/m2) | Ultrasonido endoscópico | Indicación quirúrgica | Procedimientos adicionales | Esquema de ubicación de la lesión | Tiempo quirúrgico | Pérdidahemática | Eventos adversos intraoperatorios | Seguimiento(meses) |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | M45̊a. | 31 | Lesión subepitelial.Origen: muscular propia, 20̊mm.No afecta submucosa, ni serosa | Duda diagnóstica en la citología por punción (sin posibilidad de repetir) | Colecistectomía Lap.Hernioplastiaumbilical | Hora 5≤̊1̊cm de UEG | 160̊min | 25̊cc | No | 80 |
| 2 | F58̊a. | 36 | Lesión mesenquimática, calcificada,Origen: muscular propia, 19̊mm | Duplicación del tamaño de la lesión (último año seguimiento) | No | Hora 92̊cm UEG | 90̊min | 5̊cc | Hematomaen curva menor gástrica (autolimitado) | 75 |
| 3 | F53̊a. | 29 | Lesión submucosa.Origen: muscular propia, con área de necrosis en su interior, 40̊×̊20̊mmExtensión: hasta la serosa (sin infiltrarla) | Disfagia. Tamañode la lesión | Retiro endoscópicode prótesis pancreática | Hora 3Sobre la UEG | 145̊min | 20̊cc | No | 16 |
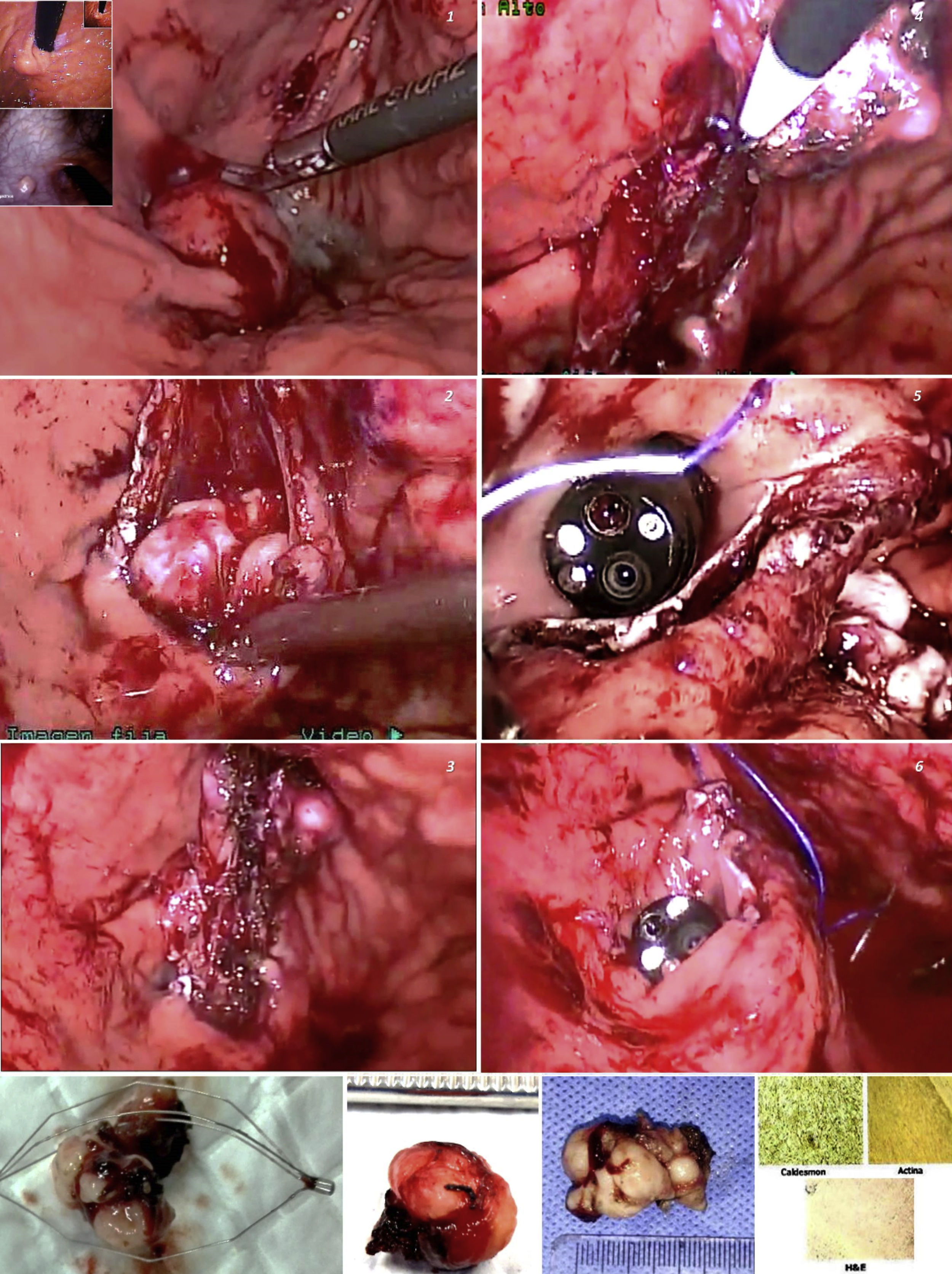
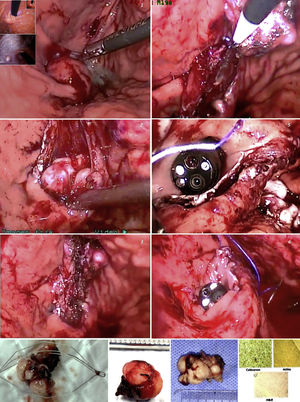
Bajo anestesia general, colocamos tres puertos abdominales y realizamos laparoscopia exploradora. Verificamos endoscópicamente la localización de las lesiones, fijamos el estómago a la pared abdominal con riendas de sutura y bajo control endoscópico, mediante transiluminación, introdujimos los trócares transgástricos evitando los vasos de su pared. Empleamos diatermia en la disección, extrajimos las lesiones a través de la boca y rafiamos la mucosa con sutura sintética absorbible. Al finalizar, realizamos prueba neumática y verificamos endoscópica y laparoscópicamente el cierre de los portales gástricos. Todas las lesiones fueron de crecimiento endofítico y el resultado de la inmunohistoquímica fue compatible con leiomiomas (anticuerpos Caldesmon y Actina positivos) (fig. 1). El tiempo quirúrgico fue de 131.6 minutos promedio y la pérdida hemática de 16.6̊cc. Observamos un evento adverso en un caso (tabla 1). Los esofagogramas postoperatorios descartaron fugas, posterior a lo cual se inició la vía oral y se indicó el egreso. No observamos complicaciones postoperatorias tempranas o tardías y el seguimiento fue de 57 meses en promedio.
Los abordajes quirúrgicos de mínimo acceso han sido adaptados a la localización y características propias de cada órgano y tipo de lesión en particular. Diversos grupos han empleado la combinación de la VEF y la LTGI demostrando beneficios adicionales a los ofrecidos por las resecciones quirúrgicas o totalmente endoscópicas5, sobre todo en aquellas lesiones grandes, las localizadas en el cardias, curva menor o antro u originadas en las capas profundas de la pared gástrica6; así como también, resulta una alternativa terapéutica en centros en donde la experiencia en endoscopia de tercer espacio no ha sido desarrollada (como en nuestro caso). La combinación de ambos abordajes contribuye a ampliar la perspectiva del cirujano al contar con una visión simultánea interna y externa del órgano. La triangulación de los instrumentos laparoscópicos en el interior de la cámara gástrica permite controlar las maniobras de disección y resección y brinda seguridad durante la rafia de los defectos, efectuándose del mismo modo el sellado de vasos o el cierre con clips, suturas o autosuturas. A su vez y ante una eventual perforación o hemorragia, el tratamiento puede realizarse empleando laparoscopia o endoscopia.
Según Ntourakis y Mavrogenis5, las técnicas de uso simultáneo de la videoendoscopia y la laparoscopia se agrupan en tres categorías, de acuerdo al papel desempeñado por estos métodos: a) resección videoendoscópica asistida por laparoscopia, b) resección laparoscópica asistida por videoendoscopia y c) resección combinada laparoscópica-endoscópica. Incluimos el procedimiento realizado en nuestros pacientes dentro del segundo grupo anteriormente mencionado, técnica inicialmente descrita por Ohashi7 y en la cual los puertos laparoscópicos transgástricos pueden utilizarse en número variable, emplearse un puerto único o combinar la videoendoscopia flexible con el uso del robot, logrando beneficios adicionales a los ofrecidos por la cirugía robótica. En los pacientes descritos la combinación de la VEF y la LTGI resultó una estrategia eficaz y segura para la resección de LS cardiales. El empleo conjunto de ambos procedimientos potenció las ventajas de su uso individual.
Responsabilidades éticasEl procedimiento quirúrgico fue explicado a cada uno de los pacientes. Obtuvimos consentimiento informado, tanto para el acto quirúrgico, como para la publicación de imágenes (estos documentos obran en poder del autor de correspondencia), siguiendo los protocolos de nuestro centro de trabajo sobre publicación de datos de pacientes, preservándose su anonimato. Declaramos no haber realizado experimentos en seres humanos.
FinanciaciónLos autores no recibimos ningún tipo de financiación para la realización del presente trabajo.
Conflicto de interesesDeclaramos no tener conflicto de intereses.