El linfoma pancreático primario (LPP) es una entidad rara. Representa aproximadamente el 0.5% de las neoplasias pancreáticas, y menos del 2% de los linfomas1. El LPP incide más comúnmente en el sexo masculino y la región pancreática afectada con mayor frecuencia es la cabeza2. El tipo histológico más habitual es el linfoma no Hodgkin. Las manifestaciones clínicas y los hallazgos radiológicos del LPP deben ser diferenciados de otros procesos pancreáticos, ya que el pronóstico, el tratamiento y la supervivencia difieren del resto3.
Presentamos un caso de LPP diagnosticado y tratado en nuestro centro.
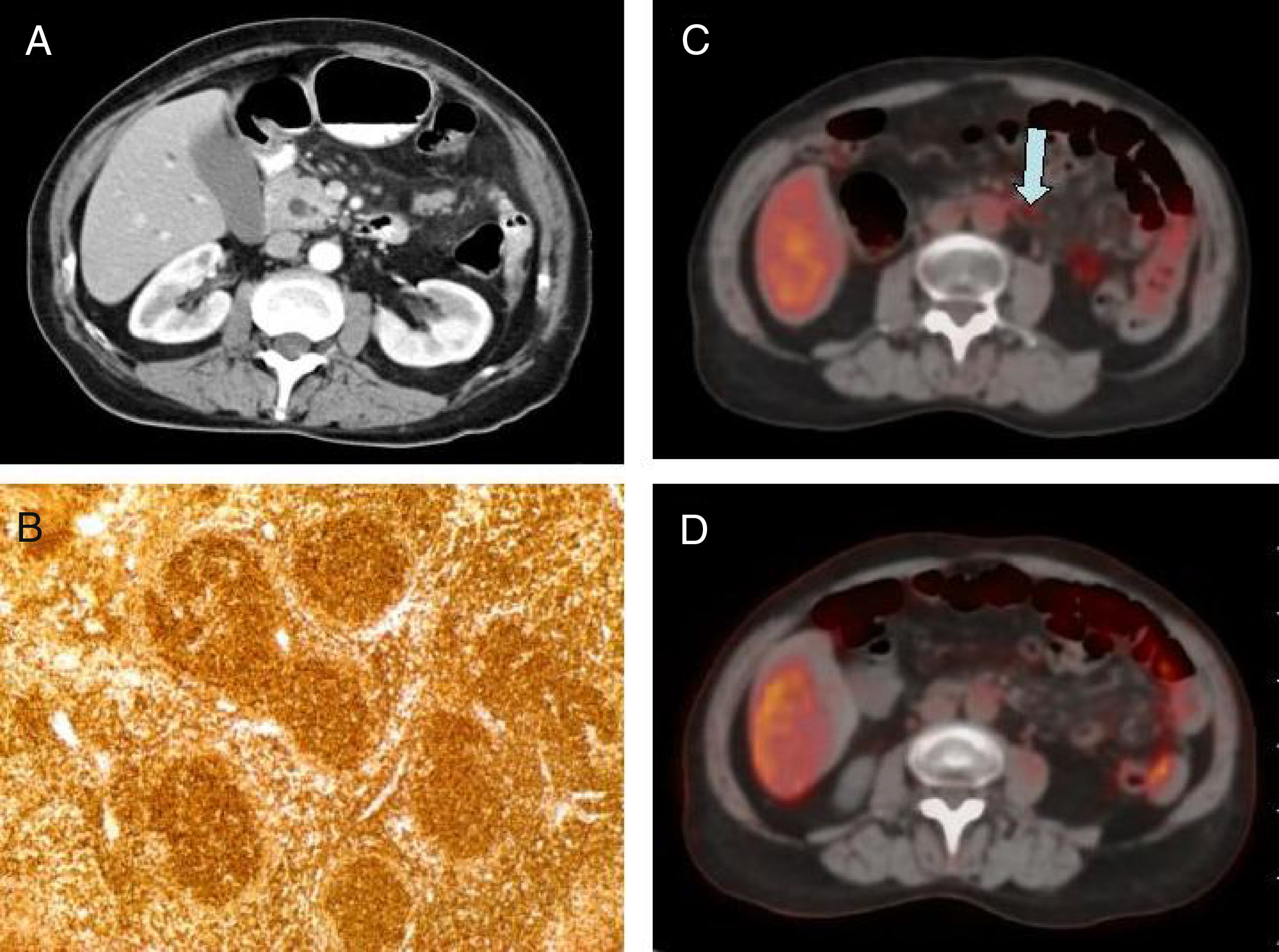
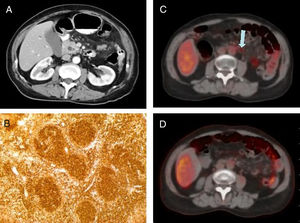
Mujer de 53 años, sin antecedentes personales de interés, que consultó por dolor epigástrico, síndrome general y pérdida de 3kg de peso en el último mes. La exploración física reveló ictericia mucocutánea y dolor abdominal en epigastrio. La analítica mostró bilirrubina total de 6.03mg/dl, GOT 318UI/l y GPT 524UI/l. La ecografía de abdomen manifestó dilatación de la vía biliar extrahepática, con afilamiento progresivo en su porción distal y una masa hipodensa de 4×3×2cm en cabeza pancreática. La tomografía computarizada mostró dilatación de la vía biliar intra y extrahepática, con un colédoco de 17mm de diámetro, un conducto Wirsung de calibre normal y adenopatías de aspecto patológico en el territorio del tronco celíaco y raíz del mesenterio (fig. 1A). En la colangiografía retrógrada endoscópica se apreció un abombamiento de la papila duodenal sugestivo de ampuloma o colangiocarcinoma distal. Se colocó una prótesis biliar plástica de 10Fr y se tomaron biopsias de la papila, que fueron compatibles con infiltrado linfoide de patrón nodular. Ante las dudas diagnósticas con los estudios complementarios realizados, la no disposición de ecoendoscopia en nuestro centro y la ausencia de afectación ganglionar periférica se decidió exploración quirúrgica para realizar una biopsia ganglionar del territorio de la arteria hepática común. El estudio histológico estableció el diagnóstico de linfoma no Hodgkin folicular (fig. 1B). Se completaron estudios de extensión con biopsia de médula ósea y citometría de flujo, que descartaron la afectación a otros niveles. Se estableció el diagnóstico definitivo de LPP, por lo que se instauró tratamiento con quimioterapia (recibió 6 ciclos de R-CHOP) y radioterapia externa (se administraron un total de 36Gy). La paciente presentó una mejoría clínica y radiológica, con resolución de la ictericia. Se retiró la prótesis biliar a los 120 días por vía endoscópica, y tras 24 meses de seguimiento, en el PET/TC se observó una adenopatía patológica en raíz del mesenterio (fig. 1C), por lo que se inició tratamiento con rituximab bimensual. Los estudios de imagen posteriores, mostraron respuesta metabólica completa al tratamiento (fig. 1D). A los 48 meses del diagnóstico la paciente se encuentra asintomática y sin enfermedad linfoproliferativa activa.
A) TC de abdomen con contraste intravenoso (corte axial de 5mm) en el que se evidencia engrosamiento de la cabeza pancreática y dilatación del colédoco. B) Estudio histopatológico de adenopatía peripancreática, bcl-2 positivo, compatible con linfoma no Hodgkin folicular. C) PET/TC (corte axial): adenopatía en raíz del mesenterio hipercaptante (flecha). D) PET/TC control tras tratamiento con rituximab (corte axial): desaparición de la actividad metabólica en la adenopatía de la raíz del mesenterio.
Clásicamente, se establece el diagnóstico de LPP cuando se cumplen los siguientes criterios: masa que afecta predominantemente al páncreas, con afectación de ganglios peripancreáticos, hemograma normal y ausencia de adenopatías palpables de afectación mediastínica y de metástasis hepatoesplénicas3. Las manifestaciones clínicas más habituales son dolor abdominal, pérdida de peso, ictericia, pancreatitis aguda, obstrucción de intestino delgado y diarrea2.
Entre los estudios de imagen, podemos destacar la ecografía, la TC y la RMN como técnicas que ayudan a diferenciar el LPP del adenocarcinoma. Radiológicamente, el LPP se caracteriza por ser un tumor voluminoso, localizado en cabeza del páncreas, sin dilatación significativa del conducto de Wirsung y con adenopatías adyacentes a las venas renales4. Generalmente, el LPP suele ser de mayor tamaño que el adenocarcinoma y a diferencia de este, crece alrededor de los vasos sanguíneos, sin infiltrarlos. El diagnóstico definitivo lo establece el estudio histopatológico, por lo que la punción guiada por ultrasonografía endoscópica se considera el método diagnóstico de elección3. Sin embargo, en muchas ocasiones la muestra de tejido obtenido, mediante las agujas convencionales con las que se realiza la PAAF, no es suficiente para llegar a un diagnóstico certero; lo que hace disminuir el rendimiento diagnóstico de la PAAF en este tipo de tumores. Por este motivo se recomienda emplear preferiblemente las agujas tipo ProCore® o Shark Tip, con las que se consigue biopsiar una mayor cantidad de muestra, que conserve la arquitectura tisular. Cuando los resultados no son concluyentes, una alternativa es la biopsia quirúrgica, que nos permite obtener mayor cantidad de tejido.
El tratamiento de elección del LPP es la quimioterapia y/o radioterapia. Se han reportado tasas de curación de hasta el 30% sin necesidad de resección pancreática3. También se ha descrito el rituximab como una opción terapéutica aceptable en casos de linfomas no Hodgkin5.
Por tanto se debe destacar que, ante una masa pancreática, el LPP debe ser incluido en el diagnóstico diferencial con el adenocarcinoma, ya que el pronóstico y tratamiento de ambas entidades son muy diferentes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades, sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.