La hepatitis autoinmune (HAI) está asociada con infiltración periportal de células plasmáticas. La detección de células plasmáticas se realiza rutinariamente por medio de tinción hematoxilina-eosina (HE). El objetivo del presente estudio fue evaluar la utilidad de CD138, un marcador inmunohistoquímico de células plasmáticas, en la evaluación de HAI.
Materiales y métodosEstudio retrospectivo; los casos compatibles con HAI se recolectaron de 2001 a 2011. Se utilizó la tinción HE para evaluación y CD138 para detectar células plasmáticas.
ResultadosSe incluyeron 60 biopsias. En el grupo HE la mediana y el rango intercuartílico (RIQ) fue 6 (4-9) células plasmáticas/campo de alto poder (CAP) y de 10 (RIQ 6-20) células plasmáticas/CAP en el grupo CD138 (p<0.001). Existió una correlación significativa entre el número de células plasmáticas determinado por HE y CD138 (p=0.31, p=0.01). No se encontró relación significativa entre el número de células plasmáticas determinadas por CD138 y el nivel IgG (p=0.21, p=0.09) o el estadio de fibrosis (p=0.12, p=0.35), o entre el nivel de IgG y el estadio de fibrosis (p=0.17, p=0.17). No se encontró correlación significativa entre la respuesta al tratamiento y el número de células plasmáticas determinadas por HE (p=0.11, p=0.38), CD138 (p=0.07, p=0.55), o el estadio de fibrosis (p=0.16, p=0.20). La expresión de CD138 fue diferente entre los grupos de respuesta al tratamiento (p=0.04).
ConclusiónEl CD138 incrementó la detección de células plasmáticas en biopsias hepáticas de pacientes con HAI, en comparación con la tinción de HE de rutina. Sin embargo, no existió correlación entre el número de células plasmáticas determinadas por CD138 y los niveles de IgG en suero, el estadio de fibrosis o la respuesta al tratamiento.
Autoimmune hepatitis (AIH) is associated with periportal infiltration by plasma cells. Plasma cell detection is routinely performed through hematoxylin and eosin (H&E) staining. The present study aimed to assess the utility of CD138, an immunohistochemical plasma cell marker, in the evaluation of AIH.
Materials and methodsA retrospective study was conducted, in which cases consistent with AIH, within the time frame of 2001 and 2011, were collected. Routine H&E-stained sections were used for evaluation. CD138 immunohistochemistry (IHC) was performed to detect plasma cells.
ResultsSixty biopsies were included. In the H&E group, the median and interquartile range (IQR) was 6 (4-9) plasma cells/high power field (HPF) and was 10 (IQR 6-20) plasma cells/HPF in the CD138 group (p<0.001). There was a significant correlation between the number of plasma cells determined by H&E and CD138 (p=0.31, p=0.01). No significant correlation was found between the number of plasma cells determined by CD138 and IgG level (p=0.21, p=0.09) or stage of fibrosis (p=0.12, p=0.35), or between IgG level and stage of fibrosis (p=0.17, p=0.17). No significant correlation was found between the treatment response and the number of plasma cells determined by H&E (p=0.11, p=0.38), CD138 (p=0.07, p=0.55), or stage of fibrosis (p=0.16, p=0.20). CD138 expression was different between the treatment response groups (p=0.04).
ConclusionCD138 increased the detection of plasma cells in liver biopsies of patients with AIH, when compared with routine H&E staining. However, there was no correlation between the number of plasma cells determined by CD138 and serum IgG levels, stage of fibrosis, or response to treatment.
La hepatitis autoinmune (HAI) es una enfermedad de etiología desconocida que se asocia con inflamación persistente del hígado. Normalmente afecta a mujeres y se caracteriza por transaminasas elevadas, la presencia de anticuerpos y niveles elevados de inmunoglobulina G (IgG) en suero1,2. Los hallazgos bioquímicos e inmunológicos en dichos pacientes son insuficientes para realizar el diagnóstico y la biopsia hepática es necesaria1. El hallazgo más común en la biopsia hepática es la presencia de hepatitis de interfase. Además, usualmente se encuentra infiltrado linfoplasmocitario portal3,4. Los reportes indican que hasta el 34% de los pacientes no presentan células plasmáticas y dicho porcentaje es desconocido en pacientes mexicanos5. La determinación de las células plasmáticas mediante tinción con hematoxilina-eosina (HE) se realiza de manera rutinaria, mientras que la utilización de CD138 (un marcador inmunohistoquímico de células plasmáticas) en la evaluación de HAI no ha sido estudiada ampliamente. La mayoría de los hepatólogos consideran que la presencia de células plasmáticas es virtualmente diagnóstica de HAI, pero las implicaciones del pronóstico son desconocidas1.
El objetivo del presente estudio fue evaluar el desempeño de la inmunohistoquímica (IHQ) CD138 para el diagnóstico histopatológico de HAI por medio de la comparación del número de células plasmáticas encontrado con la tinción HE en comparación con la tinción CD138. Un objetivo secundario del estudio fue estudiar la asociación entre el número de células plasmáticas determinado por CD138 y los niveles de IgG en suero, el estadio de fibrosis y la respuesta al tratamiento6.
Materiales y métodosSe realizó un estudio transversal retrospectivo. Los pacientes candidatos fueron aquellos con un diagnóstico histopatológico de HAI realizado en el Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán, dentro del marco temporal de 2001 a 2011. Incluimos pacientes cuyos hallazgos clínicos, serológicos e histológicos fueran todos consistentes con HAI probable o definitiva, según los criterios revisados del Grupo Internacional de Hepatitis Autoinmune (IAIHG, por sus siglas en inglés)7,8. Se evaluó IgG, anticuerpos antinucleares (ANA), anticuerpos contra músculo liso (ASMA) y anticuerpos de tipo 1 microsomales de hígado y riñón (anti-LKM-1). Un recuento sérico de 1:80 o más alto fue considerado positivo para ANA y ASMA y un recuento de 1:40 o mayor fue considerado positivo para anti-LKM-1. Excluimos a pacientes cuyos bloques de parafina faltaban, a pacientes cuya historia médica estaba incompleta, a pacientes que habían recibido tratamiento previamente, a pacientes con enfermedad hepática concomitante o a aquellos cuyo diagnóstico fue realizado en especímenes de trasplante hepático.
Se realizaron cortes de 4um del tejido fijado en formalina e incrustado en bloques de parafina y realizamos tinción de rutina en HE e inmunotinción para CD138 con todos los pacientes. Todas las secciones fueron revisadas por un gastropatólogo experimentado (P.R.M. y J.S.R.), de manera ciega. El número de espacios portales fue determinado a baja potencia (×4); las células plasmáticas fueron contadas a alta potencia (×40) tanto en las laminillas de HE como de CD138. También, se determinó el grado de inflamación y el estadio de fibrosis según el sistema de Batts y Ludwig9.
Todos los pacientes fueron tratados de la misma manera a discreción del hepatólogo. La respuesta al tratamiento fue definida como completa, incompleta o como fallo de tratamiento, según los criterios del IAIHG. La respuesta completa fue considerada una regresión bioquímica (normalización sérica de niveles de AST, ALT e IgG); la respuesta incompleta como una mejoría insuficiente en los hallazgos en pruebas de laboratorio para satisfacer los criterios de respuesta completa, y el fallo de tratamiento como un empeoramiento en los resultados de las pruebas de laboratorio, a pesar del cumplimento de la terapia estándar7,10.
Análisis estadísticoLas variables continuas fueron expresadas como mediana y rango intercuartílico (RIQ). La prueba de rangos con signo de Wilcoxon fue utilizada para comparar el número de células plasmáticas determinadas por tinción HE en comparación con la tinción CD138. La prueba de Kruskall-Wallis fue usada para comparar el número de células plasmáticas determinadas por IHQ CD138 y la respuesta al tratamiento. Un valor p de 2 colas<0.05 fue considerado estadísticamente significativo. El coeficiente de correlación de Spearman (p) fue usado para evaluar la relación entre variables continuas y discretas, y un coeficiente de correlación mayor a 0.30 fue considerado positivo. Las correlaciones fueron analizadas en función del número de pares sin datos faltantes. En las variables descriptivas se utilizó el número de valores no faltantes. En el cálculo de las frecuencias se excluyó a los valores faltantes y los porcentajes estuvieron basados en el número de valores no faltantes.
Consideraciones éticasLa presente investigación cumplió con las regulaciones actuales relativas a la investigación bioética. No obtuvimos el consentimiento de los pacientes debido a que el presente artículo no contiene información personal que permita identificar a los pacientes. El protocolo fue aprobado por el comité institucional de ética e investigación, con el número de registro GAS-1014-13/15-1.
ResultadosSe evaluó un total de 90 pacientes y biopsias. Excluimos a 10 pacientes debido a la falta de bloques de parafina, 16 pacientes debido a historia médica incompleta y 4 pacientes debido a enfermedades hepáticas concomitantes. En consecuencia, se incluyó a 60 pacientes y sus biopsias en el presente estudio. Las características demográficas, bioquímicas y serológicas de los pacientes se muestran en la tabla 1. La edad mediana fue de 39.5 (RIQ: 29-48) años, con una predominancia de mujeres (75%). Cinco pacientes presentaron HAI tipo 2, según la presencia de anti-LKM-1. La mediana del tiempo de seguimiento fue 108 (RIQ: 72-156) meses. Cinco pacientes presentaron cirrosis en el momento del diagnóstico, 17 pacientes desarrollaron cirrosis durante el seguimiento y 2 pacientes murieron de etiologías relacionadas con el hígado (uno por sangrado variceal y otro por celulitis y choque séptico).
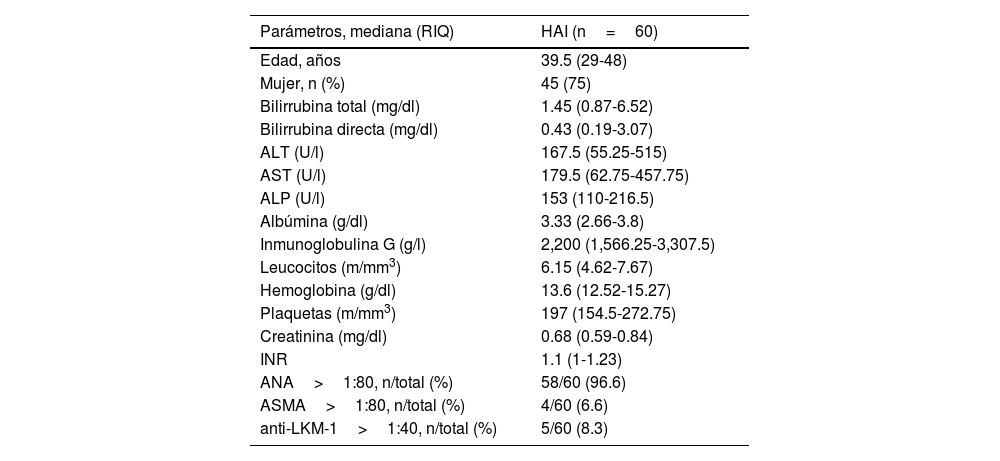
Características demográficas, clínicas y bioquímicas de pacientes con hepatitis autoinmune
| Parámetros, mediana (RIQ) | HAI (n=60) |
|---|---|
| Edad, años | 39.5 (29-48) |
| Mujer, n (%) | 45 (75) |
| Bilirrubina total (mg/dl) | 1.45 (0.87-6.52) |
| Bilirrubina directa (mg/dl) | 0.43 (0.19-3.07) |
| ALT (U/l) | 167.5 (55.25-515) |
| AST (U/l) | 179.5 (62.75-457.75) |
| ALP (U/l) | 153 (110-216.5) |
| Albúmina (g/dl) | 3.33 (2.66-3.8) |
| Inmunoglobulina G (g/l) | 2,200 (1,566.25-3,307.5) |
| Leucocitos (m/mm3) | 6.15 (4.62-7.67) |
| Hemoglobina (g/dl) | 13.6 (12.52-15.27) |
| Plaquetas (m/mm3) | 197 (154.5-272.75) |
| Creatinina (mg/dl) | 0.68 (0.59-0.84) |
| INR | 1.1 (1-1.23) |
| ANA>1:80, n/total (%) | 58/60 (96.6) |
| ASMA>1:80, n/total (%) | 4/60 (6.6) |
| anti-LKM-1>1:40, n/total (%) | 5/60 (8.3) |
ANA: anticuerpos antinucleares; anti-LKM-1: anticuerpos de tipo 1 microsomales de hígado y riñón; ALP: fosfatasa alcalina; ALT: alanina aminotransferasa; ASMA anticuerpos contra músculo liso; AST: aspartato aminotransferasa; HAI: hepatitis autoinmune; INR: índice internacional normalizado; RIQ: rango intercuartílico.
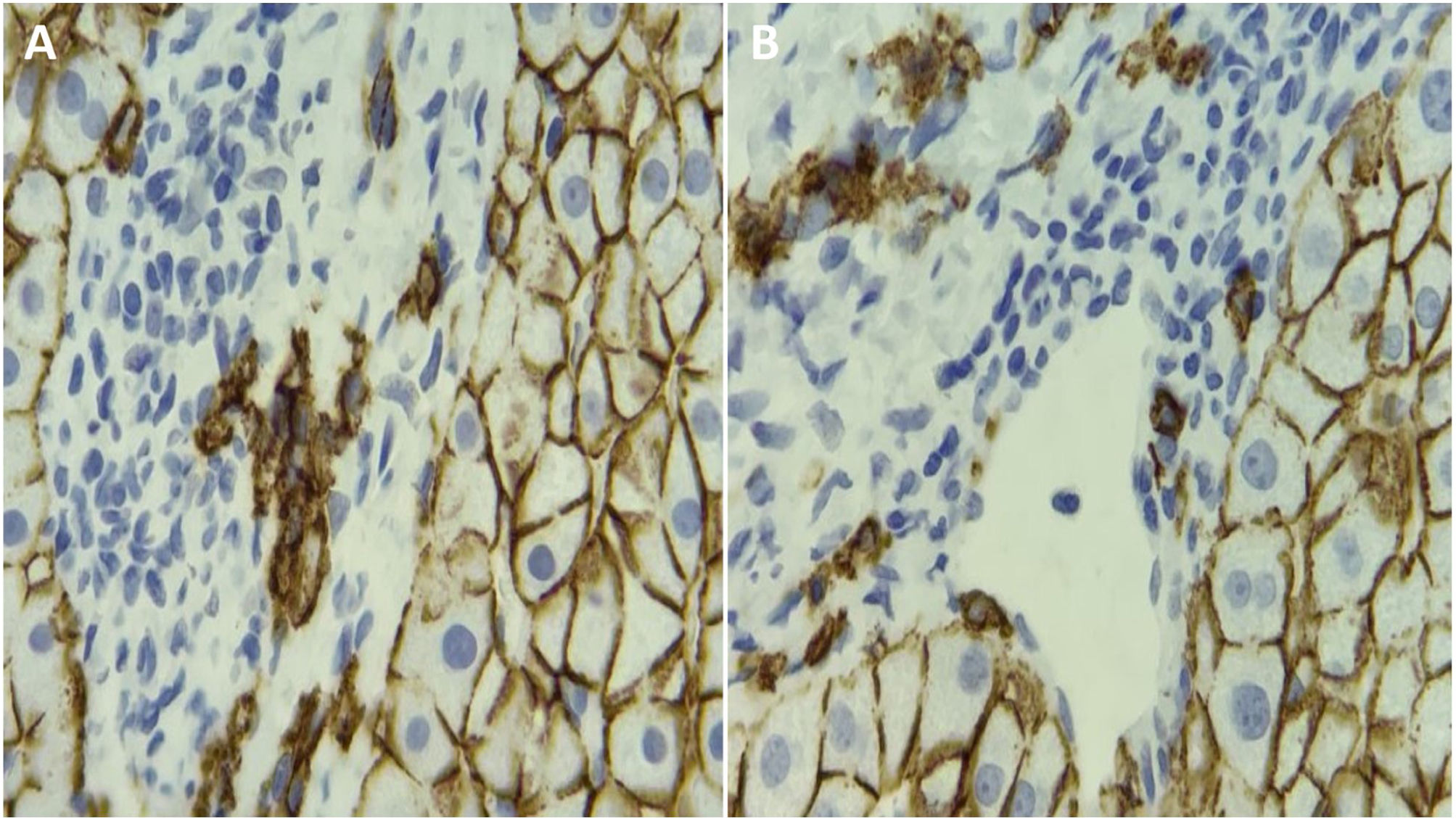
Todas las biopsias hepáticas presentaron hepatitis de interfase e infiltrados celulares en los tractos portales. Todos los pacientes con HAI tuvieron células plasmáticas determinadas por tinción HE y CD138. La cantidad de células plasmáticas fue más elevada en el grupo de CD138 (10 [6-20] células/campo de alta potencia [CAP] contra 6 [4-9] células/CAP, p<0.001). Existió una correlación significativa entre la cantidad de células plasmáticas determinada por medio de IHQ CD138 y tinción HE (p=0.31; p=0.01).
No se encontró correlación significativa entre el número de células plasmáticas determinadas por tinción CD138 y nivel de IgG (p=0.21; p=0.09) (fig. 1).
La respuesta al tratamiento fue completa en 29 pacientes e incompleta en 7. Veintidós pacientes tuvieron fallo de tratamiento y 2 pacientes no tuvieron seguimiento. No se encontró correlación significativa entre la respuesta al tratamiento y el número de células plasmáticas determinadas por tinción HE (p=0.11, p=0.38), IHQ CD138 (p=0.07, p=0.55), o estadio de fibrosis (p=0.16, p=0.20). La expresión de IHQ CD138 fue diferente entre los grupos de tratamiento (p=0.04): en pacientes con remisión la mediana fue 10 (RIQ 6-20), en casos de respuesta incompleta al tratamiento fue 6 (RIQ 3-7) y en pacientes con fallo de tratamiento fue 15 (RIQ 8-20).
DiscusiónDemostramos en el presente estudio que IHQ CD138 incrementó la detección de células plasmáticas en comparación con la tinción HE. Sin embargo, no encontramos asociación significativa entre el número de células plasmáticas determinadas por IHQ CD138 y los niveles de IgG en suero, el estadio de fibrosis o la respuesta al tratamiento11. Hasta donde sabemos, este es el primer estudio que compara la tinción HE con la IHQ CD138 en HAI. Observamos infiltrados de células plasmáticas en todos los casos de pacientes mexicanos con HAI, determinados tanto por tinción HE como por IHQ CD138.
Las células plasmáticas son prominentes en el 66% de los pacientes con HAI y son un hallazgo histológico clave, pero también son comunes en otras enfermedades hepáticas. Los pacientes con esteatohepatitis no alcohólica muestran una inflamación portal elevada con células plasmáticas, hepatitis de interfase, lesión de colangiocitos y reacción ductular prominente12. La HAI y la colangitis biliar primaria (CBP) pueden confundirse fácilmente; ambas presentan inflamación portal con células plasmáticas y hepatitis de interfase, pero la HAI presenta inflamación lobular y no causa daño importante en el ducto. Síndromes que se traslapan, como HAI con características de CBP, presentan hepatitis de interfase, infiltrado portal linfocítico, células plasmáticas portales y colangitis destructiva también.
Brandao et al. encontraron una correlación positiva entre células estelares, fibrosis y el número de células plasmáticas. Además, los mismos autores encontraron una colocalización de células plasmáticas y células estelares activadas, lo cual sugiere que las células plasmáticas podrían ser un marcador sustituto para gravedad de enfermedad, relacionado íntimamente con la cantidad de células estelares hepáticas y el estadio de fibrosis6. Sin embargo, en nuestro estudio dichos resultados no se reprodujeron. No existió asociación entre la cantidad de células plasmáticas identificadas mediante IHQ CD138 y el estadio de fibrosis, lo cual podría ser debido al hecho de que la fibrosis probablemente depende más del tiempo de evolución que de la intensidad de la infiltración celular plasmática. Es interesante que encontremos un mayor número de células plasmáticas en pacientes con fallo de tratamiento, lo cual podría tener implicaciones pronósticas importantes al inicio del tratamiento. Regos et al. reportaron que la expresión de CD138 es significativamente mayor en muestras de hígados cirróticos. Además, encontramos mayor expresión en el grupo de pacientes con fallo de tratamiento que ya tenía cirrosis o que la desarrolló13.
Algunas de las limitaciones del presente estudio son su diseño retrospectivo, su pequeña muestra, y el hecho de que el examen de biopsia hepática es susceptible de error de muestreo y variabilidad inter e intraobservador. Sin embargo, no se reportan grandes inconsistencias en evaluaciones semicuantitativas estandarizadas si dicha evaluación es realizada por un patólogo experto, como fue en el caso de nuestro estudio.
En conclusión, la IHQ CD138 incrementó la detección de células plasmáticas en biopsias hepáticas de pacientes con HAI, en comparación con la tinción de HE de rutina. Sin embargo, no existió correlación entre la cantidad de células plasmáticas determinadas por IHQ CD138 y los niveles IgG en suero, estadio de fibrosis o respuesta al tratamiento.
Responsabilidades éticasLos autores son responsables de todos los aspectos del trabajo al asegurarse de que cuestiones relacionadas con la precisión o integridad de cualquier parte del trabajo han sido adecuadamente investigadas y resueltas.
FinanciaciónNo se recibieron apoyos específicos de agencias del sector público, del sector empresarial o de organizaciones sin fines de lucro con relación a este estudio.
Conflicto de interesesLos autores declaran que no existe conflicto de intereses.