En las últimas décadas el tratamiento multidisciplinario de los pacientes con cáncer, ha permitido mejorar la supervivencia y los periodos libres de enfermedad; sin embargo, también se han elevado el número de tumores asociados al tratamiento, en particular por radioterapia1.
Esta asociación se deriva de aquellos casos presentes en los supervivientes de los desastres ocurridos en Japón y Chernóbil. La justificación para ello se basa en el concepto de oncogénesis por radiación, establecido por Cahan, et al. en 19482; cuyos criterios siguen vigentes. El único punto de estos criterios, que es controvertido, es el tiempo necesario para asociarlo con radioterapia; en los criterios originales es de 5 años, sin embargo, actualmente se ha demostrado que el periodo puede ser menor describiéndose tumores radio-inducidos desde 6 meses hasta 20 años posterior a la culminación del tratamiento3.
Se conoce que el desarrollo de estos tumores es el resultado de la interacción de muchos factores etiológicos. Se ha estudiado el papel de las mutaciones en modelos animales, en particular la de p53; siendo en sarcomas inducidos por radiación la deleción de este gen (52% de las mutaciones) su principal forma en comparación con los sarcomas esporádicos (menos de 10%); sin embargo, esto no es concluyente aún en el ser humano4,5. Las mutaciones p53, así como alteraciones genéticas por inestabilidad genómica son las más estudiadas, cuyos mecanismos incluyen la señalización anormal intracelular, producción de citocinas, generación de radicales libres y la respuesta inflamatoria desencadenada de manera secundaria6.
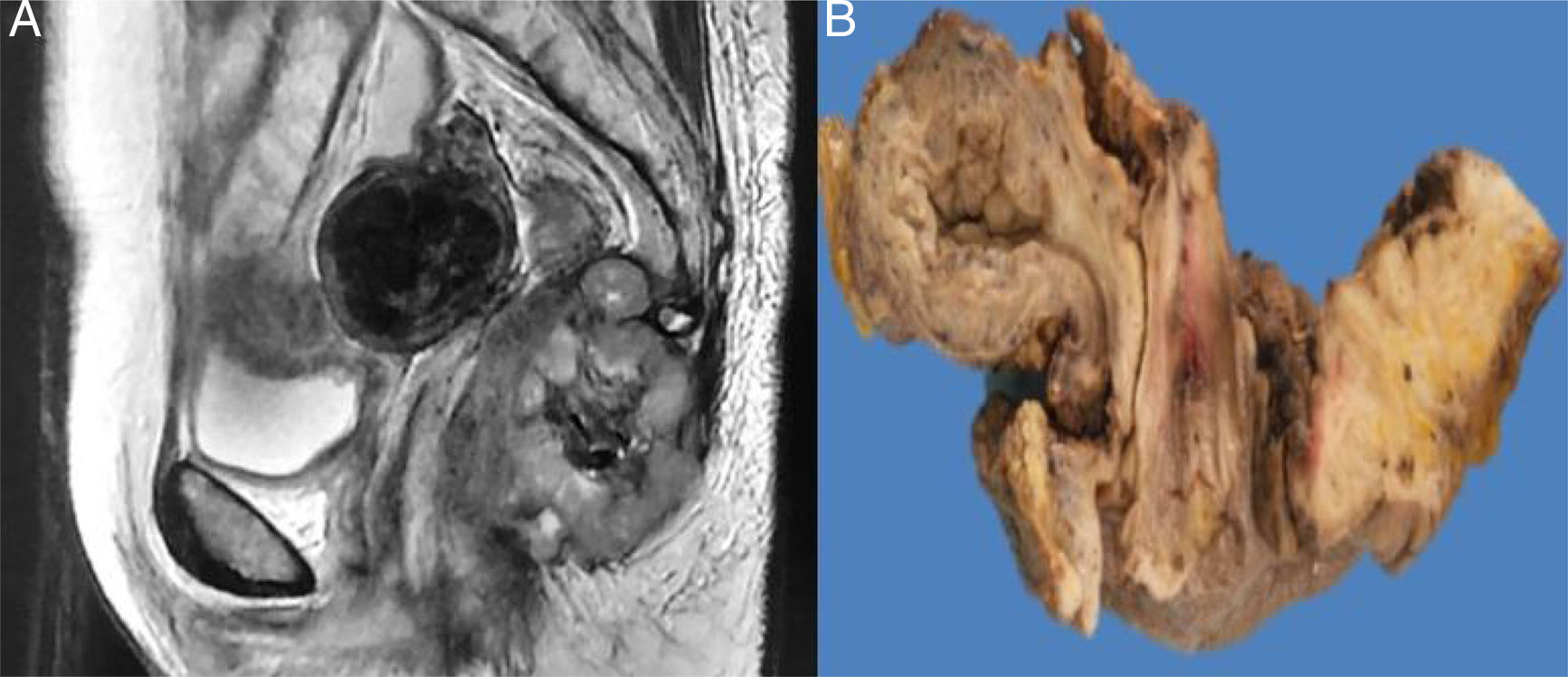
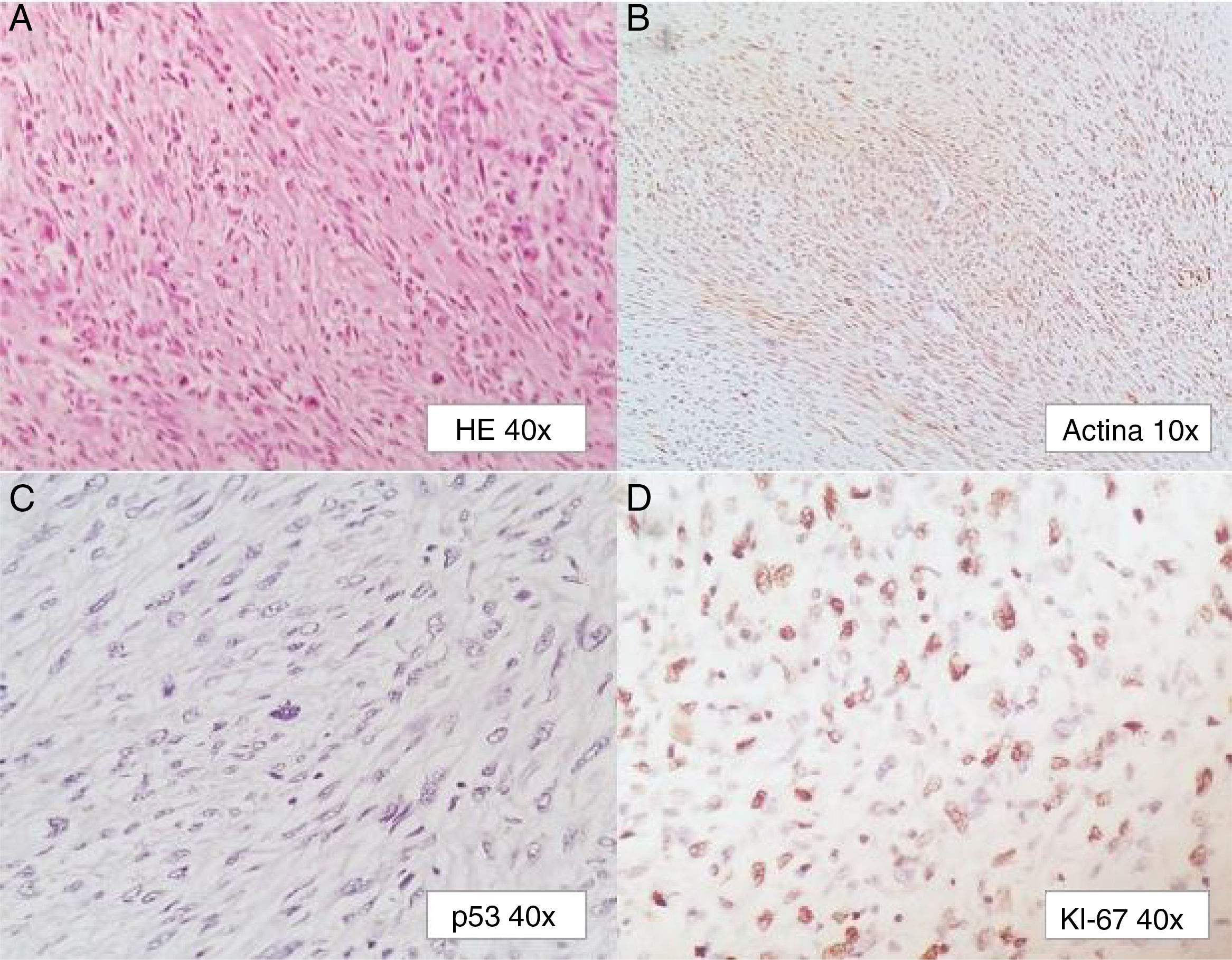
Presentamos el caso de una paciente de 58 años, con antecedente de cáncer cérvico uterino (carcinoma epidermoide) EC IIB (FIGO), tratado con quimioterapia (QT) a base de cisplatino 4 ciclos, de forma concomitante con RT 50Gy a pelvis y braquiterapia (BT) 35Gy, con respuesta completa; por lo que se mantuvo en vigilancia. Ocho años después, sin aparente recurrencia, la paciente inició con tenesmo rectal, asociado a rectorragia. En la exploración física presentó un tumor exofítico y ulcerado, a 3cm del margen anal, que ocluía el 50% de la luz, sin aparente involucro del tabique recto vaginal. En la rectosigmoidoscopia se identificó el tumor a los 6cm del margen anal, con oclusión de hasta el 70% de la luz, se realizó biopsia, esta mostró neoplasia mesenquimatosa con el siguiente inmunoperfil: actina positivo, CD34, CD117, DOG1, PS100, CKAE1/AE3 y P16 negativos, el diagnóstico fue de leiomiosarcoma de alto grado. En la resonancia magnética nuclear (RMN) se corrobora que depende de la pared rectal e involucra músculos del periné, con afectación de la grasa de ambos glúteos en la región anal (fig. 1). El resto de los estudios de extensión fueron negativos para enfermedad a distancia; por lo que se decide por el equipo multidisciplinario, iniciar tratamiento con QT de inducción (adriamicina y gemcitabina), previa realización de colostomía derivativa en asa de sigmoides. Al tercer ciclo de la QT, la respuesta fue parcial; y se indicó exenteración pélvica total con vulvectomía; con hallazgos transoperatorios de tumor en región perineal con involucro de músculo glúteo mayor y músculo elevador del ano, sin plano de separación con el útero y la vejiga. Se realizó reconstrucción urinaria mediante conducto ileal y colostomía derivativa. La paciente evolucionó adecuadamente y sin complicaciones. En la pieza se corroboró la diferenciación a músculo liso, con grado alto, que midió 7×4×3cm, afectando desde el borde perineal hasta el septo recto-vaginal, con infiltración a músculos del esfínter anal y piel, así como invasión linfovascular y perineural, márgenes quirúrgicos sin neoplasia, el patrón de inmunohistoquímica fue similar; agregándose P53 y Ki-67, siendo positivos en el 1 y el 90% de las células neoplásicas, respectivamente (fig. 2).
Los leiomiosarcomas primarios de recto constituyen menos del 0.1% de los tumores colorrectales. En la literatura se han reportado no más de 290 casos; aunque no existe ninguna asociación firme entre leiomiosarcomas rectales y la irradiación pélvica7.
Debido a su rareza, los leiomiosarcomas y en general, los sarcomas radioinducidos son de difícil diagnóstico, además de tener un comportamiento más agresivo que aquellos no radioinducidos; son habitualmente identificados en estadios avanzados, generalmente son neoplasias de alto grado, y por lo tanto de pronóstico sombrío. Se debe tener una alta sospecha clínica, debido a la rareza del tumor, su amplia gama de presentación y descartar una recurrencia del tumor primario con morfología sarcomatoide; en nuestra paciente, esto fue corroborado por ausencia de marcadores de inmunohistoquímica como p16 y CKAE1/AE3, cabe destacar que a pesar de que con relativa frecuencia existe expresión marcada de p53 la cual se asocia a mutación del p53 y un peor pronóstico, esta no es indispensable para la presencia de este tipo de neoplasias. El tratamiento de elección y que provee los mejores resultados oncológicos en estos casos, es la cirugía, que es la única forma viable de tratamiento, ya que se ha descrito muy baja respuesta al tratamiento sistémico, además de la imposibilidad de re-irradiación1,8.
FinanciaciónNo se recibió financiamiento para llevar a cabo este artículo/estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.