Los ganglios celíacos (GC) pueden ser visualizados por ultrasonido endoscópico; juegan un papel importante en el manejo del dolor y son un sitio potencial de invasión tumoral neural extrapancreática.
ObjetivosEvaluar la frecuencia de visualización de los GC durante el examen de ultrasonido endoscópico, así como la factibilidad de este para identificar la invasión tumoral neural extrapancreática en pacientes con lesiones pancreáticas.
MétodosRevisamos retrospectivamente todos los estudios de ultrasonido endoscópico que se llevaron a cabo desde noviembre de 2007 a junio de 2010. Las imágenes de la región celíaca se presentaron a un endosonografista, quien reportó la presencia o ausencia de GC.
ResultadosIncluimos 31 casos. Se identificaron GC en 14 (45%) de los casos. El tamaño promedio fue de 10mm (rango 4-25mm) por±1mm (rango 1-7mm). En 2 casos se llevó a cabo una biopsia por aspiración con aguja fina y se reportaron cuerpos de células neurales; en un caso se observaron células malignas.
ConclusionesSe identificaron GC en el 45% de los casos. La biopsia por aspiración con aguja fina puede detectar invasión tumoral neural extrapancreática inesperada en neoplasias pancreáticas.
Celiac ganglia (CG) can be seen by endoscopic ultrasound; they play an important role in pain management and are a potential site for extrapancreatic tumor neural invasion.
AimsTo evaluate the frequency of CG visualization during endoscopic ultrasound examination and to evaluate the feasibility of this technique to identify extrapancreatic tumor neural invasion in patients with pancreatic lesions.
MethodsWe retrospectively reviewed all endoscopic ultrasound studies performed between November 2007 and June 2010. Images of the celiac region were presented to an endosonographer, who reported the presence or absence of CG.
ResultsWe included 31 cases. CG were identified in 14 (45%) cases. Average size was 10mm (range 4-25mm) by±1mm (range 1-7mm). In 2 cases, fine needle aspiration biopsy was performed and reported nerve cell bodies; in one case malignant cells were seen.
ConclusionsCG were identified in 45% of the cases. Fine needle aspiration biopsy can detect unanticipated extrapancreatic tumor neural invasion in pancreatic malignancies.
El plexo celíaco incluye los ganglios celíacos (GC), los cuales han sido de interés anatómico y clínico en la pancreatitis crónica y el cáncer pancreático debido a su papel en el manejo del dolor1,2 y como sitio potencial de invasión tumoral3.
El plexo celíaco se localiza a nivel de T12 y L1, anterior a la crura diafragmática, medial a las glándulas suprarrenales, y cerca de la aorta, entre el origen del tronco celíaco y la arteria mesentérica superior4.
Los GC pueden ser visualizados hasta en un 80% de los exámenes con ultrasonido endoscópico (USE). Sin embargo, este número varía entre las distintas publicaciones, dependiendo de la experiencia del endosonografista, del tipo de ecoendoscopio utilizado, y de factores relacionados con el paciente. Los GC se observan mejor con ecoendoscopios lineales y en mujeres sin historia previa de cirugía abdominal5.
La visualización de los GC por EUS6 ha permitido una inyección directa a GC individuales para llevar a cabo bloqueos o neurolisis en pacientes con trastornos pancreáticos que sufren de dolor intratable5,7. Además, se ha identificado invasión extrapancreática neural (INEP) que compromete los GC en casos de neoplasias pancreáticas8.
Durante el examen con USE, los GC aparecen como estructuras hipoecoicas oblongas o redondas, con bordes irregulares que contienen focos o bandas hiperecoicas. Su tamaño promedio oscila entre los 2 y los 20mm7.
Aquí reportamos la frecuencia de visualización de los GC por USE utilizando las características endosonográficas previamente publicadas5–7 y la identificación de la INEP microscópica por aspiración con aguja fina (BAAF) guiada por USE en pacientes con lesiones pancreáticas.
MétodosRevisamos de manera retrospectiva nuestra base de datos de pacientes que han sido referidos por lesiones pancreáticas para USE entre noviembre de 2007 y marzo de 2010. Identificamos 81 casos, sin embargo, se perdieron las imágenes de 50 casos durante el mantenimiento a nuestro sistema de almacenamiento, por lo que finalmente se incluyeron 31 casos con imágenes o cortos de vídeo de la región celíaca; los datos clínicos fueron registrados. Un solo endosonografista experto (MPL) realizó todos los estudios utilizando un ecoendoscopio lineal (GF-UC140P-AL5, Olympus America Inc., Center Valley, PA, EE. UU.).
Todos los pacientes firmaron un consentimiento informado para el procedimiento y recibieron sedación con propofol bajo una estricta monitorización por un anestesiólogo.
La presencia de GC se determinó mediante la identificación de patrones endosonográficos característicos de acuerdo con descripciones previas6,8,9, localizados a los lados de la emergencia de la arteria celíaca y/o si la BAAF de esa estructura mostró cuerpos neurales sin linfocitos.
Las imágenes o vídeos de cada caso fueron codificados y ordenados al azar y mostrados al endosonografista, quien se encontraba ciego al informe del examen y a los hallazgos, y que reportó la presencia o ausencia de GC, además de dar una descripción detallada de las estructuras observadas.
Para evitar sesgos de memoria no incluimos imágenes de casos que se llevaron a cabo dentro de los 6 meses previos al periodo del estudio.
ResultadosLas indicaciones para el USE fueron masas pancreáticas con un diagnóstico final de adenocarcinoma (18 casos, 58%) y quistes pancreáticos con características por USE indicativas de neoplasia papilar mucinosa intraductal de la rama lateral sin características preocupantes (13 casos, 42%).
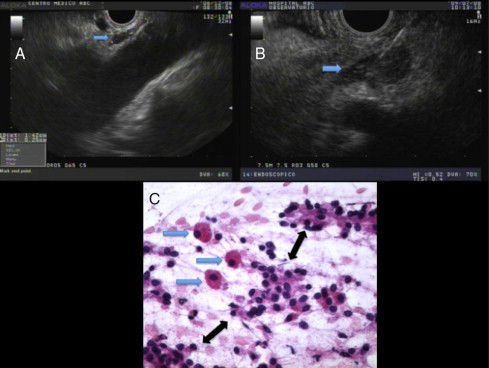
Ganglios celíacosLas estructuras consistentes con GC fueron visualizadas entre la arteria celíaca y la glándula suprarrenal izquierda en 14 casos (45%); 8 en casos benignos y 6 en casos malignos. Estas aparecían como estructuras alargadas y delgadas, que en su mayoría eran hipoecoicas, con un centro ligeramente hiperecoico y de bordes irregulares (fig. 1A). El tamaño promedio (DE) del eje fue de 10mm de largo±5mm (rango: 4-25mm), y su eje menor fue de 3mm±1mm (rango: 1-7mm).
A. La flecha azul muestra ganglios celíacos de apariencia normal. B. La flecha azul muestra ganglios celíacos aumentados de tamaño. Se realizó biopsia por aspiración con aguja fina bajo la sospecha de un ganglio linfático celíaco metastásico. C. Examen citológico de ganglio celíaco bajo aumento, que mostró un grupo de 3 células grandes, sin cohesión, que semejan células ganglionares (flechas azules), perfectamente dispersas entre grupos pequeños de células de adenocarcinoma (flechas negras). En un ambiente de equipo entrenado, este tipo de imagen podría ser interpretada con confianza como una infiltración neoplásica de los nervios ganglionares (hematoxilina-eosina, x400).
En 2 casos de masa pancreática, para excluir metástasis tumoral se llevó a cabo una biopsia con BAAF en las estructuras que, debido a su apariencia por USE, tenían la sospecha inicial de ser ganglios linfáticos celíacos (fig. 1B). La BAAF causó dolor transitorio, caracterizado por movimiento del paciente y un incremento en la frecuencia cardíaca.
El examen citológico in situ mostró la presencia de cuerpos neurales sin linfocitos y rodeados de células malignas en uno de los casos (fig. 1C), y solo cuerpos neurales sin linfocitos ni células malignas en otro caso.
DiscusiónEl dolor abdominal relacionado con la pancreatitis crónica o con el cáncer pancreático por lo general es secundario a anormalidades anatómicas y mecánicas1,2; en casos sin cambios anatómicos pancreáticos, el dolor usualmente resulta de la infiltración inflamatoria o neoplásica de las estructuras nerviosas intrapancreáticas y extrapancreáticas que regulan el dolor, incluyendo al plexo celíaco3,8.
El USE permite la visualización de los ganglios del plexo celíaco hasta en un 80% de los casos; en nuestro estudio, los visualizamos en aproximadamente el 45% de los casos. Esto podría estar en relación con errores de detección por haber perdido alrededor de 50 casos debido a eventualidades electrónicas y de computación, la utilización de un solo ecoendoscopio lineal, el hecho de que un solo endosonografista participó en el estudio, y el que hayamos basado nuestros hallazgos en las descripciones proporcionadas por otros autores6,7, en lugar de en la histología, que podría confirmar que en realidad estábamos observando GC. La BAAF de estas estructuras tiene indicaciones precisas: llevar a cabo un bloqueo o neurolisis intraganglionar, ninguno de los cuales estaba presente en nuestros casos.
Sin embargo, 2 casos con diagnóstico de cáncer pancreático fueron sometidos a BAAF de GC; esta se llevó a cabo bajo la sospecha de enfermedad metastásica a lo que parecían ser los ganglios línfáticos celíacos. Sorpresivamente, el examen citológico reveló abundantes cuerpos neurales en ambos casos y células malignas concomitantes en uno de los pacientes. En los 2 casos, durante la BAAF, se observó movimiento de los pacientes, que cesó al remover la aguja. Estos hallazgos clínicos, con la citología correspondiente, son signos de punción de estructuras nerviosas3,8.
La importancia de visualizar los GC durante el USE ha estado sujeta a debate. Existen múltiples estudios6,7, incluyendo un metaanálisis9 de pacientes con dolor abdominal secundario a pancreatitis crónica o cáncer pancreático, que reportaron que la neurolisis guiada por USE es un método efectivo y seguro con mejor control del dolor, en comparación con métodos radiológicos. Uno de los estudios incluidos en el metaanálisis llevó a cabo bloqueo intraganglionar celíaco y neurolisis en algunos pacientes, con resultados prometedores; esto llevó a la idea de que la inyección intraganglionar podría encontrarse relacionada con mejores resultados, en comparación con la técnica actual, aunque los números y el seguimiento fueron limitados5.
La invasión y la metástasis son componentes clave en la progresión del cáncer. Las vías más comunes de diseminación de un tumor son la sangre y los vasos linfáticos. Una vía diferente, y que, por lo común, se pasa por alto, es la invasión perineural. Esta, definida como la presencia de células cancerígenas en el espacio perineural, frecuentemente es utilizada por el cáncer pancreático y de próstata, y se asocia con recurrencia local y dolor3,8.
Tomando en consideración los reportes que evidencian que el plexo celíaco podría ser un sitio potencial de metástasis en el cáncer pancreático, así como el hecho de que la detección de la INEP ocurre con mayor frecuencia de lo sospechado, y se asocia con un pobre pronóstico y un mayor riesgo de recurrencia local del tumor10, parece que la detección de la INEP podría modificar su manejo, y todas estas razones explican por qué la identificación y el muestreo de los GC deben ser considerados durante el proceso de estadio del cáncer pancreático3,8.
Tras el reporte inicial de la INEP en el cáncer pancreático detectado por USE8, este es el segundo estudio que muestra hallazgos similares, aunque solo sea en un caso. Esta información limitada hace difícil determinar la relevancia clínica no solo de localizar los ganglios celíacos por USE, sino también de considerarlo como parte del proceso de estadificación en el cáncer pancreático. Si la INEP representa etapas tardías de la enfermedad o puede predecir una tasa más alta de recurrencia local en el cáncer pancreático aún se desconoce, pero es estimulante y merece ser explorado en estudios más grandes y bien diseñados.
ConclusionesUtilizando características de USE previamente publicadas, identificamos GC en el 45% de los casos. La visualización de GC por USE y BAAF podría identificar una INEP no sospechada en cáncer pancreático. El significado clínico y pronóstico de identificar CG y INEP en el cáncer pancreático necesita ser aclarado en estudios más grandes con diseño prospectivo.
FinanciaciónNo se recibió ningún apoyo financiero en relación con este artículo.
Conflicto de interesesLos autores declaran que no existe conflicto de interés.