La incontinencia fecal es una condición incapacitante con consecuencias devastadoras para los pacientes. Las opciones médicas y quirúrgicas no son muy satisfactorias, razón por la cual la medicina regenerativa ha sido considerada en este campo. En esta investigación se analizaron los efectos funcionales e histológicos posteriores al implante de células madre pluripotentes (CMP) en un modelo murino con esfinterotomía.
Material y métodosRatas hembra Wistar fueron sometidas a esfinterotomía y divididas en tres grupos. El grupo 1 (grupo control) fue tratado con 300μl de solución salina isotónica, el grupo 2 (tratamiento tardío) y el grupo 3 (tratamiento temprano) recibieron 50,000 CMP resuspendidas en 300μl de solución salina isotónica. Todos los animales fueron evaluados por medio de manometría anorrectal de alta resolución 24 h previo y posterior a la esfinterotomía y cada mes durante tres meses. Finalmente, las ratas fueron sacrificadas y se obtuvieron cortes histopatológicos del canal anal.
ResultadosTodos los grupos mostraron una disminución en las presiones anales de reposo y esfuerzo 24 h después de la esfinterotomía. Al tercer mes, se obtuvieron presiones anales más elevadas en los grupos tratados con CMP, observando una diferencia estadísticamente significativa en la presión anal de esfuerzo. En cuanto a los efectos histológicos, se observó restauración de la arquitectura microscópica, así como una disminución significativa de la respuesta inflamatoria en los grupos tratados con CMP.
ConclusiónEl implante de CMP mejora el tono anal y la microarquitectura histológica después de una esfinterotomía, presentando mejores resultados regenerativos cuando se implantan de manera temprana.
Fecal incontinence is a disabling condition with devastating consequences for the patients. Medical and surgical options are not very satisfactory, reason by which regenerative medicine has been considered in this field. In the present research, we analyzed functional and histologic effects after implanting pluripotent stem cells (PSCs) in a murine model with sphincterotomy.
Materials and methodsFemale Wistar rats were subjected to sphincterotomy and divided into three groups. Group 1 (control group) was treated with 300μL of balanced saline solution and group 2 (late treatment) and group 3 (early treatment) received 50,000 PSCs resuspended in 300μL of balanced saline solution. All animals were evaluated through high-resolution anorectal manometry 24hours before and after sphincterotomy and every month for three months. Finally, the rats were euthanized and histopathologic sections from the anal canal were obtained.
ResultsAll groups showed a decrease in resting anal pressure and squeeze anal pressure 24hours after sphincterotomy. At the third month, higher anal pressures in the groups treated with PSCs were detected. Regarding the histologic effects, the microscopic architecture was restored and there was a significant decrease in the inflammatory response in the groups treated with PSCs.
ConclusionPSCs implantation improves anal tone, as well as histologic structure, presenting better regenerative results when implanted as early treatment.
La incontinencia fecal (IF) es una condición incapacitante que afecta a un gran número de pacientes y tiene consecuencias devastadoras para la calidad de vida1. También es considerada un problema de salud pública de primera importancia en las sociedades en proceso de envejecimiento2. La prevalencia de IF es altamente variable y se reportan rangos que van del 5 al 15%. Una de las principales causas de esta variabilidad está relacionada con el hecho de que muchos pacientes se avergüenzan de su condición y no lo hablan con sus médicos. En general, la IF se define como el paso descontrolado continuo o recurrente, de materia fecal (más de 10ml) por lo menos durante un mes en una persona mayor de tres años de edad3.
La lesión del esfínter anal es una de las causas más comunes de la IF y ocurre como resultado de una lesión obstétrica del esfínter anal, de cirugía anorrectal o de trauma. En poblaciones geriátricas, se debe a la apoptosis espontánea de células musculares en los esfínteres anales2,4,5. La lesión muscular puede ser aislada o múltiple, ya sea en el músculo liso del esfínter anal interno, en el músculo estriado del esfínter anal externo, del músculo puborrectal. La manometría anorrectal es una herramienta útil para evaluar la función de los esfínteres en IF6,7.
Existen varias opciones de tratamiento médicas y quirúrgicas. Las alternativas terapéuticas incluyen fármacos que disminuyen la velocidad de la peristalsis o incrementan la consistencia de las heces, dietas especiales y biofeedback entre otras, pero solo mejoran la continencia fecal en un 50-60% de los pacientes8–10. Las opciones quirúrgicas incluyen la reparación de esfínteres anales, el implante de un esfínter anal artificial, la colostomía y la terapia de neuromodulación9,11. Desafortunadamente, ni las opciones médicas ni las quirúrgicas son muy satisfactorias, razón por la cual se ha considerado a la medicina regenerativa en este campo.
El reemplazo o regeneración de esfínter anal disfuncional por medio de terapia con células madre (CM) y técnicas de ingeniería de tejidos representa una gran promesa2, dada su capacidad de diferenciación multilinaje y autorrenovación. Así mismo, se ha reportado que dichas células tienen un efecto terapéutico a través de la secreción de factores bioactivos que dirigen a otras CM y a células progenitoras al área de la lesión12.
Varios estudios han mostrado la posible aplicación de diferentes tipos de CM mesenquimales (CMM) para restaurar las funciones del esfínter anal debido a sus propiedades antiapoptóticas, anticicatrización, de neovascularizantes e inmunomoduladoras2,13–16. Desafortunadamente, el número de células que puede ser generado por un único donante es limitado, debido a la capacidad restringida de proliferación a largo plazo de las CMM. El tiempo extendido de cultivo también incrementa el riesgo de inducir aberraciones cromosómicas y de perder su potencial de diferenciación17, resaltando la subsiguiente restricción de la capacidad de diferenciación. Además, las CMM pueden ser inadecuadas debido a condiciones de salud crónicas del paciente. En consecuencia, sugerimos el uso de CM pluripotentes (CMP), dado que tienen una mayor capacidad de diferenciación que las CMM, además de una retención a largo plazo de su estado pluripotente en cultivo. Las CMP de ratón no expresan moléculas MHC de clase I y II18, lo cual es ventajoso para su utilización en diferentes especies receptoras.
Hasta donde sabemos, no existen estudios experimentales que utilicen CMP en lesión de esfínter anal. Nuestro equipo de investigación ha demostrado la habilidad de las CMP para disminuir la respuesta inflamatoria y restaurar la integridad histológica posterior a trauma ocular19, y hemos propuesto la posibilidad de utilizar estas células en el trauma anal. En consecuencia, el presente estudio se enfocó en analizar los efectos funcionales e histológicos posteriores al implante de CMP de ratón en un modelo murino con esfinterotomía.
Materiales y métodosModelo murino con esfinterotomíaRatas albinas Wistar hembras de entre 10 y 12 semanas de edad fueron puestas en jaulas metabólicas en un ambiente de clima controlado a una temperatura de 21°C con un ciclo de luz/oscuridad de 12/12 h y tuvieron acceso libre y continuo a comida y agua. Para establecer el modelo de esfinterotomía en ratas, primero, bajo anestesia inhalatoria de isoflurano (dosis con base en respuesta), se les preparó la piel rasurando el área perineal y limpiando con solución de yodo. Después, se infiltró la región perineal con 1ml de lidocaína al 2% con 1:80,000 de epinefrina, y bajo visión directa, se realizó una lesión del canal anal hasta la línea dentada por medio de incisión de los esfínteres externo e interno a 2-3mm de profundidad. Se cerró la piel con sutura interrumpida 4-0 absorbible de Vicryl. Después de realizar la lesión, los animales recibieron tramadol 3mg/kg y enrofloxacina 5mg/kg. Se evaluó la fisiología de los esfínteres anales por medio de manometría 24 h pre y poslesión. Para la estandarización del modelo de esfinterotomía, se confirmó la lesión de canal anal por medio de análisis histopatológico.
Los procedimientos se realizaron con apego a los lineamientos de la Norma Oficial Mexicana para el uso y cuidado de animales de laboratorio (NOM-062-ZOO-1999) y el deshecho de residuos biológicos (NOM-087-ECOL-1995).
Cultivo de células madre pluripotentesSe sembraron CM embrionarias de ratón R1 (ATCC, Virginia, EE. UU.) en cajas de cultivo a una densidad de 50,000 células/cm2 sobre fibroblastos embrionarios de ratón mitóticamente inactivados, utilizando medio de cultivo de célula madre embrionaria de ratón (ATCC) suplementado con 15% de suero fetal bovino (ATCC), 0.1mM 2-mercaptoethanol (Invitrogen, California, EE. UU.), y 1,000 U/ml de factor inhibidor de leucemia de ratón (EMD Milipore, Darmstadt, Alemania). Las cajas de cultivo fueron incubadas a 37°C en una incubadora humidificada con 5% de CO2 y 95% de aire. Las CMP fueron separadas de la monocapa de fibroblastos embrionarios de ratón mitóticamente inactivados antes del implante, enfatizando que se utilizaron entre 4 y 8 pasajes celulares.
Previo al implante, las características morfológicas y fenotípicas de las CMP fueron determinadas por medio de microscopía e inmunofluorescencia, como fue reportado anteriormente20, para confirmar el estado pluripotente de las células.
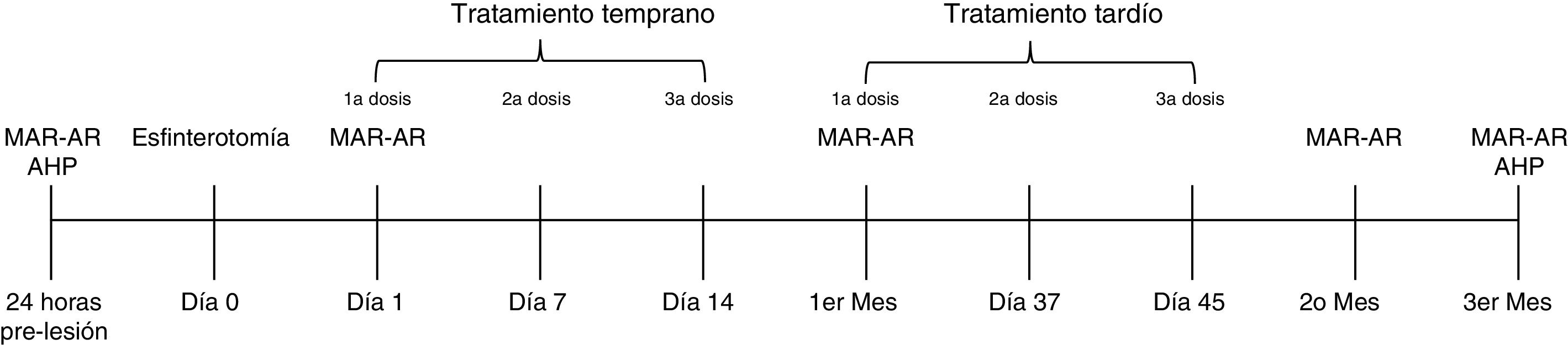
Implante de células madre pluripotentes de ratónDado que es conocido que existe una respuesta diferente con relación al momento de aplicación del tratamiento (tratamiento tardío o temprano posterior a lesión), dividimos aleatoriamente a las 43 ratas Wistar albino hembras en tres grupos: un grupo control (n = 13) y dos grupos experimentales (n = 15). De los grupos experimentales, el grupo 2 correspondió a los animales que recibieron el tratamiento tardío y el grupo 3 a los que recibieron el tratamiento temprano. Todos los miembros de los grupos fueron sometidos a esfinterotomía, como se describió anteriormente, y a continuación recibieron una inyección intramuscular de solución salina balanceada (SSB) o de CMP en el esfínter anal, de acuerdo a lo correspondiente por grupo (fig. 1). El grupo 1 (grupo control) recibió 0.3ml de SSB a los 30, 37 y 45 días después de la lesión. El grupo 2 (tratamiento tardío) recibió 50,000 CMP resuspendidas en 0.3ml de SSB a los 30, 37 y 45 días después de la lesión y las ratas en el grupo 3 (tratamiento temprano) fueron tratadas con 50,000 CMP resuspendidas en 0.3ml de SSB a las 24 h y a los 7 y 14 días posteriores a la lesión. La cantidad de CMP y el momento del tratamiento fueron establecidos de acuerdo con trabajos anteriores, en los cuales no existieron complicaciones o efectos secundarios19.
Metodología experimental, 24 h antes de la esfinterotomía, se realizaron manometría anorrectal de alta resolución (MAR-AR) y análisis histopatológico (AHP). Posterior a la esfinterotomía (día 0), el grupo de tratamiento temprano recibió el tratamiento experimental a los días 1, 7 y 14 después de la lesión, y el grupo de tratamiento tardío fue tratado al primer mes y en los días 37 y 45 posteriores a la lesión. Las presiones anales fueron evaluadas a lo largo de un periodo de 3 meses. La MAR-AR se realizó un día después de la lesión al igual que 1, 2 y 3 meses después de la lesión. Finalmente, 3 meses después de la lesión y el comienzo del tratamiento, los animales recibieron eutanasia y el canal anal de cada animal fue extirpado para realizar el AHP.
La manometría anorrectal de alta resolución (MAR-AR) fue realizada utilizando el ManoScan 360 HR ® con 12 sensores circunferenciales colocados a intervalos de 0.6cm (Sierra Scientific Instruments, EE. UU.). Las medidas de presión de esfínter anal (en reposo y esfuerzo) fueron evaluadas en ratas reactivas que estuvieron sujetas con un inmovilizador de plástico acrílico durante el proceso de medición. La presión anal de reposo (PAR) fue considerada como tono sostenido por lo menos durante 3 segundos y la presión anal de esfuerzo (PAE) fue medida cuando existió un incremento en la presión de línea base por un estímulo reactivo espontáneo. La PAE máxima fue la mayor presión alcanzada, incluso si no fue sostenida. Los datos manométricos fueron analizados utilizando el software de análisis ManoView (Sierra Scientific Instruments Inc.). Las presiones anales fueron registradas 24 h previo a la esfinterotomía, 24 h después de la lesión, y después cada mes durante tres meses (fig. 1), utilizando un globo conectado a un grabador digital.
Análisis histopatológicoTres meses después de la esfinterotomía y el comienzo del tratamiento, se les practicó eutanasia a las ratas y el canal anal de cada rata fue extirpado. Las muestras obtenidas fueron fijadas en formalina neutra amortiguada al 10% (Sigma-Aldrich, Darmstadt, Alemania) y a continuación se embebieron en parafina. Se obtuvieron secciones delgadas (3μm) utilizando un microtomo (Ecoshel, EE. UU.) y se montaron en laminillas. Finalmente, las secciones histopatológicas fueron teñidas con tricrómico de Masson y fueron observadas por medio de un microscopio óptico (TiU Eclipse, Nikon, Japón). Los grados de integridad anatómica fueron designados como alteraciones microarquitectónicas ligeras, moderadas o severas, considerando la integridad del mecanismo del esfínter y la disposición de las fibras de colágeno, al igual que el entrelazado de las fibras de colágeno con las fibras musculares.
Se sabe que una respuesta inflamatoria granulomatosa es un tipo de inflamación crónica caracterizada por conjuntos focales de macrófagos, células epitelioides y células multinucleadas gigantes, razón por la cual evaluamos la respuesta inflamatoria crónica, utilizando los siguientes criterios para el número de granulomas por campo: ligera (1-3 granulomas), moderada (4-6 granulomas) y severa (> 7 granulomas).
Análisis estadísticoPara el análisis estadístico de las presiones anales, se establecieron las diferencias entre los grupos con tratamiento y el periodo de tratamiento para cada grupo utilizando el análisis de varianza de un factor (ANOVA) y el test de Bonferroni. La prueba de chi cuadrado fue utilizada para el análisis histológico. Se consideró una p < 0.05 como estadísticamente significativa.
El Comité Institucional de Ética para la Investigación con Animales de la Escuela Militar de Medicina aprobó el protocolo. Todos los experimentos fueron revisados y aprobados por el comité de ética adecuado y fueron realizados siguiendo los estándares éticos estipulados en la Declaración de Helsinki de 1964.
ResultadosPresiones de esfínter analComo se mencionó anteriormente, la esfinterotomía fue realizada en todas las ratas sin complicaciones (fístulas, abscesos, infección de herida quirúrgica, sepsis).
Para la estandarización de la esfinterotomía obtuvimos una PAR previa a la lesión de 59 ± 12.7mmHg y una PAE de 120.39 ± 52.6mmHg. Veinticuatro h después de la lesión, la PAR y la PAE disminuyeron a 38.14 ± 10.35 y 69.02 ± 31.73mmHg respectivamente.
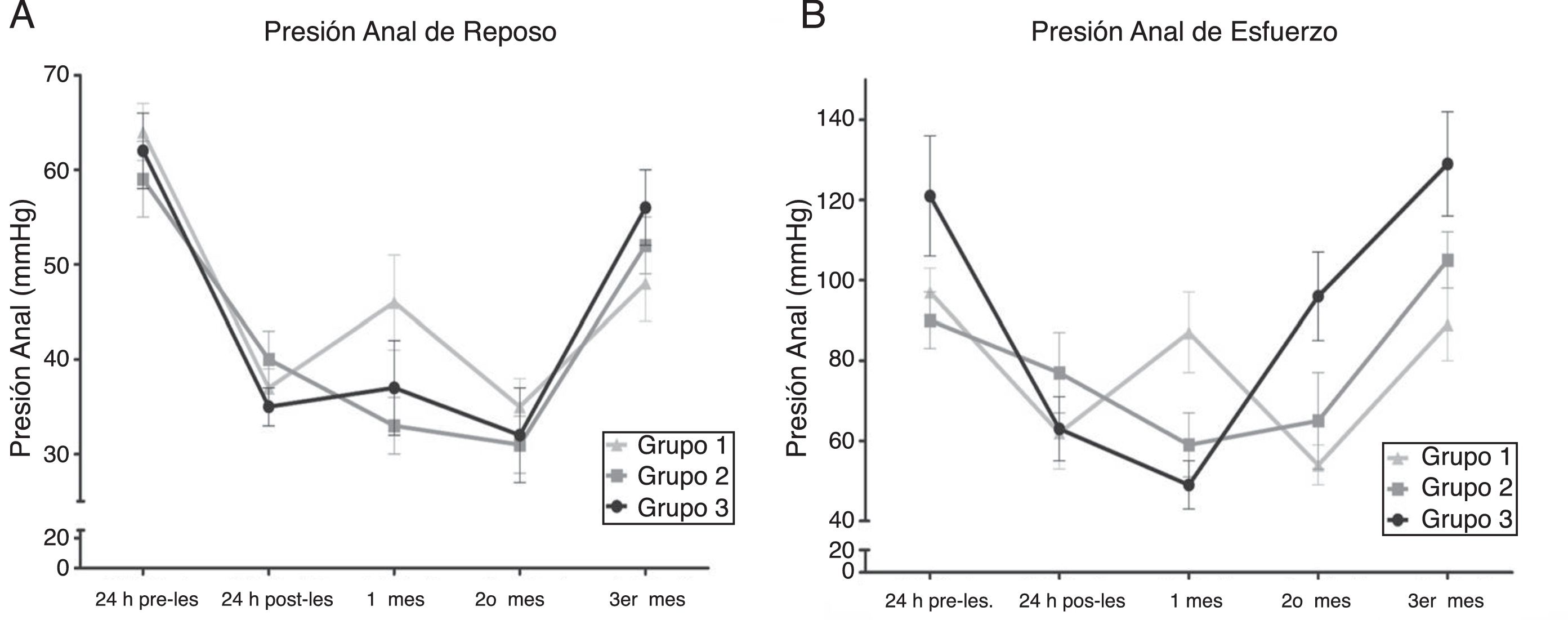
Los resultados de los grupos con tratamiento están resumidos en la tabla 1. Los resultados fisiológicos mostraron una disminución en PAR y PAE en todos los grupos 24 h después de la lesión. Sin embargo, un mes después de la lesión, existió un incremento en PAR y PAE en el grupo 1, pero una ligera disminución en los grupos 2 y 3. Al segundo mes, todos los grupos presentaron una disminución no significativa en PAR, pero los grupos 2 y 3 mostraron un incremento significativo en PAE, a diferencia de la disminución en el grupo control. Finalmente, al tercer mes, los grupos presentaron la siguiente PAR: grupo control 48mmHg, grupos 2 y 3 con tratamiento de CMP, 52mmHg y 56mmHg respectivamente. Aunque detectamos una PAR más alta en los grupos con tratamiento, la diferencia entre grupos no fue estadísticamente significativa. Por otro lado, existió una diferencia significativa con relación a la PAE. El grupo control tuvo 89mmHg y los grupos 2 y 3 tuvieron 105mmHg y 129mmHg respectivamente, y la diferencia en las presiones más altas en los grupos con tratamiento (fig. 2) en comparación con el valor más bajo del grupo control fue estadísticamente significativa (p < 0.05).
Presiones de esfínter anal (mmHg)
| Grupo | 24 h prelesión X ± SE | 24 h poslesión X ± SE | Un mes poslesión X ± SE | Dos meses poslesión X ± SE | Tres meses poslesión X ± SE | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| PAR | PAE | PAR | PAE | PAR | PAE | PAR | PAE | PAR | PAE | |
| 1 | 64 ± 3 | 97 ± 6 | 37 ± 2 | 62 ± 9 | 46 ± 5 | 87 ± 10 | 35 ± 3 | 54 ± 5 | 48 ± 4 | 89 ± 9 |
| p < 0.05 | ||||||||||
| 2 | 59 ± 4 | 90 ± 7 | 40 ± 3 | 77 ± 10 | 33 ± 3 | 59 ± 8 | 31 ± 3 | 65 ± 12 | 52 ± 3 | 105 ± 7 |
| p < 0.05 | ||||||||||
| 3 | 62 ± 4 | 121 ± 15 | 35 ± 2 | 63 ± 8 | 37 ± 5 | 49 ± 6 | 32 ± 5 | 96 ± 11 | 56 ± 4 | 129 ± 13 |
| p < 0.05 | ||||||||||
| p=0.6 | p=0.1 | p=0.5 | p=0.4 | p=0.1 | p < 0.05 | p=0.8 | p < 0.05 | p=0.4 | p < 0.05 | |
La presión anal en reposo (PAR) y la presión anal de esfuerzo (PAE) no fueron significativamente diferentes entre grupos (p>0.05) previo a la lesión y 24 h posteriores a la lesión. Sin embargo, la PAR fue más alta tres meses después de la lesión en los animales tratados con células madre pluripotentes en comparación con los tratados con solución salina balanceada. Al contrario, la PAE fue significativamente mayor en los grupos con tratamiento, con PAE más alta en el grupo 3 (p<0.05).
Presiones anales. A) Presión anal de reposo (PAR). B) Presión anal de esfuerzo (PAE). La PAR y PAE no fueron significativamente diferentes entre los grupos (p>0.05), 24 previo y 24 h posterior a la lesión. Sin embargo, la PAR fue más alta 3 meses después de la lesión en los animales tratados con CMP, en comparación con las tratadas con SSB (p>0.05). En contraste, la PAE fue significativamente mayor en los grupos con tratamiento, con una PAE más alta en el grupo 3 (p<0.05).
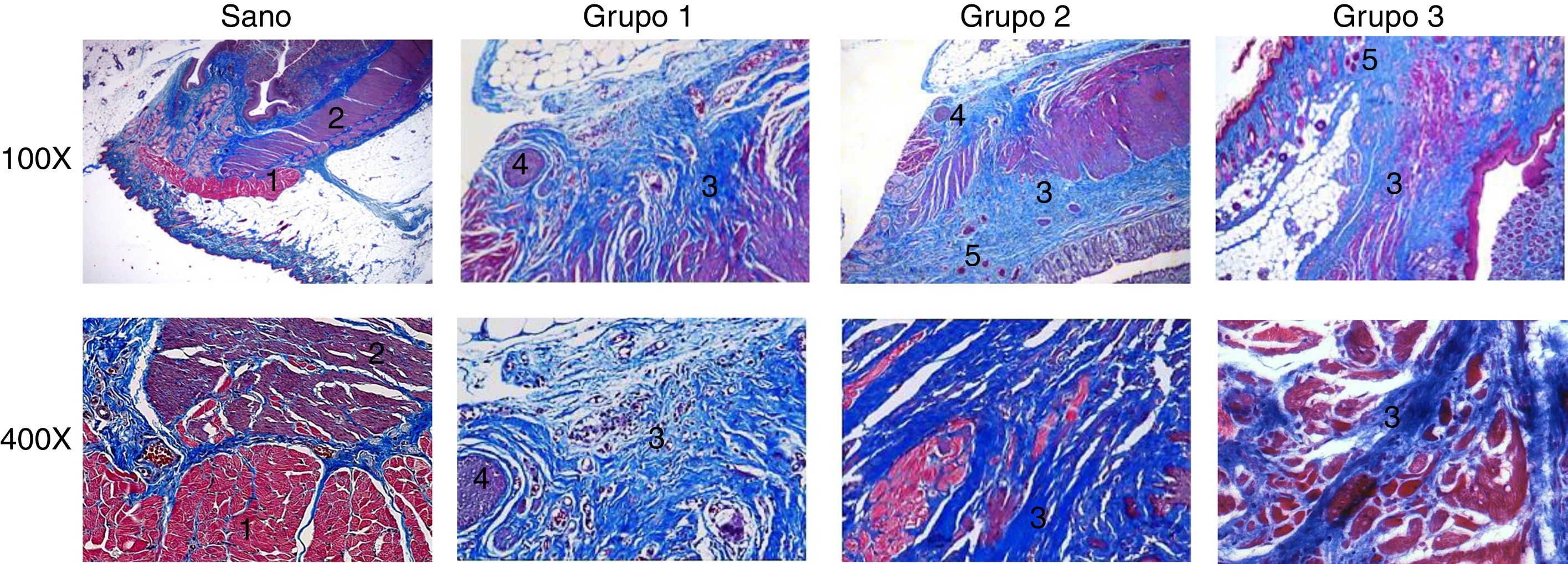
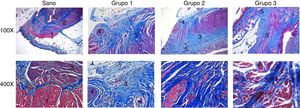
Respecto a los resultados histológicos (fig. 3), la integridad anatómica y la respuesta inflamatoria fueron evaluados. Una histología normal de un canal anal saludable consiste en anillos de tejido muscular con fibras musculares bien definidas, además de un esfínter externo voluntario y un esfínter interno involuntario. El esfínter externo está compuesto de fibras musculoesqueléticas1 y el esfínter interno está compuesto de músculo liso2.
Análisis histopatológico. Secciones histopatológicas teñidas con tricrómico de Masson. Comparación de la microestructura entre el tejido sano y el tejido lesionado de los grupos que fueron tratados. Los grupos 1, 2 y 3 presentaron alteraciones microarquitectónicas y respuesta inflamatoria severas, moderadas y ligeras respectivamente. 1: fibras musculares esqueléticas; 2: músculo liso; 3: fibras de colágeno; 4: granulomas; 5: capilares.
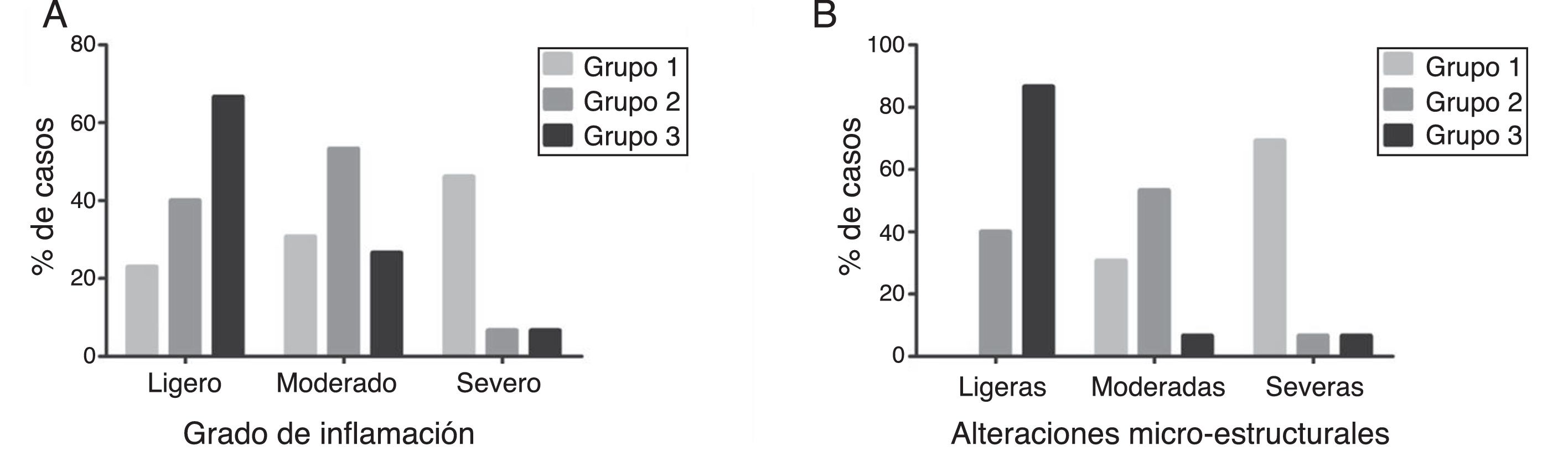
La mayoría de las ratas en el grupo 1 tenían alteraciones microarquitectónicas severas (69.23%) y una respuesta inflamatoria severa (46.15%), mostrando una pérdida total de la arquitectura en ambos esfínteres, con un patrón irregular de fibras de colágeno3 intercaladas con músculo liso y esquelético. Hubo un incremento en la deposición de colágeno que produjo una coloración azul intensa, indicando tejido cicatricial en el área del defecto. También se observaron abundantes granulomas4. La mayoría de los animales del grupo 2 presentaron alteraciones microarquitectónicas moderadas (53.3%) y respuesta inflamatoria moderada (53.3%), evidentes en las bandas gruesas y desorganizadas de colágeno maduro3, aunque con menor cantidad de fibras de colágeno que las observadas en el grupo 1. También existió neoformación capilar abundante5, al igual que un número moderado de granulomas4. En el grupo 3, la mayoría de las ratas tuvo distorsión arquitectónica del canal anal ligera (86.6%), al igual que una respuesta inflamatoria ligera (66.6%). También hubo una presencia de fibras de colágeno aparentemente más organizadas3 entremezcladas con fibras musculares y la neoformación capilar5 fue todavía evidente. En la figura 4 se muestra que el grupo 3 tuvo mejores resultados, en los cuales la mayoría de los casos presentó inflamación y alteraciones microestructurales ligeras.
Análisis del grado de inflamación y alteraciones microestructurales. A) Grado de inflamación. B) Cambios microestructurales. Se observó una disminución significativa en el nivel de inflamación, al igual que en la restauración de la integridad anatómica en los grupos tratados con células madre pluripotentes.
El empleo de CM en la medicina regenerativa se está convirtiendo en una opción terapéutica para las enfermedades crónico-degenerativas, al igual que para procesos sintomáticos de enfermedad benigna21, tales como la IF. Algunos estudios proponen la terapia celular como tratamiento alternativo para la lesión de esfínter anal14,15 y la mayoría de ellos utilizan CMM. No existe evidencia del uso de CMP evaluado por medio de MAR-AR en IF. En nuestra investigación, implantamos CMP de ratón como tratamiento temprano y tardío en ratas con esfinterotomía, evaluando fisiología e histopatología por medio de MAR-AR y microscopía óptica respectivamente.
No existen dosis o vías de administración de CM bien establecidas, debido a que la investigación sobre CM es extensa e incluye diferentes tipos de CM, como CM derivadas de tejido adiposo, CM de médula ósea y CM embrionarias (CME), entre otras. En consecuencia, se han utilizado diferentes vías de administración y dosis de CM, de 10,000 a 500,000 en el caso de las últimas. Por ejemplo, Kim et al. establecieron que existió un efecto significativo en ratones con pulmón enfisematoso con la inyección intravenosa de solamente 50,000 CMM22. Bottai et al. reportaron que dos dosis intravenosas de 500,000 CME en la vena de la cola en ratones con lesión en la médula espinal por contusión promovieron la recuperación de la función motora23. Salcedo et al. demostraron que existió un incremento significativo en la presión anal con una sola dosis de 500,000 CMM inyectada en el esfínter anal y seis dosis de 500,000 CMM inyectadas por vía intravenosa en ratas con esfinterotomía15. En trabajos previos hemos reportado que las inyecciones intravítreas de 50,000 CME pluripotentes son muy útiles para el tratamiento de trauma ocular, restaurando la microarquitectura y disminuyendo la respuesta inflamatoria19.
Con relación a las diferentes vías de administración, Sudulaguntla et al. declararon que la vía intravenosa es la más fácil, pero su principal desventaja es que solo aproximadamente un 3% del gasto cardiaco circulará por minuto a través del ventrículo izquierdo. También es limitada de forma importante por el efecto de atenuación de primer paso transpulmonar observado en las células. Sobre todo, existen algunos tipos de células principales, como los mioblastos esqueléticos, que tienen la desventaja de potencia emboligénica cuando son administradas sistémicamente24. Con base en la información anterior y nuestra propia experiencia, decidimos inyectar tres dosis de 50,000 CMP en el esfínter anal para el presente estudio.
Respecto a los resultados de la presión anal, se debe mencionar que los parámetros de manometría y la estructura del canal anal de ratas normales son similares a los de los humanos, porque las ratas cuentan con una presión de reposo y reflejo rectoanal en manometría, y esfínteres anales interno y externo25. En el presente estudio, la estandarización de la esfinterotomía mostró una PAR previa a la lesión de 59 ± 12.7mmHg y una PAE de 120.39 ± 52.6mmHg en ratas saludables, lo cual es similar a lo reportado por Hosokawa et al., quienes reportaron una PAR máxima de 70.86 ± 10.39mmHg en ratas adultas. Nuestros resultados también coinciden con Kang et al., quienes declararon que la presión de reposo del canal anal humano promedio es 51.4mmHg determinado por medio de manometría anorrectal con perfusión de agua y 51.9mmHg por medio de MAR-AR, y la presión de esfuerzo máxima promedio determinada con manometría anorrectal con perfusión de agua es 146.3mmHg y 137.7mmHg con MAR-AR. Sin embargo, es probable que la MAR-AR proporcione mejor información fisiológica y requiere de un menor tiempo de medición en comparación con la manometría anorrectal con perfusión de agua25,26.
Con respecto a las presiones registradas después de la lesión, detectamos una disminución significativa de más del 50% con relación a los niveles normales de PAR y PAE a las 24 h posterior a lesión. Estos resultados son similares a los porcentajes reportados por Cerdán et al. y Chowcat et al. En sus estudios con humanos, reportaron una reducción significativa en presión de esfínteres, con una disminución del 50% con relación a los niveles normales después de la esfinterotomía27,28.
Al primer mes posterior a la lesión, el grupo control presentó un incremento en PAR y PAE, probablemente debido a la respuesta inflamatoria. Sin embargo, los grupos experimentales mostraron una disminución en vez de incremento. Es sabido que las CM tienen propiedades inmunosupresoras e inmunomoduladoras y la capacidad de las CMP para limitar la respuesta inflamatoria se ha demostrado en múltiples estudios con animales29. Bottai et al. inyectaron CME en la vena de la cola de ratas después de inducir una lesión por contusión en la médula y reportaron una respuesta inflamatoria disminuida en los animales que recibieron CME, observando una disminución significativa en la invasión del número de macrófagos y neutrófilos23.
Respecto al tiempo para evaluar los efectos del implante de CMP, Salcedo et al. realizaron una esfinterotomía en ratas y 24 h posterior a la lesión cada animal recibió 2 millones de CMM, ya fuera por vía intramuscular en el esfínter anal o por vía intravenosa en la vena de la cola. Las presiones anales de esfínter fueron registradas 10 días después de la lesión, evaluando una fase temprana de la recuperación y reportaron un incremento en las presiones anales14. En otro estudio similar, reportaron que tanto el tratamiento intravenoso como el intramuscular con CMM después de una lesión causó un incremento en la presión anal sostenida a las 5 semanas15. En nuestro estudio, evaluamos las presiones anales a los tres meses, dado que 5 semanas no es suficiente tiempo para evaluar la restauración de las fibras musculares y la recuperación funcional subsiguiente. Como mencionamos anteriormente, al primer mes posterior a la lesión se reportó una disminución en las presiones anales en vez de un incremento, pero tres meses después de la lesión se mostró un incremento significativo en ambas presiones en ambos grupos tratados con CMP. Aunque no se logró significación estadística respecto a PAR, los grupos tratados con CMP presentaron presiones más altas. Sin embargo, respecto a PAE, existió un incremento estadísticamente significativo en los grupos tratados con CMP (grupo 2, de 59mmHg al mes posterior a la lesión a 105mmHg al tercer mes, y el grupo 3 de 37mmHg al mes posterior a la lesión a 129mmHg al tercer mes).
Es importante mencionar que nuestros resultados también concuerdan con los obtenidos por Inoue et al. quienes reportaron no existir diferencia en PAR entre los dos grupos previo a la lesión. Además, también reportaron una disminución significativa en PAR en ambos grupos a las 24 h posteriores a la lesión, para finalmente mostrar una mejora en PAR en el grupo tratado con láminas de CM de origen adiposo. En nuestros resultados, no existió significación estadística en los valores de PAR entre los grupos antes de la esfinterotomía, y 24 h después de la lesión también reportamos una disminución significativa en la PAR en ambos grupos. De igual manera, mostramos una mejoría en PAR en los grupos tratados con CMP. Sin embargo, Inoue et al. desarrollaron su modelo de esfinterotomía al remover el semicírculo izquierdo de los esfínteres anales externo e interno en las ratas y evaluaron PAR utilizando un sensor de silicón medidor de tensión microminiatura montado en un extremo30.
El daño tisular puede ser causado por diversos estímulos, incluidos infecciones, reacciones autoinmunes, toxinas, radiación, o lesión mecánica. En nuestro estudio, utilizamos una lesión mecánica para afectar las fibras musculares. El proceso de recuperación normalmente implica dos fases distintas: una fase regenerativa, en la cual las células lesionadas son reemplazadas por células del mismo tipo, y una fase conocida como fibroplasia o fibrosis, en la cual el tejido conjuntivo reemplaza al tejido parenquimal normal. Así, la reparación de tejido dañado debe ocurrir al reemplazar células parenquimales no regeneradas con tejido conjuntivo, lo cual a su vez lleva a fibrosis y cicatrización significativas, lo que puede comprometer la función. En consecuencia, el desarrollo de nuevas estrategias terapéuticas que limiten el progreso de la fibrosis sin afectar de manera adversa el proceso de recuperación general representarían un avance tecnológico significativo31. También se ha reportado que el principal impedimento para la sanación muscular óptima después de una lesión es la fibrosis, la cual se define como una sobreproliferación crónica anormal e irresoluble de componentes extracelulares de la matriz, lo que interfiere con la regeneración muscular y causa pérdida de función muscular32. Esto podría estar relacionado con nuestros resultados fisiológicos, donde los grupos tratados con CMP presentaron presiones más altas, mientras que demostraban un defecto de esfínter mínimo, al igual que una tinción disminuida de colágeno mostrando nuevas fibras musculares.
Los resultados histológicos de nuestro estudio coinciden con los de Salcedo et al. Observamos alteraciones microarquitectónicas severas en el grupo 1 (grupo control) y cambios en microarquitectura moderados y ligeros en los grupos 2 y 3 respectivamente. Salcedo et al. reportaron que 5 semanas después del tratamiento, se observó un defecto significativo en el esfínter en los grupos sin tratamiento y de solución salina, caracterizados por un incremento en la deposición de colágeno, en contraste con el grupo tratado con CMM, el cual mostró un defecto de esfínter mínimo y menor tinción de colágeno15. Nuestros resultados histológicos también concuerdan con los de Lorenzi et al., quienes realizaron una esfinterotomía en ratas, repararon ambos esfínteres anales y los trataron con inyecciones salinas o con CMM, de acuerdo con el grupo de estudio. Treinta días más tarde, se realizaron análisis histológicos y estos revelaron una disminución significativa en tejido muscular en el sitio de la reparación después de la lesión en esfínter en el grupo que recibió inyecciones salinas, mientras que se identificaron nuevas fibras musculares en el grupo que recibió CMM33. En nuestro estudio también observamos nuevas fibras musculares en el grupo 3, lo cual podría estar relacionado con un proceso de regeneración.
De igual manera, nuestros resultados coinciden con los reportados por Inoue et al. En su grupo control, 4 semanas tras la esfinterotomía, el sitio del procedimiento fue reemplazado solamente por fibras de colágeno y la cicatriz del músculo del esfínter era evidente. A diferencia de esto, en el grupo tratado con láminas de CM de origen adiposo, la cicatriz del músculo del esfínter era casi imperceptible, indicando una posible relación con regeneración del músculo de esfínter anal30. En nuestro caso, tres meses después de la esfinterotomía y el comienzo del tratamiento, detectamos señas de regeneración caracterizadas por fibras de colágeno organizadas, entremezcladas con fibras musculares y neoformación capilar.
En cuanto a la respuesta inflamatoria, la respuesta inflamatoria granulomatosa es un tipo particular de inflamación crónica caracterizada por colecciones focales de macrófagos, células epitelioides y células multinucleadas gigantes. Se sabe que existe un recambio constante de macrófagos dentro de cualquier lesión, con células que mueren siendo reemplazadas por nuevas reclutas de la circulación o a través de mitosis local. Entonces, una reacción inflamatoria granulomatosa frecuentemente resulta en daño tisular durante la fase activa, y en fibrosis durante el proceso de sanación34.
Ennis et al. declararon que el ambiente regenerativo de sanación óptimo es posible cuando la inflamación es minimizada pero no ausente, razón por la cual los tratamientos dirigidos a la supresión inmune pueden mejorar la sanación. Además, se sabe que las CMM pueden «sentir» el grado de inflamación en el microambiente y responder liberando factores de crecimiento y citocinas para reducir el proceso inflamatorio, utilizando señales bioquímicas35. Esto podría haber ocurrido en nuestro estudio: la inflamación disminuyó en los grupos tratados con CMP, permitiendo la restauración de las fibras musculares.
Los resultados de la restauración recuperan cierto grado de la estructura y función originales del músculo. Es esencial comprender que el proceso de regeneración requiere de la supervivencia de la membrana basal y de las CM de tejido, de los eventos celulares de inflamación, revascularización e inervación, y del proceso de miogénesis donde se forma el nuevo músculo36. A este respecto, dado que en nuestro estudio las CM fueron aplicadas al área lesionada, nosotros proporcionamos y modulamos algunos de los factores necesarios para estimular un proceso de regeneración satisfactorio.
En el presente trabajo, también evaluamos el mejor momento para la administración de CMP, comparando el tratamiento temprano con el tratamiento tardío. Salcedo et al. reportaron que el factor-1 derivado de quimiocina estromal y la proteína-3 quimiotáctica de monocitos son regulados al alza en su grado máximo 24 h posterior a una lesión de esfínter anal directa. Enseguida declinan y ya no están presentes a las 3 semanas después de la lesión15. Encontramos que existieron mejores resultados regenerativos cuando las CMP fueron implantadas como tratamiento temprano.
De igual manera, es importante mencionar que la investigación realizada con humanos se está desarrollando actualmente, con trabajos como el de Sarveazad et al. y Andjelkov et al., quienes trataron a pacientes con defectos de esfínter utilizando CM estromales de origen adiposo. Sarveazad et al. reportaron que dos meses después de la cirugía, se observó la presencia de islas dispersas en el sitio de reparación por medio de sonografía endorrectal, comparando con el grupo control37, y Andjelkov et al. declararon que después de tres meses todas las fisuras anales habían sanado38, lo cual podría ser comparado con los procesos de cicatrización mostrados en los análisis histopatológicos de nuestro estudio.
En conclusión, los animales con esfinterotomía tratados con un implante temprano de CMP mostraron un mejor proceso de regeneración, caracterizado por restauración histológica y fisiológica. Existió una disminución en la tinción de colágeno, mostrando nuevas fibras musculares, seguidas de una mejoría en la función del canal anal, presentando presiones anales más altas.
El presente trabajo refleja los avances realizados en la medicina regenerativa con relación a la terapia celular y su uso en cirugía regenerativa para mejorar el tratamiento de la IF y otras condiciones colorrectales. Sin embargo, es necesario realizar más estudios sobre la dosificación, la biodistribución, la integración de las CMP en el esfínter anal, y seguimientos de largo plazo, antes de pasar a la siguiente etapa.
Responsabilidades éticasProtección de personas y animalesTodos los procedimientos que involucraron animales fueron aprobados por el Comité de Ética para la Investigación Animal de la Escuela Médico Militar (SIDM-09). Los lineamientos de la Norma Oficial Mexicana para el uso y cuidado de los animales de laboratorio (NOM-062-ZOO-1999) y el deshecho de residuos biológicos (NOM-087-ECOL-1995) fueron observados.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
AgradecimientosLos autores desean agradecer al Tte. Cor. M. V. Alejandro Camacho Ibarra, veterinario de la Escuela Militar de Medicina sus importantes contribuciones a la presente investigación.