Los seudoquistes pancreáticos se definen como colecciones pancreáticas o peripancreáticas homogéneas, no asociadas a tejido necrótico, rodeadas de tejido fibroso o de granulación sin epitelio. El manejo se ha clasificado en quirúrgico (convencional y laparoscópico), y no quirúrgico (endoscópico y radiológico). El objetivo es describir nuestra experiencia inicial en el manejo de un seudoquiste pancreático, con una cistogastroanastomosis posterior laparoscópica, realizada en la Clínica de Páncreas del Hospital General “Dr. Manuel Gea González”, de la Ciudad de México. La cirugía laparoscópica de páncreas es relativamente nueva, las nuevas técnicas e instrumentales han permitido su desarrollo. Nuestra técnica tiene ventajas prácticas confirmadas por otros autores, como una hemostasia sencilla, un ángulo de visión amplio que permite una adecuada necrosectomía, la realización de una anastomosis sin necesidad de engrapadoras, y la posibilidad de resolver otras patologías intraabdominales asociadas, como en este caso.
Pancreatic pseudocysts are defined as homogeneous pancreatic or peripancreatic collections that are not associated with necrotic tissue and are surrounded by granulated or fibrous tissue with no epithelium. Management has been classified as surgical (conventional and laparoscopic) and nonsurgical (endoscopic and radiologic). The aim of this report is to describe our initial experience in the management of a pancreatic pseudocyst by means of laparoscopic posterior cyst-gastrostomy anastomosis, performed at the Pancreas Clinic of the Hospital General “Dr. Manuel Gea González” in Mexico City. New techniques and instrumentation have contributed to the relatively recent development of laparoscopic pancreatic surgery. Our technique has practical advantages that have been confirmed by other authors, such as simple hemostasis, a wide viewing angle enabling adequate necrosectomy, anastomosis that does not require the use of staples, and the possibility of resolving other associated intra-abdominal pathologies, as in this case.
Las colecciones pancreáticas y peripancreáticas secundarias a un evento de pancreatitis aguda (PA), de acuerdo a la revisión de la Clasificación de Atlanta de 1.992 por el Acute Pancreatitis Working Group, se dividen en 4 categorías mayores: colecciones agudas, colecciones agudas posnecróticas, seudoquistes pancreáticos y necrosis pancreática encapsulada; con datos de infección o sin ella1. Los seudoquistes pancreáticos se definen como colecciones pancreáticas o peripancreáticas homogéneas, no asociadas a tejido necrótico, rodeadas por tejido fibroso o de granulación sin epitelio, secundario a PA, crónica o trauma pancreático2,3. Representan la causa más común de lesiones quísticas del páncreas, con una incidencia de 0,5 a 1,0 por cada 100.000 adultos al año2.
Su historia natural fue descrita por Bradley y Yeo2. La decisión de manejo antes de 1.990, se basó en la “regla de los 6” de estos autores1–3. Las indicaciones actuales de manejo se fundamentan en la presencia de síntomas (dolor abdominal, saciedad temprana, pérdida de peso, fiebre persistente), complicaciones (infección, obstrucción gástrica o biliar, ruptura, trombosis vascular o formación de pseudoaneurismas) o incremento de tamaño del seudoquiste pancreático1,2. Las opciones de tratamiento de los seudoquistes pancreáticos se clasifican en quirúrgicas (convencionales y laparoscópicas), y no quirúrgicas (endoscópicas y radiológicas)4–6.
El propósito del presente reporte es describir nuestra experiencia inicial en el manejo de un seudoquiste pancreático secundario a pancreatitis biliar, con cistogastroanastomosis con abordaje retrogástrico, colecistectomía con colangiografía transcística laparoscópica y revisión endoscópica transoperatoria de la anastomosis, en la Clínica de Páncreas, del Servicio de Cirugía Endoscópica del Hospital General “Dr. Manuel Gea González”, de la Ciudad de México.
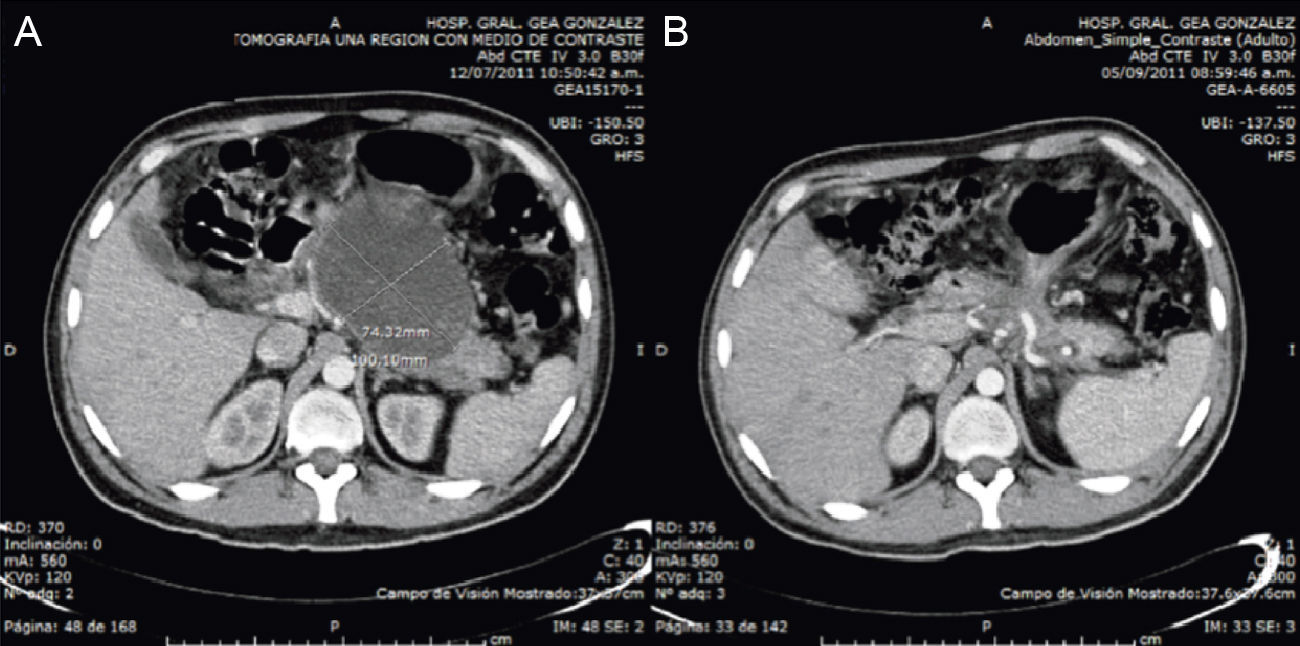
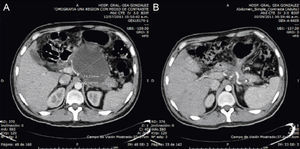
Presentación del casoMasculino de 32 años de edad, con antecedente de pancreatitis biliar grave, litiasis vesicular sin dilatación de la vía biliar extrahepática por ultrasonido, 3 meses después cursa con dolor en epigastrio, intolerancia a la vía oral, aumento de volumen a nivel de epigastrio, tomografía de abdomen con reporte de seudoquiste pancreático de 10,0 x 7,4cm, en cuerpo de páncreas con pared de 2,5cm.
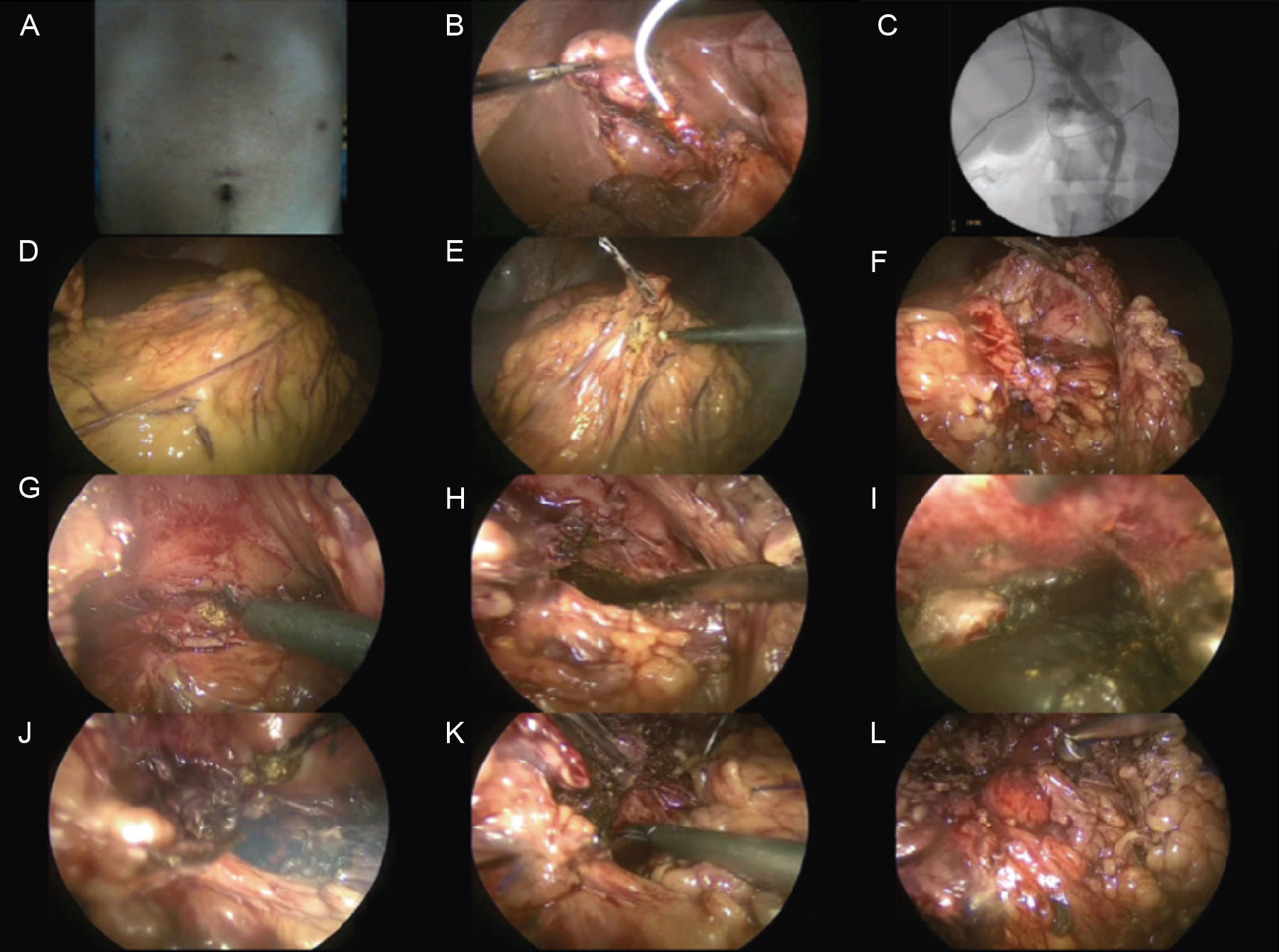
Técnica quirúrgicaBajo anestesia general, con administración de cefalotina 1g intravenoso, 30 minutos previos al procedimiento quirúrgico, se realiza un abordaje con un puerto óptico supraumbilical de 10mm y 3 puertos de trabajo de 5mm subxifoidea, línea medioclavicular región subcostal derecha e izquierda, con neumoperitoneo de 15mmHg. Se realizó una colecistectomía utilizando los principios de Strasberg, ligando la arteria cística con polipropileno 2-0, utilizando el nudo extracorpóreo tipo Gea7. Previo a la sección del cístico, se realiza colangiografía transcística utilizando un catéter Arrow periférico 16 Ga, sin evidenciar defectos de llenado en la vía biliar extrahepática y observando un adecuado vaciamiento de la misma, se liga el cístico con polipropileno del 0, utilizando el nudo extracorpóreo tipo Gea, se termina la colecistectomía de forma convencional. Se realiza cistogastroanastomosis con abordaje posterior incidiendo el ligamento gastrocólico, se localiza y diseca de la cara posterior del estómago, la cara anterior del seudoquiste pancreático incidiendo la misma con gancho monopolar, se aspira contenido tomando muestras del mismo, se procede a toma biopsia de la pared del seudoquiste pancreático y se realiza desbridación de material necrótico del interior del mismo. Se incide la cara posterior del estómago a un nivel correspondiente a la incisión de la pared del seudoquiste pancreático, se realiza anastomosis de 3cm con puntos separados con polipropileno del 0 utilizando el nudo extracorpóreo tipo Gea, se confirma permeabilidad de la cistogastroanastomosis con una valoración endoscópica transoperatoria. Finaliza procedimiento dejando drenajes tipo Jackson-Pratt en el lecho quirúrgico (fig. 1).
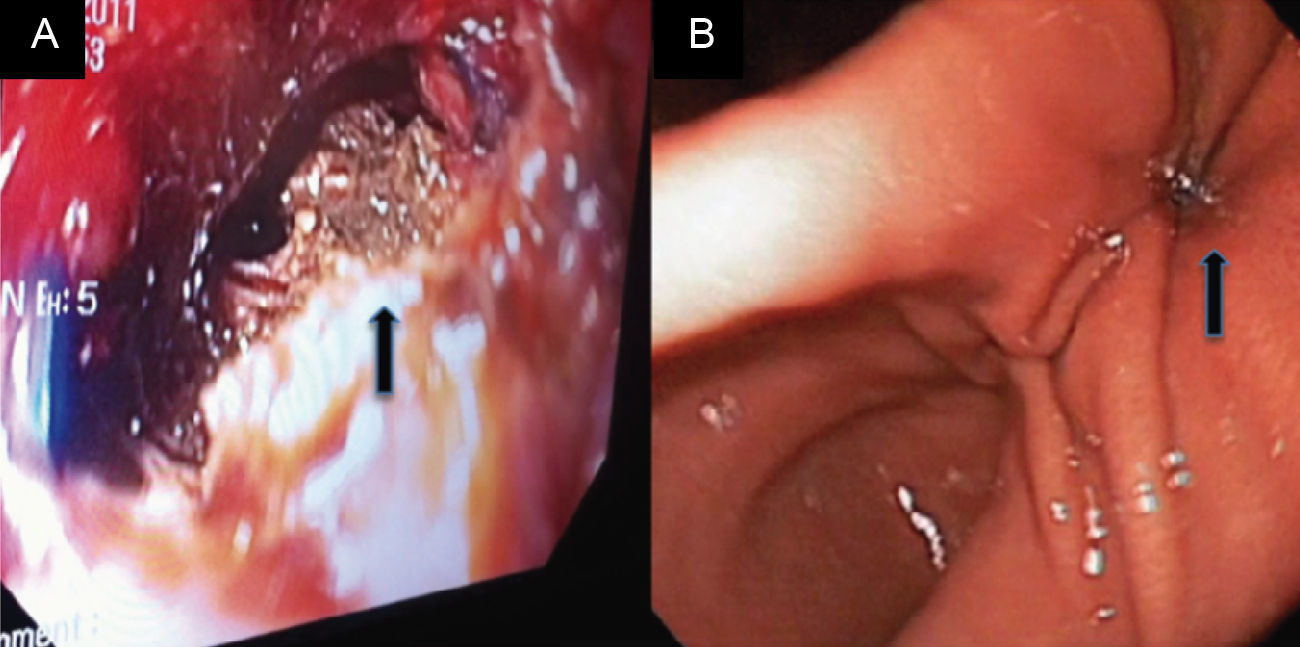
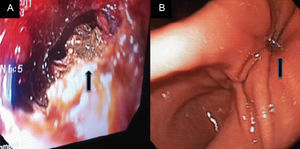
La evolución posquirúrgica fue adecuada, con tolerancia a líquidos a las 24 horas del procedimiento quirúrgico, sin presentar complicaciones posquirúrgicas y con resolución sintomática, se egresa al cuarto día de la unidad hospitalaria. Control tomográfico a los 2 meses, mostrando resolución radiológica del seudoquiste pancreático (fig. 2), la endoscopia de control a los 2 meses mostró obliteración del 90,0% de la cistogastroanastomosis (fig. 3). Control tomográfico a los 6 meses del procedimiento sin evidencia de recidiva.
La primera cistogastroanastomosis fue realizada en 1.921 por Jedlica. El drenaje quirúrgico fue considerado el método estándar de tratamiento, hasta la década de los 80¿s, cuando inician las primeras descripciones del manejo mínimo invasivo no quirúrgico con Hancke en 1.976 y Van Sonnenberg en 1.989 con el drenaje percutáneo asistido por radiología. En 1.985, Kozarek describe las primeras cistogastroanastomosis y cistoduodenoanastomosis endoscópicas2,6. Hasta 1.994 Frantzides reporta el primer drenaje interno de un seudoquiste pancreático, con una cistoyeyunoanastomosis en asa laparoscópica5.
Con el desarrollo del abordaje laparoscópico de los seudoquiste pancreático en la década de los 90¿s, se lograron disminuir los índices de morbilidad y mortalidad asociados a la cirugía convencional4–6. Se han descrito diversas técnicas de drenaje interno, cistogastroanastomosis con abordaje anterior o transgástrico, endogástrico y posterior o exogástricas descrita por Morino en 1.995, y Park en 1.999 cistoyeyunoanastomosis en Y de Roux y en asa. Se han reportado diversas series en la literatura médica de abordaje laparoscópico de los seudoquistes pancreáticos4–6,9, donde más del 80,0% se desarrollan en el contexto de una PA, siendo las 2 principales etiologías la PA biliar y alcohólica. El diámetro de los seudoquistes pancreáticos va de 8,5 a 16,6cm, la mayoría con abordajes transgástricos o endogástricos, el tiempo quirúrgico reportado varia de 85 a 240 minutos, con porcentajes de colecistectomías asociadas al drenaje interno del seudoquiste pancreático de un 11,0% a 100,0%. Las complicaciones posquirúrgicas se debieron a infecciones de la cavidad residual de seudoquiste pancreático o sangrado posquirúrgico, el manejo médico fue efectivo requiriendo reintervención quirúrgica menos del 1,8% de los casos. La mortalidad reportada en estas series es del 0,0%. La recurrencia en la serie de Palanivelu9 es del 0,0%, esta es la serie quirúrgica más grande publicada en la actualidad con un seguimiento de 54 meses.
Actualmente no existen estudios prospectivos, aleatorizados que comparen la superioridad de las diversas opciones de manejo y la visión general, basada en estudios con un nivel de evidencia grado III o IV3. La decisión en el tipo de intervención está determinada en forma primaria, por la experiencia y los recursos disponibles en cada institución1, más que por las características anatómicas, la presencia de infección o detritus sólidos del seudoquiste pancreático2,4–6,8, así como los cambios anatómicos en el conducto pancreático principal, y la comunicación o no del seudoquiste pancreático con el conducto pancreático principal10, la presencia de patologías intraabdominales asociadas a seudoquiste pancreático susceptibles de manejo quirúrgico2,5,10, entre otros.
ConclusionesActualmente no existe evidencia tipo I que avale la superioridad de una modalidad de manejo sobre la otra, y se hace difícil establecer una guía de manejo no debatible. La evidencia actual se inclina a una superioridad del manejo quirúrgico laparoscópico, en los diversos tipos de colecciones pancreáticas y peripancreáticas, infectadas o no, asociada o no a otra patología intraabdominal susceptible de manejo quirúrgico.
La cirugía laparoscópica de páncreas es relativamente nueva y las mejoras en las técnicas quirúrgicas, en la experiencia de los diversos grupos y en el instrumental han permitido su desarrollo. Nuestra técnica de cistogastroanastomosis con abordaje posterior, muestra ventajas prácticas confirmadas por otros autores, al evitar una gastrostomía anterior, no requerir una compresión extrínseca del seudoquiste pancreático en la cara posterior del estómago para su localización, presentar una hemostasia adecuada, poder realizar una necrosectomía con un ángulo de visión adecuado, realizar una anastomosis amplia confirmada endoscópicamente sin necesidad de una engrapadora, y la resolución de otras patologías intraabdominales, como la litiasis vesicular de forma laparoscópica.
FinanciamientoNo se recibió patrocinio de ningún tipo para llevar a cabo este estudio.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.