El cáncer gástrico es el cuarto tipo de cáncer más común de reciente diagnóstico y la segunda causa de muerte relacionada con cáncer en el mundo. El desarrollo de tomografía multidetector ha mejorado la estadificación preoperatoria del cáncer gástrico.
ObjetivoCorrelacionar los informes tomográficos preoperatorios con los resultados definitivos de patología de acuerdo con el sistema TNM.
MétodosAnálisis transversal, retrospectivo. De enero del 2009 a diciembre del 2013, se incluyó a 67 pacientes, todos tenían endoscopia superior, tomografía preoperatoria, fueron sometidos a cirugía resectiva y contaban con resultado histopatológico. El análisis estadístico se realizó con el programa de computadora SPSS versión 15.0. El cálculo de sensibilidad y especificidad se realizó con el programa Excel 2011 para Mac.
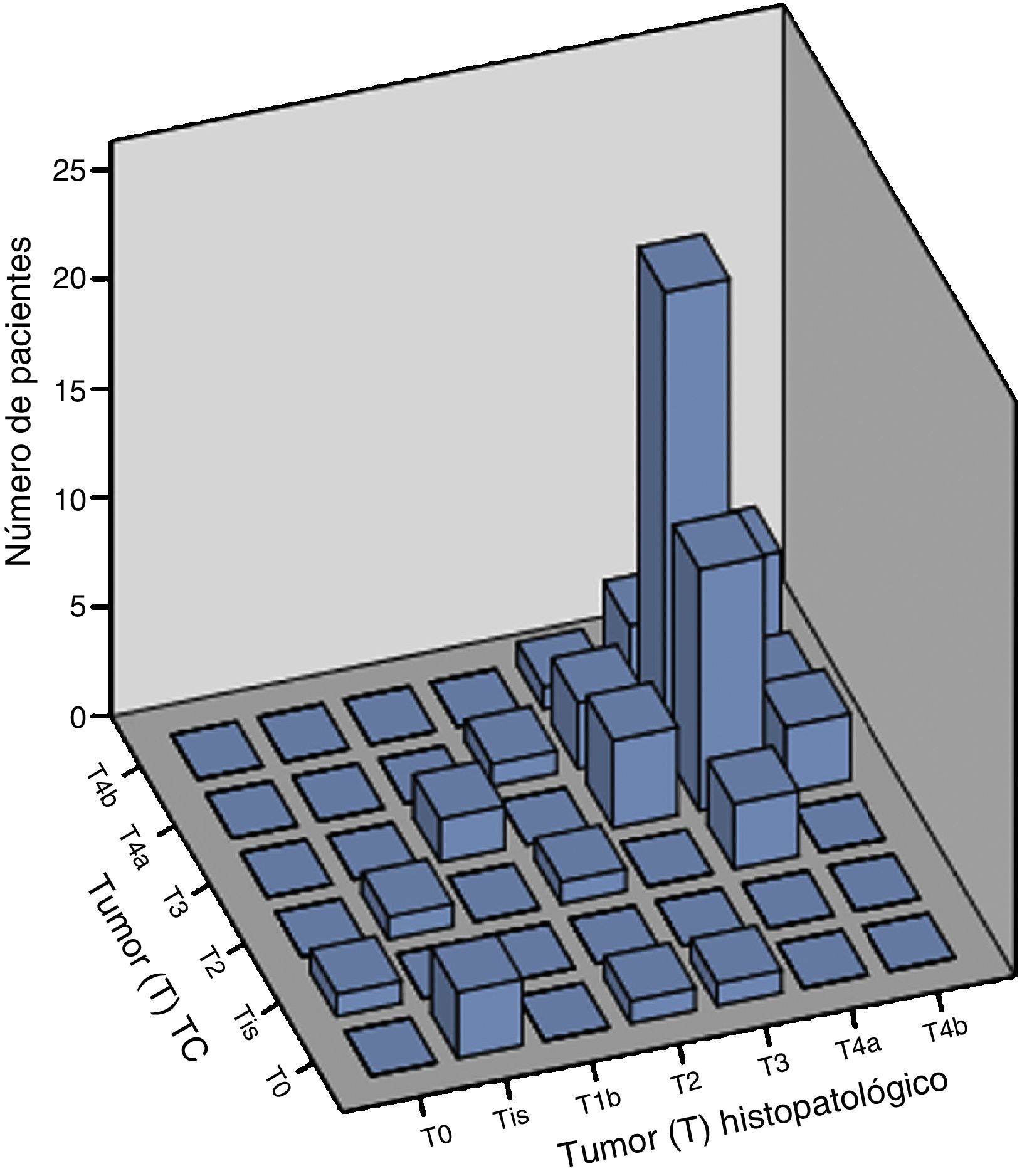
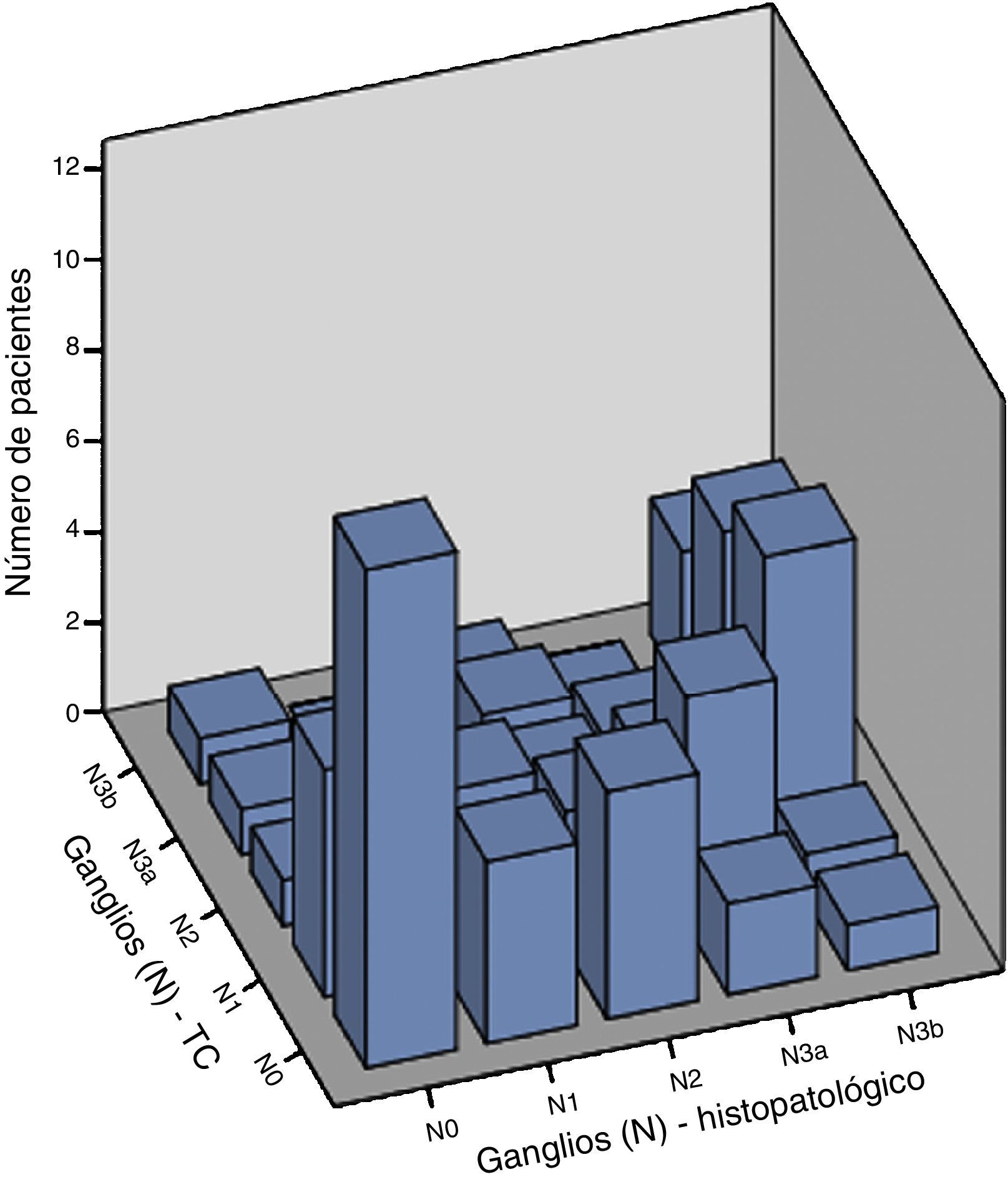
ResultadosLa mayoría de los pacientes de la serie se encontraban en estadio clínico iii y iv. La precisión global de la tomografía computarizada (TC) multidetector comparado con el resultado histopatológico para el tamaño del tumor (T) fue del 83% (T0 96%, T1 94%, T2 93%, T3 67% y T4 67%) y para N del 70% (N0 72%, N1 73%, N2 70% y N3 66%), la sensibilidad global para T fue del 48% (T0 100%, T1 0%, T2 33%, T3 44% y T4 65%) y para N del 41% (N0 58%, N1 56%, N2 15% y N3 35%). Así mismo se demostró, mediante correlación de Spearman, una fuerte asociación entre los resultados de la TC multidetector y el resultado de patología, sobre todo en T4 y N3.
ConclusionesLa TC multidetector mostró mayor congruencia en detectar las etapas T4, N0 y N3 en cáncer gástrico, comparadas con los resultados histopatológicos definitivos.
In relation to the number of new cases diagnosed, gastric cancer is the fourth most common cancer worldwide, and the second cause of cancer death. The development of multidetector tomography has improved the preoperative staging of gastric cancer.
AimTo correlate preoperative tomographic studies with the definitive pathologic results according to the TNM staging system.
MethodsA retrospective, cross-sectional study within the time frame of January 2009 to December 2013 was conducted that included the case records of 67 patients. They all had upper endoscopy and preoperative multidetector tomography examinations, underwent surgical resection, and had the corresponding histopathology study. Statistical analysis was carried out with the SPSS version 15.0 software and the sensitivity and specificity calculations were made using the Excel 2011 program for Mac.
ResultsThe majority of the patients included in the case series had clinical stage iii and iv disease. When compared with the histopathologic result, the overall accuracy of multidetector CT was 83% (T0 96%, T1 94%, T2 93%, T3 67%, and T4 67%) for tumor size (T) and was 70% (N0 72%, N1 73%, N2 70%, and N3 66%) for lymph node involvement (N). Overall sensitivity was 48% (T0 100%, T1 0%, T2 33%, T3 44%, and T4 65%) for T and was 41% (N0 58%, N1 56%, N2 15%, and N3 35%) for N. A strong association between the multidetector CT results and the pathology results was demonstrated through the Spearman's correlation, especially in T4 and N3.
ConclusionsMultidetector computed tomography showed greater congruency in detecting stages T4, N0, and N3 in gastric cancer, when compared with the definitive histopathologic results.
Hay una amplia variación en la incidencia del cáncer gástrico a nivel mundial. Todavía es el cuarto tipo de cáncer más común de reciente diagnóstico y es la segunda causa de muerte relacionada con cáncer en todo el mundo1. A pesar de los avances en las herramientas de diagnóstico y tratamiento multimodal, la tasa de supervivencia a 5 años para todos los pacientes en todos los estadios sigue siendo inferior al 30%2. La valoración preoperatoria de los pacientes con adenocarcinoma gástrico implica establecer el diagnóstico, la evaluación de la enfermedad local, la búsqueda de enfermedad a distancia y valorar la condición médica general del paciente. La tomografía computarizada (TC) con 3D combinada con distensión por agua y aire puede mejorar la precisión de la estadificación del tamaño del tumor (T) y la afección ganglionar (N) preoperatoria del cáncer gástrico, con precisión diagnóstica del 78% para ganglios linfáticos3.
El cáncer gástrico es una enfermedad locorregional con alta tendencia para metástasis ganglionar. Por lo tanto, el estado ganglionar sigue siendo uno de los factores predictivos independientes más críticos de supervivencia para los pacientes después de una gastrectomía4,5. La resección quirúrgica sigue siendo la base del tratamiento curativo para el cáncer gástrico. De acuerdo con la Unión Internacional para el Control del Cáncer (UICC, por sus siglas en inglés), el tratamiento quirúrgico con intención curativa busca eliminar toda la enfermedad tumoral, consiguiendo márgenes de seguridad sin restos microscópicos de enfermedad, denominada cirugía R0, y reporta un mejor control de la enfermedad a largo plazo. Hay controversias en las series occidentales y series japonesas respecto a la extensión de la disección linfática, tanto que en Asia Oriental la gastrectomía total o subtotal con disección D2 es el estándar de oro del tratamiento quirúrgico para el cáncer gástrico. Un metaanálisis que compara la gastrectomía con disección D1 contra D2 concluye que la primera se asocia con menor fuga de anastomosis, menor tasa de complicaciones postoperatorias y reoperaciones, disminución de la estancia hospitalaria y de la tasa de mortalidad a los 30 días; en cuanto a la tasa de supervivencia a 5 años, fue similar para ambos procedimientos6.
El desarrollo de TC multidetector ha mejorado la estadificación del cáncer gástrico; sin embargo, los resultados con estas técnicas no son satisfactorios, especialmente para la evaluación de la profundidad del tumor y la N. En nuestro hospital no hay estudios que comparen la precisión diagnóstica preoperatoria de la tomografía con el resultado histopatológico definitivo; es importante evaluar dicha información ya que está documentado que resecciones mayores presentan mayor número de complicaciones, estancias hospitalarias prolongadas y mayor consumo de recursos materiales y humanos. Por lo anterior, el objetivo de nuestro estudio es correlacionar los informes emitidos por el departamento de radiación ionizante sobre la base de los criterios tomográficos de cáncer gástrico con los resultados definitivos de patología en relación con el T y la N, y el estadio clínico (EC) de acuerdo con el sistema de estadificación TNM.
MétodosSe realizó un estudio descriptivo, transversal, observacional y retrospectivo consistente en revisión de expedientes clínicos. Se incluyeron expedientes de pacientes con diagnóstico de cáncer gástrico de tipo adenocarcinoma identificados mediante biopsia obtenida por endoscopia. Todos los pacientes contaban con TC de abdomen completo con informe escrito y fueron sometidos a cirugía gástrica resectiva, con informe definitivo de patología durante el período de enero del 2009 a diciembre del 2013. Se eliminó a pacientes que recibieron tratamiento neoadyuvante y con diagnóstico de otro tipo de neoplasia. Se generó una base de datos en tablas de Excel (Microsoft Office M.R.). Las variables categóricas se reportan como valor absoluto y porcentajes. Se probó si la distribución de las variables ordinales o continuas era normal mediante pruebas de Kolmogorov-Smirnov. La mayoría de las variables no tuvo distribución normal (p<0.05), por lo tanto, los resultados se muestran como medianas (p25-p75). Las correlaciones entre estadificación tomográfica y resultados histopalógicos se calcularon mediante los métodos de Spearman y de Kendall. La asociación entre la estadificación tomográfica e histopatológica para T se calculó con pruebas de correlación de Spearman. Se consideró significativo un valor de p (error alfa) < 0.05. El análisis estadístico se realizó con el programa de computadora SPSS versión 15.0. El cálculo de la sensibilidad y especificidad se realizó con el programa Excel 2011 para Mac.
ResultadosSe revisaron un total de 138 expedientes, se excluyeron del estudio 16 que correspondieron a otros tumores (8 linfomas y 8 tumores del estroma gastrointestinal de estómago), 42 sometidos a cirugía paliativa por EC avanzado (biopsia, derivación), 10 tuvieron expediente incompleto y 3 se excluyeron por recibir tratamiento neoadyuvante. Se incluyó en el estudio a 67 pacientes en el período comprendido; de estos, en 11 se documentó metástasis a distancia en la TC preoperatoria, sin embargo, se realizó cirugía resectiva por lo que se incluyeron en el estudio. Todos contaban con endoscopia superior con información de la ubicación y el grado de infiltración del tumor, así como TC multidetector preoperatoria (31 gastro-TC y 36 simple y contrastada), con informe escrito, y todos fueron sometidos a procedimiento quirúrgico resectivo y contaban con resultado histopatológico definitivo. El T y la N se clasificaron según el manual de estadificación del American Joint Committee on Cancer, séptima edición7. La correlación entre informe tomográfico e histopatológico para el T y la N se realizó sobre la base de la tabla 1, de acuerdo con los criterios mencionados por Hallinan y Venkatesh8. Todos los estudios de tomografía fueron evaluados por 4 diferentes médicos radiólogos de abdomen con al menos 3 años de experiencia, de acuerdo con los criterios antes descritos.
Criterios de comparación entre hallazgos tomográficos y patológicos en las diferentes etapas clínicas del cáncer gástrico
| Tamaño del tumor (T) | |
|---|---|
| Etapa T (patología) | Etapa T (tomografía) |
| pT1: invasión tumoral de la lámina propia, muscular de la mucosa o submucosa | T1: engrosamiento focal irregular con o sin reforzamiento de la pared gástrica interna. Se preserva una línea hipodensa e hipovascular visible a lo largo de la capa externa de la pared; reforzamiento focal intenso en la pared gástrica sin engrosamiento nodular |
| pT2: invasión tumoral de la muscular propia | T2-3: engrosamiento de la totalidad de la pared gástrica en una extensión variable, pero la capa externa de la pared gástrica esta íntegra, la grasa perigástrica de apariencia normal |
| pT3: invasión tumoral de la subserosa | |
| pT4a: invasión tumoral de la serosa | T4a: la totalidad de la pared gástrica está engrosada con un reforzamiento homogéneo; la superficie de la capa externa de la pared gástrica es irregular y hay presencia de micronódulos o reticulación de la grasa perigástrica |
| pT4b: invasión tumoral de estructuras adyacentes | T4b: hay extensión del tumor a órganos adyacentes además del engrosamiento y reforzamiento de la pared gástrica |
| Afección ganglionar (N) | |
|---|---|
| Etapa N (patología) | Etapa N (tomografía) |
| N1: infiltración en 1-2 ganglios linfáticos regionales | N1: infiltración de 1 a 2 ganglios regionales (compartimento perigástrico y vascular) |
| N2: infiltración en 3-6 ganglios linfáticos regionales | N2: infiltración de 3 a 6 ganglios regionales |
| N3a: infiltración en 7- 15 ganglios linfáticos regionales | N3: infiltración de 7 a 15 ganglios regionales |
| N3b: en 16 o más ganglios linfáticos regionales | |
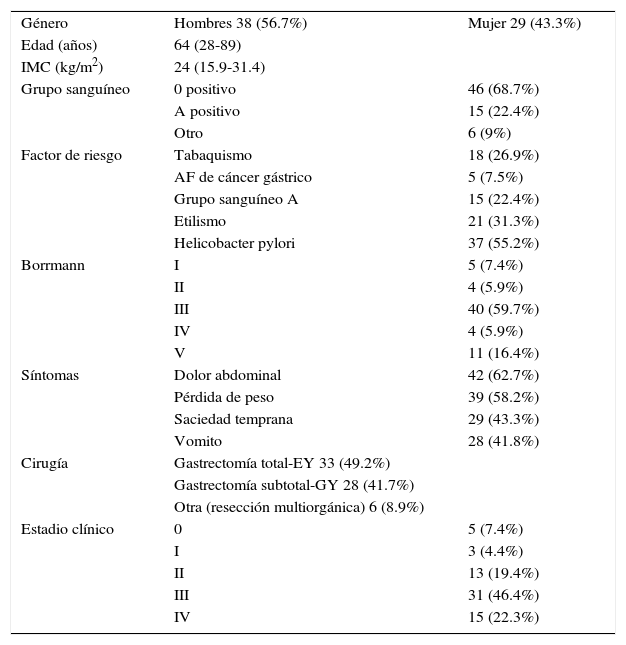
El grupo de estudio se integró por 38 hombres (56.7%) y 29 mujeres (43.3%), la mediana de edad fue de 64 años, con un rango de 28 a 89 años, se identificó antecedente de Helicobacter pylori en 37 (55.2%), etilismo en 21 (31.3%) y grupo sanguíneo A en 15 (22.4%). Los síntomas predominantes fueron dolor abdominal en 42 (62.7%), pérdida de peso en 39 (58.2%) y saciedad temprana en 29 (43.3%). En relación con la endoscopia superior, 40 pacientes (59.7%) se clasificaron como Borrmann III. Por tipo de cirugía realizada, 33 (49.2%) fueron sometidos a gastrectomía total, 28 (41.7%) a gastrectomía subtotal y 6 pacientes (8.9%) a resección multiorgánica. La mayoría de los pacientes, 31 (46.4%), se clasificaron como EC III y 15 (22.3%) estadio iv (tabla 2).
Datos demográficos de los pacientes con diagnóstico de adenocarcinoma gástrico
| Género | Hombres 38 (56.7%) | Mujer 29 (43.3%) |
| Edad (años) | 64 (28-89) | |
| IMC (kg/m2) | 24 (15.9-31.4) | |
| Grupo sanguíneo | 0 positivo | 46 (68.7%) |
| A positivo | 15 (22.4%) | |
| Otro | 6 (9%) | |
| Factor de riesgo | Tabaquismo | 18 (26.9%) |
| AF de cáncer gástrico | 5 (7.5%) | |
| Grupo sanguíneo A | 15 (22.4%) | |
| Etilismo | 21 (31.3%) | |
| Helicobacter pylori | 37 (55.2%) | |
| Borrmann | I | 5 (7.4%) |
| II | 4 (5.9%) | |
| III | 40 (59.7%) | |
| IV | 4 (5.9%) | |
| V | 11 (16.4%) | |
| Síntomas | Dolor abdominal | 42 (62.7%) |
| Pérdida de peso | 39 (58.2%) | |
| Saciedad temprana | 29 (43.3%) | |
| Vomito | 28 (41.8%) | |
| Cirugía | Gastrectomía total-EY 33 (49.2%) | |
| Gastrectomía subtotal-GY 28 (41.7%) | ||
| Otra (resección multiorgánica) 6 (8.9%) | ||
| Estadio clínico | 0 | 5 (7.4%) |
| I | 3 (4.4%) | |
| II | 13 (19.4%) | |
| III | 31 (46.4%) | |
| IV | 15 (22.3%) |
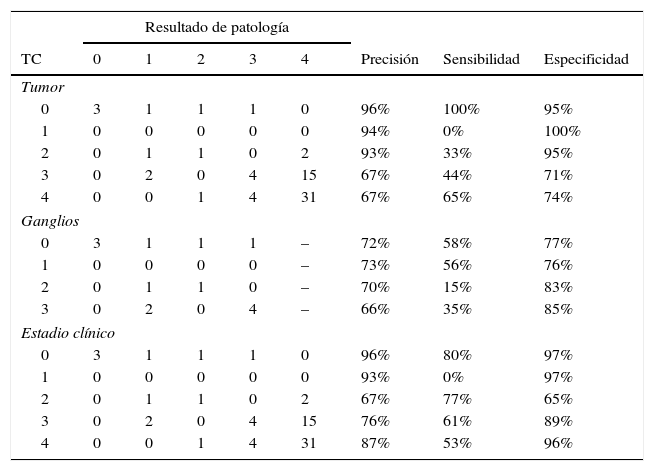
El cálculo de la sensibilidad, especificidad y precisión diagnóstica para T, N y EC se realizó con el programa Excel 2011 para Mac. Los resultados se presentan en la siguiente tabla (tablas 3 y 4).
Sensibilidad, especificidad y precisión diagnóstica por niveles de la TC comparada con el resultado histopatológico para T, N y EC en cáncer gástrico
| Resultado de patología | ||||||||
|---|---|---|---|---|---|---|---|---|
| TC | 0 | 1 | 2 | 3 | 4 | Precisión | Sensibilidad | Especificidad |
| Tumor | ||||||||
| 0 | 3 | 1 | 1 | 1 | 0 | 96% | 100% | 95% |
| 1 | 0 | 0 | 0 | 0 | 0 | 94% | 0% | 100% |
| 2 | 0 | 1 | 1 | 0 | 2 | 93% | 33% | 95% |
| 3 | 0 | 2 | 0 | 4 | 15 | 67% | 44% | 71% |
| 4 | 0 | 0 | 1 | 4 | 31 | 67% | 65% | 74% |
| Ganglios | ||||||||
| 0 | 3 | 1 | 1 | 1 | – | 72% | 58% | 77% |
| 1 | 0 | 0 | 0 | 0 | – | 73% | 56% | 76% |
| 2 | 0 | 1 | 1 | 0 | – | 70% | 15% | 83% |
| 3 | 0 | 2 | 0 | 4 | – | 66% | 35% | 85% |
| Estadio clínico | ||||||||
| 0 | 3 | 1 | 1 | 1 | 0 | 96% | 80% | 97% |
| 1 | 0 | 0 | 0 | 0 | 0 | 93% | 0% | 97% |
| 2 | 0 | 1 | 1 | 0 | 2 | 67% | 77% | 65% |
| 3 | 0 | 2 | 0 | 4 | 15 | 76% | 61% | 89% |
| 4 | 0 | 0 | 1 | 4 | 31 | 87% | 53% | 96% |
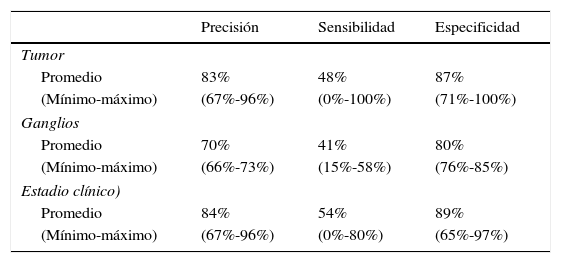
Sensibilidad, especificidad y precisión diagnóstica global de la TC para T, N y EC comparada con el resultado histopatológico en cáncer gástrico
| Precisión | Sensibilidad | Especificidad | |
|---|---|---|---|
| Tumor | |||
| Promedio | 83% | 48% | 87% |
| (Mínimo-máximo) | (67%-96%) | (0%-100%) | (71%-100%) |
| Ganglios | |||
| Promedio | 70% | 41% | 80% |
| (Mínimo-máximo) | (66%-73%) | (15%-58%) | (76%-85%) |
| Estadio clínico) | |||
| Promedio | 84% | 54% | 89% |
| (Mínimo-máximo) | (67%-96%) | (0%-80%) | (65%-97%) |
En el resultado histopatológico se reportaron 13 pacientes con metástasis, de los cuales 6 fueron a hígado, uno a ovario, uno a bazo, uno a páncreas, uno con metástasis a epiplón mayor y 3 con metástasis a múltiples órganos (diafragma, ovario y colon). De estos, 11 fueron detectados previamente por la TC, mientras que en los 2 pacientes restantes no se detectó metástasis en la TC.
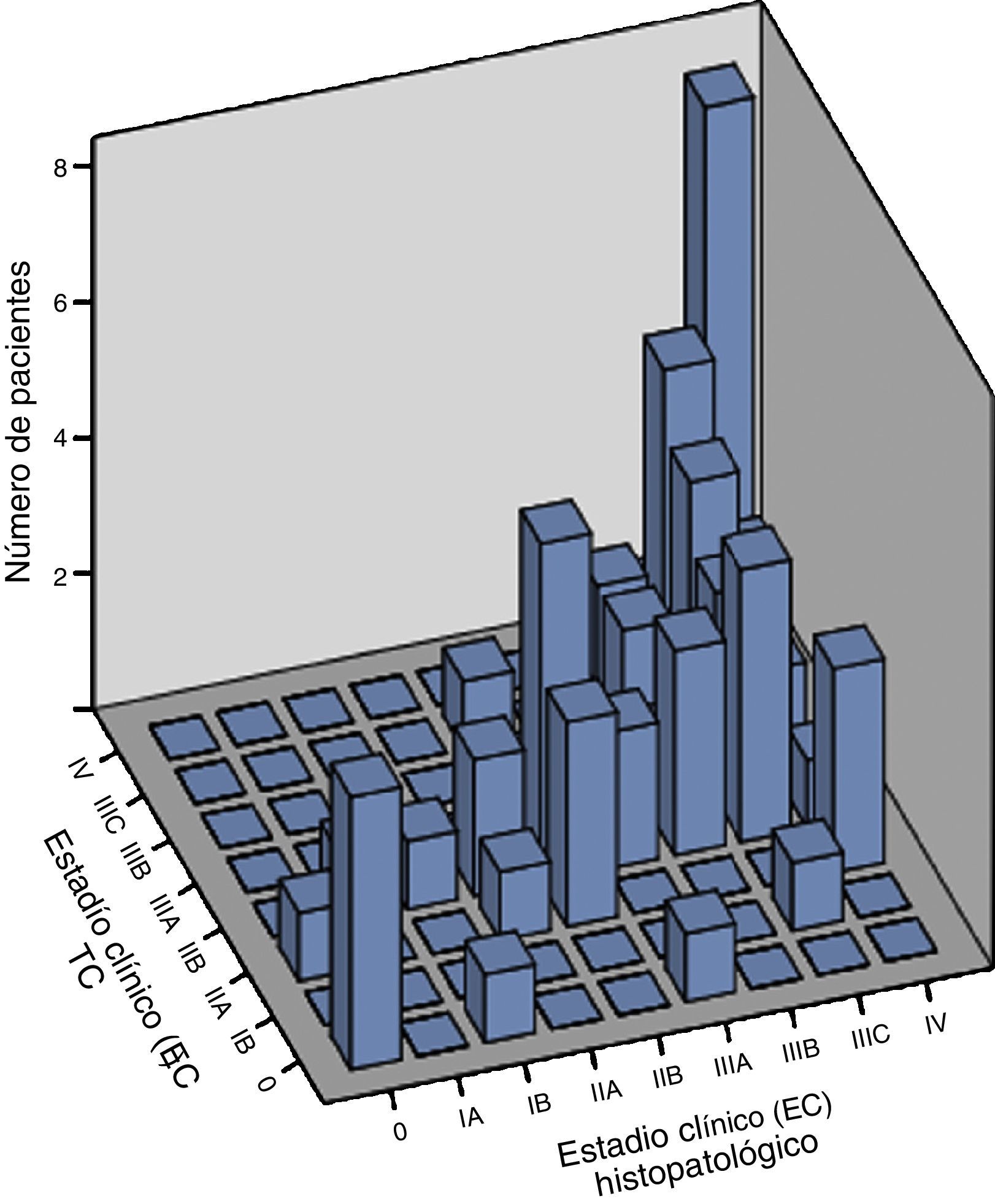
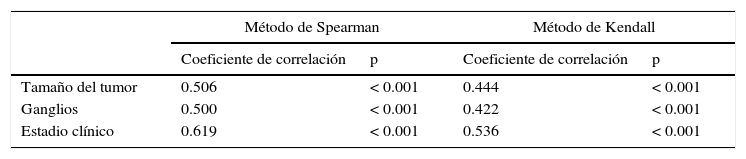
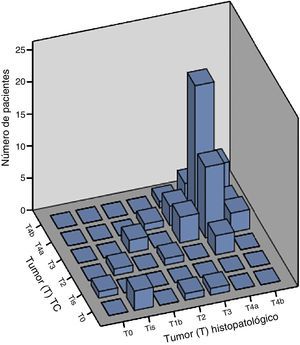
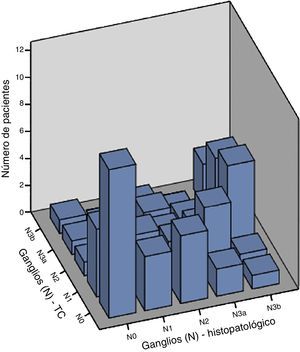
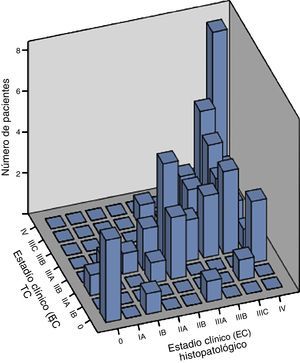
Las correlaciones entre estadificación tomográfica y resultados histopalógicos para T, N y EC se calcularon mediante los métodos de Spearman y de Kendall, con coeficiente de correlación estadísticamente significativo (p<0.001), como se muestra en la tabla 5 y las figuras 1-3. El tiempo promedio entre la estadificación preoperatoria con TC multidetector y el procedimiento quirúrgico fue de 14 días, lo cual disminuye el riesgo de progresión de la enfermedad, limitando la variación de nuestros resultados.
Correlación entre la estadificación tomográfica preoperatoria con el reporte histopatológico definitivo
| Método de Spearman | Método de Kendall | |||
|---|---|---|---|---|
| Coeficiente de correlación | p | Coeficiente de correlación | p | |
| Tamaño del tumor | 0.506 | < 0.001 | 0.444 | < 0.001 |
| Ganglios | 0.500 | < 0.001 | 0.422 | < 0.001 |
| Estadio clínico | 0.619 | < 0.001 | 0.536 | < 0.001 |
Fuente: directa.
Actualmente, el cáncer gástrico es una de las neoplasias con peor pronóstico, ya que es bien sabido que la mayoría de los pacientes se diagnostican en etapas avanzadas. El tratamiento de elección sigue siendo quirúrgico, realizando cirugía resectiva, ya sea con intento curativo o paliativo. La TC es una herramienta indispensable para una adecuada estadificación preoperatoria y con el desarrollo de TC multidetector ha incrementado la precisión diagnóstica para T y N.
Chen et al.3 compararon los resultados quirúrgicos e histopatológicos reportando precisión global de la TC multidetector en la estadificación de la etapa T del 73.8% (T1 45.93%, T2 53.03%, T3 86.49% y T4 85.79%) y la precisión global en la estadificación de la etapa N de 75.22% (N0 76.17%, N1 68.81% y N2 80.63%). En nuestro estudio, los valores obtenidos fueron superiores para T e inferiores para N, con una precisión global para T de 83% (T0 96%, T1 94%, T2 93%, T3 67% y T4 67%) y para N de 70% (N0 72%, N1 73%, N2 70% y N3 66%). Un factor relevante en los resultados fue la interpretación del estudio, en nuestra serie fue realizada por un médico radiólogo de abdomen y en el estudio en mención, cada TC fue interpretada por 2 radiólogos que desconocían los hallazgos de la endoscopia.
En un estudio Yan et al.9, de igual forma, compararon los resultados quirúrgicos e histopatológicos, reportando una precisión diagnóstica global mediante TC multidetector para T del 90,9% (560/616); dicha precisión aumenta para estadios avanzados (T4), encontrando resultados similares en nuestra serie.
En 2014, un estudio mexicano10 en 27 pacientes sometidos a cirugía determinó la sensibilidad de la TC para T y N comparada con los resultados histopatológicos definitivos y reportó el 0% para T2, el 53.8% para T3 y el 40% para T4; en cuanto a N, la sensibilidad fue del 61.5% para N0, el 10% para N1 y el 66.7% para N2. Comparado con nuestros resultados, en los que la sensibilidad fue del 33% para T2, el 44% para T3 y el 65% para T4, y para N la sensibilidad fue del 58% para N0, el 56% para N1 y el 15% para N2, dichos resultados fueron inferiores a los reportados en nuestra serie; cabe mencionar que ambos fueron retrospectivos y el equipo de TC fue de 64 detectores. En nuestro estudio no hubo diferencia estadísticamente significativa entre el protocolo de estudio (gastro-TC vs. TC simple y contrastada); esto difiere de lo reportado en la literatura9 y consideramos que es por el estado avanzado de la enfermedad.
Sarela et al.11 realizaron un estudio de 657 pacientes con diagnóstico de cáncer gástrico potencialmente resecable se sometieron a laparoscopia estadificadora, encontrando un 31% de metástasis a distancia; como factor independiente y mayor prevalencia en tumores de la unión esofagogástrica, los que afectan la totalidad del estómago y la presencia de adenopatías. Concluyen que la estadificación con TC multidetector puede evitar la laparoscopia estadificadora si el tumor primario no está en la unión esofagogástrica, ni en la totalidad del estómago, y no hay linfadenopatías abdominales.
La laparoscopia estadificadora ha demostrado que es muy útil en diferenciar enfermedad diseminada, en comparación con otras modalidades, pero la diferencia es pequeña, y es en centros donde se cuenta con ultrasonido endoscópico y se usa para tomar mejores decisiones en cáncer gástrico avanzado y donde observan 1,319 pacientes con cáncer gástrico en 10 años. En el servicio de Oncología quirúrgica del HCM se hace gastrectomía laparoscópica y estadificación preoperatoria en algunos, pero no en todos los casos, por eso no se analizó en el estudio. Además, la incidencia de cáncer gástrico en nuestro hospital es de 60 casos al año y son en promedio 2 cirujanos oncólogos quienes realizan el trabajo de dichos pacientes. Además, las tendencias actuales han demostrado que la cirugía laparoscópica estadificadora en cáncer gástrico avanzado sin enfermedad peritoneal ni ascitis sigue siendo necesaria, y el tratamiento que se tiene como base es siempre el quirúrgico12,13.
La tomografía por emisión de positrones (PET) no es un procedimiento de diagnóstico de primera línea en cáncer gástrico; sin embargo, puede desempeñar un papel importante en la detección de metástasis a distancia, como a hígado, pulmones, glándulas suprarrenales, ovarios y hueso; además, puede ser útil en el seguimiento de los pacientes sometidos a quimioterapia, ya que permite valorar la respuesta temprana al tratamiento. Existen estudios que reportan precisión significativamente mayor en la estadificación preoperatoria al combinar PET/TC (68%) comparada con la PET (47%) o la TC (53%) por sí solas14.
ConclusiónLa TC multidetector tiene utilidad en la estadificación del cáncer gástrico, con alta precisión diagnóstica, sobre todo en estadios avanzados, lo cual disminuye la posibilidad de someter al paciente a cirugía estadificadora. La TC multidetector mostró mayor congruencia en detectar las etapas T4, N0 y N3 en cáncer gástrico, comparadas con los resultados histopatológicos definitivos.
El tiempo promedio entre la tomografía multidetector y la cirugía fue de 14 días. El tiempo entre la estadificación preoperatoria con TC multidetector y la cirugía debe ser el menor posible, ya que al incrementarse el mismo, la congruencia entre el informe de la TC y el resultado histopatológico definitivo puede variar por la evolución natural de la enfermedad.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses por la realización de este trabajo.
Agradecemos a los gastroenterólogos que participaron en el estudio.