El tratamiento de la infección por virus de hepatitis C (VHC) con esquemas basados en antivirales de acción directa de segunda generación (AAD) se ha asociado con altas tasas de respuesta viral sostenida (RVS) y escasos efectos secundarios (1%). Sin embargo, poca información existe respecto al impacto que tiene la carga viral detectable al final del tratamiento con AAD sobre la RVS1. Por este motivo hacemos referencia al caso de un paciente masculino de 49 años de edad, mexicano, con antecedente de falla a tratamiento con interferón pegilado en 2006 y ribavirina durante 48 semanas. La biopsia hepática en ese momento reportó grado 2 de fibrosis (Metavir F2). En 2016, recibió 12 semanas de paritaprevir/ritonavir/ombitasvir/dasbuvir (3D), con adherencia completa, sin eventos adversos significativos. La carga viral al final del tratamiento fue detectable [Abbott Real Time PCR assay (ART)], con RVS 3 meses después (tabla 1).
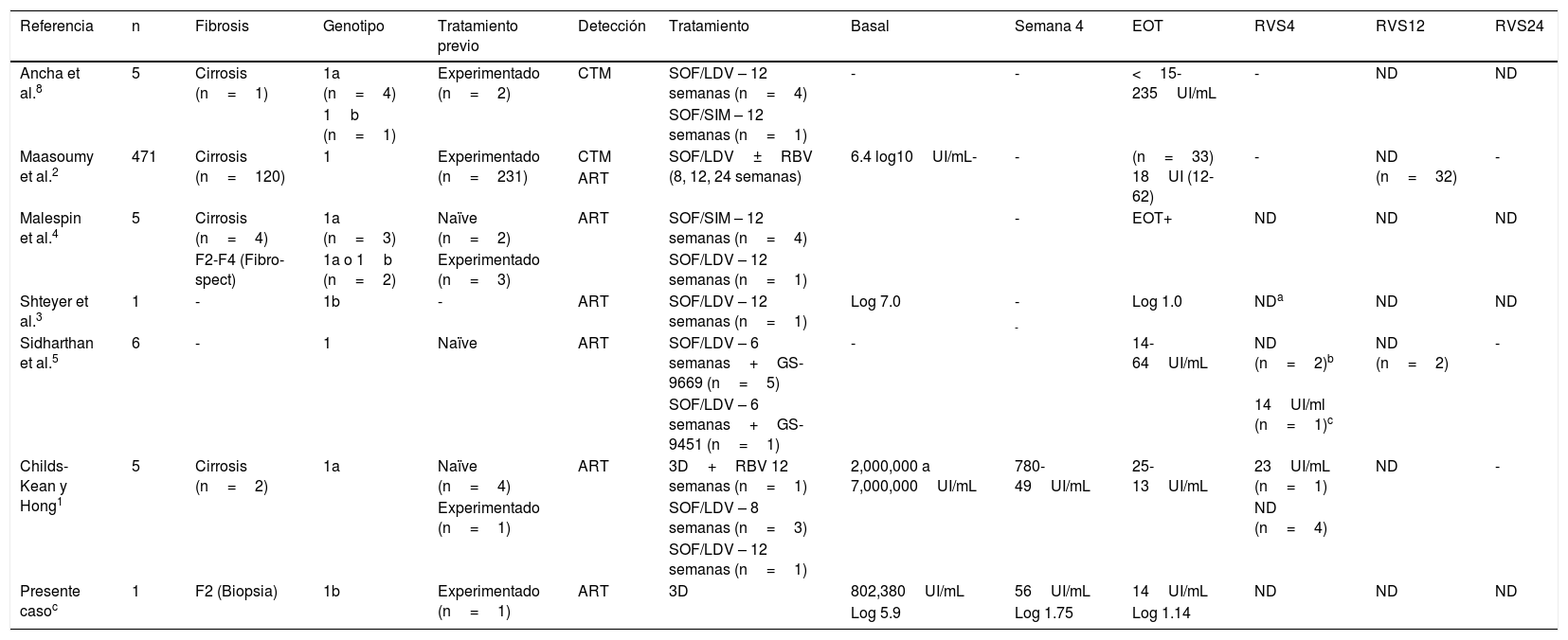
Características de pacientes con carga viral detectable a final del tratamiento y respuesta viral sostenida posterior
| Referencia | n | Fibrosis | Genotipo | Tratamiento previo | Detección | Tratamiento | Basal | Semana 4 | EOT | RVS4 | RVS12 | RVS24 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ancha et al.8 | 5 | Cirrosis (n=1) | 1a (n=4) | Experimentado (n=2) | CTM | SOF/LDV – 12 semanas (n=4) | - | - | <15-235UI/mL | - | ND | ND |
| 1b (n=1) | SOF/SIM – 12 semanas (n=1) | |||||||||||
| Maasoumy et al.2 | 471 | Cirrosis (n=120) | 1 | Experimentado (n=231) | CTM | SOF/LDV±RBV (8, 12, 24 semanas) | 6.4 log10UI/mL- | - | (n=33) 18UI (12-62) | - | ND (n=32) | - |
| ART | ||||||||||||
| Malespin et al.4 | 5 | Cirrosis (n=4) | 1a (n=3) | Naïve (n=2) | ART | SOF/SIM – 12 semanas (n=4) | - | EOT+ | ND | ND | ND | |
| F2-F4 (Fibro-spect) | 1a o 1b (n=2) | Experimentado (n=3) | SOF/LDV – 12 semanas (n=1) | |||||||||
| Shteyer et al.3 | 1 | - | 1b | - | ART | SOF/LDV – 12 semanas (n=1) | Log 7.0 | - | Log 1.0 | NDa | ND | ND |
| Sidharthan et al.5 | 6 | - | 1 | Naïve | ART | SOF/LDV – 6 semanas+GS-9669 (n=5) | - | - | 14-64UI/mL | ND (n=2)b | ND (n=2) | - |
| SOF/LDV – 6 semanas+GS-9451 (n=1) | 14UI/ml (n=1)c | |||||||||||
| Childs-Kean y Hong1 | 5 | Cirrosis (n=2) | 1a | Naïve (n=4) | ART | 3D+RBV 12 semanas (n=1) | 2,000,000 a 7,000,000UI/mL | 780-49UI/mL | 25-13UI/mL | 23UI/mL (n=1) | ND | - |
| Experimentado (n=1) | SOF/LDV – 8 semanas (n=3) | ND (n=4) | ||||||||||
| SOF/LDV – 12 semanas (n=1) | ||||||||||||
| Presente casoc | 1 | F2 (Biopsia) | 1b | Experimentado (n=1) | ART | 3D | 802,380UI/mL | 56UI/mL | 14UI/mL | ND | ND | ND |
| Log 5.9 | Log 1.75 | Log 1.14 |
3D: paritaprevir/ritonavir/ombitasvir/dasabuvir; ART: Abbott RealTime PCR assay; CTM: Cobas TaqMan HCV Test; EOT: (end of treatment) fin de tratamento; ND: no detectado; RBV: ribavirina; RVS: respuesta viral sostenida; SOF/LDV: sofosbuvir/ledipasvir; SOF/SIM: sofosbuvir/simeprevir.
Análisis previos han reportado un 5-7% de carga viral detectable al final del tratamiento con RVS posterior a diferentes regímenes de AAD1-4. Encontramos 6 reportes en relación con este interesante fenómeno, los cuales se resumen en la tabla 1. Para explicar la viremia al final del tratamiento, algunos autores sugieren un mecanismo que involucra la cinética viral, en el cual partículas virales no infecciosas o viriones defectuosos pueden ser detectados de manera transitoria al final del tratamiento5. Además, como ya es conocido, la infección por VHC afecta la inmunidad celular; una reducción de la carga viral después de un tratamiento efectivo podría de manera subsecuente restaurar los mecanismos inmunes que permitan la depuración de los virus residuales al final de la terapia antiviral1,4. Llama la atención que la mayor parte de los casos con viremia positiva que posteriormente alcanzaron RVS fueron descritos utilizando ensayos altamente sensibles, como reacción en cadena de polimerasa en tiempo real1,2. La depuración del virión de VHC ocurre a una tasa de 10-12 viriones por día, pero se ha observado que la apoptosis de las células infectadas se puede extender más de 70 días6. Consideramos que nuestro caso no se trata de un resultado falso positivo, ya que las cargas virales se determinaron usando el mismo método y estas resultaron no detectables 24 semanas después de haber concluido el tratamiento.
Hasta el momento no se han descrito predictores asociados con carga viral detectable al final del tratamiento. En la serie más grande reportada por Maasoumy et al.2, ni la carga viral basal, ni el esquema utilizado, estuvieron asociados con el fenómeno descrito. La información disponible sugiere que tener carga detectable al final del tratamiento parece no tener relevancia clínica, ya que casi el total de los pacientes de las series reportadas alcanzaron RVS (tabla 1). En las recomendaciones de las guías EASL de 20187 se omite la determinación de carga viral al final del tratamiento, evaluando la respuesta 12 semanas después, lo cual tiene su fundamento en que la eficacia de los esquemas de AAD es cercana al 100%.
Consideraciones éticasSe solicitó consentimiento informado del paciente para recibir el tratamiento. Esta carta científica cumple con la normativa vigente en investigación bioética, obtuvo la autorización del comité de ética del Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán. No se puede reconocer o identificar al paciente a través de las imágenes o datos del artículo.
FinanciaciónEste trabajo no tuvo fuente de financiación.
Conflicto de interesesLos autores de este documento declaran no tener conflicto de intereses.