El esófago de Barrett es un trastorno premaligno del esófago en el cual el epitelio escamoso de la porción distal del esófago es reemplazado por epitelio columnar. Debido a que la incidencia de adenocarcinoma esofágico se encuentra al alza, la mayoría de las sociedades de Gastroenterología han emitido sus propias recomendaciones para el tamizaje y la vigilancia. Factores específicos como la obesidad, la raza blanca, la edad por encima de los 50 años, el inicio del ERGE a edad temprana, el tabaquismo y la hernia hiatal han sido identificados como factores que incrementan el riesgo de esófago de Barrett y adenocarcinoma. El diagnóstico requiere tanto de la identificación endoscópica de mucosa con revestimiento columnar como de la confirmación histológica con biopsia. La mayoría de las sociedades médicas recomiendan tamizar a todas las personas con ERGE, así como aquellos con otros factores de riesgo con endoscopia; sin embargo, otras alternativas que utilizan métodos menos invasivos se encuentran bajo estudio en la actualidad. Las estrategias de vigilancia varían dependiendo de los hallazgos endoscópicos y se recomienda el protocolo de biopsias de Seattle con un muestreo de 4 cuadrantes aleatorizado. Algunos biomarcadores han mostrado resultados prometedores, aunque se requieren de más estudios en el futuro. La endoscopia de luz blanca es el estándar en la práctica, sin embargo, otras modalidades de imagen más avanzadas han mostrado resultados variables y, por lo tanto, se esperan más estudios para obtener validación adicional. Las técnicas de erradicación endoscópica, incluyendo tanto la resección como la ablación, han mostrado buenos resultados, aunque variables, en el tratamiento de lesiones displásicas confinadas a la mucosa. Los procedimientos de resección para remover las lesiones visibles seguida por la ablación de la mucosa displásica han mostrado los mejores resultados, con tasas de erradicación más altas y menores tasas de recurrencia. El manejo quirúrgico está reservado para lesiones con invasión de la submucosa y propagación a ganglios linfáticos con un riesgo incrementado de metástasis.
Barrett's esophagus is a premalignant condition of the esophagus in which the squamous epithelium of the lower end of the esophagus is replaced with columnar epithelium. Since the incidence of esophageal adenocarcinoma is on the rise, the major gastroenterology societies have come up with their recommendations for screening and surveillance. Specific factors like obesity, white race, age over 50 years, early age of onset of GERD, smoking and hiatal hernia have been identified as increasing the risk of Barrett's esophagus and adenocarcinoma. The diagnosis requires both endoscopic identification of columnar-lined mucosa and histological confirmation with biopsy. Most medical societies recommend screening people with GERD and other risk factors with endoscopy, but other alternatives employing less invasive methods are currently being studied. Surveillance strategies vary depending on the endoscopic findings and the Seattle biopsy protocol with random 4-quadrant sampling is recommended. Biomarkers have shown promising results, but more studies are needed in the future. White light endoscopy is the standard practice, but other advanced imaging modalities have shown variable results and hence more studies are awaited for further validation. Endoscopic eradication techniques, including both resection and ablation, have shown good but variable results for treating dysplastic lesions confined to the mucosa. Resection procedures to remove visible lesions followed by ablation of the dysplastic mucosa have shown the best results with higher eradication rates and lower recurrence rates. Surgical management is reserved for lesions with sub-mucosal invasion and lymph node spread with increased risk of metastasis.
El esófago de Barrett (EB) es una lesión premaligna del esófago en la cual el epitelio escamoso del extremo inferior del esófago es remplazado por epitelio columnar. Generalmente, se debe a un daño crónico de la mucosa causando la enfermedad por reflujo gastroesofágico (ERGE). La incidencia del EB en los Estados Unidos se ha estimado en alrededor del 5.6% de la población en general1. En los últimos años, el EB se ha convertido en el foco de los estudios ya que la incidencia del adenocarcinoma esofágico (ACE) se encuentra en aumento en el mundo occidental y actualmente es la quinta causa de muertes debidas a cáncer entre los hombres a nivel mundial2. La secuencia de ERGE que lleva al EB, el cual es premaligno y eventualmente lleva al ACE, ha llamado la atención a los médicos a lo largo del mundo, lo cual resulta en la elaboración de directrices para el tamizaje y la vigilancia del mismo.
EpidemiologíaLa prevalencia de EB ha sido difícil de estimar, ya que la mayoría de los pacientes se encuentran asintomáticos y permanece sin diagnosticar. Se han reportado múltiples tasas en las distintas partes del mundo. En un estudio prospectivo reportado por Rex et al., basado en endoscopia alta (EGD) que fue ofrecida a pacientes sometidos a colonoscopia, la prevalencia de EB fue del 6.8% con una tasa de EB de segmento corto del 5.5%3. Un estudio similar, con una cohorte más pequeña, llevado a cabo por Ward et al. reveló un EB de segmento corto del 15% y un EB de segmento largo del 4%; sin embargo, esta cohorte contaba con una población significativamente mayor4. Ronkainen et al. publicaron un estudio de Suecia basado en EGD practicadas en 1,000 individuos al azar y reportaron una prevalencia de EB del 1.6%, con EB de segmento corto del 1.1% y EB de segmento largo del 0.5%5. Zagari et al., de Italia, publicaron un estudio con una prevalencia de EB del 1.3% y de EB de segmento largo del 0.2%6, mientras que Zou et al., de China, reportaron un EB en el 1.9% y un EB de segmento largo en el 0.5%7. Algunos estudios publicados han reportado una incidencia en aumento y una prevalencia de EB en la población masculina con una relación de casi 2:1, también asociada con una presentación más temprana en hombres que en mujeres8. Esto podría deberse, en parte, al efecto protector de los estrógenos en mujeres9, lo cual podría perderse a medida que van envejeciendo, y al desarrollo de la obesidad, desencadenando esofagitis por reflujo10 y EB, consecuentemente.
Existen otros factores de riesgo para el EB y el ACE, los cuales han sido identificados en estudios clínicos. La obesidad, la raza blanca, la edad avanzada, la pirosis crónica, la edad temprana de aparición del ERGE, la hernia hiatal, el tabaquismo y la historia familiar de esófago de ERGE o formas familiares de EB, así como la apnea del sueño obstructiva, han sido reconocidos como factores de riesgo asociados11. Se ha encontrado que el uso de medicamentos antiinflamatorios no esteroideos y estatinas, la infección por Helicobacter pylori (H. pylori) y una dieta rica en frutas y verduras ayuda a proteger contra el EB. La infección por H. pylori causa gastritis, lo cual lleva a una disminución en la producción de ácido gástrico y, por lo tanto, disminuye el reflujo ácido, lo cual ofrece un efecto protector contra el EB11.
Hay un incremento en la incidencia de EB y de ACE en los países en desarrollo en las últimas décadas, que ha sido atribuida a varios factores. La incidencia en aumento de obesidad, específicamente en obesidad troncal, la cual promueve la ERGE y, por lo tanto, la carcinogénesis, ha sido un gran factor de riesgo. Se ha mostrado que aumenta la ERGE en un 1.5-2% y el riesgo de ACE en un 2-2.5%11. La circunferencia abdominal (radio cintura-cadera) ha sido identificada como un factor de riesgo independiente12. La obesidad visceral también lleva a un estado proinflamatorio con el aumento de varias citocinas, como las interleucinas, factor de necrosis tumoral alfa, proteína C reactiva y leptina, llevando a proliferación celular elevada y apoptosis reducida, y eventualmente a ACE13,14. La disminución en la incidencia de la infección por H. pylori en estos países, que lleva a la secreción aumentada de ácido y a la ERGE, también ha sido postulada15. Las modificaciones dietéticas que involucran mayor cantidad de nitritos, tanto en los alimentos como en los fertilizantes que se utilizan en su cultivo, en conjunto con los bajos niveles de antioxidantes en la comida, también podrían ser factores contribuyentes16.
Criterios de diagnósticoEl diagnóstico de EB requiere tanto la identificación endoscópica de la mucosa columnar como la presencia histológica de metaplasia de tipo intestinal17. La mucosa del esófago se encuentra, por lo general, revestida con epitelio escamoso estratificado y cambia a epitelio columnar a nivel de la unión gastroesofágica (GE), la cual se identifica por la presencia de la cúpula de los pliegues proximales de la mucosa gástrica. El epitelio escamoso es pálido y brillante en su arquitectura, mientras que el epitelio columnar es de color salmón. Normalmente, la unión escamocolumnar coincide con la unión GE, pero cuando se encuentra proximal a la unión GE, existe un esófago con revestimiento columnar, lo cual se considera EB. Si el segmento es<3cm, se denomina EB de segmento corto, y si es ≥ 3cm es EB de segmento largo18. El EB de segmento corto no fue reconocido ampliamente hasta 1994 y los estudios previos generalmente reportaban el EB de segmento largo19. Los estudios más recientes han mostrado que existen proporciones variables de ambos y, por lo tanto, podrían tener una influencia en los síntomas y las complicaciones. La medida endoscópica del segmento de Barrett deberá ser reportada utilizando los criterios de Praga, los cuales incluyen tanto la extensión circunferencial (C) como la máxima extensión (M) del revestimiento columnar visible con endoscopia y los islotes separados por encima del segmento principal marcado en centímetros desde la unión GE20. Varias sociedades, incluyendo las sociedades americanas, requieren para diagnosticar EB la presencia de células columnares especializadas con células secretoras llamadas células calciformes, conocido también como metaplasia intestinal, en las biopsias del esófago21-23. Existe controversia acerca de aceptar células columnares de tipo cardiales (sin células calciformes) como criterio; sin embargo, la Sociedad Británica de Gastroenterología los acepta de acuerdo con las directrices recientemente actualizadas24.
TamizajeLa estrategia tradicional ha sido evaluar a los pacientes con ERGE con una endoscopia e identificar el epitelio columnar metaplásico, obtener biopsias para confirmar el EB e identificar displasia, para entonces darles tratamiento. Existen varios problemas asociados con esta estrategia. A pesar de la incidencia en aumento del ACE, únicamente se ha mostrado una incidencia anual de ACE por EB del 0.1 al 0.3%, lo cual continúa siendo relativamente bajo25-28. Cerca del 40% de los pacientes con ACE no tienen una historia previa de ERGE y solo el 10% de los pacientes con ACE tienen un diagnóstico previo de EB29-31.
La mayoría de las sociedades médicas recomiendan un tamizaje endoscópico en pacientes con ERGE, aunado a otros factores de riesgo para el EB, tales como edad > 50 años, sexo masculino, raza blanca, distribución de grasa corporal intraabdominal con obesidad troncal, tabaquismo, índice de masa corporal (IMC) elevado y hernia hiatal17,22,23,32.
Nuevas modalidades de tamizaje menos invasivas, como la endoscopia transnasal sin sedación y la cápsula endoscópica, han sido estudiadas. Conllevan mejores tasas de participación que la endoscopia con sedación33 y también mostraron ser más costo-efectivas. La cápsula endoscópica ha mostrado alta ganancia diagnóstica en algunos estudios pilotos34,35, mientras que otros estudios han reportado baja sensibilidad y especificidad36 con mayor costo, lo cual es una desventaja. La prueba de citoesponja, un dispositivo de muestreo ingerible que permite la colección de muestras citológicas del esófago para ensayos inmunohistoquímicos, ha mostrado resultados prometedores37,38, con una reducción en la mortalidad cuando se compara con la ausencia de tamizaje39. Actualmente, ninguna de estas ha remplazado la endoscopia tradicional con sedación debido a la falta de evidencias que indiquen que son superiores a los métodos de tamizaje tradicionales.
VigilanciaLa meta de la vigilancia endoscópica es identificar las lesiones precancerosas en una etapa temprana e intervenir con una intención curativa. El ACE tenía una tasa de sobrevida muy pobre, de tan solo 13% al cabo de 5 años40. Los pacientes con EB fueron inscritos en programas de vigilancia endoscópica y se estratificaron de acuerdo con su riesgo sobre la base de la presencia de los diferentes grados de displasia después del estudio histopatológico. No existen ensayos prospectivos controlados y aleatorizados que demuestren la eficacia y la superioridad de estas estrategias de vigilancia para identificar a los pacientes en riesgo, ya que la incidencia anual de ACE continúa siendo baja y una proporción significativa de estos pacientes no tienen EB. En un estudio de cohorte holandés, solo el 5.6% de los pacientes con EB fallecieron a causa de ACE41.
El protocolo de biopsias que se recomienda actualmente durante la endoscopia es el protocolo de Seattle. Comprende un muestreo específico de las lesiones visibles por endoscopia seguido por biopsias aleatorias de los 4 cuadrantes cada 1-2cm, comenzando por los pliegues gástricos proximales hacia la parte más alta de la unión escamocolumnar. La biopsia se debe tomar desde la porción distal hasta la proximal. Se ha demostrado que esto incrementa la ganancia con respecto al diagnóstico de displasia en el EB42. Aun siguiendo este protocolo, solo es posible tomar muestras del 6% del área del EB43. Los estudios han demostrado que este protocolo riguroso no se sigue por completo en la mayoría de los casos, especialmente en pacientes con mayor riesgo de displasia, llevando a tasas disminuidas de detección44,45. Además, es difícil adherirse a este protocolo en pacientes con EB de segmento corto. Por lo tanto, se necesitan mejores modalidades visuales y de imagen, como se describe a continuación, para una mejor identificación de la displasia y en aquellos con mayor riesgo de ACE.
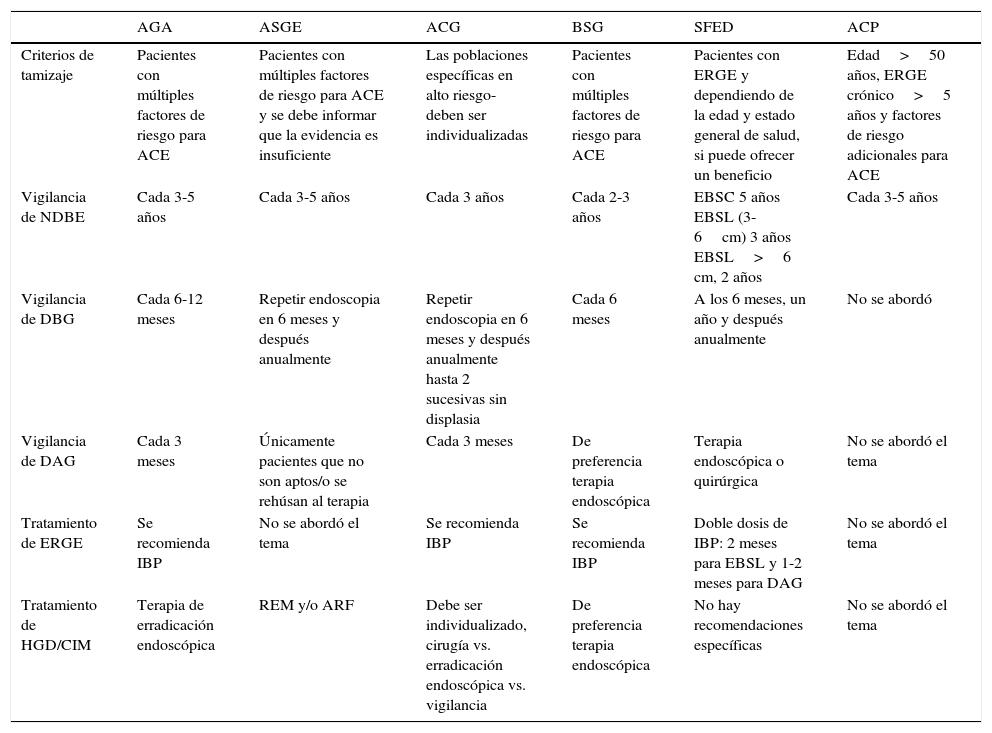
Recomendaciones de varias sociedades de Gastroenterología para el tamizaje y vigilancia del esófago de Barrett| AGA | ASGE | ACG | BSG | SFED | ACP | |
|---|---|---|---|---|---|---|
| Criterios de tamizaje | Pacientes con múltiples factores de riesgo para ACE | Pacientes con múltiples factores de riesgo para ACE y se debe informar que la evidencia es insuficiente | Las poblaciones específicas en alto riesgo- deben ser individualizadas | Pacientes con múltiples factores de riesgo para ACE | Pacientes con ERGE y dependiendo de la edad y estado general de salud, si puede ofrecer un beneficio | Edad>50 años, ERGE crónico>5 años y factores de riesgo adicionales para ACE |
| Vigilancia de NDBE | Cada 3-5 años | Cada 3-5 años | Cada 3 años | Cada 2-3 años | EBSC 5 años EBSL (3-6cm) 3 años EBSL>6 cm, 2 años | Cada 3-5 años |
| Vigilancia de DBG | Cada 6-12 meses | Repetir endoscopia en 6 meses y después anualmente | Repetir endoscopia en 6 meses y después anualmente hasta 2 sucesivas sin displasia | Cada 6 meses | A los 6 meses, un año y después anualmente | No se abordó |
| Vigilancia de DAG | Cada 3 meses | Únicamente pacientes que no son aptos/o se rehúsan al terapia | Cada 3 meses | De preferencia terapia endoscópica | Terapia endoscópica o quirúrgica | No se abordó el tema |
| Tratamiento de ERGE | Se recomienda IBP | No se abordó el tema | Se recomienda IBP | Se recomienda IBP | Doble dosis de IBP: 2 meses para EBSL y 1-2 meses para DAG | No se abordó el tema |
| Tratamiento de HGD/CIM | Terapia de erradicación endoscópica | REM y/o ARF | Debe ser individualizado, cirugía vs. erradicación endoscópica vs. vigilancia | De preferencia terapia endoscópica | No hay recomendaciones específicas | No se abordó el tema |
ARF: ablación con radiofrecuencia; ACE: adenocarcinoma esofágico; ACG: American College of Gastroenterology; ACP: American College of Physicians; AGA: American Gastroenterology Association; ASGE: American Society for Gastrointestinal Endoscopy; BSG: British Society of Gastroenterology; CIM: carcinoma intramucoso; DAG: displasia de alto grado; DBG: displasia de bajo grado; EBND: esófago de Barret no displásico; EBSC: esófago de Barret de segmento corto; EBSL: esófago de Barret de segmento largo; ERGE: enfermedad por reflujo gastrosofágico; IBP: inhibidor de bomba de protones; REM: resección endoscópica de la mucosa; SFED: French Society of Gastrointestinal Endoscopy.
La estratificación de riesgo para el desarrollo de cáncer en pacientes con EB se encuentra en la actualidad basada en la presencia de displasia por histología, a pesar de que el diagnóstico y la evaluación de la displasia se encuentran limitados debido a un bajo grado de acuerdo interobservador. Se han propuesto varios biomarcadores para predecir la progresión neoplásica del EB; sin embargo, únicamente se han llevado a cabo estudios transversales y no existen ensayos prospectivos validados. La tinción inmunohistoquímica del p53ha sido estudiada y propuesta como diagnóstico adjunto a la displasia. La expresión aberrante de p53ha sido asociada con un riesgo incrementado de progresión hacia el cáncer con la sobreexpresión teniendo un riesgo relativo del 5.6 y la pérdida de la expresión un riesgo relativo de 14. El valor predictivo positivo aumentó del 15% con DBG sola al 33% con DBG concurrente con expresión de p53 aberrante46. Otros biomarcadores, como aneuploidía/tetraploidía47,48, pérdida de heterocigosidad (LOH) 17p49, LOH 9p y biomarcadores basados en la metilación de genes, han mostrado resultados prometedores50. Los datos actuales sugieren que estos biomarcadores no son mejores que el hallazgo histológico de displasia de alto grado (DAG) para predecir la progresión del cáncer, aunque podrían ser mejores en la predicción en comparación con el esófago de Barrett no displásico (EBND), la displasia indeterminada o la DBG. La combinación de biomarcadores e histología podrían dar aún mejores resultados. En el futuro, puede haber más estudios y, por lo tanto, estos biomarcadores podrían utilizarse para predecir cuáles pacientes podrían beneficiarse de vigilancia vs. ablación.
Modalidades de imagenología avanzadaAparte de la endoscopia de alta resolución de luz blanca, otras técnicas avanzadas, tales como imagen de banda estrecha (NBI), la cromoendoscopia, la imagen autofluorescente (AFI), la microendoscopia de láser confocal, la espectroscopia de reflectancia difusa, la espectroscopia de dispersión de luz y la tomografía de coherencia óptica (OCT), han surgido recientemente. En la actualidad, la inspección del esófago con luz blanca utilizando endoscopia de alta resolución es el estándar de la práctica y las guías no recomiendan el uso de imagenología endoscópica avanzada para el tamizaje o la vigilancia de pacientes con EB. Con los avances de la tecnología, combinando la endoscopia normal de luz blanca con dispositivos de magnificación y sistemas televisivos de alta resolución, ha permitido la producción de imágenes con mayor calidad, que han mostrado una mayor sensibilidad para la detección de displasia y de lesiones neoplásicas tempranas en el EB51,52.
La cromoendoscopia virtual involucra la aplicación de agentes químicos y de colorantes que resaltan las áreas específicas de la mucosa esofágica y, por lo tanto, ayudan a dirigir la colección de las biopsias. Varios agentes, tales como el azul de metileno, la solución de yodo de Lugol, el índigo carmín y el ácido acético, han sido utilizados con este propósito. El yodo de Lugol tiñe las células escamosas del epitelio que contienen glicógeno y, por lo tanto, permite la identificación de islotes de Barrett con mucosa columnar después de la terapia de erradicación para el EB53. Los estudios que utilizan el azul de metileno para teñir las zonas no displásicas en el EB han reportado resultados mixtos. Horwhat et al. llevaron a cabo un ensayo aleatorizado, prospectivo y cruzado en 48 pacientes, y demostraron que la ganancia en la detección de EB o displasia fue similar entre los pacientes que recibieron biopsias dirigidas utilizando azul de metileno que en aquellos que se sometieron a biopsias de 4 cuadrantes aleatorios; sin embargo, requerían significativamente de menos biopsias cuando se comparaban con aquellos a quienes se les tomaron biopsias aleatorias de los 4 cuadrantes (9.23±2.89 y 18.92±6.36, respectivamente) (p < 0.001)54. Lim et al. concluyeron un estudio aleatorizado cruzado con 30 pacientes con una extensión promedio del segmento de EB de 5 cm. Entre ellos, se encontró que 18 pacientes tenían displasia. En total, 17 de los 18 pacientes con displasia fueron identificados por biopsias aleatorias de los 4 cuadrantes, mientras que únicamente 9 fueron identificados utilizando azul de metileno (p = 0.02)55. Ngamruengphong et al. llevaron a cabo un metaanálisis, reportando la ganancia diagnóstica utilizando la cromoendoscopia con azul de metileno. No hubo incremento significativo en la ganancia (IY) sobre las biopsias aleatorias de 4-cuadrantes para metaplasia (IY 4%), displasia (IY 9%) y cáncer temprano (IY 5%)56. Olliver et al. aseguran que podría llevar a daño en el ADN del epitelio de Barrett y, por lo tanto, podría potencialmente acelerar la carcinogénesis57. En los estudios se han identificado 4 patrones de foveolas específicas utilizando la aplicación tanto de ácido acético como del índigo carmín-redondo, reticular, rugoso y velloso. Guelred et al. describieron que los patrones rugoso y velloso se asociaron con metaplasia intestinal utilizando ácido acético, mientras que otro estudio utilizando índigo carmín en 80 pacientes reportó que el patrón rugoso/velloso tenía una sensibilidad del 97% y una especificidad del 76% para metaplasia intestinal53.
La NBI es una forma de cromoendoscopia electrónica que utiliza filtros ópticos de banda espectral estrecha, imágenes de banda óptica, tecnología i-scan para resaltar los patrones vasculares o para diferenciar el contraste entre el epitelio escamoso y el columnar58. Se han publicado algunos ensayos prospectivos comparando NBI con endoscopia de luz blanca de alta resolución. En el estudio llevado a cabo por Wolfsen et al. con 65 pacientes conocidos por tener con displasia en el EB, el NBI identifica a más pacientes con displasia, así como grados de displasia más altos en comparación con la endoscopia de luz blanca59. En otro ensayo cruzado, multicéntrico, aleatorizado, que comparó a ambos, el NBI detectó el mismo número de pacientes con metaplasia, pero una mayor proporción de áreas con displasia (30% vs. 21%, p=0.01)60. La mucosa y los vasos de apariencia regular con NBI no albergaban ninguna displasia de alto grado (DAG). Más aún, requerían significativamente de menos biopsias que con la endoscopia de luz blanca (3.6 vs. 7.6, p<0.0001).
La endoscopia de AFI se basa en el principio de que cuando la luz del láser es emitida por endoscopia, las células vuelven a emitir una luz fluorescente con características espectroscópicas distintas. Kara et al. encontraron que es un estudio con muy buena sensibilidad para la identificación de DAG, pero con una pobre especificidad y una alta tasa alta de falsos positivos61. Mannath et al. publicaron un reporte reciente que estudiaba el acuerdo interobservador entre expertos y no expertos para la AFI62. Concluyeron que existía un acuerdo de justo a moderado para AFI por sí sola, lo cual mejoraba cuando se combinaba con endoscopia de luz blanca de alta resolución. Curvers et al. publicaron un reporte que utilizó la técnica de «imagen trimodal», en la cual el esófago se revisaba en primera instancia utilizando luz blanca de alta resolución seguido por AFI para resaltar las zonas anormales no observadas con luz blanca, seguido con NBI para confirmar las áreas anormales con AFI63. AFI diagnosticó una proporción significativamente mayor de áreas anormales que la luz blanca, pero con una tasa más alta de falsos positivos del 81%, lo cual se redujo a un 26% con NBI. Sin embargo, aún no puede reemplazar a la biopsia tradicional de 4 cuadrantes, ya que el 10% de los casos no se detectaron con las 3 modalidades.
La microendoscopia confocal utiliza la técnica de traslación de la luz de laser derivada de endoscopia reflejada en la computadora en una imagen en sección transversal de la arquitectura de la mucosa. Con esta, se puede llevar a cabo un análisis en tiempo real de los vasos sanguíneos y las criptas. Los reportes que se han publicado hasta el momento han mostrado buenas tasas de precisión (85%-94%) en detección de displasia64,65. Pohl et al. condujeron un estudio prospectivo de 2 centros y reportaron que los criterios de microscopia de láser confocal para el EB se detectaban con mayor frecuencia en DAG y cáncer temprano que en displasia de bajo grado, con un buen acuerdo interobservador, con un valor kappa de 0.666. Las técnicas de espectroscopia se basan en el análisis de la luz diseminada del tejido. La espectroscopia de reflectancia difusa analiza la luz diseminada en múltiples ocasiones dentro del tejido, mientras que la espectroscopia de dispersión de luz utiliza la luz que se refleja una sola vez. Se ha reportado que estas técnicas pueden distinguir displasia de grados más altos de displasia de grados bajos y también de no displasia hasta un 88%, con una sensibilidad y una especificidad cercanas al 90%. La OCT utiliza luz casi infrarroja para proporcionar imágenes de alta resolución y los estudios iniciales han reportado tasas de sensibilidad y especificidad >90% en la detección de metaplasia67-69.
A pesar de tener resultados prometedores, se necesitan más estudios para validar estas técnicas, optimizando los costos asociados y desarrollando métodos de enseñanza ideales para que esta tecnología llegue a los gastroenterólogos más allá de los centros terciarios. En la actualidad, la endoscopia de alta resolución con biopsias de 4 cuadrantes aleatorizadas ha sido la modalidad más aceptada para el diagnóstico de metaplasia y displasia en el EB.
Técnicas de erradicación endoscópicaLa erradicación utilizando técnicas endoscópicas incluye ya sea un procedimiento como la resección endoscópica de mucosa (REM) y disección endoscópica de la submucosa (DES) o procedimientos ablativos de la mucosa del EB con varias técnicas. La ventaja de los procedimientos de resección es que son tanto diagnósticos como terapéuticos, ya que se obtiene una muestra de tejido, mientras que los procedimientos de ablación únicamente son terapéuticos. Todos los procedimientos endoscópicos deben ser seguidos por una terapia de supresión de ácido que permitan la cicatrización y la reepitelización de la mucosa esofágica con epitelio escamoso.
Los procedimientos quirúrgicos solían ser el tratamiento de elección aun en las lesiones premalignas; sin embargo, los tratamientos endoscópicos, gracias a los avances, ahora son utilizados más ampliamente. Un criterio importante que se debe considerar antes de elegir la terapia endoscópica es evaluar el grado de extensión de la displasia en el EB. Debe estar confinada a la mucosa únicamente (etapa T1a) y no debe estar comprometida la submucosa, en cuyo caso el manejo quirúrgico es el estándar de tratamiento. Se ha probado que las neoplasias tempranas que comprometen solamente a la mucosa tienen un riesgo del 1-2% de metástasis a ganglios linfáticos70, mientras aquellos con invasión de la submucosa tienen un 10% de riesgo de linfoadenopatías71, y unos cuantos reportes han indicado que podría ser hasta de un 20%72,73. Por lo tanto, una acertada evaluación de las etapas T de neoplasias es esencial para la elección de la terapia a utilizar. El ultrasonido endoscópico (UE) es la modalidad de imagen más acertada para la evaluación de la etapa T de las neoplasias, pero puede predecir la profundidad de invasión en tan solo 50-60% de los casos. Por otro lado, los estudios de REM con biopsia de espécimen han mostrado una mejor tasa de predicción en la evaluación de las etapas de T y ser superiores a los estudios de UE74,75.
Los estudios retrospectivos que han comparado la cirugía con la terapia endoscópica para neoplasias tempranas han mostrado que la cirugía tiene una mortalidad a corto plazo más alta76-80, mientras que la endoscopia tiene menor morbilidad, mejor costo-efectividad81 y un menor riesgo de complicaciones82,83.
Resección endoscópicaLa REM y la DES son 2 procedimientos de resección. Estos involucran la resección sistemática de una zona específica del esófago con un bisturí endoscópico o pinza diatérmica. Se utilizan específicamente con displasia nodular visible o EB displásica de segmento corto, para lo cual son preferibles sobre las técnica de ablación. El BSG recomienda 2 técnicas básicas que son el principio por el que esta se rige. La técnica de ligadura de banda incluye la succión de la zona deseada y la colocación de una banda que crea un seudopólipo, el cual se puede resecar con una pinza diatérmica24. La técnica de capuchón y lazado involucra el levantamiento de la zona deseada por medio de una inyección submucosa para colocar un capuchón por encima de la mucosa y así poder extraerlo con un asa24. La REM para DAG y ACE en etapas T1ha sido exitosa en el 91-98% de los casos84-86. Más aún, algunos estudios de cohortes han mostrado que la REM erradica el EB en 75-100% de los pacientes y erradica la displasia en 86-100% de los casos87-92. La DES asistida con agua a chorro ha sido intentada con una tasa de resección en bloque de cerca del 90%93. No existen muchos estudios directos que hayan comparado la REM con la DES, sin embargo, un estudio de Ishihara et al. comparando REM con DES para carcinoma de células escamosas del esófago reveló que la REM tenía una tasa de recurrencia local más alta (23.91% vs. 3.13%), lo cual indica que la DES es la técnica preferible cuando esta se encuentre disponible, aun cuando sea más demandante técnicamente94. Su estudio también sugiere que, a pesar de la resección de la mucosa displásica, el EB no displásico remanente aún se encuentra en riesgo y, por lo tanto, debe ser erradicado por resección o ablación. Wani et al. reportaron que, en su estudio multicéntrico de cohortes, la REM podría cambiar el diagnóstico histológico en hasta un 30% de los pacientes, lo cual potencialmente podría cambiar el curso del manejo95. Las complicaciones de la REM son sangrado inmediato hasta en un 10%76,85,96, perforación en el 3-7% de los pacientes83,86,97 y formación tardía de estenosis en el 17-37% de los pacientes98.
Técnicas de ablación endoscópicaLas técnicas de ablación pueden ser térmica, ablación por radiofrecuencia (ARF), terapia fotodinámica (TFD), electrocoagulación multipolar (ECMP), crioterapia, coagulación con argón plasma (CAP). Estas técnicas generalmente se llevan a cabo cuando no existen lesiones visibles en el epitelio displásico, en cuyo caso las técnicas de resección pueden tener una tasa más exitosa.
La TFD involucra el uso de químicos fotosensibles, como el ácido 5-aminolevulínico o porfímero sódico, para sensibilizar los tejidos y destruirlos con luz láser endoscópica. La luz láser causa la generación de radicales libres cuando se encuentran expuestos a las células sensibilizadas, lo cual conduce al daño. Se ha logrado obtener una tasa de éxito de la erradicación de DAG de hasta un 77% en 5 años99,100. En un estudio retrospectivo de cohortes por Overholt et al., en 103 pacientes con EB con displasia e IMC que tuvieron un seguimiento de hasta 50 meses, el éxito por intención de tratar y de erradicación fue del 92% para displasia de bajo grado, el 77.5% para DAG y el 44.4% para IMC99. Las complicaciones incluyeron la tasa de formación de estenosis de hasta el 30%, la fotosensibilidad de la piel en hasta el 33% (p<0.05) y el epitelio de EB enterrado debajo de epitelio escamoso, que fue significativamente superior en hasta el 48% de los pacientes y podría eventualmente volverse maligno99-102. El dolor durante el postoperatorio inmediato ha sido reportado como un efecto secundario significativo en la mayoría de los pacientes, con estudios reportando tasas tan altas como del 86% de los pacientes103,104. Debido a tasas comparativamente más altas, la TFD no es una opción favorable para la terapia de EB.
La terapia con crioablación es una técnica sin contacto que se lleva a cabo mediante el rocío de nitrógeno líquido o dióxido de carbono para congelar y destruir la mucosa del Barrett105,106. El nitrógeno líquido o el dióxido de carbono se rocía para congelar el tejido durante 10 a 20 s, seguidamente se deja descongelar por un minuto, con 3-4 ciclos por sesión. Se puede volver a repetir una sesión un par de meses más tarde, en caso de que hubiese necesidad. Se ha demostrado que esto erradica la metaplasia y la displasia intestinal en el 46-78% y el 79-87% de los casos, respectivamente106,107. Dumont et al. demostraron, en su ensayo de cohorte no aleatorizado de 30 pacientes, que hasta el 68% de los pacientes con DAG y el 80% de IMC tenían una disminución del DAG o eliminación del cáncer108.
La ECMP y la CAP son otras técnicas de erradicación endoscópica que no han sido estudiadas extensamente para el manejo de EB, a pesar de que existen varias series de casos prospectivos que describen su uso y éxito. Montes et al. reportaron una tasa de erradicación del 100% en los casos de esófago de Barrett no displásico (EBND) en su serie de 14 pacientes, con un seguimiento promedio de 21.6 meses109, mientras que Sampliner et al. reportaron una tasa de tan solo el 78% en el seguimiento de 6 meses110. Para la CAP, Madisch et al. reportaron una tasa de erradicación del 98% y una tasa de recurrencia del 12% en su serie con un seguimiento promedio de 51 meses111, mientras que otro estudio reportó una tasa de erradicación solo del 84% y una tasa de recurrencia de hasta el 66% en el seguimiento a 30 meses112. Algunos estudios aleatorizados controlados comparando ECMP con APC no mostraron diferencias significativas en sus tasas de erradicación, aunque ambos necesitaron de múltiples sesiones de tratamiento.
La ARF se trata de la colocación de electrodos ubicados con cercanía para enviar energía de radiofrecuencia a la mucosa esofágica, lo cual produce la ablación. Esto genera energía térmica uniforme en forma circunferencial, mientras que la fuerza, la duración y la densidad de la energía térmica pueden variar. Varios estudios han comparado la ARF con otras terapias de ablación y han mostrado que la ARF tiene una tasa de éxito mayor, una tasa disminuida de recurrencia de la displasia y es comparativamente más segura que otras técnicas. Un estudio prospectivo multicéntrico demostró una remisión del 70% en el EB con el tratamiento circunferencial113; sin embargo, Ganz et al. publicaron un reporte subsecuente que describió una tasa de erradicación del 98% cuando se utilizaba una técnica de ablación focal después de haber utilizado la ablación circunferencial114. En un ensayo multicéntrico controlado con simulación en 127 pacientes con EB displásico hubo una erradicación completa de DBG en un 90.5% (p>0.001) de los pacientes y en el 81% de los pacientes con DAG (p<0.001) durante un seguimiento a 12 meses115. En un ensayo multicéntrico, aleatorizado, controlado, de Phoa et al., comparando ARF con vigilancia endoscópica para EB con DBG, se demostró que la ARF redujo el riesgo de progresión a DAG en un 25% (p<0.001) y a adenocarcinoma en un 7.6% (p=0.03) durante el seguimiento a 3 años116. Hubo resolución completa de la displasia en el 92.6% de los pacientes. En un registro en el Reino Unido llevado a cabo en 335 pacientes con EB, en el cual el 72% tenía DAG, la ablación con ARF llevó a la resolución en el 86% y la resolución del DAG en el seguimiento a 12 meses117. El Barrett de segmento corto respondió mejor y la reversión de la displasia era un 15% menos probable por cada centímetro aumentado en la longitud del segmento de Barrett117. Una revisión sistemática que comparaba la metaplasia subescamosa en pacientes tratados con ARF y TPD mostró que el 0.9% de los pacientes tratados con ARF y el 14.2% de los que recibieron tratamiento con TPD tenían metaplasia, demostrando de esta manera la superior eficacia de la ARF118. En una revisión sistemática y metaanálisis por Orman et al., la complicación más frecuente era la formación de estenosis (5%), seguida por dolor (3%) y sangrado (1%), lo cual refleja los resultados en la mayoría de los demás artículos publicados y estudios retrospectivos119. La ARF también ha demostrado tener una tasa menor de incidencia de estenosis en comparación con la resección endoscópica radical escalonada (14% vs. 88%, p < 0.001)120. A pesar de los resultados positivos con los procedimientos de ablación en la eliminación de la displasia y la reducción en la progresión neoplásica, su papel en EBND ha sido cuestionado en los estudios en relación con la recurrencia de la metaplasia durante el seguimiento debido a metaplasia subescamosa, durabilidad de la respuesta y, en algunos análisis, una tasa de recurrencia de hasta el 33%121. Por lo tanto, los procedimientos de ablación podrían ser un enfoque positivo en el tratamiento de DBG, dada la tasa reducida de progresión a cáncer. Sin embargo, el sometimiento innecesario de los pacientes con EBND a estos procedimientos endoscópicos, con un aumento en las tasas de complicaciones, demandan la publicación de datos a largo plazo. Bajo las circunstancias actuales, los procedimientos por ablación no son recomendados por las sociedades médicas.
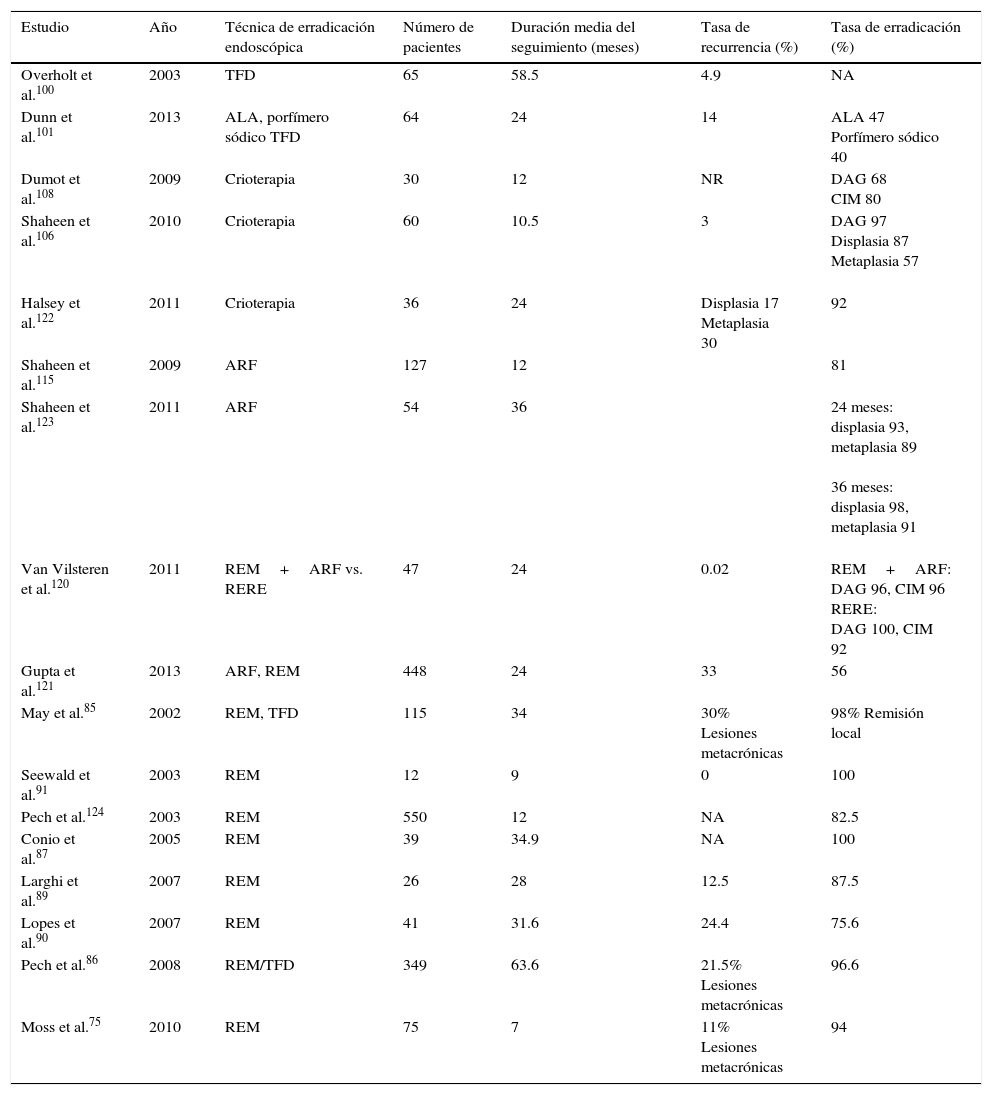
Tasa de recurrencia de la displasia de alto grado y cáncer intramucoso en esófago de Barrett con varias técnicas de erradicación endoscópica| Estudio | Año | Técnica de erradicación endoscópica | Número de pacientes | Duración media del seguimiento (meses) | Tasa de recurrencia (%) | Tasa de erradicación (%) |
|---|---|---|---|---|---|---|
| Overholt et al.100 | 2003 | TFD | 65 | 58.5 | 4.9 | NA |
| Dunn et al.101 | 2013 | ALA, porfímero sódico TFD | 64 | 24 | 14 | ALA 47 Porfímero sódico 40 |
| Dumot et al.108 | 2009 | Crioterapia | 30 | 12 | NR | DAG 68 CIM 80 |
| Shaheen et al.106 | 2010 | Crioterapia | 60 | 10.5 | 3 | DAG 97 Displasia 87 Metaplasia 57 |
| Halsey et al.122 | 2011 | Crioterapia | 36 | 24 | Displasia 17 Metaplasia 30 | 92 |
| Shaheen et al.115 | 2009 | ARF | 127 | 12 | 81 | |
| Shaheen et al.123 | 2011 | ARF | 54 | 36 | 24 meses: displasia 93, metaplasia 89 36 meses: displasia 98, metaplasia 91 | |
| Van Vilsteren et al.120 | 2011 | REM+ARF vs. RERE | 47 | 24 | 0.02 | REM+ARF: DAG 96, CIM 96 RERE: DAG 100, CIM 92 |
| Gupta et al.121 | 2013 | ARF, REM | 448 | 24 | 33 | 56 |
| May et al.85 | 2002 | REM, TFD | 115 | 34 | 30% Lesiones metacrónicas | 98% Remisión local |
| Seewald et al.91 | 2003 | REM | 12 | 9 | 0 | 100 |
| Pech et al.124 | 2003 | REM | 550 | 12 | NA | 82.5 |
| Conio et al.87 | 2005 | REM | 39 | 34.9 | NA | 100 |
| Larghi et al.89 | 2007 | REM | 26 | 28 | 12.5 | 87.5 |
| Lopes et al.90 | 2007 | REM | 41 | 31.6 | 24.4 | 75.6 |
| Pech et al.86 | 2008 | REM/TFD | 349 | 63.6 | 21.5% Lesiones metacrónicas | 96.6 |
| Moss et al.75 | 2010 | REM | 75 | 7 | 11% Lesiones metacrónicas | 94 |
ALA: ácido 5-aminolevulínico; ARF: ablación con radiofrecuencia; CIM: carcinoma intramucoso; DAG: displasia de alto grado; NA: no se abordó; REM: resección endoscópica de la mucosa; RERE: resección endoscópica radical escalonada; TFD: terapia fotodinámica.
Durante varias décadas, la esofagectomía era la opción terapéutica tradicional para la DAG. Elimina tanto el EB displásico como el no displásico, proporcionando una biopsia de tejido, así como la opción de remover los ganglios linfáticos con metástasis. El tratamiento quirúrgico es considerado el tratamiento de elección cuando existe una invasión a la submucosa con riesgo aumentado de metástasis. Existen varias técnicas de esofagectomía y todos muestran resultados similares. Se realizan la transhiatal, toracoabdominal, preservadora del vago, segmentaria de Merendino, laparoscopia o esofagectomía de invasión mínima24. Cuando se compara con las terapias endoscópicas, tiene una tasa de mortalidad y morbilidad significativamente mayor, especialmente a corto plazo, pero con tasas de sobrevida casi similares80. La mayoría de los estudios se han llevado a cabo en pacientes sintomáticos, ancianos y debilitados, que presentaban tasas de mortalidad más altas que las series pequeñas en población más joven, las cuales tenían una tasa de mortalidad de menos del 3.3%79. También se ha demostrado que afectan a la calidad de vida en el corto plazo, mientras que los estudios a largo plazo han mostrado resultados comparables con aquellos en la población general. Se han reportado en raras ocasiones una neometaplasia en el esófago remanente debido al reflujo125; sin embargo, el riesgo es muy bajo. Por lo tanto, la esofagectomía es definitivamente una opción que debe ser considerada en casos de pérdida de la continuidad de la mucosa o con linfoadenopatías, en especial en la población más joven y con mejor salud.
FinanciamientoNo se recibió apoyo económico en relación con este estudio/artículo.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de interés.