La incidencia del cáncer de esófago viene aumentando progresivamente a nivel mundial. Su pronóstico es pobre ya que en su mayoría el diagnóstico se realiza en estadios avanzados. Sin embargo, cuando es detectado en estadio precoz, las neoplasias esofágicas pueden ser tratadas de forma curativa y por métodos menos invasivos, resultando en una sobrevida de más del 90% en 5 años. Por lo tanto, es clave identificar la población de alto riesgo del cáncer esofágico y recomendarles endoscopia de alta resolución de cribado, agregando recursos de cromoendoscopia con lugol (o digital) y magnificación. Este examen sistematizado permite reconocer la neoplasia esofágica en estadio temprano, donde se puede proponer tratamiento endoscópico mediante la disección endoscópica submucosa (DES) realizándose la resección en bloque de la lesión tumoral con disminución de la morbimortalidad en comparación con el tratamiento estándar previo, incluso en estadios tempranos como lo era la esofagectomía. El objetivo de este artículo es revisar los últimos avances en el manejo de las neoplasias esofágicas superficiales a través de la DES.
The incidence of esophageal cancer is steadily increasing worldwide. Outcome is poor, given that the majority of cases are diagnosed at advanced disease stages. However, when detected at early stages, esophageal tumors can be curatively treated through less invasive methods, resulting in a 5-year survival rate above 90%. Therefore, it is essential to identify the high-risk population and recommend those patients undergo screening using high-resolution endoscopy, adding the resources of chromoendoscopy with Lugol’s solution (or digital chromoendoscopy) and magnification. Such systematized examination makes it possible to recognize early-stage esophageal neoplasia and propose endoscopic submucosal dissection as treatment. In that procedure, the tumor is resected en bloc, resulting in lower morbidity and mortality, compared with previous standard treatment, including early-stage esophagectomy. The present article is a review of the latest advances in the management of superficial esophageal tumors through endoscopic submucosal dissection.
La neoplasia maligna de esófago es el octavo cáncer más frecuente y la sexta causa de muerte en el mundo, se estima que hubo 450,000 nuevos casos que fueron diagnosticados en el 2012 y cerca de 400,000 muertes atribuibles a esta condición el mismo año, y esto guarda relación con la presentación de los síntomas en etapas ya avanzadas, presentando en ese momento un pobre pronóstico, ya que una cura definitiva no es una opción, por lo que es esencial su diagnóstico en estadios tempranos1-4. La incidencia de esta neoplasia se incrementó a nivel mundial y en los Estados Unidos, donde en este se observó un aumento de su incidencia de hasta 7 veces en los últimos 30 años, sobre todo en la población masculina de raza blanca; sin embargo, el promedio de sobrevida a los 5 años del cáncer de esófago no mejora y se mantiene por debajo del 15%1,3.
En el esófago existen 2tipos de neoplasias primarias: carcinoma de células escamosas (CCE) y el adenocarcinoma. El CCE es el tipo más frecuente en Asia y en el resto del mundo, y está asociado al tabaco, el abuso de alcohol, el uso de nitrosaminas, la ingesta de cáusticos, la acalasia, la injuria térmica debido a bebidas calientes, la tilosis y la deficiencia de micronutrientes (riboflavina, retinol, ácido ascórbico, alfatocoferol, selenio, magnesio, cinc). El adenocarcinoma, a su vez, es frecuente en Europa y Norte América, siendo sus factores de riesgo la enfermedad por reflujo gastroesofágico (esófago de Barrett) y el índice de masa corporal aumentado1,2,5-7. El CCE de esófago es más frecuente en los varones (3.6:1) entre la quinta y séptima década de vida, teniendo una tasa de mortalidad en Brasil de 14.3 en varones y 4.2 en mujeres por cada 100,000 personas8. Estos 2tipos de cáncer difieren en la tasa de linfoadenopatías metastásicas, observándose mayor riesgo en los pacientes con CCE en comparación con los pacientes con adenocarcinoma7.
El desarrollo de nuevas técnicas de endoscopia que incluyen la cromoendoscopia con lugol o por imagen de banda estrecha (narrow band imaging [NBI] o flexible spectral imaging color enhancement [FICE], por sus siglas en inglés), magnificación endoscópica, microscopia confocal, endoscopia de alta resolución y espectroscopia han incrementado la sensibilidad y la especificidad en la detección de este tipo de neoplasia en estadios tempranos, siendo esto trascendente, ya que con un diagnóstico temprano de CCE su pronóstico mejora con tasas de sobrevida a los 5 años hasta en un 95%3,4,8-11.
Tradicionalmente, el tratamiento de elección del cáncer de esófago era el quirúrgico incluso en estadios tempranos; sin embargo, la esofagectomía está asociada a mayores tasas de morbimortalidad6. En las últimas 2décadas el tratamiento endoscópico en el cual se incluye a la resección de mucosa endoscópica (EMR, por sus siglas en inglés) y la disección endoscópica submucosa (DES) han progresado, siendo una alternativa curativa viable a la cirugía en casos seleccionados del cáncer de esófago temprano. Las ventajas del tratamiento endoscópico son la preservación del órgano, la tasa de mortalidad prácticamente nula y las bajas tasas de complicaciones, las cuales se encuentran entre el 1 y el 8% incluyendo sangrado, perforación y estenosis2,6,9,11.
La EMR fue la primera terapia endoscópica desarrollada y ha sido usada como tratamiento del CCE superficial, siendo efectiva y menos invasiva que la esofagectomía. Sin embargo, esta técnica solo retira lesiones pequeñas en bloque (< 10mm), por lo que lesiones más grandes requieren resecciones tipo piecemeal, lo cual predispone a una evaluación histopatológica imprecisa y está asociada a tasas elevadas de recurrencia local2,4,10. En el caso de la DES, fue una técnica desarrollada en Japón y propone la resección en bloque incluso en lesiones mayores de 20mm, reduciendo la necesidad de resección tipo piecemeal y permitiendo una evaluación precisa de los márgenes de resección (vertical y lateral), obteniendo como resultado tasas de recurrencia local mucho menores que la EMR y una excelente sobrevida libre de cáncer a largo plazo4,6,12-14.
El presente artículo tiene como objetivo contribuir al entendimiento de los avances recientes del manejo del cáncer de esófago temprano con una revisión detallada de la técnica de DES en pacientes con CCE, difundiendo dicho procedimiento para su incorporación en los centros occidentales de endoscopia, especialmente en los países latinoamericanos. Dado que el tratamiento endoscópico del CCE de esófago es distinto en varios aspectos del manejo del adenocarcinoma y de la displasia de alto grado del esófago de Barrett, en esta revisión enfocaremos los aspectos técnicos relacionados con el diagnóstico y el tratamiento del CCE de esófago.
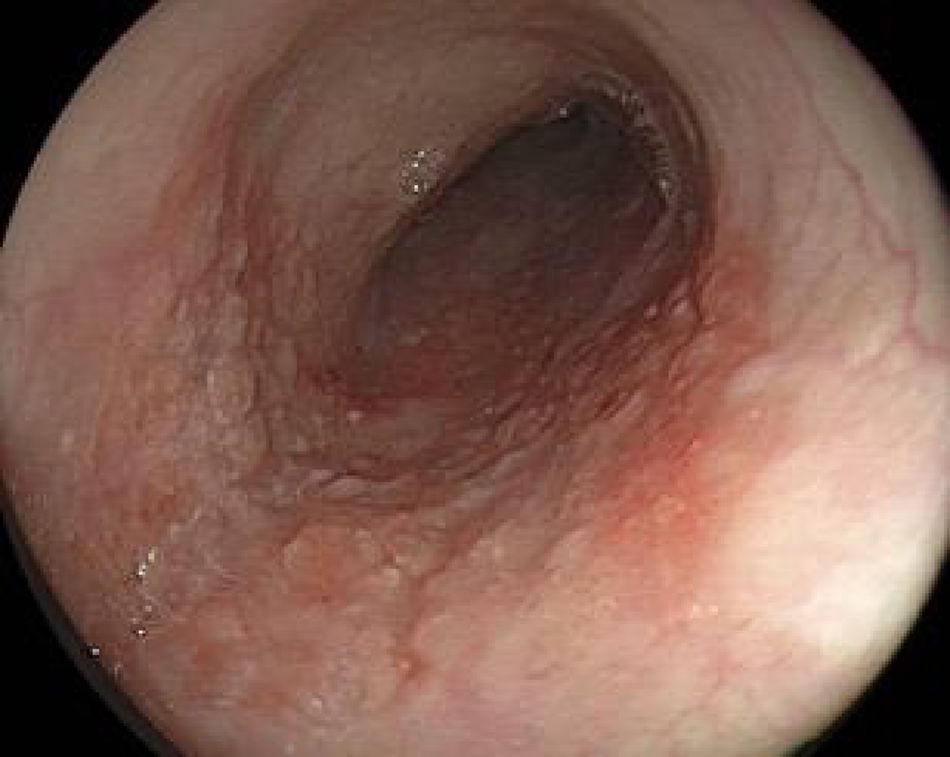
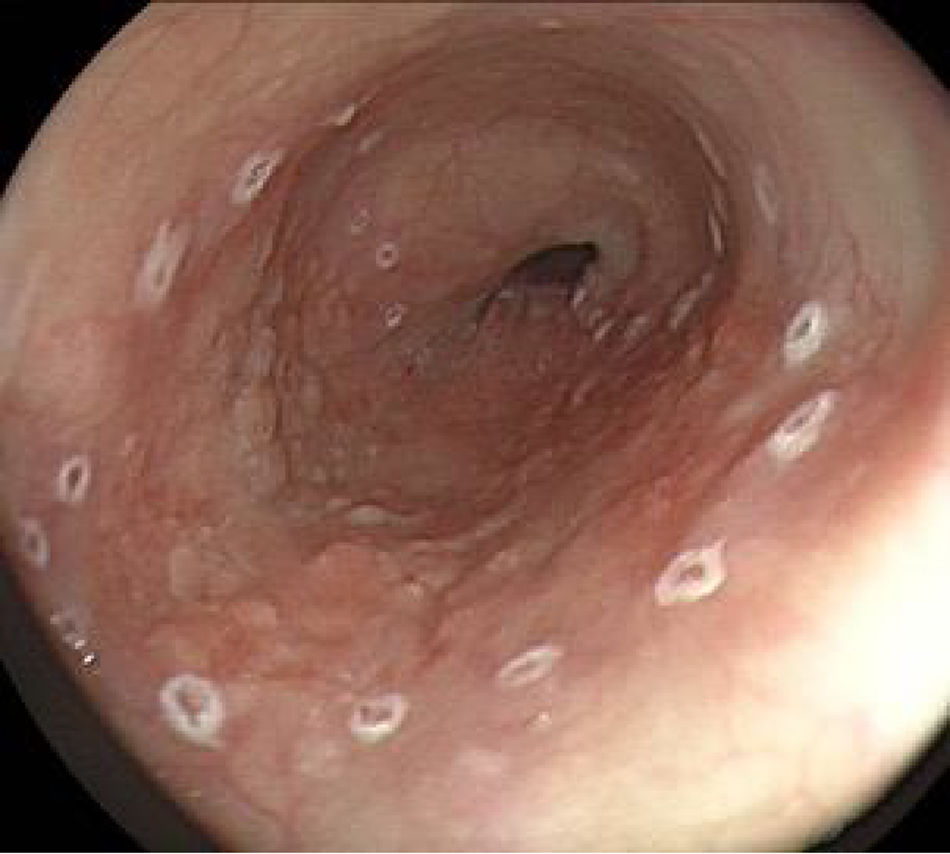
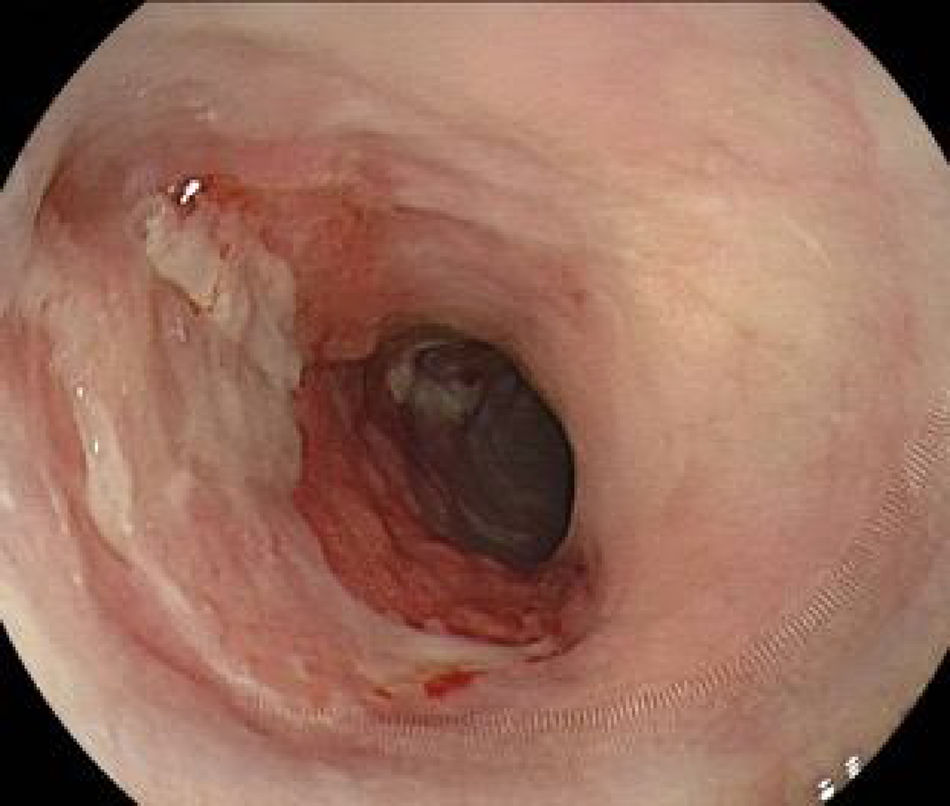
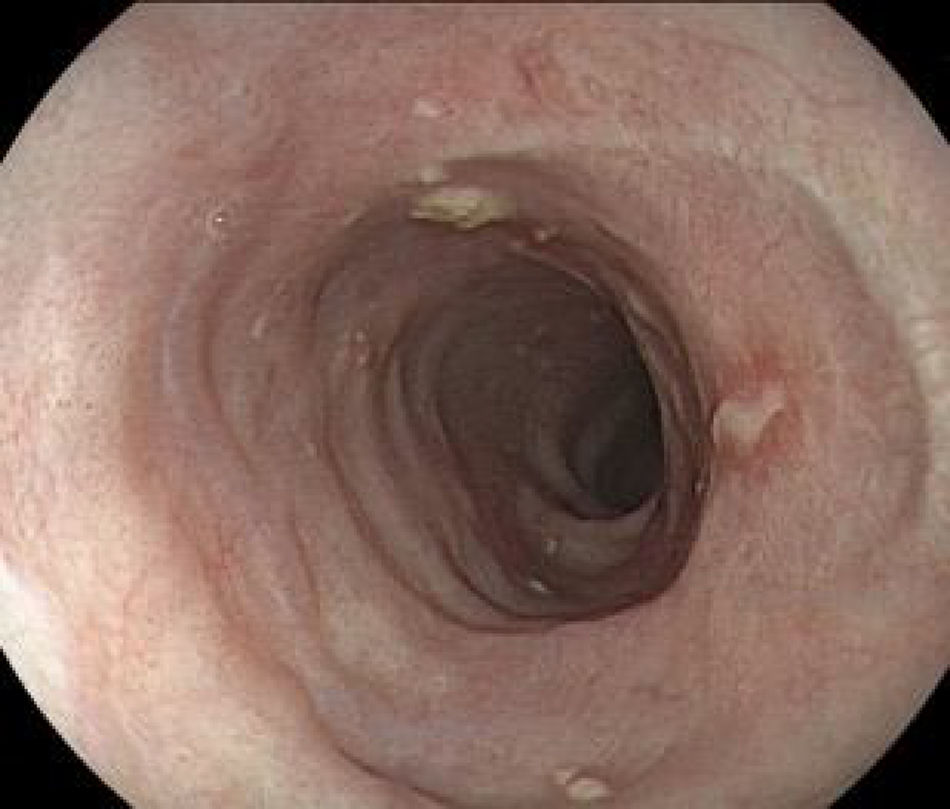
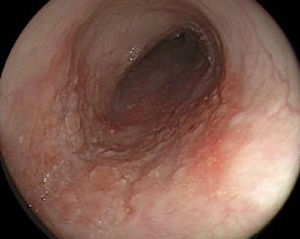
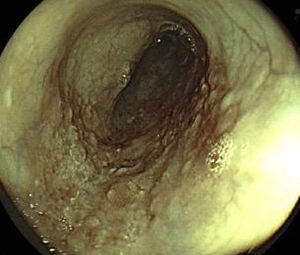
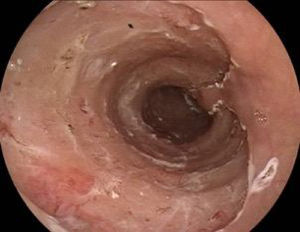
DiagnósticoLa neoplasia del esófago clásicamente puede presentarse con disfagia progresiva y pérdida de peso. Cuando hay dolor torácico debe sospecharse invasión al mediastino y si existe ulceración o esofagitis proximal asociada el paciente puede manifestar odinofagia1. En estos casos los tumores suelen ser avanzados y no hay posibilidad de tratamiento endoscópico curativo. Por lo tanto, el primer desafío es establecer el diagnóstico de cáncer de esófago en estadio temprano, es decir, cuando los pacientes son asintomáticos y con cambios endoscópicos sutiles y difíciles de reconocer entre los que se describe una mucosa con epitelio pálido o rojo, alteración en el patrón microvascular con elevación o depresión leve de su superficie (fig. 1)1,8.
El mejor método diagnóstico es la endoscopia, más aún si es combinada con la técnica de la cromoendoscopia, con la cual mejora la detección, dado que la displasia escamosa puede ser de difícil reconocimiento con el uso de la endoscopia estándar2,8. No obstante, realizar una endoscopia a la población general como tamización de CCE de esófago no es justificable debido a los costos del procedimiento, pero en la población de alto riesgo, como por ejemplo en pacientes con carcinoma escamo-celular de cabeza y cuello, dicha vigilancia es costo-efectiva8.
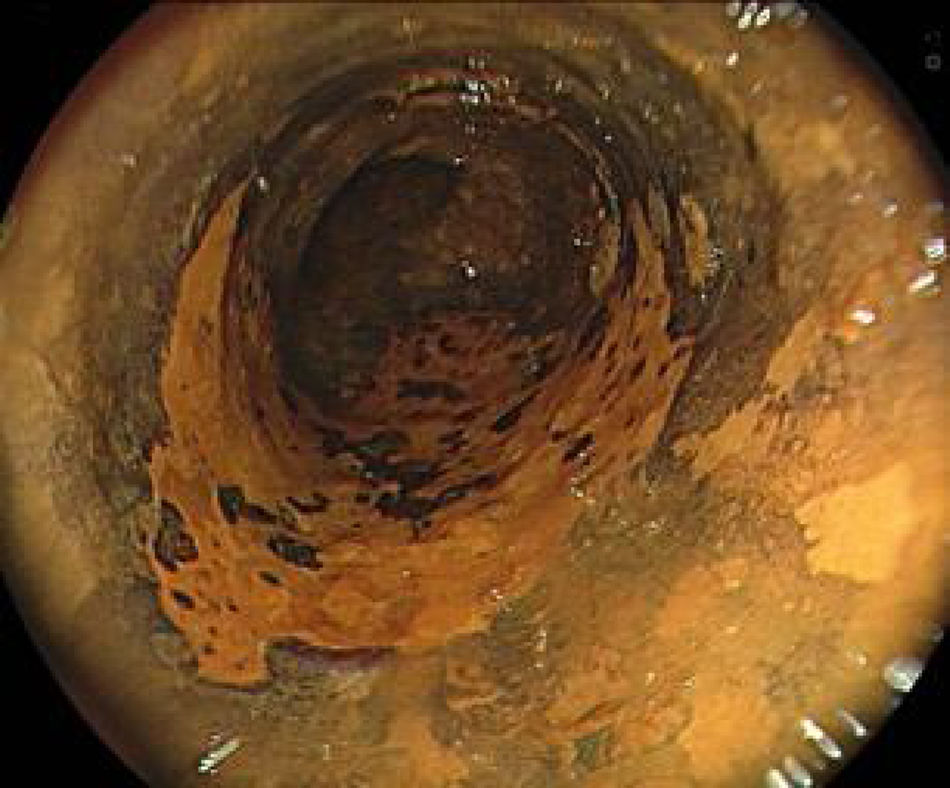
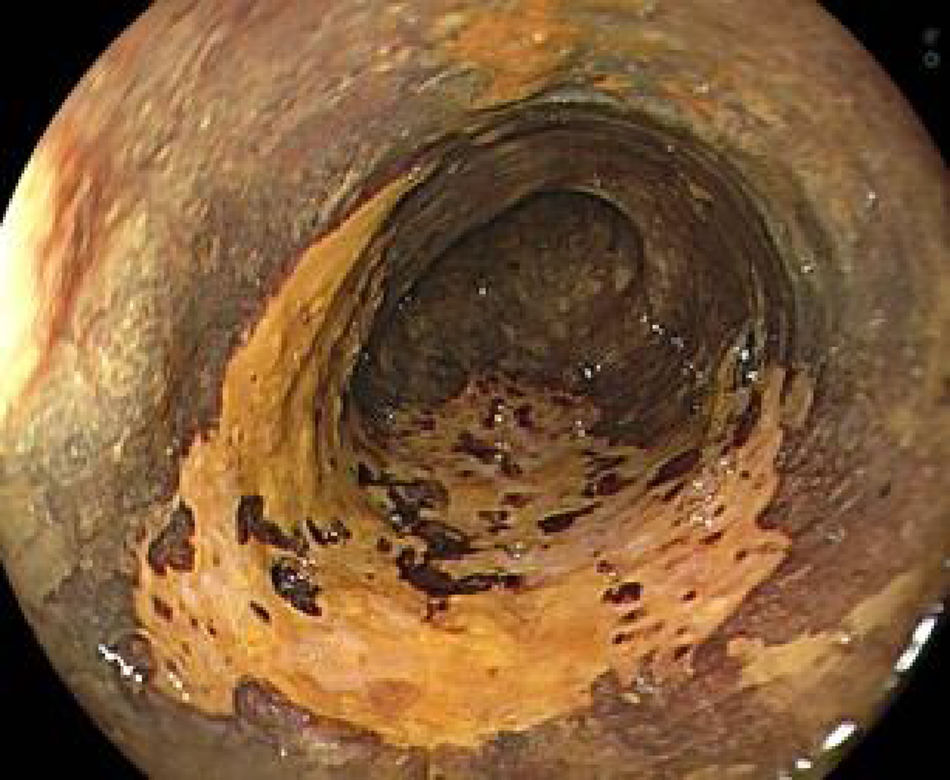
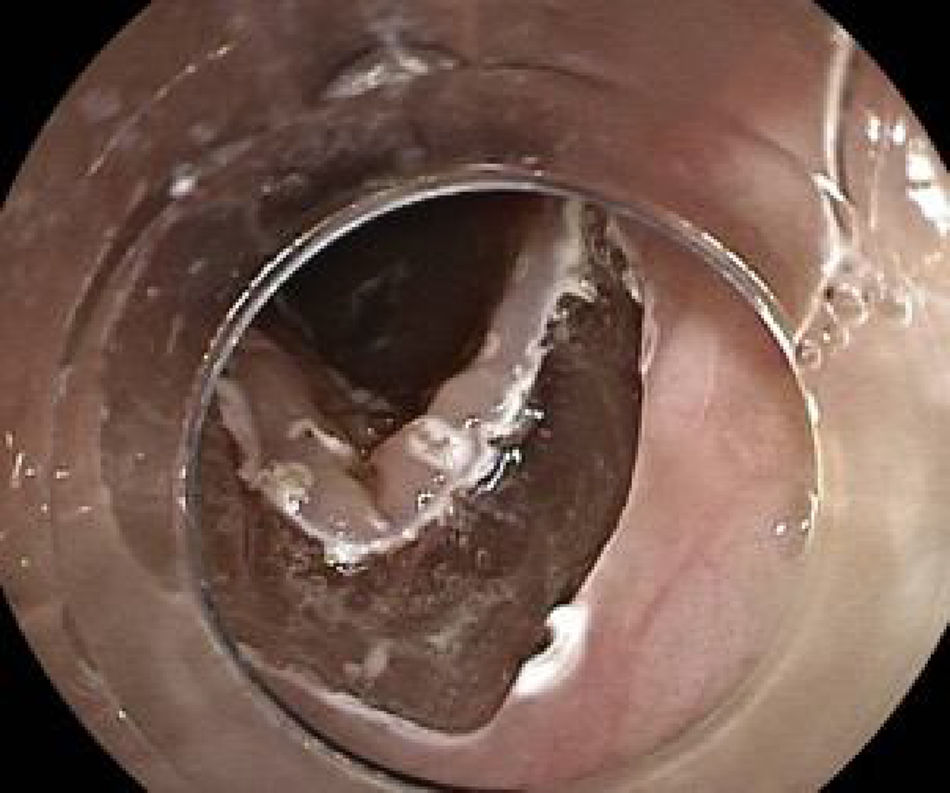
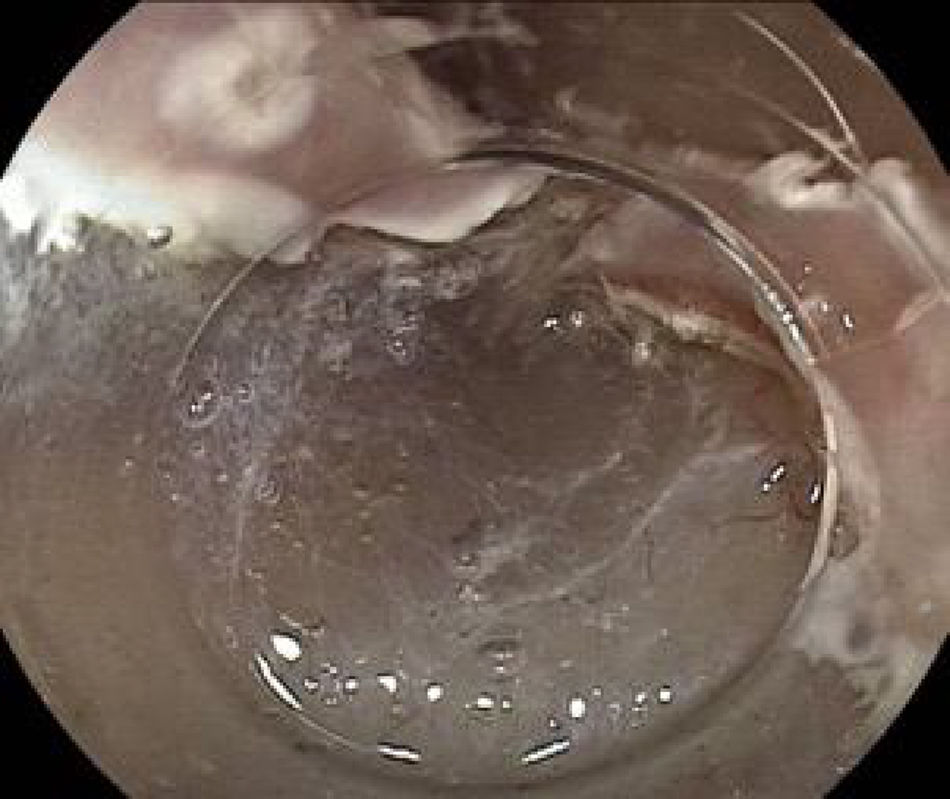
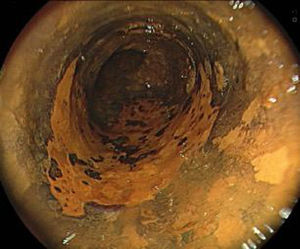
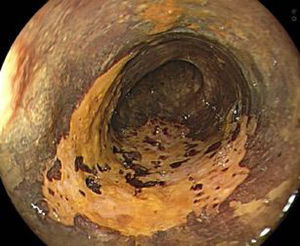
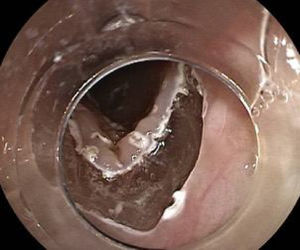
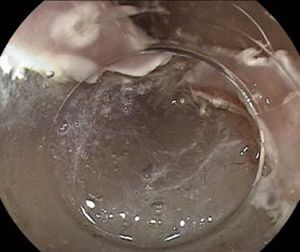
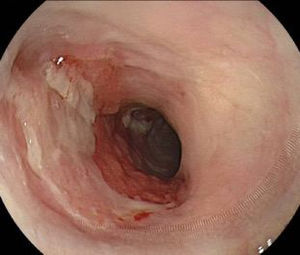
La cromoendoscopia utilizando la solución de lugol es considerada el método de elección para el diagnóstico de CCE, con una sensibilidad del 96% y una especificidad del 63% comparado con la endoscopia convencional con luz blanca, con una sensibilidad del 62%, aunque con una mejor especificidad de 79% (fig. 2)2,8. El lugol es una coloración que reacciona con las células escamosas del esófago que presentan alto contenido de glucógeno, por lo tanto las células neoplásicas o displásicas no presentan dicha reacción por el pobre almacenamiento de dicho carbohidrato. Sin embargo, se debe evaluar el «signo de color rosa», que consiste en el cambio de color de la lesión neoplásica de amarillo a rosado luego de 2 a 5 min de ser aplicado el lugol (fig. 3), teniendo este signo una alta especificidad de existencia de displasia o CCE4,8.
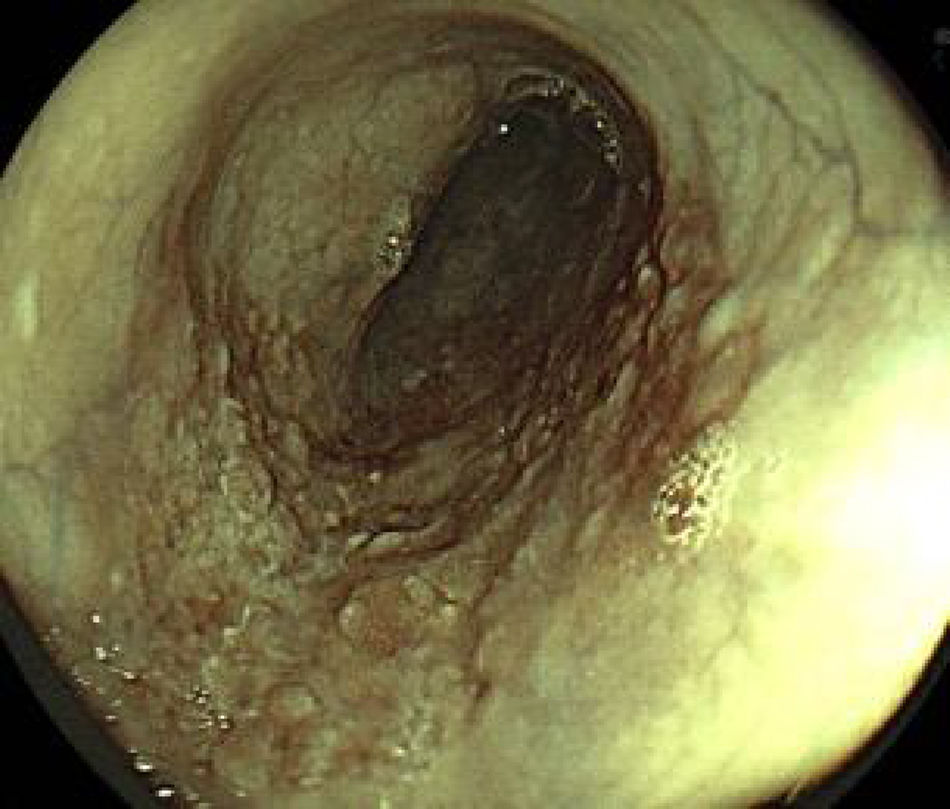
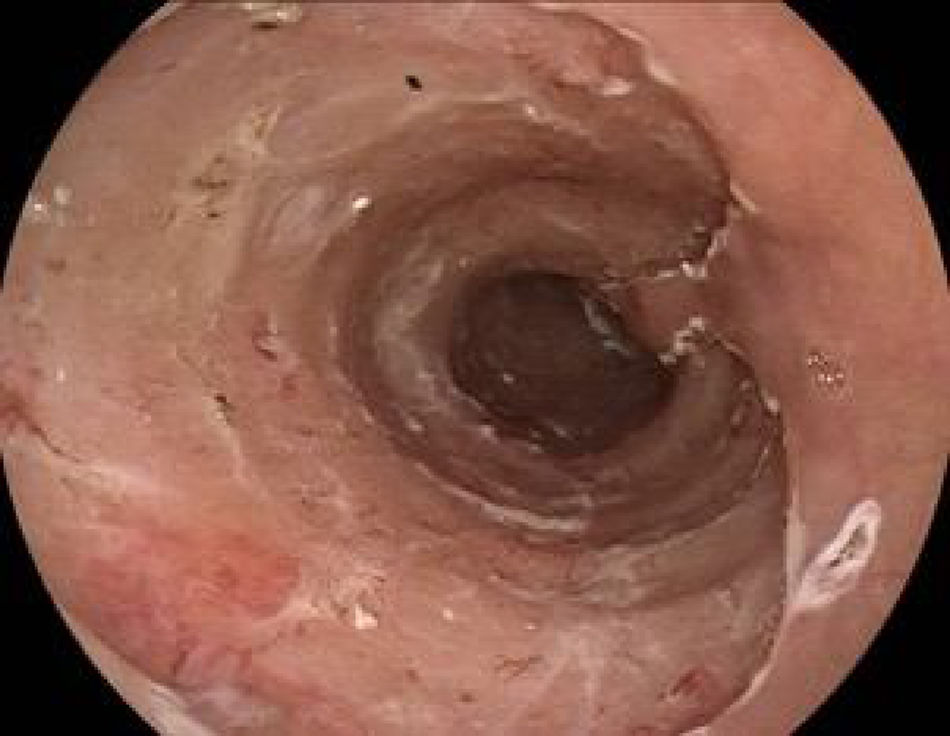
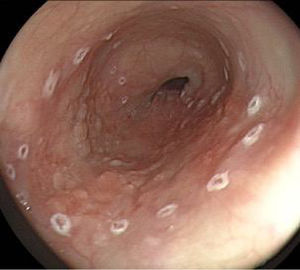
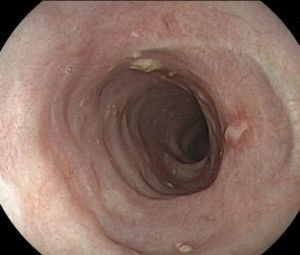
No obstante, la reacción con lugol implica mayor tiempo y costos, teniendo además efectos adversos y complicaciones, como reacción alérgica, dolor torácico o aspiración de la solución, por lo que actualmente se cuenta con nuevos métodos de la cromoendoscopia digital como: FICE y NBI, que pueden reducir dichas situaciones15,16 (fig. 4). Arantes et al.15 realizaron un estudio en el que se utilizó a la endoscopia transnasal como método de detección de CCE de esófago en pacientes con cáncer de células escamosas de cabeza y cuello, y se aplicó como técnica diagnóstica la luz blanca, FICE, comparándolo con el método de referencia: lugol, encontrando que los 2primeros métodos fueron similares en la detección de CCE con valores de sensibilidad y especificidad elevados. Recientemente, Morita et al.16 publicaron una revisión sistemática y metaanálisis sobre el diagnóstico de displasia de alto grado y CCE en el esófago utilizando NBI en comparación con lugol, encontrando que ambos métodos tienen la misma tasa de detección. Por lo tanto, los nuevos métodos digitales de cromoendoscopia son útiles para un tamización adecuada.
Estadificación endoscópica del cáncer de esófago tempranoEl pronóstico y la selección adecuada del tratamiento del cáncer de esófago está en estricta relación a la estadificación del mismo7. El cáncer de esófago temprano se define como lesiones cuyo aspecto morfológico compromete las capas de la mucosa y la submucosa sin infiltración de la muscular propia7,9,17. En el esófago predominan las neoplasias superficiales planas que se subdividen en superficialmente elevadas con relación a la mucosa adyacente (IIA), planas (IIB) y deprimidas (IIC), siendo raras las formas protruidas y excavadas con base en la clasificación de París17. Las neoplasias superficiales son subdivididas de acuerdo con el grado de penetración transmural, así se considera: m1: corresponde al epitelio y la capa basal, m2: lámina propia, y m3: muscular de la mucosa, si existe invasión de la submucosa se clasifica en sm1: tercio superior, sm2: intermedio y sm3: tercio inferior, en ausencia de invasión de la lámina propia la lesión se denomina neoplasia intraepitelial con displasia de alto grado y se puede utilizar el término carcinoma in situ, tal como se describe en la (tabla 1)2,7,17.
Definiciones de la categoría T para el cáncer de esófago
| Tx | Tumor primario que no puede ser definido | |
| T0 | No evidencia de tumor primario | |
| Tis, m1 | Displasia de alto grado, limitado a la capa mucosa | |
| T1 | Tumor invade la lámina propia, muscular de la mucosa o submucosa | T1a |
| T1, m2 | Tumor invade la lámina propia | |
| T1, m3 | Tumor invade la muscular de la mucosa | T1b |
| T1, sm1 | Tumor invade hasta el tercio superior de la mucosa | |
| T1, sm2 | Tumor invade hasta el tercio medio de la submucosa | |
| T1, sm3 | Tumor penetra el tercio inferior de la submucosa | |
| T2 | Tumor invade la muscular propia | |
| T3 | Tumor invade la adventicia | |
| T4 | Tumor invade órganos adyacentes | |
| T4a | Tumor resecable que invade pleura, pericardio o diafragma | |
| T4b | Tumor irresecable que invade aorta, vértebra, tráquea u otro órgano adyacente |
Tis: carcinoma in situ.
La clasificación descrita anteriormente ayuda a definir el riesgo de presentar linfoadenopatías metastásicas, ya que estas tienen estrecha relación con la profundidad o nivel de la lesión de forma vertical en la pared del órgano afectado, siendo este un factor clave para la selección de pacientes para tratamiento endoscópico curativo exitoso. Así cuando el compromiso tumoral se limita a la porción epitelial superficial (m1 y m2), el riesgo de compromiso linfático metastásico es casi nulo, por lo que realizar un tratamiento por vía endoscópica es suficiente para obtener cura, pero si el tumor invade la muscular de la mucosa (m3) y la porción proximal de la submucosa a una profundidad menor de 200μm debajo de la muscular de la mucosa (sm1), el riesgo puede llegar al 9 y el 19%, respectivamente, sobre todo si hay invasión linfática o vascular. Estos casos se ubican en el límite del tratamiento endoscópico curativo, por lo que una evaluación integral es esencial para definir parámetros como: tamaño del tumor, presencia de invasión linfovascular y la extensión horizontal de la invasión de la muscular de la mucosa, ya que el tumor que invade profundamente la submucosa tiene un alto riesgo de presentar linfoadenopatías metastásicas4,6,9,12,17,18.
El estadificación del cáncer de esófago se debe iniciar con una tomografía computarizada de tórax y abdomen para evaluar metástasis a distancia; sin embargo, la tomografía tiene una pobre sensibilidad para detectar linfoadenopatías celíacas y metástasis pequeñas (particularmente peritoneales), y además no es capaz de definir la profundidad de la lesión. La ultrasonografía endoscópica permite definir de forma más precisa la profundidad de invasión de la lesión y la presencia de linfoadenopatías metastásicas en el mediastino o el tronco celíaco, determinando de esta forma los estadios T1a y T1b, con una sensibilidad y especificidad de más del 80% en ambos7,9,19. En caso de pacientes con invasión completa de la submucosa o la muscularis propia, o con presencia de metástasis regionales o a distancia por tomografía o ultrasonografía endoscópica, no deben ser tratados mediante DES19.
Indicaciones del tratamiento endoscópico del cáncer de esófago tempranoEntre los criterios definidos para la resección endoscópica del cáncer de esófago temprano con fines curativos, se cuentan los siguientes17:
- 1.
Profundidad de la lesión restringida a los estadios m1 y m2 (capa basal y lámina propia).
- 2.
Longitud máxima de 3cm y extensión lateral menor a los 3/4 de la circunferencia.
- 3.
Máximo 4 lesiones.
Con la incorporación de DES se acepta que las lesiones pueden ser mayores de 3cm incluso si ocupa la totalidad de la circunferencia del esófago y además sin tener un límite en el número de lesiones, siempre que todas sean neoplasias tempranas17. La Sociedad Japonesa de Esófago define las indicaciones absolutas de DES en el cáncer temprano de esófago por CCE: lesión esofágica limitada al epitelio (m1) o la lámina propia (m2) pero que compromete menos de los 2/3 de la circunferencia. Entre las indicaciones relativas a las que se debe considerar adicionar terapia con quimioterapia y radioterapia figuran: lesión que invade la muscular de la mucosa (m3) o submucosa (sm1) pero sin presencia se linfoadenopatías o metástasis previa a la DES y lesión limitada al epitelio (m1) o la lámina propia (m2) comprometiendo a más de los 2/3 de la circunferencia del esófago4,6,17.
Disección endoscópica submucosa del cáncer de esófago tempranoLa EMR fue desarrollada a finales de la década del 80, siendo rápidamente aceptada como tratamiento de la neoplasia superficial de esófago alternativo a la terapia quirúrgica20,21. Sin embargo, en lesiones de mayor tamaño (15mm), la extracción completa no era posible, por lo que se desarrolló la resección tipo piecemeal para este tipo de tumores, pero la recurrencia local era elevada; es en ese contexto que una nueva terapia endoscópica (DES) solucionó estas desventajas2,6,19,20.
La DES es una técnica de endoscopia avanzada cuyo objetivo es permitir la resección en bloque de las lesiones mayores de 2cm y que además comprende la detección, el diagnóstico, el tratamiento, la prevención y el manejo de complicaciones (hemorragia, perforación, estenosis) con un seguimiento a largo plazo, por lo que se debe tener un entrenamiento adecuado. A pesar de que el número mínimo de casos que se requiere para poder realizar una DES de esófago no está definido, expertos japoneses recomiendan realizar al menos 50 DES en localizaciones como (estómago distal o recto) antes de realizarlo en el esófago4,17,22,23.
Esta técnica se diseñó originalmente para su aplicación en el estómago; sin embargo, el empleo de esta en el esófago, el colon y el recto fue posterior a dicha aplicación, ya que en el caso del esófago este es un órgano con una pared de 3.5-4mm y que presenta mayor dificultad técnica por lo reducido del espacio luminal en comparación con el estómago. Sin embargo, a pesar de las mayores dificultades técnicas, la DES ha demostrado ser un tratamiento efectivo y seguro en el CCE del esófago, logrando aumentar la sobrevida del paciente7,17,19,22,24.
Cabe resaltar que la pared del aparato digestivo está formada por 2componentes principales: la mucosa y la muscular propia, ambos están separados por la submucosa (tejido conectivo), por lo que al realizar la resección en bloque de la lesión presenta un riesgo de lesión involuntaria de la capa muscular llevando a una perforación de la víscera. Para disminuir dicho evento se requiere la inyección de la submucosa para separar la neoplasia temprana de la muscular propia, pudiéndose utilizar soluciones viscosas como el hialuronato de sodio, hidroxipropilmetilcelulosa, carboximetilcelulosa sódica, glucosa hipertónica, salino hipertónico, fibrinógeno o glicerina7,12,17.
Técnica de disección endoscópica submucosa esofágicaEl procedimiento se realiza en el paciente con sedación profunda, generalmente con intubación endotraqueal, ya que facilita una mejor sedación y previene el riesgo de aspiración. El uso de antibiótico profiláctico es controversial y no se encuentra bien definido, a pesar que en diversos centros de endoscopia de Japón se utilizan cefalosporinas de segunda generación por 3días por vía intravenosa4,17,20.
Luego de realizar una evaluación completa de la lesión utilizando endoscopios con magnificación y cromoendoscopia digital, se debe realizar la cromoendoscopia con lugol al 0.8% para definir adecuadamente los límites de la lesión (fig. 2)4,17,19,24,25. El equipo de electrocirugía más recomendado es VIO 200D o 300D (Erbe Elektromedizin GmbH, Tu¿bingen, Alemania). La DES puede ser realizada con diferentes tipos de endoknives: Hook Knife (KD- 620LR, Olympus, Tokio, Japón); Dual Knife (KD-650, Olympus, Tokio, Japón); IT Knife (KD-612, Olympus, Tokio, Japón) es el más usado en la DES gástrica, pero en la DES de esófago presenta una alta tasa de perforación, por lo que recientemente se presentó el IT Knife nano (KD- 612, Olympus), que fue desarrollado para DES de colon y esófago20. También se tiene el estilete de aguja corta de 1.5mm de largo con punta redondeada: Flush Knife (FK) (Fujifilm, Tokio, Japón), el cual, además de permitir la marcación, la incisión, la disección de la submucosa y la hemostasia, posibilita la inyección simultánea de solución salina9,12,17,20,23. Se indica el uso de insuflación con CO2, el cual es absorbido más rápidamente en comparación con el aire y excretado durante la respiración, siendo este útil para prevenir enfisema mediastinal severo, y en caso de perforación brinda un tiempo suficiente para poder realizar el cierre endoscópico con endoclip4,12,20. En esta revisión describiremos la DES esofágica utilizando el estilete FK.
Después de la cromoendoscopia se procede a marcar los límites de la lesión con el FK con parámetros ERBE: soft coagulation, efecto 5, 100W, con una distancia mínima de la lesión de 2mm de los márgenes laterales y a 5mm de los márgenes proximales para reducir el riesgo de estenosis por DES (fig. 5)4,17,20. En seguida se procede a la inyección de la submucosa, la cual se debe realizar en el margen oral de la lesión de un extremo al otro; primero se realiza una inyección con solución salina y luego se inyecta solución de hialuronato de sodio 0.4% (Muco-Up®, Seikagaku, Japón), que mantiene elevada la lesión por un tiempo más prolongado4,12,17,26.
Luego se realiza la incisión con el FK de forma transversal y lateral, el cual debe ser profundo para llegar al plano submucoso (parámetros: Endocut I, efecto 4, duración de corte: 2, intervalo de corte: 3) (fig. 6); además se utiliza el cap para presentar el tejido submucoso y se realiza la disección submucosa endoscópica en dirección oral-anal, siempre paralelo al eje de la pared del esófago para evitar el riesgo de perforación (parámetros de disección de la capa submucosa: coagulación forzada, efecto: 2, 40 W) (fig. 7)4,17,20; cabe señalar que siempre que se realice la disección con el corte eléctrico se puede agregar la inyección de solución salina a nivel de la submucosa17.
Una parte importante del procedimiento para que sea más seguro es prevenir el sangrado durante la DES y una hemostasia adecuada es esencial, para lo cual, en caso de identificar algún vaso submucoso o de presentar un sangrado inesperado, se debe realizar hemostasia con FK (parámetros: coagulación soft, efecto 5, 100 W) por 3 a 5 s en cada lado del vaso, seguido luego de coagulación forzada12,17,20. En caso de que la hemostasia no pueda ser controlada luego de 3intentos, se debe utilizar la pinza de fórceps para hemostasia COAG grasper (Olympus, Tokio, Japón)20,25.
Finalmente, la muestra debe ser retirada con pinza de cuerpo extraño, debiendo ser atrapado por el lado submucoso para no dañar el lado mucoso de la lesión. El lugar de la disección debe ser revaluado (fig. 8) en caso de observarse vasos prominentes; estos deben de recibir hemostasia y, si se presenta laceraciones de la capa muscular, se debe realizar terapia con clip endoscópico. La muestra se fija con alfileres sobre una placa de tecnopor y se coloca en formol (fig. 9). El patólogo debe cortar la muestra en fragmentos paralelos y perpendiculares a la lesión de 2mm de ancho y debe ser evaluado según la clasificación de Viena, mediante la cual se identifican: el tamaño, el grado de diferenciación y la profundidad de la lesión; además se deben evaluar los márgenes proximal, distal, lateral y vertical8,17,25. La profundidad de invasión de la submucosa se realiza con una medición en micrómetros (μm) desde la última capa de la muscular de la mucosa, con un punto de corte de 200μm para sm125.
Posdisección endoscópica submucosa esofágicaUsualmente, el paciente permanece en ayunas las primeras 24 h posterior a la terapia de DES, con sucralfato por vía oral y recibe inhibidor de bomba de protones (IBP) 40mg cada 12 h. La dieta líquida puede ser iniciada al día siguiente con progresión de la misma4,19. Los pacientes con reflujo gastroesofágico deben recibir terapia con IBP por 2meses luego del procedimiento. El control endoscópico debe ser realizado a los 3meses de la DES y luego se debe realizar una endoscopia anual incluyendo cromoendoscopia para evaluar recurrencia o lesiones metacrónicas (fig. 10)4.
Complicaciones de la terapia de disección endoscópica submucosa esofágicaLas tasas de complicación son bajas, entre el 0 y el 4%, para hemorragia significativa, definida como sangrado mayor de 500ml o caída de la hemoglobina> 2g/dl, y la perforación, cuya frecuencia se encuentra entre el 2.6 y el 6.9%; esta última puede causar enfisema mediastinal, que se presenta como complicación en diversas series de estudios publicados. El enfisema incrementa la presión mediastinal disminuyendo la luz del esófago, lo que lleva a una inadecuada visualización de la mucosa del mismo, pero también se puede presentar el enfisema mediastinal severo, el cual tiene como complicación el desarrollo de neumotórax que puede terminar en shock, por lo que durante el procedimiento se debe monitorizar al paciente con el electrocardiograma, saturación de oxígeno, capnografía, presión arterial y observación periódica del paciente con la palpación cervical para evaluar la presencia de enfisema subcutáneo14,20,24,25. En caso de presentarse una perforación después de la DES, esta puede ser tratada de forma conservadora con el uso de endoclip, NPO, hidratación adecuada y terapia antibiótica4.
La estenosis es la complicación con mayor incidencia, entre el 3 y el 18%, después de una DES en esófago, siendo el predictor más importante la extensión de la resección, la cual si es mayor del 75% de su circunferencia tiene una mayor probabilidad de presentarse este evento. La estenosis esofágica es un factor que disminuye la calidad de vida del paciente y que puede requerir múltiples sesiones de dilatación con balón4,17,20,27. Se ha descrito la eficacia del uso de prednisolona oral para la prevención de estenosis (fig. 11) en un estudio realizado en Japón por Kataoka et al.28, donde se compararon 2grupos: uno que recibió tratamiento con esteroides sistémicos por vía oral con prednisolona con una dosis inicial de 30mg la primera semana y con disminución progresiva de la dosis semanalmente, y el otro que no recibió tratamiento alguno preventivo. Los autores encontraron que la tasa de estenosis y el número de sesiones de dilatación con balón eran significativamente menores en el grupo que recibió corticoides vs. el que no lo recibió, con diferencias estadísticamente significativas. Otra opción es realizar la inyección de 4ml de acetato de triamcinolona 10mg/ml a través de un catéter inyector, efectuando 20 punciones de la solución de 0.2ml cada una en el borde y en el centro de la resección4,17,20. Otras opciones de prevención de la estenosis esofágica post-DES circunferencial incluyen la dilatación con balón hidrostático, el uso de membranas de ácido poliglicólico, el autotrasplante de tejido gastroesofágico o el uso de prótesis metálicas29.
ConclusionesLa DES es el tratamiento de elección para el CCE temprano, con una tasa de recurrencia baja y reducción de la morbimortalidad. El mayor desafío es obtener un diagnóstico precoz del cáncer de esófago, por lo que se deberían plantear programas de cribado y vigilancia en los pacientes con alto riesgo. La DES del esófago es técnicamente más difícil que el estómago, ya que posee una luz estrecha y requiere endoscopistas con un adecuado entrenamiento para su ejecución segura y eficiente. Es fundamental desarrollar centros de entrenamiento en América Latina para los profesionales interesados en aprender la DES, lo cual tendrá un efecto beneficioso en la vida de los pacientes necesitados en nuestras comunidades.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades, sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.