La microbiota intestinal se altera significativamente en pacientes cirróticos. Sin embargo, la composición de la microbiota intestinal en pacientes cirróticos mexicanos no ha sido reportada. En este trabajo nos propusimos determinar el tipo de microbiota intestinal en sujetos sanos y pacientes con cirrosis hepática de origen mestizo-mexicano.
Material y métodosSe determinaron los parámetros bioquímicos de la función hepática (ALT, AST, GGT, BIL-T, etc.) en 23 pacientes cirróticos y 21 sujetos control. Se determinó la microbiota intestinal mediante secuenciación del gen ribosomal 16S.
ResultadosLos pacientes cirróticos presentan niveles elevados de ALT, AST, GGT (105.2±77.7 vs. 20.99±8.5UI/L; 110±68.6 vs. 23.39±5.2 y 119.1±79.1 vs. 19.3±15.2UI/L, respectivamente) e IL-6 (1.64±0.38pg/ml, p<0.001) o TNFα (1.78±0.3, p<0.05). La microbiota intestinal de los pacientes cirróticos es menos diversa comparada con sujetos control. A nivel de phylum, las Proteobacteria y los Bacteroidetes aumentan significativamente en cirróticos (6.2 vs. 4.9% y 44 vs. 46% vs. controles, respectivamente, p<0.01). En contraste, los Firmicutes así como Actinobacteria y Fusobacteria, disminuyeron en los pacientes cirróticos. Las familias Campylobacter y Gemella aumentan en los pacientes cirróticos, mientras que Streptococcus y Veillonella se asocian positivamente con los niveles séricos de ALT o AST.
ConclusionesDemostramos por vez primera el tipo de microbiota intestinal en pacientes cirróticos mexicanos. La extensión de los hallazgos en una cohorte más amplia de sujetos y el análisis del metagenoma permitirán generar datos que pueden tener implicaciones relevantes para el tratamiento de este grupo de pacientes en México.
The intestinal microbiota is significantly altered in cirrhotic patients, but the composition of the intestinal microbiota in Mexican patients with the pathology has not been reported. The present study is an attempt to determine the type of intestinal microbiota in healthy subjects and in patients of Mexican mestizo origin that present with cirrhosis of the liver.
Materials and methodsBiochemical liver function parameters (ALT, AST, GGT, BIL-T, etc.) were determined in 23 cirrhotic patients and 21 control subjects. The intestinal microbiota was established through 16S ribosomal RNA gene sequencing.
ResultsThe cirrhotic patients had elevated levels of ALT, AST, GGT (105.2±77.7 vs. 20.99±8.5UI/L, 110±68.6 vs. 23.39±5.2, and 119.1±79.1 vs. 19.3±15.2UI/L, respectively), IL-6 (1.64±0.38pg/ml, P<.001), or TNFα (1.78±0.3, P<.05). The intestinal microbiota of the cirrhotic patients was less diverse, compared with that of the control subjects. At the level of the phylum, there was a significant increase in Proteobacteria and Bacteroidetes in the patients with cirrhosis, compared with the controls (6.2 vs. 4.9% and 44 vs. 46%, respectively, P<.01). In contrast, there was a decrease in Firmicutes, Actinobacteria, and Fusobacteria in the cirrhotic patients. There was an increase in the Campylobacter and Gemella families in the cirrhotic patients, whereas Streptococcus and Veillonella had a positive association with serum ALT or AST levels.
ConclusionsTo the best of our knowledge, the present study is the first to demonstrate the type of intestinal microbiota in Mexican patients with cirrhosis of the liver. The extension of the findings in a larger cohort of subjects and the metagenome analysis will enable the creation of data that can have relevant treatment implications for this group of patients in Mexico.
La cirrosis hepática se caracteriza por la presencia de procesos inflamatorios crónicos, hipertensión portal, alteraciones en el metabolismo de las grasas, los hidratos de carbono y el amonio, entre otros; además puede ocasionar daño cognitivo en el largo plazo1. Se ha reportado que el daño en el hígado por la cirrosis puede resultar en la reducción de flujo sanguíneo que va a través del eje intestino-hígado, alterando la secreción biliar y la peristalsis intestinal, lo que promueve el daño en la barrera de la mucosa y posiblemente la alteración de la microbiota intestinal2. En condiciones normales la microbiota intestinal está constituida principalmente por las phyla Firmicutes (60%) y Bacteroidetes (15-20%), mientras que Actinobacteria (<10%) y Proteobacteria (1%) son menos abundantes3; sin embargo, esta composición puede cambiar en respuesta a diversas dolencias, como la enfermedad hepática. Estudios previos indican que pacientes cirróticos presentan incrementos en las phyla Fusobacteria y Proteobacteria, al igual que las familias Enterobacteriaceae, Veillonellaceae y Streptococacceae; mientras que Bacteroidetes y Actinobacteria disminuyen respecto de los pacientes sanos4–6. En población norteamericana se ha observado que pacientes cirróticos por alcohol o esteatohepatitis (esteatohepatitis no alcohólica) presentan cambios en la composición de la microbiota intestinal dependiendo del estadio de la enfermedad. En cirróticos compensados o descompensados, se ha observado aumento en el número de Bacteroidetes, comparados con los pacientes sanos1; mientras que pacientes hospitalizados muestran disminución de este phylum7. Evidencia adicional indica que las familias Enterobacteriaceae, Alcaligenaceae y Fusobacteriaceae se encuentran elevadas en pacientes cirróticos, mientras que Ruminococcaceae y Lachnospiraceae disminuyen, comparadas con sujetos control8. Thalheimer et al. plantean la idea de que la microbiota, o al menos parte de las bacterias que la componen, puede compensar la pérdida de la capacidad metabólica en pacientes afectados por cirrosis hepática derivada de la infección por virus B; existiendo una correlación negativa o positiva con el score Child-Pug entre el phylum Bacteroidetes o la familia Enterobacteriaceae y Veillonella, respectivamente, y que dichos marcadores se pueden utilizar como factores para distinguir la microbiota de pacientes con cirrosis de la de sujetos sanos9.
Por otro lado, la translocación bacteriana representa un importante factor de riesgo para el desarrollo de ciertas complicaciones de la cirrosis hepática, como son la peritonitis bacteriana espontánea, la encefalopatía hepática y el síndrome hepatorrenal9,10. La translocación bacteriana en pacientes con cirrosis se ha corroborado mediante la cuantificación de ADN bacteriano en fluidos biológicos como la sangre y el líquido ascítico11,12.
Estas evidencias en conjunto revelan que los cambios en la composición de la microbiota intestinal de pacientes con cirrosis hepática es un área de interés por los efectos metabólicos y fisiológicos que conlleva. No obstante, la mayoría de los estudios realizados para caracterizar la microbiota intestinal en estos pacientes se han realizado en poblaciones asiáticas y estadounidenses. Datos que contribuyan a la caracterización de la microbiota de personas sanas y pacientes cirróticos en la población mexicana aún no están disponibles. Por lo tanto, su determinación será de gran utilidad para establecer las diferencias y coincidencias entre dichas poblaciones y la mestizo-mexicana, por lo que nuestro objetivo principal fue el determinar los patrones de la microbiota intestinal en sujetos sanos y pacientes con cirrosis hepática de origen mestizo-mexicano, así como también identificar y correlacionar los cambios en la abundancia de las bacterias que constituyen la microbiota intestinal de pacientes con cirrosis hepática y con parámetro de daño hepático.
Material y métodosEl estudio fue avalado por el Comité de Ética e Investigación del Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán. Todos los participantes fueron informados de acuerdo a los lineamientos establecidos por dicho comité y se obtuvo el consentimiento informado de los participantes.
Se realizó un estudio transversal de casos y controles, para el que se reclutaron 21 sujetos sanos y 23 pacientes con cirrosis hepática compensada cuyos expedientes clínicos fueron revisados por un hepatólogo experto; esto permitió reclutar solo a aquellos pacientes con ≤5 puntos en la escala Child-Pugh, que equivale a la clasificación A13. Fueron excluidos todos aquellos pacientes con diagnóstico no confirmado de cirrosis, así como aquellos sujetos sanos cuyo resultado de análisis de hígado por ultrasonido resultara con hígado graso grado 1 o mayor, los pacientes con consumo de probióticos, prebióticos, antibióticos, antifúngicos, antiparasitarios, antivirales, esteroides o cualquier droga de abuso o consumo de alcohol por más de 8 semanas previas al estudio que pudiesen alterar las características de la microbiota, al igual que los sujetos con obesidad mórbida, diabetes tipo 2, enfermedad intestinal crónica, cáncer, infección por VIH o hepatitis A. Se evaluó la antropometría mediante impedancia bioeléctrica con electrodos táctiles tetrapolares de 8 puntos para determinar la composición corporal mediante el dispositivo InBody 770 (InBody, Corea). Se colectaron muestras de heces en la mañana previa al día de la entrega en condiciones de refrigeración.
Determinación de metabolitos en sangreLas pruebas de función hepática completa (ALT, AST, GGT, albúmina, creatinina, bilirrubina total, directa e indirecta, triglicéridos y colesterol total) fueron determinadas en el equipo automatizado Cobas C111 (Roche, EUA). La determinación de la expresión de citosinas proinflamatorias en suero de TNFα, IL-6, IL-8, IL-10, IL-12 mediante el uso del kit de ELISA magnético (LuminexAssay, R&D, EUA) y LPS mediante el uso del reactivo lisado de amebocitos de Limulus (QCL-1000™ Assay, Lonza EUA).
Extracción de ADN genómico de hecesLa extracción de ADN genómico fecal se realizó de acuerdo con las instrucciones del kit comercial QIAamp Fast Stool DNA Mini Kit (Qiagen, EUA). El ADN genómico se almacenó a −70°C hasta su procesamiento para la etapa de secuenciación de nueva generación.
Secuenciación del gen 16S rRNA y análisis de datosEl ADN genómico obtenido se cuantificó utilizando el reactivo Qubit® dsDNA HS Assay (Molecular Probes, EUA). Se generó un amplicón mediante PCR de punto final y los oligonucleótidos reportados para la región hipervariable V3-V4 del gen bacteriano 16S rRNA14. Los amplicones se utilizaron para generar la biblioteca de índices individuales que posteriormente se normalizaron y agruparon para cargar en la celda de flujo NextSeq (Illumina, EUA). Los datos se analizaron con el programa Micca (Microbial Community Analysis, GPL v3)15 y en el programa Qiime v 1.9.1.16. El programa Lefse en la plataforma Galaxy Work Framework17 se utilizó para establecer los taxa asociados con los sujetos sanos o los pacientes cirróticos.
Análisis estadísticoEl análisis de datos antropométricos, de pruebas bioquímicas, así como de citosinas y LPS, se realizaron con el programa Prism7 (Graph-Pad, EUA), utilizando la prueba no pareada de t de Student; las diferencias se consideraron significativas con p<0.05. Los conglomerados para comparar datos antropométricos, bioquímicos, interleucinas o LPS en conjunto con la abundancia relativa de bacterias (unidad taxonómica operativa [OTU, por sus siglas en inglés]), fueron generados con los datos analizados en el programa SPSS (IBM, v21, EUA), utilizando correlaciones de Pearson. La diferencia en la abundancia (alfa-diversidad) de bacterias entre ambos grupos se comparó utilizando la prueba t de Student de 2 vías, usando los índices Shannon y Chao1. Los análisis de correlaciones entre las variables bioquímicas y los OTU se realizaron en el programa SPSS (IBM v21, EUA); mientras que las correlaciones entre los diferentes taxones se obtuvieron en el programa MEGAN v618 y SPSS v 21 (IBM, EUA).
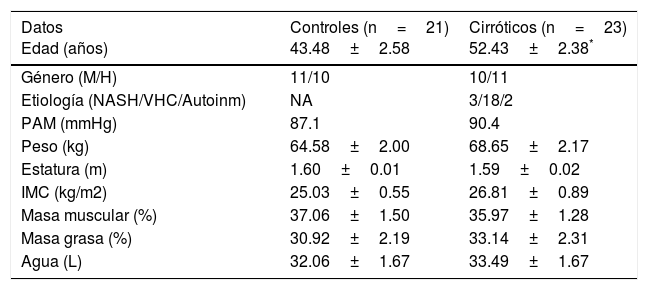
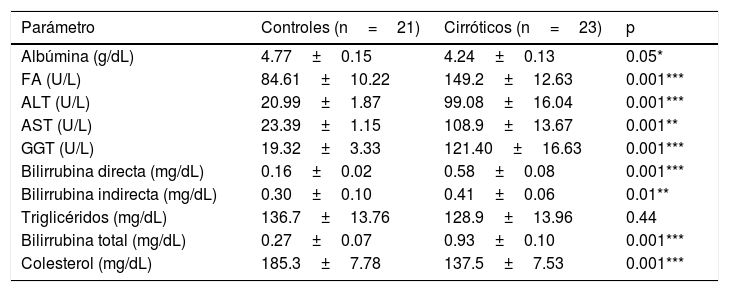
ResultadosCaracterísticas antropométricas y bioquímicas de los participantesSe reclutaron en total 44 pacientes, 23 cirróticos y 21 controles sanos. Del total de pacientes cirróticos, 3 (13%) fueron por etiología de esteatohepatitis no alcohólica, 2 (8.7%) por etiología autoinmune y 18 (78%) por infección de virus C. Las características clínicas y antropométricas de ambos grupos se presentan en las tablas 1 y 2. Los datos indican que las enzimas de daño hepático, como ALT, AST, GGT y FA, se encontraron elevadas en los pacientes cirróticos de forma significativa, comparado con los sujetos control (tabla 2).
Características generales de los participantes
| Datos Edad (años) | Controles (n=21) 43.48±2.58 | Cirróticos (n=23) 52.43±2.38* |
|---|---|---|
| Género (M/H) | 11/10 | 10/11 |
| Etiología (NASH/VHC/Autoinm) | NA | 3/18/2 |
| PAM (mmHg) | 87.1 | 90.4 |
| Peso (kg) | 64.58±2.00 | 68.65±2.17 |
| Estatura (m) | 1.60±0.01 | 1.59±0.02 |
| IMC (kg/m2) | 25.03±0.55 | 26.81±0.89 |
| Masa muscular (%) | 37.06±1.50 | 35.97±1.28 |
| Masa grasa (%) | 30.92±2.19 | 33.14±2.31 |
| Agua (L) | 32.06±1.67 | 33.49±1.67 |
Autoinm: autoinmune; IMC: índice de masa corporal; NA: no aplicable; NASH: esteatohepatitis no alcohólica; PAM: presión arterial media; VHC: virus hepatitis C.
Los datos se presentan como promedio±DE.
Parámetros bioquímicos de los participantes
| Parámetro | Controles (n=21) | Cirróticos (n=23) | p |
|---|---|---|---|
| Albúmina (g/dL) | 4.77±0.15 | 4.24±0.13 | 0.05* |
| FA (U/L) | 84.61±10.22 | 149.2±12.63 | 0.001*** |
| ALT (U/L) | 20.99±1.87 | 99.08±16.04 | 0.001*** |
| AST (U/L) | 23.39±1.15 | 108.9±13.67 | 0.001** |
| GGT (U/L) | 19.32±3.33 | 121.40±16.63 | 0.001*** |
| Bilirrubina directa (mg/dL) | 0.16±0.02 | 0.58±0.08 | 0.001*** |
| Bilirrubina indirecta (mg/dL) | 0.30±0.10 | 0.41±0.06 | 0.01** |
| Triglicéridos (mg/dL) | 136.7±13.76 | 128.9±13.96 | 0.44 |
| Bilirrubina total (mg/dL) | 0.27±0.07 | 0.93±0.10 | 0.001*** |
| Colesterol (mg/dL) | 185.3±7.78 | 137.5±7.53 | 0.001*** |
ALB: albúmina; ALT: alanino-aminotransferasa; AST: aspartato-aminotransferasa; FA: fosfatasa alcalina; GGT: gamma glutamil-transferasa.
Los datos se presentan como el promedio±DE.
*p<0.05; **p<0.01; ***p<0.001.
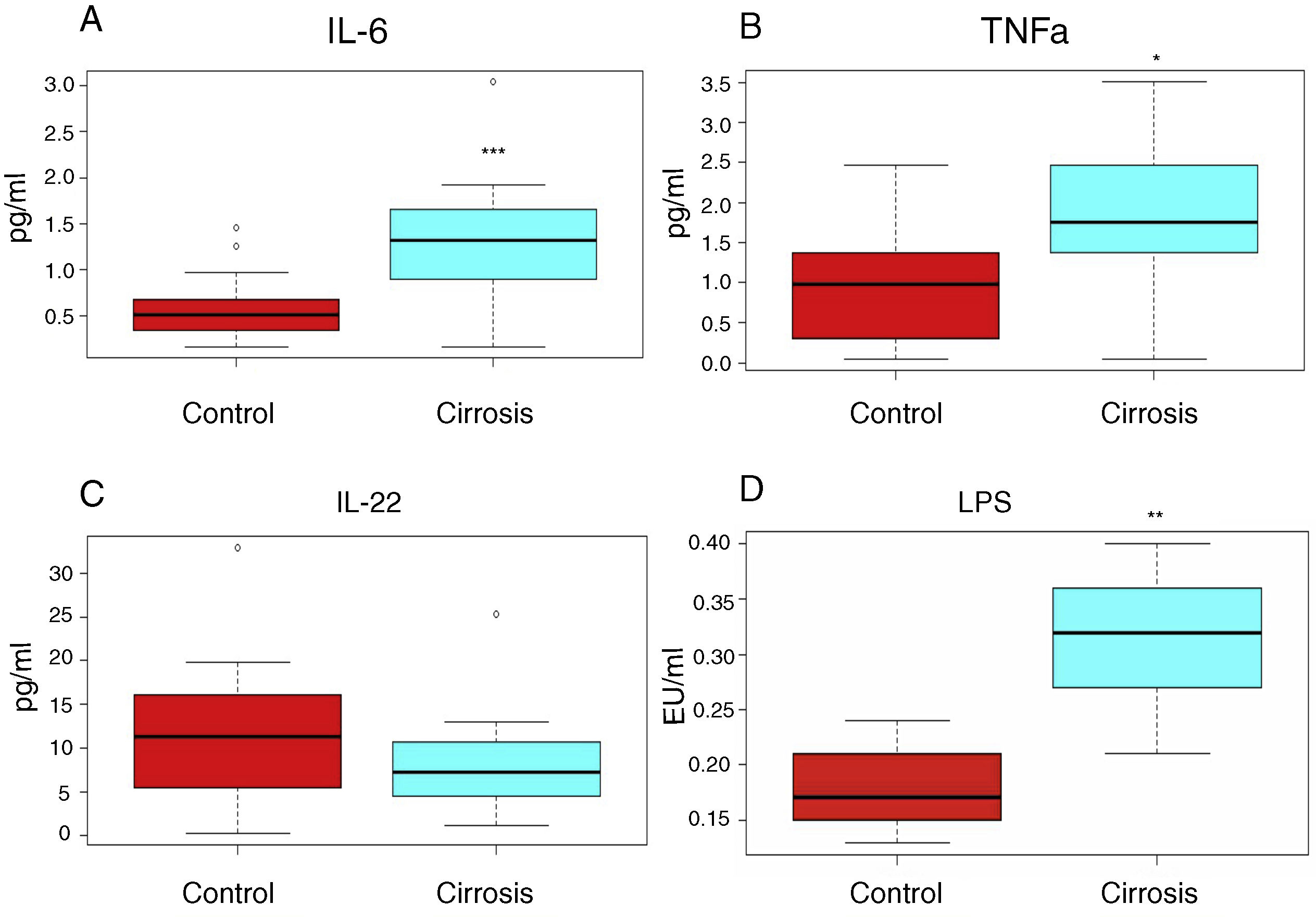
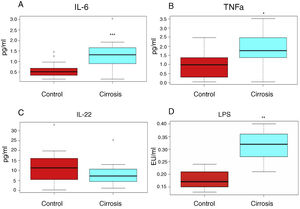
Adicionalmente, observamos que los niveles de citosinas proinflamatorias (IL-6, TNFalfa) se encuentran elevados (1.64±0.38pg/ml vs. 0.558±0.08pg/ml, 1.78±0.29pg/ml vs. 0.94±0.21pg/ml, respectivamente), mientras que la interleucina antiinflamatoria IL-22, registró niveles por debajo de los observados en los sujetos control (8.32±1.53pg/ml vs. 11.96±2.55pg/ml) (fig. 1A-C).
Los pacientes cirróticos presentan mayor grado de inflamación comparados con sujetos sanos. Se presentan las determinaciones de interleucinas (figs. 1A, 1B, 1C) o de lipopolisacárido (LPS) (fig. 1D), determinadas en el suero de sangre periférica de los pacientes cirróticos (cajas azules) o sujetos control (cajas rojas). Las gráficas representan las medianas y los rangos intercuartílicos. Los asteriscos indican significación estadística ***p<0.001;** p<0.01; *p<0.05 vs. control.
En cuanto a los niveles de LPS, que pueden ser utilizados como indicadores de la endotoxemia leve a moderada y por tanto del grado de inflamación en cirróticos, se observó que los niveles en los pacientes cirróticos están incrementados en comparación con los sujetos sanos (fig. 1D)
En conjunto, estos datos indican que nuestra población cirrótica tiene inflamación que puede estar relacionada con la translocación bacteriana.
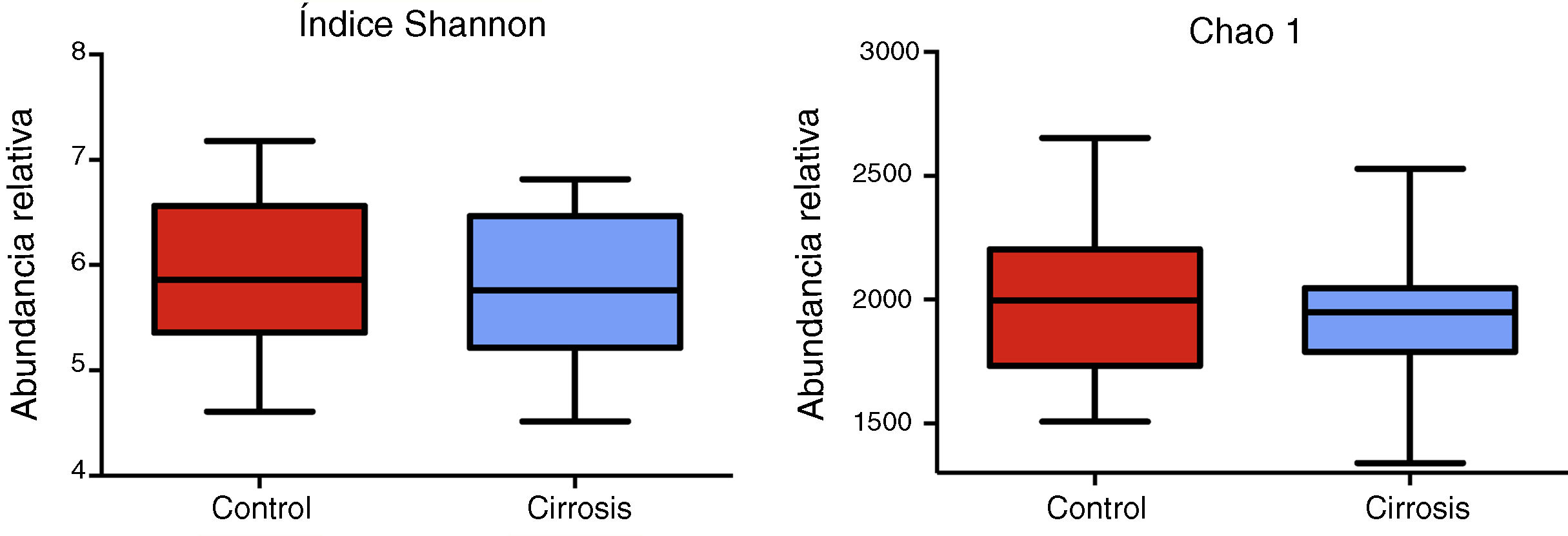
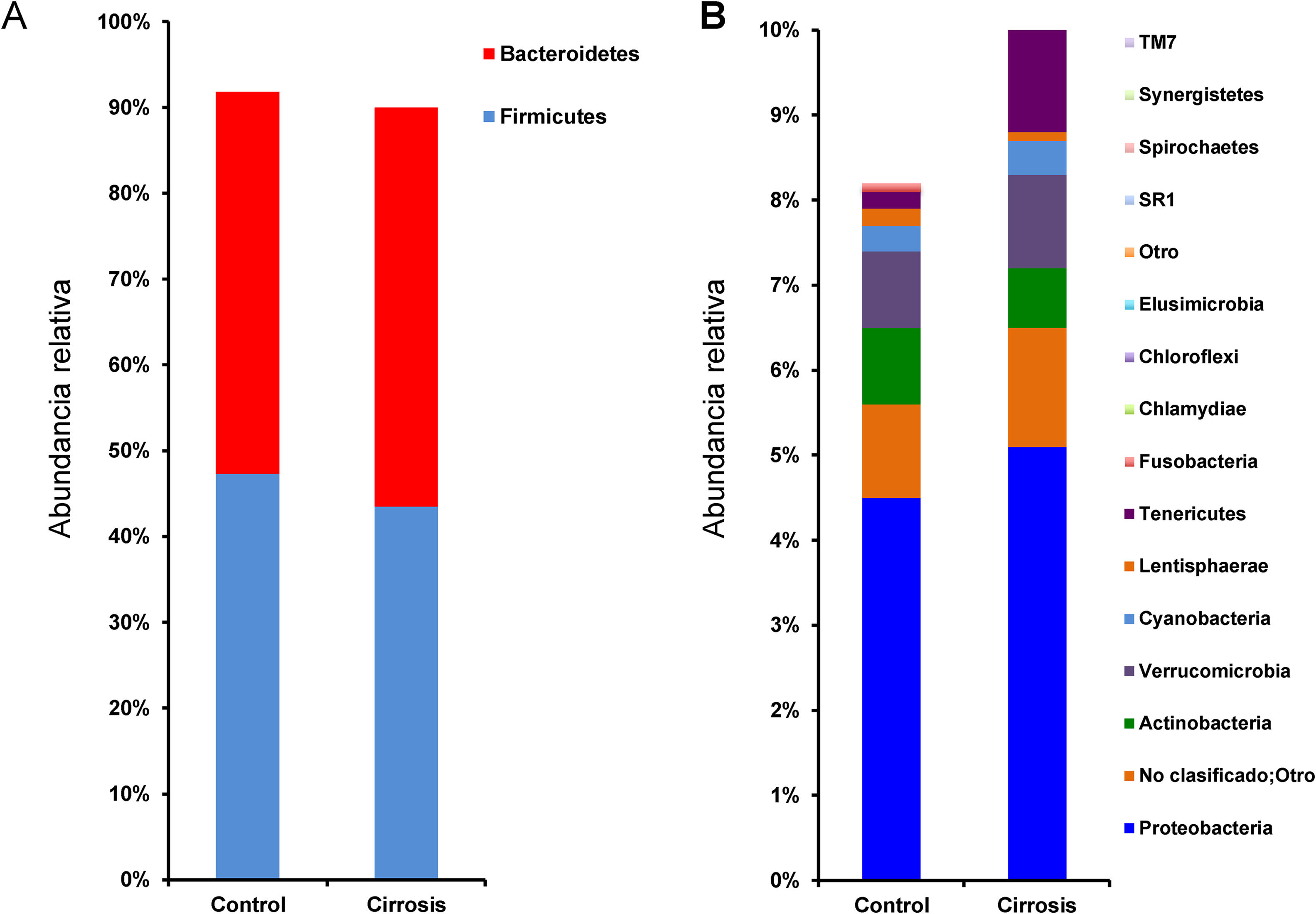
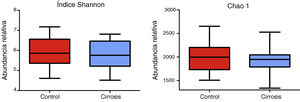
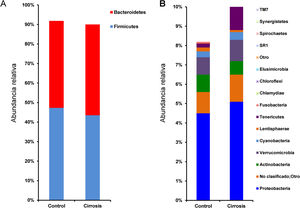
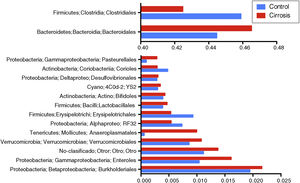
Composición y análisis funcional de la microbiota de los pacientes cirróticosLos análisis de diversidad mediante los índices Chao1 y Shannon entre los sujetos cirróticos y los controles mostraron que aquellos tienen una menor diversidad bacteriana comparada con los sujetos control; sin embargo, aunque esta diferencia no alcanza la significación estadística, sí indica que la diversidad en la microbiota de los pacientes cirróticos se ve afectada de forma directa o indirecta por la enfermedad (fig. 2). El análisis de las frecuencias taxonómicas en cada grupo mostró que los pacientes cirróticos tienen mayor número de OTU que pertenecen a las phyla Bacteroidetes, Proteobacteria, Verrucomicrobia, Cyanobacteria y Tenericutes; así como menor abundancia de OTU en las phyla Actinobacteria, Fusobacteria, Lentisphaerae, Synergistetes, TM7, SR1, Spirochaetes entre otros (fig. 3A, 3B).
Los pacientes cirróticos presentan menor diversidad bacteriana comparada con sujetos control. Se presenta el alfa-diversidad de ambos grupos utilizando los índices Shannon y Chao1 para los 44 pacientes. Las gráficas describen los rangos intercuartílicos entre el primer y tercer cuartiles (25 y 75 percentil) y la línea que divide a la caja representa la mediana de cada grupo. Shannon p<0.58; Chao1 p<0.29 vs. control, prueba de Mann-Whitney.
Comparación de la abundancia relativa de OTU a nivel de phylum entre los pacientes cirróticos y los sujetos control. (Figura 3 A) Se muestra una gráfica de barras sobrepuestas que indican los promedios de las phyla más abundantes y que presentan niveles mayores de cambio±error estándar, en cada caso. (Figura 3 B) Las barras indican, al igual que en A, los niveles de cambio.
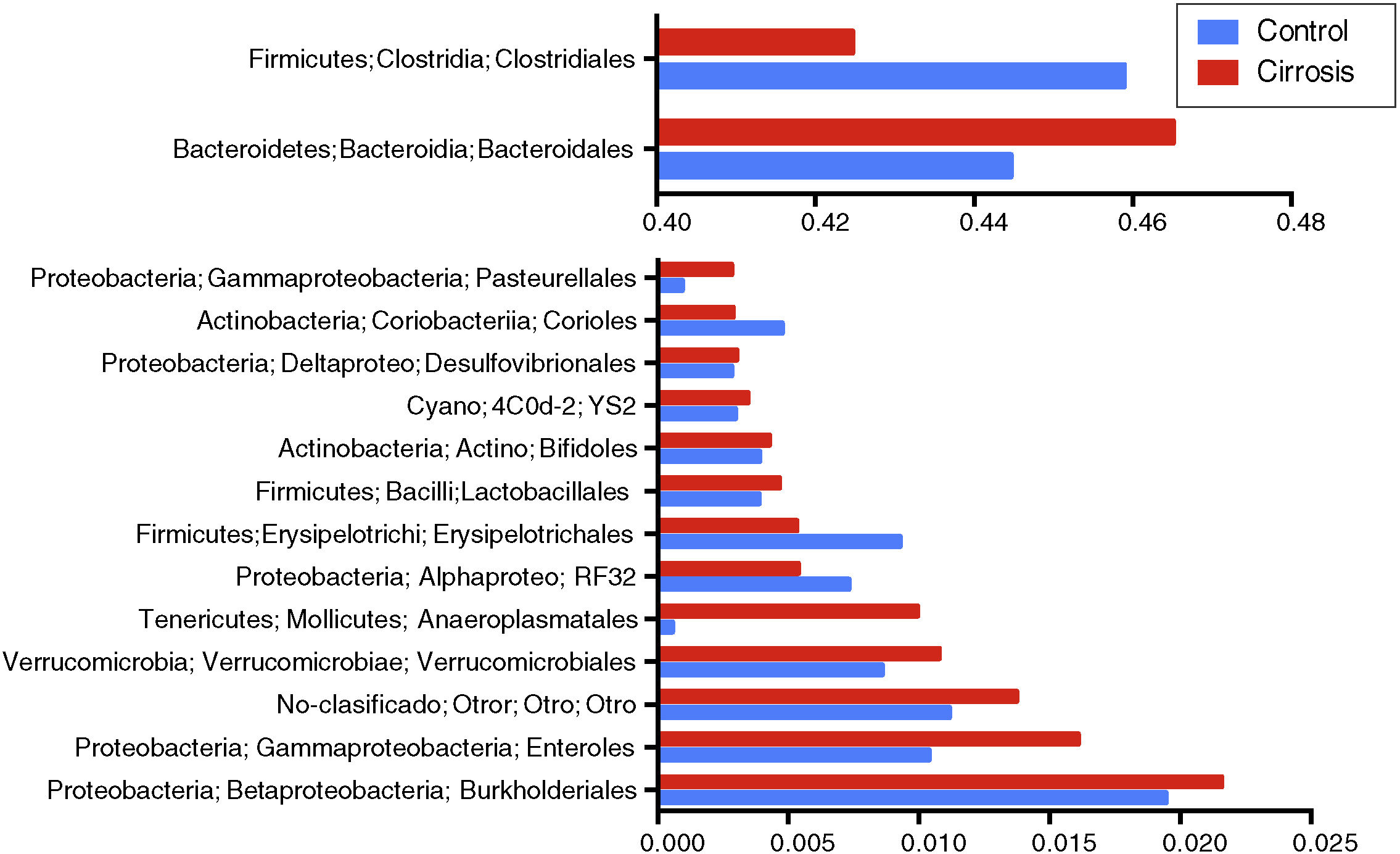
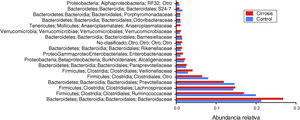
A nivel de orden encontramos que los Bacteroidales y los Anaeroplasmatales, Verrucomicrobiales, Enterobacteriales, así como Burkholderiales y un grupo de bacterias no clasificadas dominan la microbiota intestinal en los pacientes cirróticos, mientras que las Clostridiales, Erysipelotrichales y los Coriobacteriales lo hacen en el grupo de sujetos control (fig. 4).
Representación gráfica de la abundancia relativa del orden taxonómico. En las muestras de pacientes cirróticos (barras rojas) y los sujetos control (barras azules). En el panel superior aparecen los grupos con los mayores niveles de cambio, mientras que en el panel inferior aparecen los que contribuyen en menor medida.
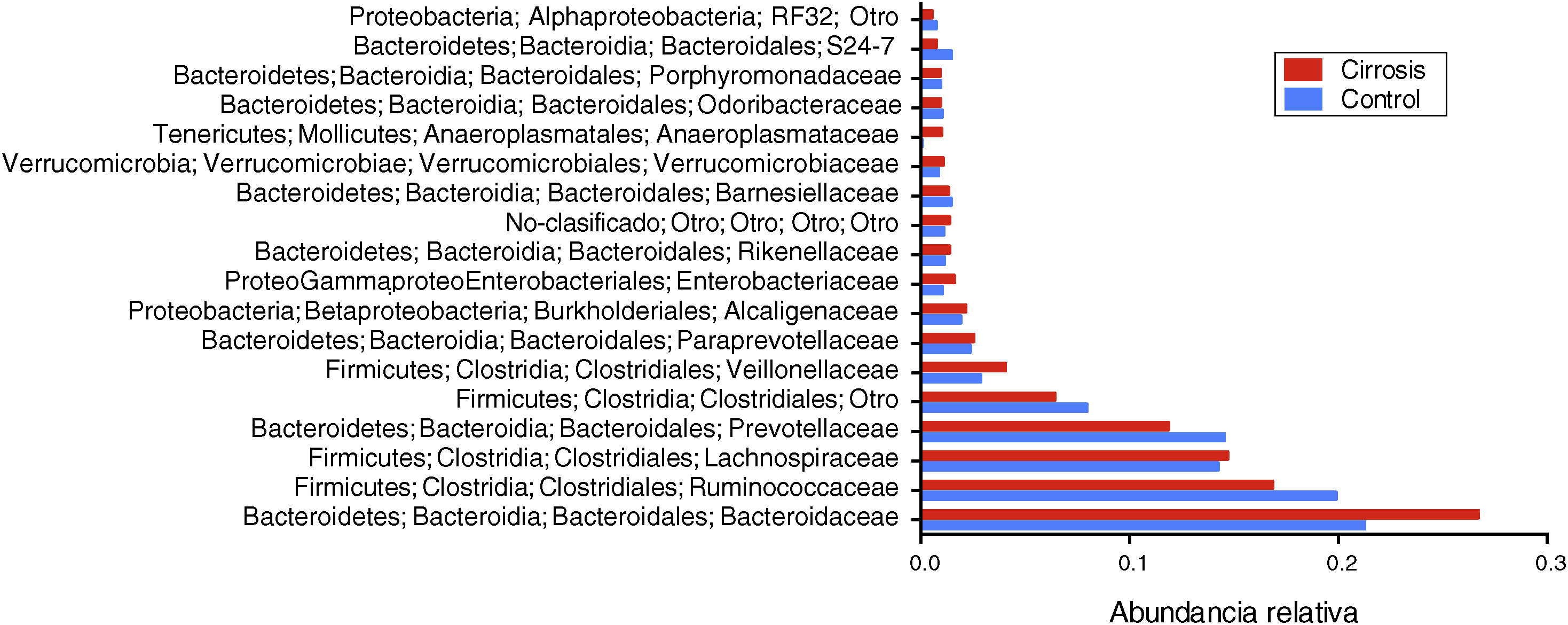
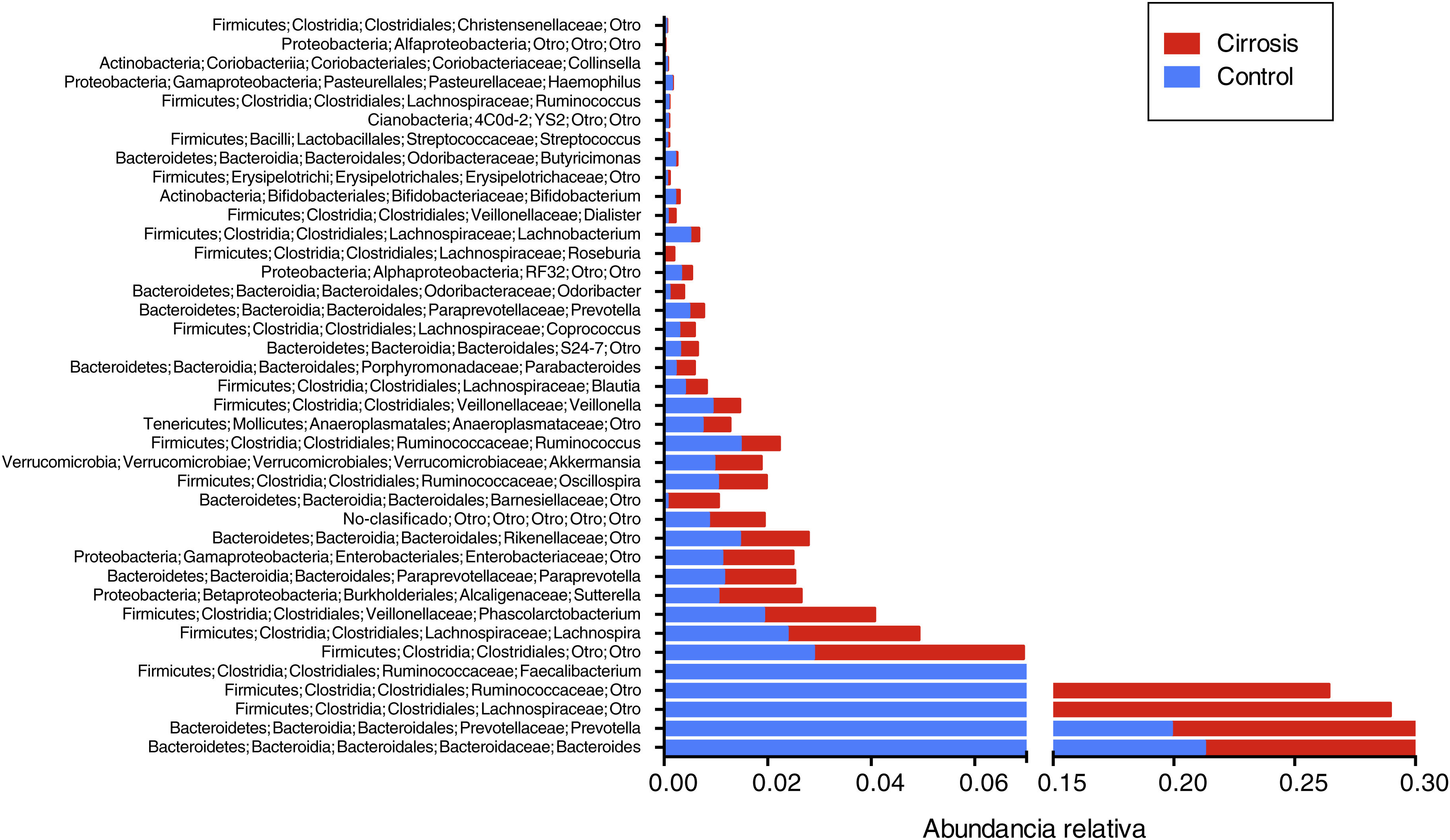
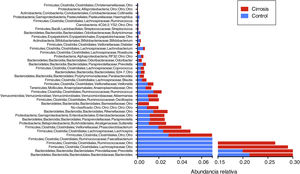
Cuando el análisis de la microbiota intestinal se realizó a nivel de familia y género, encontramos que en el primer caso Bacteroidaceae, Enterobacteriaceae, Rickenellaceae y Veillonellaceae son las que presentan aumento en los pacientes cirróticos, cuando se compara con el grupo control (fig. 5); mientras que en el segundo caso, Bacteroides, Phascolarctobacterium, Sutterella, Paraprevotella, Veillonella y Blautia son los géneros que se encuentran aumentados en los pacientes cirróticos. Por otro lado encontramos que Prevotella, Ruminococcaceae no clasificado, Clostridiales no clasificados, así como Lachnospiraceae son más abundantes en los sujetos control (fig. 6).
Representación gráfica de la abundancia relativa a nivel de familia en las muestras de pacientes cirróticos (barras rojas) y los sujetos control (barras azules). Las barras representan el promedio de cada grupo de cada familia bacteriana. Se presentan solo las 20 familias que tienen mayores niveles de cambio.
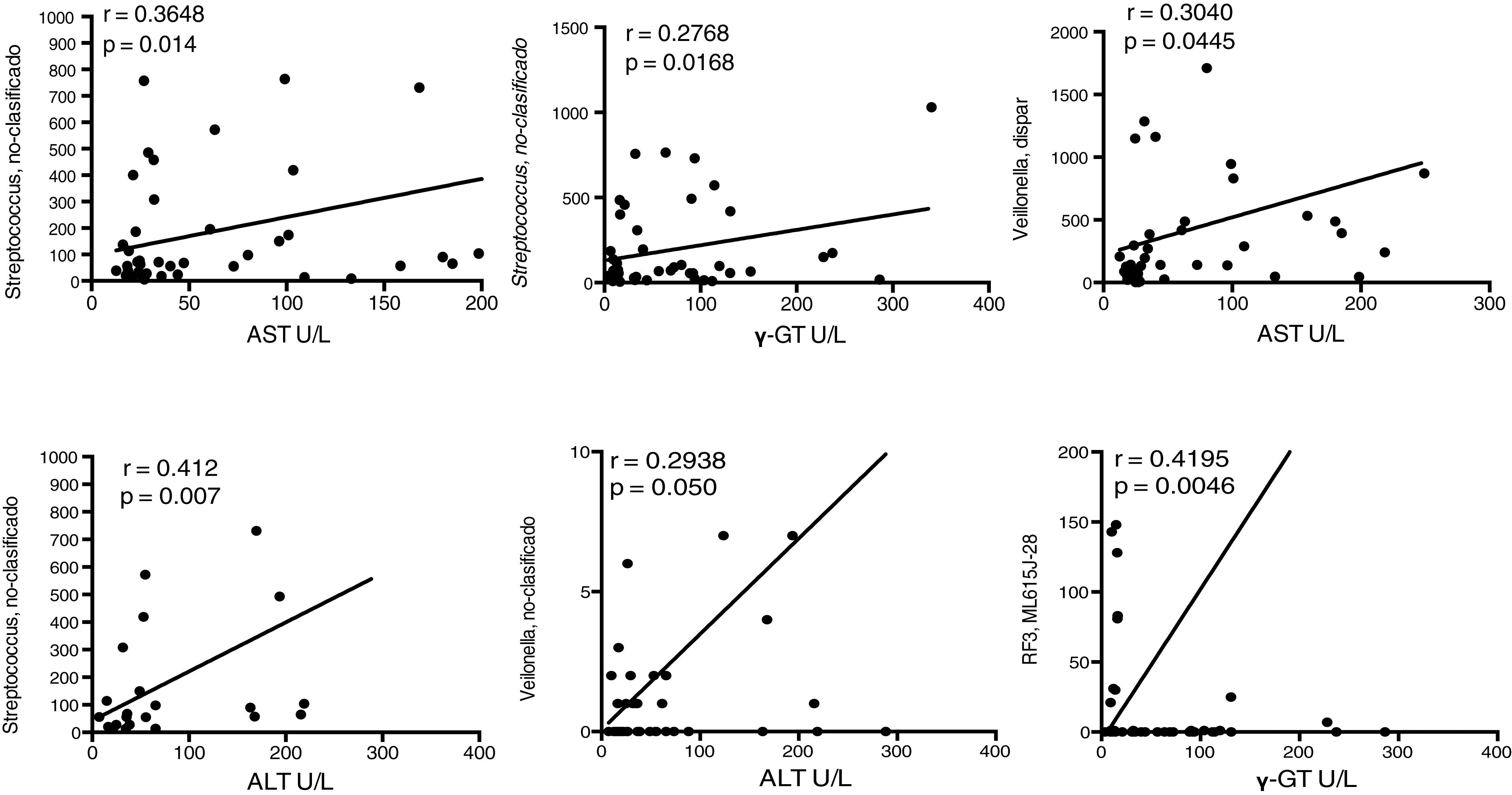
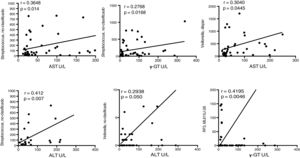
Con la finalidad de establecer las asociaciones entre las familias de bacterias en los pacientes cirróticos con los indicadores de daño hepático decidimos realizar las correlaciones de dichas alteraciones bioquímicas con los cambios en la abundancia de OTU en ambos grupos. En este análisis encontramos que varios OTU presentaron correlaciones positivas con el grupo de pacientes cirróticos (fig. 7), indicando que los cambios en estos grupos de bacterias, en este caso de incremento en su abundancia relativa, podrían estar relacionados con el inicio o la progresión, o quizás ambos, del daño hepático, principalmente debido a la infección por virus C.
Fragmento de la firma de bacterias que presentan asociaciones significativas con la etiología del daño hepático. Las gráficas indican los niveles de asociación entre algunos OTU a nivel de familia con los niveles séricos de las enzimas que indican daño hepático. La curva de correlación y la r cuadrada, así como la significación de la prueba de Pearson, se presentan en cada caso. ALT: alanino-aminotransferasa; AST: aspartato-aminotransferasa; γ-GT: gamma-glutaminotransferasa; U/L: unidades/litro.
En conjunto, nuestros datos muestran que la abundancia relativa de la microbiota en pacientes cirróticos de origen mexicano presenta diferencias significativas respecto de un grupo de sujetos control, sin antecedentes de o con enfermedad hepática manifiesta. Además, permiten establecer una potencial firma de bacterias que están directamente asociadas con la falla hepática.
DiscusiónLos estudios más recientes sobre la diversidad de la microbiota en pacientes con enfermedad hepática indican que aquella tiene un papel preponderante en su fisiopatología y progresión19. Sin embargo, gran parte de dichos reportes han sido obtenidos a partir de pacientes cuyo origen étnico es distinto al de la población mexicana. En nuestro laboratorio creemos que es necesario obtener información local que nos permita conocer si la diversidad microbiana en los pacientes cirróticos es similar o difiere respecto de otras poblaciones. Para responder a dicha pregunta, reclutamos a un grupo piloto de pacientes de origen mestizo-mexicano con enfermedad hepática, en la fase de cirrosis. La mayoría de los pacientes reclutados fueron diagnosticados con cirrosis por infección por virus C y están en la fase compensada de la enfermedad, clasificada como A en la escala Child-Pugh13; por lo que las complicaciones como la ascitis, el sangrado de varices esofágicas, así como la ingesta de medicamentos que pudiesen modificar la composición de la microbiota, han sido en gran medida controladas para evitar que interfieran en la determinación.
De los estudios publicados que abordan el problema de la composición de la microbiota en los pacientes con cirrosis, se ha demostrado que uno de los grupos que más aumenta en número es el de Proteobacteria8. La proporción en el aumento de este grupo de bacterias se incrementa de forma significativa cuando la enfermedad está en su fase descompensada o en fase de hospitalización, comparada con la fase compensada, por lo que se podría decir que este grupo de bacterias puede tener un papel en el detrimento de las condiciones fisiológicas de los pacientes afectados7. Cabe aclarar que, en la fase de hospitalización, el aumento de este taxón podría obedecer a las infecciones intrahospitalarias; eso es algo que aún está por determinarse.
Resulta interesante observar que los pacientes cirróticos reclutados para nuestro trabajo, al igual que en otros reportes, tienen menor diversidad bacteriana, también presentan el mismo patrón de incremento en la abundancia del grupo de Proteobacterias (fig. 2), como Campylobacteraceae, Helicobacteraceae y Neisseriaceae; además, observamos que el orden de los Clostridiales, específicamente Veillonella (dispar o parvula), Blautia (obeum o producta), Selenomonas y Anaerofustis, también tienen mayor presencia en estos pacientes cuando se comparan con el grupo de sujetos sanos. Este patrón se complementa además con los datos de las correlaciones entre los datos de algunos parámetros bioquímicos y la presencia de bacterias de géneros específicos como Streptococcus, Veillonella y RF3, todos los cuales tienen fuerte asociación con el estado patológico de los pacientes (fig. 7). En este sentido, se ha reportado que pacientes con cirrosis con grados avanzados de daño y cuyo desenlace es el cáncer hepático tienen asociaciones significativas entre parámetros como la bilirrubina total o la creatinina sérica y la presencia de diversos grupos de bacterias, como Enterobacteria y Clostridium20.
Se sabe además que diversas vías metabólicas se encuentran enriquecidas en los pacientes cirróticos, cuando se comparan con sujetos sanos. Entre las más abundantes están la vía del transporte y metabolismo de los aminoácidos, la biosíntesis, el transporte y metabolismo de metabolitos secundarios, la producción de energía a partir de fuentes diferentes de los hidratos de carbono, y el tráfico intracelular y la secreción, entre otras; mientras que aquellas que disminuyen incluyen la replicación, recombinación y reparación de ADN, entre muchas otras4. Un análisis más detallado del metagenoma de la microbiota en nuestros pacientes permitirá establecer si dichas vías también se encuentran alteradas. Es importante resaltar que varios autores coinciden en el hecho de que los pacientes cirróticos al tener problemas de metabolismo de proteínas y de hidratos de carbono presentan incrementos en las vías de producción de energía, en términos de su metagenoma intestinal. Por lo pronto, está por determinarse si dichas vías también se ven alteradas en la población de pacientes cirróticos mestizo-mexicanos.
Por último, diversas publicaciones han demostrado la utilidad del uso del trasplante de materia fecal en pacientes afectados por Clostridium difficile21–23, y los resultados de estas intervenciones parecen tener un grado aceptable de éxito. No obstante, existe un intenso debate sobre los posibles efectos a mediano y largo plazo, que aún están en fase de análisis en diversos ensayos clínicos24,25. Por tanto, otros investigadores han optado por el uso de probióticos (microorganismos vivos), especialmente del género Lactobacillus. Algunos de los hallazgos obtenidos en ensayos clínicos indican que la administración de Bulgaricus, Bifidobacterium, Plantarum, la variedad Nissle de E. coli, Bifidobacterium longum, así como Lactobacillus casei o rhamnosus, tiene efectos positivos en la disminución de algunos de los parámetros que se usan para indagar daño hepático, como ALT, AST, GGT, LPS26. Esto indica claramente que una estrategia simple y a bajo costo es el consumo de probióticos y prebióticos que incrementen, por un lado, la masa de bacterias «benignas» que desplacen a las patógenas del nicho que representa el tracto gastrointestinal, y por otro, la producción de metabolitos que contribuyan a la obtención o mayor eficiencia de energía a partir de los alimentos que pueden consumir los pacientes afectados.
En este trabajo determinamos los cambios en la abundancia relativa de bacterias intestinales en una muestra de pacientes cirróticos de origen mestizo-mexicano, con relación a un grupo de sujetos sin enfermedad hepática. Nuestros datos muestran que los grupos de bacterias intestinales más abundantes encontrados en los pacientes cirróticos son las Proteobacterias y los Clostridiales, que además contribuyen a las asociaciones entre algunos de los parámetros bioquímicos y la etiología.
Logramos identificar con buenos niveles de confianza que algunos de los taxones identificados coinciden con los reportados por otros grupos de trabajo en regiones distintas a las encontradas en México, lo cual es algo novedoso. Este trabajo es uno de los primeros reportes en cuanto a la descripción de la microbiota en este tipo de pacientes de origen mestizo-mexicano. Los resultados de este trabajo serán complementados a posteriori con los resultados del análisis de la microbiota oral de este mismo grupo de pacientes y otros que están por reclutarse.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónEl presente trabajo ha sido financiado parcialmente por el Departamento de Gastroenterología del INCMNSZ, a través de la Secretaria de Salud Pública de México. I. Escalona es becaria del programa de becas de posgrado de excelencia del CONACyT.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.
A B. Riveros y C.C. Ruíz, por su asistencia técnica con el ultrasonido hepático; a la Dra. M. Guevara por su asistencia técnica con la determinación de analitos en COBAS C111; a la M. en C. I. Medina por la discusión en la parte estadística; y al Dr. Luis F. Uscanga Domínguez por su apoyo incondicional para la realización de este trabajo.