La gastritis folicular se asocia con la infección por Helicobacter pylori; sin embargo, su relación con los genotipos bacterianos es poco conocida. Nuestro objetivo fue establecer la relación entre la gastritis folicular y distintas cepas del H. pylori.
Material y métodosEstudio analítico de casos y controles que incluyó 36 pacientes con gastritis folicular (casos) y 83 con gastritis no atrófica (controles). La información sociodemográfica se obtuvo mediante un cuestionario. Se obtuvieron biopsias que se evaluaron según las clasificaciones de Sydney y Wotherspoon. La genotipificación de H. pylori se realizó mediante reacción en cadena de la polimerasa. Para las variables cuantitativas se empleó la media y la desviación estándar. Las variables categóricas se presentan como proporciones y frecuencia absoluta. La OR con su IC del 95% evaluó el efecto de cada variable sobre el desenlace (gastritis folicular). Un valor de p<0.05 se consideró significativo.
ResultadosLa gastritis folicular se asoció con la infección por Helicobacter OR: 13.41 IC (1.7-103) p=0.01. El genotipo CagA+ estuvo presente en el 56.5% de los casos y 58% de los controles. El 82% de los aislamientos presentó la cepa citotóxica VacAs1m1 en los 2 grupos. La frecuencia de iceA1 fue de 34.8% y 26% en casos y controles respectivamente, diferencias que no fueron estadísticamente significativas.
ConclusionesLas cepas citotóxicas de Helicobacter exhiben elevadas frecuencias en la población estudiada. El genotipo iceA1 fue más frecuente en la gastritis folicular.
Follicular gastritis is associated with Helicobacter pylori infection, but little is known of its relation to bacterial genotypes. Our aim was to establish the relation between follicular gastritis and different H. pylori strains.
Materials and methodsAn analytic case-control study was conducted that included 36 patients with follicular gastritis (cases) and 83 with nonatrophic gastritis (controls). The sociodemographic information was obtained through a questionnaire. Biopsies were evaluated according to the Sydney System and the Wotherspoon scoring system. Helicobacter pylori genotyping was performed using the polymerase chain reaction technique. The quantitative variables were presented as mean and standard deviation and the qualitative variables as proportions and absolute frequency. The effect of each variable on outcome (follicular gastritis) was evaluated through the odds ratio and its 95% confidence interval. Statistical significance was set at a P<0.05.
ResultsFollicular gastritis was associated with Helicobacter pylori infection (OR: 13.41, CI: 1.7-103, P=0.01). The CagA+ genotype was present in 56.5% of the cases and 58% of the controls. The cytotoxic VacAs1m1strain was present in 82% of the isolates in both groups. IceA1 frequency was 34.8% in the cases and 26% in the controls and the difference was not statistically significant.
ConclusionsThe population studied had elevated frequencies of cytotoxic Helicobacter pylori strains and the iceA1 genotype was more frequent in follicular gastritis.
La gastritis folicular se caracteriza por un marcado infiltrado inflamatorio de tipo mononuclear y la formación de folículos linfoides con centro germinal en la lámina propia1,2. Para algunos autores se deben identificar al menos 2 folículos linfoides secundarios en un área de 1cm de la mucosa gástrica para establecer el diagnóstico3. La prevalencia de la enfermedad es variable. En Japón se reportan prevalencias de 0.19%, mientras que datos aportados por investigadores griegos y franceses demuestran prevalencias del 12.7% y 14.2%, respectivamente4,5. Otros estudios muestran tasas de prevalencia que oscilan entre el 27.4% y el 79.9%6–8. En un estudio colombiano se encontró una prevalencia del 8.4%9.
La enfermedad se asocia con la edad, la infección por Helicobacter pylori (H. pylori) y el desarrollo del linfoma tejido linfoide asociado a mucosas (MALT)1,10. En cuanto a la edad se ha determinado mayor frecuencia de la enfermedad en pacientes pediátricos con síntomas dispépticos persistentes, en adolescentes y en adultos jóvenes, mientras que el género femenino parece representar una condición especial para el desarrollo de la enfermedad5,11. De mayor importancia es la relación de la gastritis folicular con el linfoma MALT. Si bien es cierto que la etiología del linfoma puede estar ligada a múltiples factores, la infección por Helicobacter parece desempeñar un rol preponderante. Este rol ha quedado demostrado tras la regresión de gastritis foliculares y aun de linfomas MALT tras la erradicación bacteriana12. No obstante, es poco lo que se conoce en relación con la cascada de eventos que ocurren desde la gastritis folicular hasta la aparición del linfoma13.
Es sabida la relación de los genotipos bacterianos con algunos tipos de enfermedad. Los genotipos cagA+ y vacAs1m1 se consideran las cepas más virulenta asociadas con úlcera péptica, cáncer gástrico e inflamación severa14, mientras que la cepa s2m2 genera una inflamación limitada; sin embargo, el papel de los genotipos bacterianos en la génesis de la gastritis folicular es poco conocido. En este contexto, esta investigación busca establecer la relación entre la variabilidad genética de la bacteria (genotipos cagA, vacA y iceA1) y la gastritis folicular. Se pretende así ampliar el conocimiento que se tiene acerca de los factores determinantes de esta condición, y si existe un genotipo bacteriano asociado a la misma. Por ser la gastritis folicular una entidad relacionada con el linfoma gástrico se plantea la hipótesis de que los genotipos bacterianos más agresivos se asocien a este tipo de inflamación.
Material y métodosSe realizó un estudio analítico de casos y controles no pareado en pacientes que ingresaron en las unidades de gastroenterología del Hospital Universitario San José y Endovideo en la ciudad de Popayán (ubicada al Suroccidente colombiano sobre el área montañosa de los Andes, y catalogada un área de alto riesgo de cáncer gástrico)15 durante el periodo de tiempo comprendido entre enero de 2008 y diciembre de 2011. La muestra se obtuvo por conveniencia incluyendo pacientes mayores de 18 años, con diagnóstico histopatológico de gastritis folicular o gastritis crónica no atrófica (grupo control). Los participantes incluidos debieron nacer en algún municipio del Cauca y ser hijos de padres caucanos. Se excluyeron pacientes con presencia de atrofia, metaplasia, displasia, cáncer gástrico o de otro tipo, cirugía gástrica, tratamiento previo para H. pylori o infección por el VIH.
Biólogos del Grupo de Investigación en Genética Humana y Aplicada (GIGHA) de la Universidad del Cauca practicaron un cuestionario para colectar las variables de tipo sociodemográfico (edad, sexo, nivel educativo, ingresos económicos y grupo étnico). Las muestras gástricas fueron obtenidas a través de endoscopia digestiva por gastroenterólogos de amplia experiencia. Los pacientes asistieron a endoscopia referidos por síntomas dispépticos y en condiciones de ayuno de al menos 8horas. Los participantes no fueron sedados, pero recibieron una solución tópica para anestesiar la faringe. Se tomaron 5 muestras correspondientes a 2 biopsias de antro (curvatura mayor y menor), 2 de cuerpo (curvatura mayor y menor) y una biopsia de incisura angularis. Las biopsias se fijaron en formol tamponado y fueron coloreadas con las tinciones de hematoxilina-eosina y Giemsa. El análisis histopatológico de cada muestra lo realizaron 2 patólogos. Se emplearon escalas visuales análogas de acuerdo al sistema de Sydney. Se evaluó la presencia de actividad histológica (inflamación por polimorfonucleares neutrófilos), así como la presencia de H. pylori. La gastritis folicular se definió como la presencia de uno o más folículos linfoides con centro germinal en la lámina propia, y su severidad se estadificó en una escala de 1 a 5 según el sistema de Wotherspoon16 (tabla 1).
Grado de severidad de la gastritis folicular. Incluye el grado de sospecha histológica de linfoma MALT
| Grado 0 | Normal | Escasas células inflamatorias en la lámina propia. No hay folículos linfoides |
| Grado 1 | Gastritis crónica | Pequeños grupos de linfocitos en la lámina propia. No hay folículos linfoides |
| Grado 2 | Gastritis folicular | Folículos linfoides prominentes con células plasmáticas y zona del manto |
| Grado 3 | Infiltrado inflamatorio sospechoso probablemente reactivo | Folículos linfoides rodeados por pequeños linfocitos que infiltran difusamente la lámina propia y ocasionalmente el epitelio |
| Grado 4 | Infiltrado sospechoso probablemente linfoma | Folículos linfoides rodeados por células de tipo centrocítico que infiltran la lámina propia y el epitelio en pequeños grupos |
| Grado 5 | Linfoma MALT | Presencia de un denso infiltrado por mononucleares de tipo centrocítico en la lámina propia y que invaden la lámina epitelial —lesión linfoepitelial— |
Fuente: Modificada de Wotherspoon et al.16.
Los estudios de genotipificación bacteriana fueron realizados a partir de la extracción de ADN de las biopsias embebidas en parafina, utilizando la técnica de Chelex (No. C7901; Sigma, St. Louis, MO). Para la amplificación de los genes cagA, iceA1 y vacA se utilizó la técnica de reacción en cadena de la polimerasa (PCR) descrita previamente por Yamaoka et al.12. Las mezclas de PCR se prepararon con 50ng de DNA genómico, 100μmol dNTPs, 2.5μl de 10X PCR buffer, 1.0mM MgCl2, 1U de Taq ADN polimerasa (No. M1665; Promega, Madison, WI), y 30pmol de cada uno de los cebadores, como se indica en la tabla 2. Las reacciones iniciaron con un paso de desnaturalización a 95°C por un 1minuto, seguido de 35 ciclos de desnaturalización a 94°C por 1minuto, hibridación a 52°C por 1minuto y extensión a 72°C por 1minuto, y un paso de extensión final a 72°C por 10minutos. Los productos fueron analizados por electroforesis en geles de agarosa al 2% a 80 voltios por 40minutos y los genotipos se reconocieron acorde con el tamaño en pares de bases esperado.
Secuencia de cebadores para amplificación por PCR
| Genes y regiones | Secuencia (5’→3’) | Tamaño (pb) |
|---|---|---|
| cagA | GATAACAGGCAAGCTTTTGAGG | 349 |
| CGTCAAAAGATTGTTTGGCAGA | ||
| iceA1 | GTGTTTTTAACCAAAGTATC | 247 |
| CTATAGCCASTYTCTTTGCA | ||
| vacA s1/s2 | ATGGAAATACAACAAACACAC | 259/286 |
| CTGCTTGAATGCGCCAAAC | ||
| vacA m1/m2 | CAATCTGTCCAATCAAGCGAG | 570/645 |
| GCGTCTAAATAATTCCAAGG |
Las cepas de H. pylori NCTC-11637, NCTC-11638 y el aislado clínico 3062 fueron facilitadas por el Instituto Nacional de Cancerología de Colombia para ser utilizadas como controles positivos. Adicionalmente, todas las pruebas de PCR incluyeron controles internos de amplificación y marcadores moleculares (escaleras) adecuados.
Los sesgos de información demográfica se controlaron mediante la aplicación de un cuestionario con preguntas cerradas realizado por miembros del GIGHA, quienes recibieron instrucciones y asesoría por parte de médicos gastroenterólogos y patólogos. La valoración histopatológica fue validada por un segundo patólogo.
Las pruebas de biología molecular se efectuaron de acuerdo a protocolos mundialmente aceptados, se realizaron pruebas piloto para verificar la calidad de los reactivos y kits de extracción y se verificó la calibración previa de los equipos de laboratorio. Para evitar sesgos en la interpretación de la información genética y estimar el efecto real de cada genotipo sobre la variable respuesta se excluyeron del análisis los casos de coinfección bacteriana determinada mediante la presencia de más de un genotipo.
Como la variable edad tuvo distribución normal mediante la prueba de Kolmogorov-Smirnov, esta se presenta con promedio y desviación estándar. Las diferencias entre las medias se evaluaron con la prueba «t» de Student, mientras que las diferencias de proporciones se evaluaron mediante la prueba de Chi cuadrado de independencia. La OR con su valor de p fueron usadas para evaluar el efecto de cada variable del estudio sobre la variable respuesta (gastritis folicular). Se efectuó un análisis de regresión logística multivariado, incluyendo como posibles variables confusoras la edad y el género. Un valor de p<0.05 se consideró significativo. El análisis estadístico se realizó con el programa SPSS versión 23.
Los participantes aceptaron su participación y firmaron el consentimiento informado. La investigación fue aprobada por el Comité de Ética para la Investigación Científica de la Universidad del Cauca.
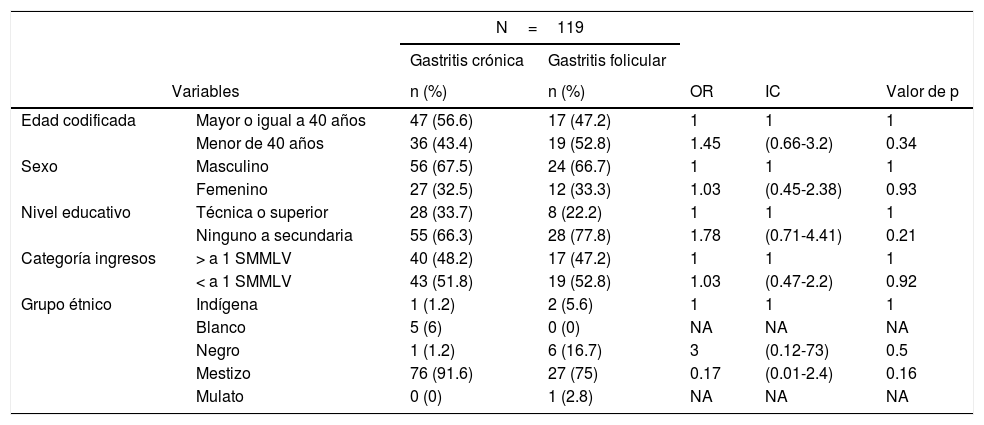
ResultadosDe un total de 808 participantes seleccionados durante el tiempo de estudio, un total de 119 pacientes cumplieron los criterios de inclusión. De estos, 83 participantes correspondientes al 70% presentaron el diagnóstico de gastritis crónica no atrófica y 36 (30%) el diagnóstico de gastritis folicular. En los pacientes con gastritis crónica no atrófica el rango de edad fue de 19 a 81 años, con una media de 44.11 años. El rango de edad para los pacientes con gastritis folicular fue de 21 a 82, con una media de 41.86 años. La prueba «t» de Student para comparar diferencias entre las medias de edad no mostró diferencias significativas (p=0.48). En relación con la etnia la gran mayoría de pacientes fueron mestizos; sin embargo, en el grupo de gastritis folicular se encontraron 6 (17%) pacientes de raza negra. No se observaron diferencias estadísticamente significativas en las variables sociodemográficas (tabla 3).
Características sociodemográficas de los pacientes
| N=119 | ||||||
|---|---|---|---|---|---|---|
| Gastritis crónica | Gastritis folicular | |||||
| Variables | n (%) | n (%) | OR | IC | Valor de p | |
| Edad codificada | Mayor o igual a 40 años | 47 (56.6) | 17 (47.2) | 1 | 1 | 1 |
| Menor de 40 años | 36 (43.4) | 19 (52.8) | 1.45 | (0.66-3.2) | 0.34 | |
| Sexo | Masculino | 56 (67.5) | 24 (66.7) | 1 | 1 | 1 |
| Femenino | 27 (32.5) | 12 (33.3) | 1.03 | (0.45-2.38) | 0.93 | |
| Nivel educativo | Técnica o superior | 28 (33.7) | 8 (22.2) | 1 | 1 | 1 |
| Ninguno a secundaria | 55 (66.3) | 28 (77.8) | 1.78 | (0.71-4.41) | 0.21 | |
| Categoría ingresos | > a 1 SMMLV | 40 (48.2) | 17 (47.2) | 1 | 1 | 1 |
| < a 1 SMMLV | 43 (51.8) | 19 (52.8) | 1.03 | (0.47-2.2) | 0.92 | |
| Grupo étnico | Indígena | 1 (1.2) | 2 (5.6) | 1 | 1 | 1 |
| Blanco | 5 (6) | 0 (0) | NA | NA | NA | |
| Negro | 1 (1.2) | 6 (16.7) | 3 | (0.12-73) | 0.5 | |
| Mestizo | 76 (91.6) | 27 (75) | 0.17 | (0.01-2.4) | 0.16 | |
| Mulato | 0 (0) | 1 (2.8) | NA | NA | NA | |
NA: no aplica; SMMLV: salario mínimo mensual legal vigente.
Un valor de p<0.05 se consideró significativo.
En el estudio histopatológico se evaluó la relación entre la infección por H. pylori y la respuesta inflamatoria folicular. En el grupo de gastritis folicular se encontró que en 35 pacientes (97.2%) estaba presente la infección, mientras que la infección se documentó solo en 60 (72.3%) de los pacientes del grupo control. Se demostró una asociación estadísticamente significativa entre la infección y la gastritis folicular; OR: 13.41, IC (1.7-103) p=0.01.
Se evaluó también la relación entre infección bacteriana y actividad inflamatoria, encontrándose una asociación estadísticamente significativa (OR: 337.33, IC: [53.1-2142], p=0.00).
La mayoría de pacientes con gastritis folicular (23/36) fueron clasificados como gastritis grado 2 de Wotherspoon, 12 pacientes fueron clasificados como gastritis grado 3 (33%) y un solo paciente se clasificó como grado 4. De los pacientes con gastritis grado 2 fueron hombres 6 y mujeres 17; entre los pacientes con grado 3, fueron hombres 6 y mujeres 6, mientras que la única paciente clasificada como grado 4 correspondió a una mujer de 42 años. No se documentaron casos de linfoma MALT.
Del total de 119 participantes se excluyeron del análisis genético 46 pacientes: 20 pacientes que mostraron más de un genotipo bacteriano vacA (coinfección) y 26 pacientes en los cuales no se logró amplificación de genes para el análisis (tabla 4).
Con las pruebas moleculares se pudo caracterizar el H. pylori de 73 participantes (50 pacientes con gastritis crónica no atrófica y 23 pacientes con gastritis folicular). La distribución de las cepas en el grupo control correspondió a: 29 (58%) con genotipo cagA positivo, mientras que en los pacientes con gastritis folicular este genotipo se encontró en 13 (56.5%) pacientes. No se encontraron diferencias estadísticamente significativas en relación con el genotipo cagA (la OR de desarrollar gastritis folicular en pacientes cagA+ fue de 0.79 IC=0.29-2.13 y p=0.64).
En los pacientes con gastritis folicular 8 (34.8%) fueron iceA1 positivos, mientras que en el grupo control se encontró dicho genotipo en 13 pacientes correspondientes al 26%. Dichas diferencias no fueron estadísticamente significativas (OR: 1.83, IC: 0.64-5.22, p=0.26). Para el análisis de los genotipos bacterianos vacA se determinaron los subtipos s1, s2, m1, m2 y se agruparon en 4 categorías de acuerdo a su perfil de virulencia. Estos grupos se relacionaron con los demás genotipos (iceA1 y cagA). Se seleccionaron como grupos de contraste los genotipos cagA–/iceA1– y los subtipos s2m2 de vacA. El análisis demostró una alta prevalencia (82%) del genotipo vacA subtipos s1m1 para los 2 grupos de pacientes sin diferencias significativas (OR: 1.04, IC: 0.28-3.81, p=0.95).
En ninguno de los 2 grupos se documentaron subtipos s2m1. El análisis de los demás subtipos no reveló diferencias estadísticamente significativas (tabla 5).
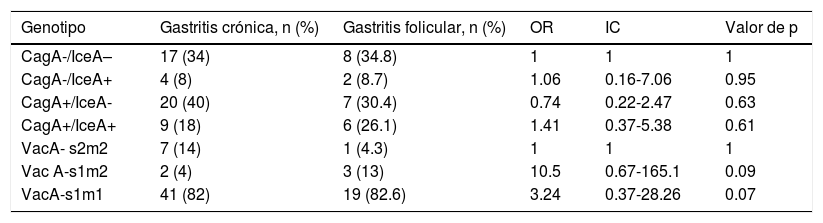
Distribución de genotipos cagA, iceA1 y vacA en los grupos de estudio; n=73
| Genotipo | Gastritis crónica, n (%) | Gastritis folicular, n (%) | OR | IC | Valor de p |
|---|---|---|---|---|---|
| CagA-/IceA– | 17 (34) | 8 (34.8) | 1 | 1 | 1 |
| CagA-/IceA+ | 4 (8) | 2 (8.7) | 1.06 | 0.16-7.06 | 0.95 |
| CagA+/IceA- | 20 (40) | 7 (30.4) | 0.74 | 0.22-2.47 | 0.63 |
| CagA+/IceA+ | 9 (18) | 6 (26.1) | 1.41 | 0.37-5.38 | 0.61 |
| VacA- s2m2 | 7 (14) | 1 (4.3) | 1 | 1 | 1 |
| Vac A-s1m2 | 2 (4) | 3 (13) | 10.5 | 0.67-165.1 | 0.09 |
| VacA-s1m1 | 41 (82) | 19 (82.6) | 3.24 | 0.37-28.26 | 0.07 |
Un valor de p<0.05 se consideró significativo.
Aunque el análisis bivariado no mostró asociaciones estadísticamente significativas entre la gastritis folicular y las variables género y edad, la revisión bibliográfica muestra una probable relación con la variable respuesta; por lo tanto, se exploró el posible efecto confusor de estas variables en un modelo de regresión logística que incluyó la infección por H. pylori (tabla 6).
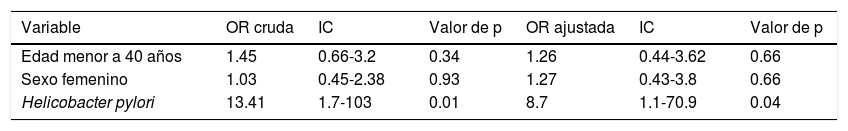
Modelo multivariado ajustado por la edad categorizada y el género. Se muestran las medidas de asociación de las variables de interés en relación con el desenlace (gastritis folicular)
| Variable | OR cruda | IC | Valor de p | OR ajustada | IC | Valor de p |
|---|---|---|---|---|---|---|
| Edad menor a 40 años | 1.45 | 0.66-3.2 | 0.34 | 1.26 | 0.44-3.62 | 0.66 |
| Sexo femenino | 1.03 | 0.45-2.38 | 0.93 | 1.27 | 0.43-3.8 | 0.66 |
| Helicobacter pylori | 13.41 | 1.7-103 | 0.01 | 8.7 | 1.1-70.9 | 0.04 |
Un valor de p<0.05 se consideró significativo.
La relación entre gastritis folicular y edad ha sido referenciada por varios autores3,8,17. Aunque en nuestro estudio cabría esperarse una población adulta joven (dado que se excluyeron pacientes con atrofia, metaplasia, displasia y cáncer que son condiciones asociadas a edades avanzadas)18 el rango etario de los participantes varió entre 19 y 82 años. Nuestros resultados mostraron que la población con gastritis folicular tiene en términos generales menor edad que los pacientes con gastritis crónica. Este hallazgo es similar a los publicados por otros autores19,20.
La asociación entre patrones de respuesta inflamatoria y etnia ha sido referenciada como un factor importante en el riesgo o protección frente a distintas enfermedades, incluyendo el cáncer gástrico21–23. Recientemente se ha propuesto por ejemplo que el riesgo de cáncer gástrico y el grado de inflamación gástrica es producto de un fenómeno de tolerancia inmunológica dependiente de la ancestría poblacional y la ancestría bacteriana del H. pylori22. En nuestro estudio se incluyen participantes que nacieron en el Cauca con padres caucanos, y se encontró que la mayoría de los pacientes con gastritis folicular pertenecen a categoría racial de mestizo. Dado el reducido número de pacientes nuestras conclusiones son limitadas; sin embargo, resulta un dato interesante puesto que no se encuentra descrito en la literatura y plantea la posibilidad de que la ancestría poblacional y el origen étnico de los pacientes podría influir en el patrón de inflamación folicular.
En pacientes con gastritis folicular la prevalencia de la infección por Helicobacter varía entre el 68% y 100%, en concordancia con el número de biopsias tomadas9,24. En esta investigación se aplicó el protocolo de Sydney que estipula la toma de 5 biopsias, las cuales permiten un muestreo significativo de la mucosa gástrica y una determinación fiable de los hallazgos histológicos25. El estudio microscópico permitió la detección de la infección en el 97.2% de los pacientes con gastritis folicular, mostrando diferencias significativas con el grupo control —OR: 13.41, IC (1.7-103), p=0.01. Esta relación persiste aún en el modelo multivariado en el que se incluyeron variables confusoras. Se demostró igualmente una asociación significativa entre la actividad inflamatoria y la presencia de infección bacteriana. El vínculo entre infección y gastritis activa y folicular es ampliamente reconocido en la comunidad médica y ha sido documentado por distintos investigadores3,5,26,27.
Diferentes investigaciones han evaluado el papel de los genotipos bacterianos en relación con el linfoma MALT. Los trabajos de Eck, Ye, y Koehler, et al. lograron establecer asociaciones estadísticamente significativas entre este linfoma y los genotipos cagA, vacAs1m1 e iceA128–30, sin embargo son pocos los estudios que relacionan genotipos bacterianos y gastritis folicular. En concreto, el estudio de Soltermann et al. evaluó la presencia de folículos linfoides en el antro y el cuerpo y correlacionaron la información con alelos y genotipos de cagA y vacA, demostrando que no existe una relación significativa31. Estos hallazgos son similares a los encontrados en esta investigación. En América Latina se han realizado algunos estudios descriptivos y otros analíticos que muestran asociaciones entre genotipos bacterianos y enfermedades como la úlcera, el cáncer y la gastritis32–35. Según el conocimiento de los autores esta es la primera investigación que explora la relación de genotipos bacterianos con la gastritis folicular en una población colombiana.
En Colombia, Quiroga y Citelly han documentado en pacientes con gastritis frecuencias para el genotipo cagA del 50% y 51.4%35,36; dato muy similar al encontrado en esta investigación (58% para los controles).
En relación con los genotipos vacAs1m1 el estudio de Citelly et al. mostró prevalencias del 43% para la cepa s1 y del 40% para la cepa m1, mientras que nosotros observamos prevalencias superiores al 80%. Esta información muestra que la población de estudio tiene genotipos bacterianos más agresivos aún en estadios tempranos de enfermedades gástricas. Cabe resaltar que ninguno de los pacientes incluidos en este estudio presentó atrofia, metaplasia o displasia, y que la mayoría de los pacientes en el grupo de casos presentó una gastritis folicular grado 2 o 3. De acuerdo al conocimiento que se tiene de las cascadas de carcinogénesis propuesta por Pelayo Correa, y el modelo de Wotherspoon16,37, los hallazgos histológicos en la población de estudio plantearían un bajo riesgo de desarrollo de cáncer (tanto adenocarcinoma intestinal como linfoma MALT), no obstante la presencia de cepas citotóxicas haría necesario un seguimiento endoscópico e histopatológico más cuidadoso de nuestros pacientes. Estas diferencias genotípicas explicarían al menos en parte por qué los pacientes caucanos exhiben tasas de incidencia de cáncer sobresalientes cuando se comparan con otras zonas del país15.
Para algunos autores el genotipo iceA1 es considerado un factor de virulencia involucrado en la adhesión celular y el desarrollo de úlceras, mientras que otros consideran que su prevalencia depende de la distribución geográfica de la bacteria38–40. En esta investigación la distribución del genotipo iceA1 no varió significativamente entre los grupos comparados; sin embargo, se evidencia que es más frecuente en la gastritis folicular que en la gastritis crónica no atrófica. Estos datos sugieren una probable relación entre la respuesta inflamatoria de tipo folicular y el genotipo iceA1.
Entre las limitaciones del estudio se encuentra el reducido número de datos que se incluyeron para los análisis genéticos. Se sugiere en futuras investigaciones la verificación del pH en el formol empleado para la recolección de las biopsias, o el uso de medios de transporte y cultivo como alternativas que facilitarían la recuperación del ADN bacteriano. Esperamos motivar a la comunidad científica para evaluar el papel del genotipo iceA1 con tamaños de muestra más grande.
En conclusión, los resultados de esta investigación demuestran que la gastritis folicular y la actividad inflamatoria son marcadores fiables de infección por H. pylori, y que en la población de estudio predominan los genotipos de alto riesgo oncogénico. Por lo tanto, su diagnóstico debe alertar al clínico con el fin de evitar progresión a enfermedades de mayor morbimortalidad. Además, se sugiere un posible rol del genotipo iceA1 en la génesis de la gastritis folicular.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo.
FinanciaciónEste estudio fue financiado por el Programa de Salud de Colciencias, proyecto código 1103-519-29123.
Conflicto de interesesLos autores del presente artículo declaramos no presentar conflicto de intereses alguno.
Los autores expresan su agradecimiento a los pacientes por su participación en el estudio y al personal del Hospital Universitario San José y Endovideo por su valiosa asistencia. Además, agradecen al Laboratorio de Genética Humana y al Departamento de Patología de la Facultad de Ciencias de la Salud de la Universidad del Cauca por su apoyo en la ejecución de este proyecto.